Establishment of an indirect ELISA method for detecting serum antibodies based on the human endogenous retrovirus-K envelope protein antigen and its application in lung cancer patients
-
摘要:
目的 利用原核表达系统表达、纯化人内源性逆转录病毒-K(HERV-K)包膜蛋白(env蛋白),建立基于HERV-K env蛋白抗原的间接ELISA检测方法,并分析肿瘤患者血清HERV-K env抗体表达与临床病理特征的相关性。
方法 构建原核表达载体pET32a-env,转化至大肠埃希菌BL21(DE)感受态细胞中,用异丙基-β-D-硫代半乳糖苷(IPTG)作为诱导剂在37 ℃条件下过夜震荡诱导表达,高压破碎菌体后分离包涵体蛋白,经过8 mol/L尿素变性、镍柱纯化、透析法复性得到纯化的HERV-K env蛋白;用得到的抗原蛋白作为包被抗原建立ELISA检测方法。运用建立的间接ELISA检测方法检测2025年5月1日至5月31日在海军军医大学第一附属医院就诊的128例肺癌患者血清样本,分析HERV-K env抗体表达与患者临床病理特征的相关性。
结果 成功获取HERV-K env蛋白,SDS-PAGE检测蛋白分子量大小正确、肽指纹鉴定显示蛋白氨基酸序列正确。建立的间接ELISA检测方法最佳反应条件为:抗原最佳包被量为4 μg/mL(4 ℃/16 h)、封闭条件为5%脱脂奶粉溶液(37 ℃/120 min)、一抗稀释倍数为1∶100(37 ℃/60 min)、二抗稀释倍数为1∶4 000(37 ℃/60 min)。HERV-K env蛋白间接ELISA检测方法在特异性(抑制率77.6%)、灵敏性(可检测至1∶400稀释倍数)和重复性(变异系数<5%)方面表现良好。对128例肺癌患者进行血清检测发现,晚期(Ⅲ~Ⅳ期)患者的HERV-K env抗体阳性率高于早期(Ⅰ~Ⅱ期)患者[58.0%(51/88)vs 37.5%(15/40),
P <0.05],有远处转移患者的HERV-K env抗体阳性率高于无远处转移的患者[68.9%(42/61)vs 35.8%(24/67),P <0.001]。结论 成功建立了一种基于HERV-K env蛋白的间接ELISA检测方法,并在肺癌患者人群中揭示了血清HERV-K env抗体与疾病分期和远处转移状态呈正相关。HERV-K env抗体有望成为一种反映肺癌侵袭和预后的新型血清学生物标志物。
Abstract:Objective To express and purify the human endogenous retrovirus K (HERV-K) envelope (env) protein using a prokaryotic expression system, to establish an indirect enzyme-linked immunosorbent assay (ELISA) based on the HERV-K env antigen, and to analyze the correlation between serum HERV-K env antibody expression and clinicopathological characteristics in lung cancer patients.
Methods The prokaryotic expression vector pET32a-env was constructed and transformed into
Escherichia coli BL21 (DE) competent cells. Protein expression was induced overnight at 37 ℃ with shaking using isopropyl β-D-1-thiogalactopyranoside (IPTG). After high-pressure cell disruption, inclusion body proteins were isolated. The HERV-K env protein was purified through denaturation with 8 mol/L urea, nickel affinity chromatography, and refolding by dialysis. The purified antigen was used as the coating antigen to establish an ELISA detection method. With this indirect established ELISA method, serum samples from 128 lung cancer patients treated at The First Affiliated Hospital of Naval Medical University between May 1 and May 31, 2025 were tested, and the correlation between HERV-K env antibody expression and patients' clinicopathological characteristics was analyzed.Results The HERV-K env protein was successfully obtained. Sodium dodecylsulfate-polyacrylamide gel electrophoresis analysis confirmed the correct molecular weight, and peptide mass fingerprinting verified the correctness of the amino acid sequence. The optimal conditions for the indirect ELISA were determined as follows: antigen coating concentration of 4 μg/mL (4 ℃, 16 h), blocking with 5% skim milk (37 ℃, 120 min), primary antibody dilution of 1∶100 (37 ℃, 60 min), and secondary antibody dilution of 1∶4 000 (37 ℃, 60 min). The HERV-K env indirect ELISA showed good performance in specificity (inhibition rate 77.6%), sensitivity (detectable up to a 1∶400 dilution), and reproducibility (coefficient of variation < 5%). Serum analysis of the 128 lung cancer patients revealed that the HERV-K env antibody positivity rate was significantly higher in patients with advanced-stage disease (stage Ⅲ-Ⅳ) than in those with early-stage disease (stage Ⅰ-Ⅱ) (58.0%[51/88] vs 37.5%[15/40],
P < 0.05), and was also higher in patients with distant metastasis than in those without distant metastasis (68.9% [42/61] vs 35.8% [24/67],P < 0.001).Conclusion This study has successfully established an indirect ELISA detection method based on the HERV-K env protein. Innovatively, which revealing a significantly positive correlation between serum HERV-K env antibody and both disease stage and distant metastasis status in the lung cancer patient cohort. This suggests that serum HERV-K env antibody has the potential to serve as a novel serological biomarker reflecting lung cancer aggressiveness and prognosis.
-
人内源性逆转录病毒(human endogenous retrovirus,HERV)是数百万年前经外源性逆转录病毒感染宿主生殖细胞后遗留下的残余物,其被整合到宿主生殖细胞DNA中并通过孟德尔方式遗传下来,占人类基因组的8%~10%[1]。在进化过程中,由于内部编码区域和长末端重复序列(long terminal repeat,LTR)的突变、插入或缺失以及宿主的表观遗传调控作用,大多数HERV在正常生理状态下丧失了复制和表达功能;相较于传染性逆转录病毒,人类基因组中约85%的HERV片段是不具备编码能力的单独LTR,只有极少数HERV序列保留了完整的基因组[2]。HERV曾被认为是无用的“垃圾”DNA片段,然而,近年来越来越多的证据表明HERV在众多生物学过程中扮演着关键角色。一方面,HERV在调节宿主功能稳态中发挥重要作用,包括早期胚胎发生、多能遗传调控网络的协调活动以及细胞衰老的调控[3]。另一方面,HERV在疾病发生、发展中扮演重要角色[4]。HERV-K、HERV-H、HERV-P等特定HERV亚家族的异常活化与多种疾病(包括癌症、自身免疫病和神经退行性疾病)存在关联[5-6]。HERV-K是最年轻的HERV亚家族,其整合事件发生在20万~3 500万年前,累积的突变较少,具有最完整的前病毒序列和最高的转录活性[7]。HERV-K的完整结构包括gag、pol、pro、env 4个开放阅读框和两侧的LTR[8]。其中,env基因编码含有3个结构域的包膜蛋白(envelope,env蛋白),分别为信号肽、表面单位以及1个跨膜结构域[9]。近年来,有研究揭示了HERV-K的表达增加与肿瘤发生之间的紧密联系,以及其在肿瘤的扩散、复发和预后中的作用[10]。HERV-K的表达已在多种类型的肿瘤组织中被检测到,其与肿瘤免疫微环境及肿瘤的预后特征相关, 有望成为解决恶性肿瘤治疗难题的新途径,为癌症的早期诊断和预后判断提供潜在的生物标志物。
肺癌是目前全球范围内最常见、致死率最高的恶性肿瘤,其死亡人数约占癌症总死亡人数的18%[11]。尽管目前肺癌的诊断和治疗手段不断进步,但肺癌的早期诊断率仍然较低,晚期确诊患者的治疗效果和预后差异较大,5年生存率仍不理想[12]。血清等体液样本具有无创或微创、易于重复获取、可动态监测等优势,是理想的临床生物标志物来源,尤其适用于早期筛查、疗效评估和预后监测。目前临床常用的肺癌血清标志物主要包括癌胚抗原、鳞状上皮细胞癌抗原、神经元特异性烯醇化酶等,但它们在灵敏性、特异性、早期诊断价值或预后判断准确性方面仍存在不足[13]。因此,迫切需要寻找更有效的早期诊断标志物、预后评估指标和潜在治疗靶点,以改善患者管理、指导临床决策。虽然HERV-K在肿瘤组织中的表达已有报道,但系统性地检测肺癌患者血清中HERV-K特异性蛋白或反应性抗体的表达水平,并将其与患者的临床病理特征和长期生存结局进行关联分析的研究尚未完善。ELISA适用于大批量的抗原抗体检测,具有高灵敏性、强特异性及检测快速、操作简便、设备简单、试剂稳定、成本较低等优点,在疾病检测中广泛应用。目前,市面上尚没有可以快速检测患者血清HERV-K表达水平的ELISA试剂盒。本研究通过原核表达系统表达并纯化HERV-K env蛋白,建立了基于HERV-K env蛋白抗原的间接ELISA检测方法,并用于肺癌患者血清相关抗体的检测,同时对检测结果与临床病理特征进行相关性分析,探讨其作为预后生物标志物的潜力。
1 材料和方法
1.1 细胞与质粒
大肠埃希菌(Escherichia coli,E.coli)DH5α感受态细胞和E.coli BL21(DE)感受态细胞购自生工生物工程(上海)股份有限公司,原核表达载体pET32a-env由海军军医大学基础医学院生物医学工程实验室保存。
1.2 主要试剂
异丙基-β-D-硫代半乳糖苷(isopropyl β-D-1-thiogalactopyranoside,IPTG)、透析袋、ELISA包被液、TMB显色试剂盒购自北京索莱宝科技有限公司;FastRun蛋白凝胶制备试剂盒、彩色预染蛋白Marker购自上海雅酶生物医药科技有限公司;上样缓冲液购自美国Thermo公司;考马斯亮蓝染液、96孔酶标板购自上海碧云天生物技术有限公司;镍-亚氨基二乙酸(nickel-iminodiacetic acid,Ni-IDA)/镍-次氮基三乙酸(nickel-nitrilotriacetic acid,Ni-NTA)/镍-三羧甲基乙二胺(nickel-Tris carboxymethyl ethylenediamine,Ni-TED)琼脂糖填料蛋白结合/平衡缓冲液(含8 mol/L尿素)、咪唑、尿素、组氨酸标签镍离子蛋白纯化预装重力柱购自生工生物工程(上海)股份有限公司;50 mL 30000超滤管购自美国Millipore公司;重组anti-HERV-K-env抗体、HRP标记的山羊抗人IgG购自英国Abcam公司。
1.3 表达载体设计与合成
从UniProt网站(https://www.uniprot.org/)获取已公布的ENK7_HUMAN蛋白氨基酸序列(ID:P61567),使用Navopro在线工具预测蛋白跨膜区,发现该蛋白1~354氨基酸位于胞内,355~588氨基酸存在2个跨膜区,因此选择表达1~354氨基酸,将该氨基酸序列反向翻译为DNA碱基序列(1 062 bp)。用SnapGene软件(美国Dotmatics公司)设计重组质粒,选择pET32a作为载体,将目的基因env插入EcoR Ⅰ和Hind Ⅲ酶切位点之间,将重组质粒基因序列交由生工生物工程(上海)股份有限公司合成。
1.4 重组蛋白诱导与表达形式分析
将pET32a-env重组质粒转化到E.coli BL21(DE)感受态细胞中,将菌液涂布在含有氨苄青霉素的LB琼脂培养板上37 ℃过夜培养。挑取阳性单菌落接种于含有氨苄青霉素抗性的LB液体培养基中37 ℃震荡培养,取200 μL菌液送生工生物工程(上海)股份有限公司测序,测序回报结果与原序列进行BLAST比对确认相似性达到100%后进行扩菌。在培养菌液的D550=0.8时(D550为550 nm波长处的光密度值)加入1 mmol/L IPTG诱导剂,在37 ℃、2.7×g条件下诱导表达过夜。离心获得菌体沉淀,用PBS重悬、高压细胞破碎仪裂解细菌(8×107 Pa、5 min)、离心获得上清和沉淀。分别取上清和沉淀与5×上样缓冲液混合、100 ℃金属浴加热10 min后制备蛋白样品,配制12.5%的分离胶进行SDS-PAGE,电泳胶用考马斯亮蓝染色30 min、脱色液脱色过夜。
1.5 包涵体蛋白纯化
包涵体沉淀中加入8 mol/L尿素溶液吹打混匀,摇床过夜震荡后离心获得变性蛋白上清;用Ni-IDA/Ni-NTA/Ni-TED琼脂糖填料蛋白结合/平衡缓冲液(含8 mol/L尿素)为本底溶液配制20 mmol/L咪唑作为结合/洗脱缓冲液,配制200 mmol/L咪唑作为洗脱缓冲液;用2倍柱体积的结合/洗脱缓冲液平衡组氨酸标签镍离子蛋白纯化预装重力柱;蛋白溶液过柱5次,收集流穿液;2倍柱体积结合/洗脱缓冲液冲洗杂质4次,2倍柱体积洗脱缓冲液洗脱目的蛋白4次;分别收集每次的洗杂液和洗脱液。分别取样前、流穿、4次洗杂、4次洗脱溶液与5×上样缓冲液混合,100 ℃金属浴加热10 min后制备蛋白样品,配制12.5%的分离胶进行SDS-PAGE,电泳胶用考马斯亮蓝染色30 min、脱色液脱色过夜。透析袋剪成适当长度,放入透析袋处理液中,煮沸10 min,再用蒸馏水清洗。将变性的蛋白溶液装入透析袋中,将透析袋依次放入含6、4、2、0 mol/L尿素的包涵体复性缓冲液中,分别于4 ℃条件下透析12 h,用超滤管超滤浓缩复性后的蛋白溶液,并用NanoDrop紫外分光光度计检测蛋白浓度,取少量蛋白样品送上海中科新生命生物科技有限公司进行肽指纹鉴定。
1.6 间接ELISA检测方法的建立
1.6.1 反应条件
用包被液将HERV-K env蛋白梯度稀释成0.25、0.5、1、2、4、8 μg/mL,每孔100 μL包被96孔酶标板,4 ℃条件下包被过夜。收集50例在海军军医大学第一附属医院国际健康管理中心常规体检的30岁以下健康人群血生化检测剩余血液样本,均匀混合后作为阴性血清;用样本稀释液按1∶1 000比例对重组anti-HERV-K-env抗体进行倍比稀释作为阳性血清。将阳性、阴性血清分别按1∶25、1∶50、1∶100、1∶200进行倍比稀释。其余步骤按照ELISA常规检测步骤[14]进行,用正交筛选法、根据阳性/阴性比值(positive/negative,P/N)确定抗原最佳包被浓度和血清最佳稀释倍数。以5%脱脂奶粉溶液、1% BSA在37 ℃封闭不同时间(30、60、90、120 min),根据P/N确定最佳封闭条件。按照前述得到最佳包被条件、封闭条件的血清,分别在37 ℃不同时间(30、60、90 min)下孵育,根据P/N确定最佳孵育时间。以HRP标记的山羊抗人IgG分别按1∶3 000、1∶4 000、1∶5 000、1∶6 000比例稀释作为二抗,分别于37 ℃孵育不同时间(30、60、90 min),根据P/N确定最佳反应浓度和时间。
1.6.2 临界值的确定
根据1.6.1节建立的检测方法,将1.6.1节中所述的50份健康人血清样品进行ELISA检测以确定临界值,根据酶标仪读取的D450值计算平均值(X)和标准差(standard deviation,SD),根据公式X+3SD计算临界值。
1.6.3 特异性实验
通过竞争抑制实验验证检测方法的特异性。将稀释后的anti-HERV-K-env抗体分别与HERV-K env重组蛋白(抑制组)和BSA(阴性抑制组)于37 ℃预孵育1 h后进行间接ELISA检测。根据公式计算抑制率:抑制率(%)=(1-D抑制组/D未抑制组)×100%。
1.6.4 灵敏性实验
将阳性血清按1∶25、1∶50、1∶100、1∶200、1∶400、1∶800、1∶1 600、1∶3 200、1∶6 400进行倍比稀释,在最佳反应条件下进行间接ELISA检测,以确定该方法的灵敏性。
1.6.5 重复性实验
按照最佳反应条件,对2025年5月1日至5月31日在海军军医大学第一附属医院就诊的5例肺癌患者的血清进行检测,每个血清样本设置5个重复孔,进行组内重复性实验;同时采用不同批次的纯化抗原进行5次组间重复性实验,计算变异系数(coefficient of variation,CV)。
1.7 建立的间接ELISA检测方法在肺癌中的临床应用
选取2025年5月1日至5月31日在海军军医大学第一附属医院就诊的肺癌患者共128例,其中男78例(60.9%)、女50例(39.1%);年龄39~79(62.5±9.8)岁;有吸烟史77例(60.2%),无吸烟史51例(39.8%);Ⅰ~Ⅱ期共40例(31.2%),Ⅲ~Ⅳ期共88例(68.7%);腺癌76例(59.4%),鳞状细胞癌32例(25.0%),小细胞肺癌15例(11.7%),其他5例(3.9%);有远处转移61例(47.7%),无远处转移67例(52.3%)。用于ELISA检测的血清均为患者血生化检测剩余样本。
1.8 统计学处理
应用SPSS 26.0软件对数据进行分析,计量资料以 x±s表示,计数资料以例数和百分数表示。采用χ2检验和Fisher确切概率法分析血清HERV-K env抗体表达与患者年龄、性别、病理类型、病理分期等的相关性。检验水准(α)为0.05。
2 结果
2.1 重组蛋白表达载体构建与测序结果
经优化合成的HERV-K env基因片段插入pET-32a载体的EcoR Ⅰ和Hind Ⅲ酶切位点之间(图 1A),经EcoR Ⅰ和Hind Ⅲ双酶切鉴定获得的插入片段大小与预期一致(图 1B)。对重组表达质粒进行测序,提示插入序列与理论序列一致且读码框正确,表明重组质粒pET-32a-env构建成功。
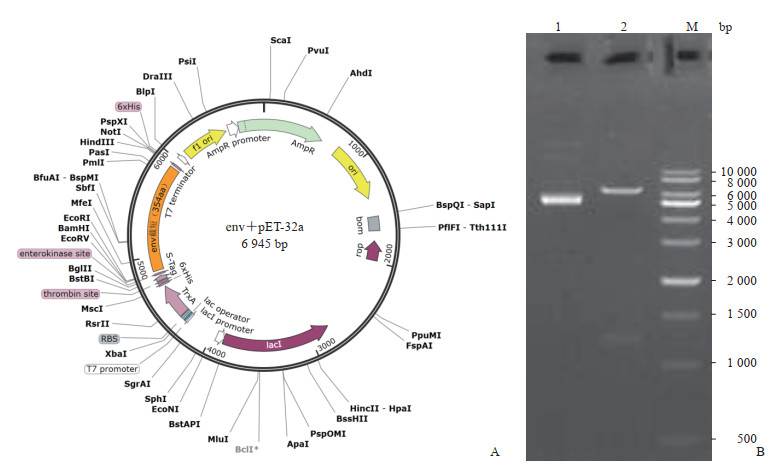 图 1 pET-32a-env重组质粒构建示意图及酶切鉴定Fig. 1 Schematic diagram of pET-32a-env recombinant plasmid construction and restriction enzyme digestion verificationA: Diagram of the pET-32a-env recombinant plasmid; B: Electrophoresis identification results. 1: pET-32a-env plasmid; 2: pET-32a-env plasmid double digestion product; M: DNA marker. env: Envelope.
图 1 pET-32a-env重组质粒构建示意图及酶切鉴定Fig. 1 Schematic diagram of pET-32a-env recombinant plasmid construction and restriction enzyme digestion verificationA: Diagram of the pET-32a-env recombinant plasmid; B: Electrophoresis identification results. 1: pET-32a-env plasmid; 2: pET-32a-env plasmid double digestion product; M: DNA marker. env: Envelope.2.2 重组蛋白诱导表达与纯化结果
用E.coli BL21(DE)原核表达系统表达pET-32a-env重组质粒,用1 mmol/L IPTG作为诱导剂,在37 ℃、2.7×g条件下诱导表达,收集菌体细胞进行高压破碎裂解,分离上清和沉淀并进行SDS-PAGE,结果证明目的蛋白在包涵体沉淀表达(图 2)。用8 mol/L尿素变性包涵体蛋白后,使用组氨酸标签镍离子蛋白纯化预装重力柱纯化env蛋白,通过SDS-PAGE鉴定洗脱的目的蛋白及其纯度,可见目的蛋白条带明显,杂带不明显,证明纯化后的蛋白纯度较高(图 2)。测得蛋白浓度为0.127 mg/mL,产量较高。蛋白样品经上海中科新生命生物科技有限公司肽指纹鉴定,结果显示蛋白氨基酸序列正确,搜库结果与Endogenous retrovirus group K member 7 Env polyprotein(UniProt ID: Q4JM60)匹配。
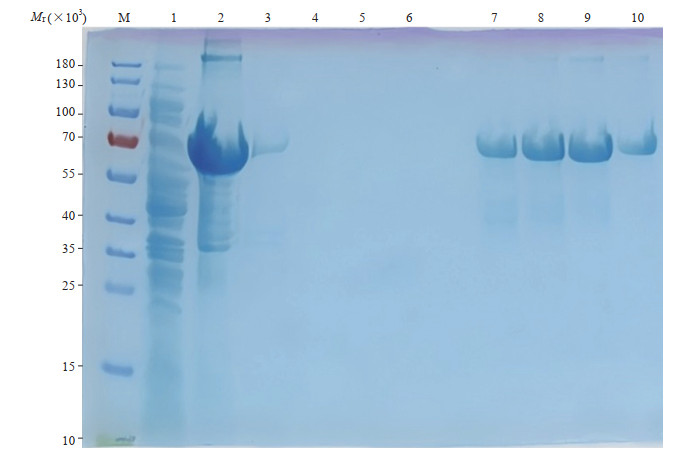 图 2 SDS-PAGE鉴定蛋白表达形式及纯化效果Fig. 2 SDS-PAGE verification of protein expression and purification efficiencyM: Protein marker; 1: Supernatant after lysis of pET-32a-env recombinant bacteria; 2: Pellet after lysis of pET-32a-env recombinant bacteria; 3-6: Wash fractions from 4 rounds of column purification of denatured inclusion body proteins; 7-10: Elution fractions from 4 rounds of column purification of denatured inclusion body proteins. SDS-PAGE: Sodium dodecylsulfate-polyacrylamide gel electrophoresis; env: Envelope.
图 2 SDS-PAGE鉴定蛋白表达形式及纯化效果Fig. 2 SDS-PAGE verification of protein expression and purification efficiencyM: Protein marker; 1: Supernatant after lysis of pET-32a-env recombinant bacteria; 2: Pellet after lysis of pET-32a-env recombinant bacteria; 3-6: Wash fractions from 4 rounds of column purification of denatured inclusion body proteins; 7-10: Elution fractions from 4 rounds of column purification of denatured inclusion body proteins. SDS-PAGE: Sodium dodecylsulfate-polyacrylamide gel electrophoresis; env: Envelope.2.3 间接ELISA检测方法的建立
2.3.1 最佳一抗稀释倍数、抗原包被量及反应条件的确定
经过正交筛选,以D450接近1、P/N最大为判定标准,确定最佳一抗稀释倍数和抗原包被量,结果显示抗原最佳包被量为4 μg/mL,一抗最佳稀释倍数为1∶100。按照同样方法确定其他最佳反应条件:抗原包被量为4 μg/mL(4 ℃/16 h)、封闭条件为5%脱脂奶粉溶液(37 ℃/120 min)、待检血清稀释倍数1∶100(37 ℃/60 min)、山羊抗人IgG稀释倍数1∶4 000(37 ℃/60 min)。
2.3.2 临界值的确定
50份健康人血清以最佳稀释倍数1∶100稀释后,经建立的间接ELISA方法检测D450的X为0.105,SD为0.032,则阴性血清的临界值为0.201,即当待检血清D450≥0.201判为阳性、<0.201则判为阴性。
2.3.3 特异性实验结果
未抑制组(阳性血清)D450为1.25,抑制组(阳性血清+env)的D450为0.28,抑制率为77.6%;阴性抑制(阳性血清+BSA)组的D450为1.22,抑制率为2.4%。抑制率>70%,表明该方法特异性合格。
2.3.4 灵敏性实验结果
血清稀释倍数D450分别为1∶25(D450 2.806)、1∶50(D450 2.414)、1∶100(D450 1.055)、1∶200(D450 0.487)、1∶400(D450 0.302)、1∶800(D450 0.221)、1∶1 600(D450 0.072)、1∶3 200(D450 0.031)、1∶6 400(D450 0.001)。当阳性血清稀释至1∶400时仍可判断为阳性,表明所建立的方法具有较高的灵敏性。
2.3.5 重复性实验结果
对5例肺癌患者血清进行检测,血清1组内平均数为1.04±0.02(CV 1.92%),组间平均数为1.03±0.03(CV 2.91%);血清2组内平均数为1.38±0.02(CV 1.45%),组间平均数为1.40±0.03(CV 2.14%);血清3组内平均数为0.76±0.01(CV 1.32%),组间平均数为0.77±0.01(CV 1.30%);血清4组内平均数为1.71±0.03(CV 1.75%),组间平均数为1.70±0.04(CV 2.35%);血清5组内平均数为1.01±0.04(CV 3.96%),组间平均数为1.03±0.02(CV 1.94%)。重复性实验结果显示,组内、组间的CV均<5%,表明该方法具有较好的重复性。
2.4 肺癌患者血清的ELISA检测与临床病理资料相关性分析
用已建立的ELISA检测方法检测128例肺癌患者的血清HERV-K env抗体表达情况,结果(表 1)发现性别、吸烟史、病理类型与患者血清HERV-K env抗体表达无相关性(均P>0.05),患者年龄、病理分期、远处转移情况与血清HERV-K env抗体表达有关(均P<0.05),其中年龄<65岁患者的血清HERV-K env抗体阳性率较年龄≥65岁患者高,病理分期Ⅲ~Ⅳ期患者的血清HERV-K env抗体阳性率较Ⅰ~Ⅱ期高,有远处转移患者的血清HERV-K env抗体阳性率较无远处转移患者高。
表 1 血清HERV-K env抗体表达与肺癌患者临床病理特征的相关性Table 1 Correlation between serum HERV-K env antibody expression and clinicopathological characteristics of lung cancer patientsn (%) Characteristic N Antibody-positive Statistic P value Age χ2=4.93 0.026 <65 years 41 27 (65.9) ≥65 years 87 39 (44.8) Gender χ2=0.42 0.518 Male 78 42 (53.8) Female 50 24 (48.0) Smoking history χ2=1.35 0.245 Yes 77 43 (55.8) No 51 23 (45.1) Pathological stage χ2=4.61 0.032 Ⅰ-Ⅱ 40 15 (37.5) Ⅲ-Ⅳ 88 51 (58.0) Pathological type Fisher’s exact test 0.863 Adenocarcinoma 76 41 (53.9) Squamous cell carcinoma 32 15 (46.9) Small cell lung cancer 15 7 (46.7) Others 5 3 (60.0) Distant metastasis χ2=13.95 <0.001 Yes 61 42 (68.9) No 67 24 (35.8) HERV-K: Human endogenous retrovirus K; env: Envelope. 3 讨论
本研究成功利用原核表达系统获得了HERV-K env蛋白,并基于此建立了检测血清HERV-K env抗体的间接ELISA方法。应用该方法对128例肺癌患者血清样本进行检测,获得了关于HERV-K env抗体与肺癌临床病理特征之间关联的重要初步发现。这些结果为理解HERV-K在肺癌中的作用机制及其作为潜在生物标志物的价值提供了新线索。
本研究发现,血清HERV-K env抗体的阳性率与患者年龄显著相关,年轻(<65岁)患者阳性率高于老年(≥65岁)患者,这一发现提示年龄因素可能对HERV-K env的免疫原性或表达水平具有调节作用。这一结果与肿瘤的发生、发展过程受宿主免疫状态和年龄相关免疫衰老影响的现象一致。在肺癌患者中,年轻患者通常表现出更为活跃的免疫系统及更强的体液免疫应答能力。随着年龄增长,免疫系统功能逐渐下降,表现为免疫衰老,包括B细胞功能减弱、抗体产生能力降低等[15],这可能部分解释了老年患者HERV-K env抗体阳性率较低的现象[16]。此外,HERV-K的表达本身可能受表观遗传调控影响,而表观遗传变化与年龄密切相关。因此,年龄可能通过影响宿主免疫应答效率及HERV元件的表观遗传沉默状态,间接调节HERV-K env抗体的检出率。本实验结果提示,在评估HERV-K相关生物标志物时,年龄是一个不可忽视的协变量,未来研究需进一步阐明年龄影响HERV-K免疫反应的具体机制及其在肺癌发生、发展中的潜在作用。
本研究发现,血清HERV-K env抗体的阳性率与肺癌的疾病进展程度相关,晚期(Ⅲ~Ⅳ期)患者阳性率高于早期(Ⅰ~Ⅱ期)患者,这一发现强烈提示HERV-K env的表达或其诱导的体液免疫反应可能随着肿瘤的进展而增强。这与许多研究中观察到的HERV-K元件,特别是HERV-K-HML-2亚家族在多种恶性肿瘤(如黑色素瘤、乳腺癌、生殖细胞肿瘤)中被异常激活[17-19]的现象一致。在肺癌中,晚期肿瘤通常表现出更高的基因组不稳定性、表观遗传失调以及更强的免疫抑制微环境[20-21],这些因素可能共同促进了原本沉默的HERV-K元件的转录和翻译,导致env蛋白的表达增加,进而诱发或增强宿主的抗体反应。本实验结果支持HERV-K的再激活是肺癌进展过程中的一个伴随事件或潜在参与者。
另外,本实验发现有远处转移的患者血清HERV-K env抗体阳性率高于无远处转移患者,这一结果进一步强化了HERV-K env与肿瘤侵袭性行为的关联。远处转移是肺癌最致命的特征,其过程涉及复杂的上皮-间质转化、血管生成、免疫逃逸等机制[22-23]。HERV-K env蛋白具有免疫抑制和促融合活性,可能通过干扰免疫监视或促进细胞间相互作用间接参与肿瘤细胞的播散与定植[24]。因此,检测到的较高抗体阳性率可能反映了转移灶中HERV-K的活跃状态,或者是对更具侵袭性原发肿瘤特征的一种体液免疫应答标志。这提示HERV-K env抗体可能作为评估肺癌转移潜能或监测转移状态的潜在血清学指标。
HERV-K的激活在多种恶性肿瘤中均有报道。研究发现,HERV-K在卵巢癌细胞中特异性表达并呈递抗原,可激发特异性T细胞杀伤肿瘤,且不损伤正常细胞,是具有潜力的卵巢癌免疫治疗新靶点[25]。另有研究发现,HERV-K在黑色素瘤中异常激活,通过表达病毒蛋白、维持干细胞特性、调控免疫微环境等多种机制促进肿瘤恶性进展,是潜力巨大的诊断标志物和治疗靶点[26]。此外,HERV在转移性透明细胞肾细胞癌中不仅是潜在的预后生物标志物,还通过调控肿瘤免疫微环境影响免疫治疗疗效,为个体化免疫治疗策略提供了新方向[27]。本研究表明,HERV-K表达水平和抗体反应可能与肺癌的进展阶段具有关联性,未来将进一步与其他癌症类型对比,以明确其在肺癌中的相对特异性。
本研究未发现血清HERV-K env抗体阳性率与患者年龄、性别、吸烟史或肺癌病理类型存在相关性。这一结果提示,HERV-K env抗体的产生可能相对特异地与肿瘤生物学行为(如进展和转移)本身相关,而非一般性风险因素或人口学特征驱动。这增加了其作为反映肿瘤内在活性标志物的特异性。跨病理亚型的潜在普适性也暗示HERV-K的激活可能在不同组织学类型的肺癌中均存在,并且其与疾病进展的关联可能具有一定程度的普遍性。未来需要在更大样本中进一步验证这一观察。本研究建立的原核表达系统获取HERV-K env蛋白并结合间接ELISA检测的策略,具有操作相对简便、成本较低、通量较高的优势,为在较大规模临床样本中筛查HERV-K env抗体状态提供了一种可行的技术路径,也为后续开展更深入的研究和潜在的临床应用奠定了基础。
本研究存在以下局限性。第一,本研究采用的包被抗原来自原核表达系统,缺乏真核细胞的翻译后修饰,可能无法完全模拟其天然构象和抗原表位[28]。这可能导致检测到的抗体谱与使用真核表达或天然蛋白时存在差异,可能影响检测的灵敏性和特异性。未来的研究可考虑使用哺乳动物细胞表达系统获取更接近天然的env蛋白进行对比。第二,本研究只开发了间接ELISA检测方法,还需要通过免疫动物筛选多克隆抗体,开发双抗夹心ELISA检测方法,用于检测血清中HERV-K env抗原,从而实现对患者血清env抗原、抗体同时检测的方法,更全面地反映患者env基因表达情况和机体的免疫应答状态。第三,本研究为横断面研究,检测的是某一时间点的抗体水平,无法确定抗体阳性是出现在肿瘤进展之前还是之后。因此需要开展前瞻性队列研究,阐明HERV-K env抗体产生与肿瘤进展的时间顺序及因果关系。此外,本研究的样本量(128例)有限,特别是进行亚组分析时统计效力可能不足,未来需扩大样本量以验证和细化当前发现。第四,本研究主要聚焦于肺癌患者内部的比较,虽然发现了与疾病进展的关联,但未设立健康人群或其他肺部良性疾病(如肺炎、肺结核、慢性阻塞性肺疾病)患者的对照组,因此无法评估HERV-K env抗体作为肺癌诊断标志物的特异性。将其与良性病变区分是未来验证的关键步骤。未来我们将开展前瞻性队列研究,纳入健康对照和肺部良性疾病患者,进一步评估HERV-K env抗体在肺癌早期诊断中的灵敏性和特异性,验证其临床适用性。此外,后续研究将收集患者的随访数据进行总生存期和无进展生存期分析,进一步验证HERV-K env抗体的独立预后价值。
综上所述,本研究利用原核表达的HERV-K env蛋白成功建立了间接ELISA检测方法,并在肺癌患者人群中揭示了血清HERV-K env抗体与疾病分期和远处转移状态呈正相关,而与年龄、性别、吸烟史和病理类型无关。这些发现强烈支持HERV-K的再激活与肺癌的恶性进展,尤其是转移过程存在密切联系。HERV-K env抗体有潜力成为一种反映肺癌侵袭和预后的新型血清学生物标志物。
-
图 1 pET-32a-env重组质粒构建示意图及酶切鉴定
Fig. 1 Schematic diagram of pET-32a-env recombinant plasmid construction and restriction enzyme digestion verification
A: Diagram of the pET-32a-env recombinant plasmid; B: Electrophoresis identification results. 1: pET-32a-env plasmid; 2: pET-32a-env plasmid double digestion product; M: DNA marker. env: Envelope.
图 2 SDS-PAGE鉴定蛋白表达形式及纯化效果
Fig. 2 SDS-PAGE verification of protein expression and purification efficiency
M: Protein marker; 1: Supernatant after lysis of pET-32a-env recombinant bacteria; 2: Pellet after lysis of pET-32a-env recombinant bacteria; 3-6: Wash fractions from 4 rounds of column purification of denatured inclusion body proteins; 7-10: Elution fractions from 4 rounds of column purification of denatured inclusion body proteins. SDS-PAGE: Sodium dodecylsulfate-polyacrylamide gel electrophoresis; env: Envelope.
表 1 血清HERV-K env抗体表达与肺癌患者临床病理特征的相关性
Table 1 Correlation between serum HERV-K env antibody expression and clinicopathological characteristics of lung cancer patients
n (%) Characteristic N Antibody-positive Statistic P value Age χ2=4.93 0.026 <65 years 41 27 (65.9) ≥65 years 87 39 (44.8) Gender χ2=0.42 0.518 Male 78 42 (53.8) Female 50 24 (48.0) Smoking history χ2=1.35 0.245 Yes 77 43 (55.8) No 51 23 (45.1) Pathological stage χ2=4.61 0.032 Ⅰ-Ⅱ 40 15 (37.5) Ⅲ-Ⅳ 88 51 (58.0) Pathological type Fisher’s exact test 0.863 Adenocarcinoma 76 41 (53.9) Squamous cell carcinoma 32 15 (46.9) Small cell lung cancer 15 7 (46.7) Others 5 3 (60.0) Distant metastasis χ2=13.95 <0.001 Yes 61 42 (68.9) No 67 24 (35.8) HERV-K: Human endogenous retrovirus K; env: Envelope. -
[1] MCPHERSON J D, MARRA M, HILLIER L, et al. A physical map of the human genome[J]. Nature, 2001, 409(6822): 934-941. DOI: 10.1038/35057157. [2] LIU X, LIU Z, WU Z, et al. Resurrection of endogenous retroviruses during aging reinforces senescence[J]. Cell, 2023, 186(2): 287-304.e26. DOI: 10.1016/j.cell.2022.12.017. [3] VIOT J, LOYON R, ADIB N, et al. Deciphering human endogenous retrovirus expression in colorectal cancers: exploratory analysis regarding prognostic value in liver metastases[J]. EBioMedicine, 2025, 116: 105727. DOI: 10.1016/j.ebiom.2025.105727. [4] JIA L, SONG Y, CHEN M, et al. Editorial: the evolution, characterization, and role of human endogenous retroviruses in health and diseases[J]. Front Cell Infect Microbiol, 2024, 14: 1449864. DOI: 10.3389/fcimb.2024.1449864. [5] RUSS E, IORDANSKIY S. Endogenous retroviruses as modulators of innate immunity[J]. Pathogens, 2023, 12(2): 162. DOI: 10.3390/pathogens12020162. [6] BARISIC S, BRAHMBHATT E M, CHERKASOVA E, et al. Regression of renal cell carcinoma by T cell receptor- engineered T cells targeting a human endogenous retrovirus[J]. J Immunother Cancer, 2024, 12(9): e009147. DOI: 10.1136/jitc-2024-009147. [7] BHARDWAJ N, MONTESION M, ROY F, et al. Differential expression of HERV-K (HML-2) proviruses in cells and virions of the teratocarcinoma cell line Tera-1[J]. Viruses, 2015, 7(3): 939-968. DOI: 10.3390/v7030939. [8] DAI L, DEL VALLE L, MILEY W, et al. Correction: Transactivation of human endogenous retrovirus K (HERV-K) by KSHV promotes Kaposi's sarcoma development[J]. Oncogene, 2024, 43: 2372. DOI: 10.1038/s41388-024-03083-4. [9] MAVRAGANI C P, KIROU K A, NEZOS A, et al. Expression of APOBEC family members as regulators of endogenous retroelements and malignant transformation in systemic autoimmunity[J]. Clin Immunol, 2021, 223: 108649. DOI: 10.1016/j.clim.2020.108649. [10] EVANS E F, SARAPH A, TOKUYAMA M. Transactivation of human endogenous retroviruses by viruses[J]. Viruses, 2024, 16(11): 1649. DOI: 10.3390/v16111649. [11] ETTINGER D S, WOOD D E, AGGARWAL C, et al. NCCN guidelines insights: non-small cell lung cancer, version 1.2020[J]. J Natl Compr Canc Netw, 2019, 17(12): 1464-1472. DOI: 10.6004/jnccn.2019.0059. [12] NICHOLAS BODOR J, BOUMBER Y, BORGHAEI H. Biomarkers for immune checkpoint inhibition in non-small cell lung cancer (NSCLC)[J]. Cancer, 2020, 126(2): 260-270. DOI: 10.1002/cncr.32468. [13] HONRUBIA-PERIS B, GARDE-NOGUERA J, GARCÍA-SÁNCHEZ J, et al. Soluble biomarkers with prognostic and predictive value in advanced non-small cell lung cancer treated with immunotherapy[J]. Cancers, 2021, 13(17): 4280. DOI: 10.3390/cancers13174280. [14] OSTUNI A, FRONTOSO R, CRUDELE M A, et al. Comparative evaluation of a multistrain indirect ELISA targeting anti- p26 and gp45 antibodies for EIAV detection[J]. Pathogens, 2025, 14(6): 575. DOI: 10.3390/pathogens14060575. [15] MANTOVANI F, KITSOU K, MAGIORKINIS G. HERVs: expression control mechanisms and interactions in diseases and human immunodeficiency virus infection[J]. Genes, 2024, 15(2): 192. DOI: 10.3390/genes15020192. [16] ZHOU H, ZHENG Z, FAN C, et al. Mechanisms and strategies of immunosenescence effects on non-small cell lung cancer (NSCLC) treatment: a comprehensive analysis and future directions[J]. Semin Cancer Biol, 2025, 109: 44-66. DOI: 10.1016/j.semcancer.2025.01.001. [17] HUANG G, LI Z, WAN X, et al. Human endogenous retroviral K element encodes fusogenic activity in melanoma cells[J]. J Carcinog, 2013, 12: 5. DOI: 10.4103/1477-3163.109032. [18] JOHANNING G L, MALOUF G G, ZHENG X, et al. Expression of human endogenous retrovirus-K is strongly associated with the basal-like breast cancer phenotype[J]. Sci Rep, 2017, 7: 41960. DOI: 10.1038/srep41960. [19] NGUYEN Q T T, SHIN S G, NGUYEN T T T, et al. Human endogenous retrovirus-K envelope protein is aberrantly expressed in serous ovarian cancer and promotes chemosensitivity via NF-κB/P-glycoprotein pathway inhibition[J]. J Ovarian Res, 2025, 18(1): 146. DOI: 10.1186/s13048-025-01722-2. [20] JIN X, WUYUN T, ZHANG Y, et al. Overcoming acquired immunotherapy resistance in non-small cell lung cancer using ginsenoside Rb1-loaded, peptide-enhanced exosome delivery systems[J]. J Nanobiotechnology, 2025, 23(1): 443. DOI: 10.1186/s12951-025-03456-1. [21] CHE M, WEI W, YANG X, et al. Radiation-induced upregulation of itaconate in macrophages promotes the radioresistance of non-small cell lung cancer by stabilizing NRF2 protein and suppressing immune response[J]. Redox Biol, 2025, 85: 103711. DOI: 10.1016/j.redox.2025.103711. [22] SHI Z, ZENG H, ZHAO B, et al. Sulforaphane reverses the enhanced NSCLC metastasis by regulating the miR-7-5p/c-Myc/LDHA axis in the acidic tumor microenvironment[J]. Phytomedicine, 2024, 133: 155874. DOI: 10.1016/j.phymed.2024.155874. [23] LIU Y, CHUDGAR N, MASTROGIACOMO B, et al. A germline SNP in BRMS1 predisposes patients with lung adenocarcinoma to metastasis and can be ameliorated by targeting c-fos[J]. Sci Transl Med, 2022, 14(665): eabo1050. DOI: 10.1126/scitranslmed.abo1050. [24] KAPLAN M H, CONTRERAS-GALINDO R, JIAGGE E, et al. Is the HERV-K HML-2 Xq21.33, an endogenous retrovirus mutated by gene conversion of chromosome X in a subset of African populations, associated with human breast cancer?[J]. Infect Agent Cancer, 2020, 15: 19. DOI: 10.1186/s13027-020-00284-w. [25] BONAVENTURA P, PAGE A, TABONE O, et al. HERV-derived epitopes represent new targets for T-cell-based immunotherapies in ovarian cancer[J]. J Immunother Cancer, 2025, 13(8): e010099. DOI: 10.1136/jitc-2024-010099. [26] LIN Y, SATTA R R, SIMULA E R, et al. The role of human endogenous retroviruses in the initiation and progression of melanoma[J]. Biomedicines, 2025, 13(7): 1662. DOI: 10.3390/biomedicines13071662. [27] LU X, VANO Y A, SU X, et al. Stratification system with dual human endogenous retroviruses for predicting immunotherapy efficacy in metastatic clear-cell renal cell carcinoma[J]. J Immunother Cancer, 2025, 13(1): e010386. DOI: 10.1136/jitc-2024-010386. [28] LI F, GE H, LIN P, et al. Genome-based screening and immunogenicity evaluation of outer membrane protein antigens for Vibrio harveyi subunit vaccine in pearl gentian grouper (Epinephelus lanceolatus×Epinephelus fuscoguttatus)[J]. Fish Shellfish Immunol, 2025, 165: 110440. DOI: 10.1016/j.fsi.2025.110440.

 下载:
下载:
