工业革命以来,由人类活动排放到大气中的CO2温室气体逐年增加,引起一系列严重的环境问题(王广华等,2013),得到世界各国的关注(Holloway,2001; IPCC,2007)。在经过合理的选址论证后,将CO2集中注入到地面以下800 m(CO2以超临界态存在)的封闭地质构造中(CO2地质储存),被认为是减少向大气中排放CO2的最直接有效的技术之一(Bachu,2003; IPCC,2005)。沉积盆地深部咸水层以其独特的优点,常被国际上公认为适宜CO2地质储存的理想的储存场所(Bachu,2003; IPCC,2005; 李小春等,2006; 杨潇瀛,2012; 郭建强等,2014)。世界上首个深部咸水层封存CO2示范工程是1996年开工的挪威北海Sleipner工程,该工程区的概念模型结果揭示了CO2的储存机理。2010年6月,中国建成亚洲规模最大的深部咸水层封存CO2的示范工程。此外,美国、加拿大、澳大利亚、日本、韩国等示范工程建设也比较成熟。基于示范工程获取的实际资料进行的理论研究表明,CO2在深部咸水层中的储存主要涉及构造圈闭、溶解捕获、矿物捕获3种机理(孙枢,2006; Saadatpoor et al.,2010; 郭建强等,2014; 莫绍星等,2014)。其中,矿物捕获可以将CO2长久的封存在岩石圈中,具有较高的安全性(Liu et al.,2011; 范基姣等,2013; 李兰兰等,2013)。
目前,在矿物封存方面已有大量研究。Gulf Coast模型,模拟分析了方解石、白云石和片钠铝石等矿物的固碳作用(Xu et al., 2003,2004,2005)。此外,矿物的溶解与CO2封存量也有关系(Dalkhaa et al.,2013),并得到De Silva等(2015)的验证,表明地层的初始矿物组分是影响矿物封存的一个重要因子。不同深部咸水层的初始矿物组分,导致CO2矿物储存形式以及储存量发生较为复杂的改变,很大程度上影响到矿物储存的安全性(于炳松和赖兴运,2006; 万玉玉,2012; 岳高凡,2014; 杨志杰等,2014)。因此,针对指定的研究区域开展地质储集层初始矿物组分变化对矿物储存量的影响是十分必要的。
目前,中国已经在蒙陕交界地带的鄂尔多斯盆地开展了CGS示范工程研究。前期的地质探测结果表明深部咸水含水层中的刘家沟组砂岩地层具备良好的岩性条件,是CO2地质储存的有利层位。本文以刘家沟组为研究对象,利用数值模拟的方法探究不同初始矿物组分条件下CO2矿物封存量的变化规律,以期为CO2地质储存工程的储集层优选、储存能力评估、储盖层合理划分等实施过程提供有价值的参考。
1 模型建立 1.1 程序概述本次模拟使用非等温-多相流体反应运移模拟程序TOUGHREACT V2.0,该程序在TOUGH2的框架上扩展了地球化学反应运移方面的功能(Pruess et al.,2012),由美国劳伦斯伯克利国家重点实验室开发。求解方法为隐式时间加权法; 水流、溶质迁移与化学反应模块之间用顺序迭代法耦合。适用于一维、二维以及三维问题求解,考虑了水溶液中气体溶解与脱气过程等化学反应、矿物的溶解沉淀等局部平衡反应和动力学过程(Xu et al.,2011)等。该程序现已被广泛应用于如CO2地质储存、地热资源开发等多个领域的工作中,并取得了令人满意的成果(Pruess et al.,2012)。
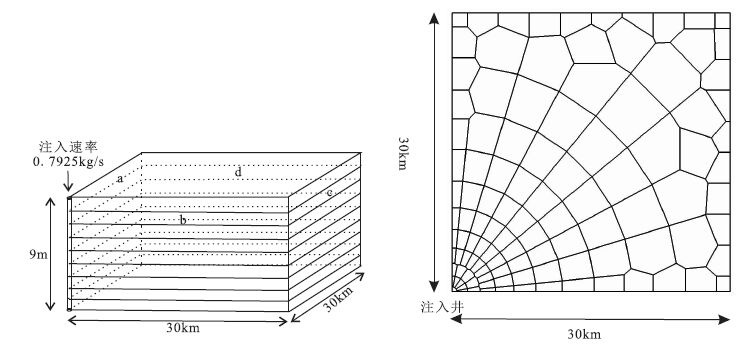
1.2 模型设置 1.2.1 概念模型及边界条件本文研究目标储集层为顶板埋深1690 m、底板埋深1699 m的刘家沟组含水层。根据该层的实测数据,建立了以注入井为角点的三维物理模型(图 1a),模型的长、宽和厚度分别为30 km、30 km和9 m。
|
(a)砂层简化概念模型图;(b)平面剖分图 图 1 CO2注入砂层简化概念模型图及平面剖分图 Figure 1 Simplified conceptual model for the CO2 injecting into sandstone reservoirs and its section |
如 图 1b所示,本次模拟在平面上将储集层概化为30 km×30 km的矩形区域,进行不规则网格剖分,剖分为111个网格; 垂向为9 m,均匀剖分为9层,每层1 m。
如 图 1a所示,本次研究仅针对储集层内CO2矿物封存量的转化,不考虑上覆盖层问题,因此,将模型顶、底部设为非渗透性边界; 研究对象为实际注入区右上1/4区域,研究区域边界a 、 b与其他区域相邻,由于模型为均质各向同性的地层,具有很好的对称性,边界两侧储集层压力相等,压差为零,边界上没有水流通过,因此,将模型边界a 、 b设为零流量边界; 为了避免边界对模拟结果的影响,径向边界距离设为30 km,并将此边界(c、d)设为具有固定压力和温度的一类边界。
1.2.2 储存物性参数设置本次模拟主要为了讨论CO2矿物储存形式以及改变矿物初始体积分数对矿物封存量的影响趋势,不做定量分析,因此将储集层概化为均质各向同性、无限延伸的砂岩地层。结合鄂尔多斯盆地实测资料,得到储集层物性参数(表 1); 模拟采用的液相和气相(超临界)相对渗透率计算模型及毛细管力计算模型由文献获得(Xu et al.,2004)。参数设置如 表 1所示。
|
|
表 1 储集层岩石物性参数 Table 1 Physical property parameters of rocks of the reservoir |
模型所采用的储集层初始矿物组分根据岩石露头样品的XRD测试资料得到,如 表 2所示。
|
|
表 2 矿物初始体积分数 Table 2 The initial volume fraction of minerals |
天然情况下,地下水系统中水岩相互反应已达到平衡状态。但是实际所得水样在离开原位环境以后发生变化,导致某些矿物不再平衡,因此模拟之前需要确定初始水成分。模拟中初始水的获得方法采用目前文献中比较通用的一种方式,将地层所获取水样的实际盐度转化为相应浓度的NaCl溶液,再将NaCl溶液与地层初始矿物相互反应,将与地层矿物达到平衡的地下水作为模拟的初始水成分(表 3)。
|
|
表 3 储集层初始水化学组分浓度 Table 3 Chemical compositions of the initial water of the reservoir |
根据工程资料,垂向9层均设计CO2注入孔。注入速率为0.7925 kg/s,注入时间为20 a,总注入量为50×104 t,模拟时间为1000 a。
2 模拟结果与讨论将鄂尔多斯盆地刘家沟组地层作为基础方案。为了更清楚的查明CO2在垂向和侧向上的运移规律,在三维模型的X-Z方向做切片,进行相关分析。
CO2以超临界状态被注入储集层,形成CO2高浓度区、CO2-水两相混合区和纯水区。并发生反应:
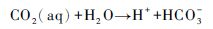
|
导致地层水的pH值降低,原有的平衡被破坏,出现矿物的溶解和沉淀。由于CO2-水两相混合区pH值较低,且存在丰富的溶解有CO2的水溶液,因此矿物溶解沉淀主要发生在两相混合区。
2.1 溶解矿物CO2的溶解使地层水的pH值迅速降低,方解石、奥长石、钾长石和绿泥石发生溶解反应:
CaCO3(方解石)+H+→Ca2++HCO3-
CaNa4Al6Si14O40(奥长石)+34H2O+6H+→4Na++Ca2++6Al(OH)3+14H4SiO4
2KAlSi3O8(钾长石)+8H+→2Al3++6SiO2+2K++4H2O
2Mg2.5Fe2.5Al2Si3O10(OH)8(绿泥石)+20H+→5Mg2++5Fe2++4Al(OH)3+6H4SiO4
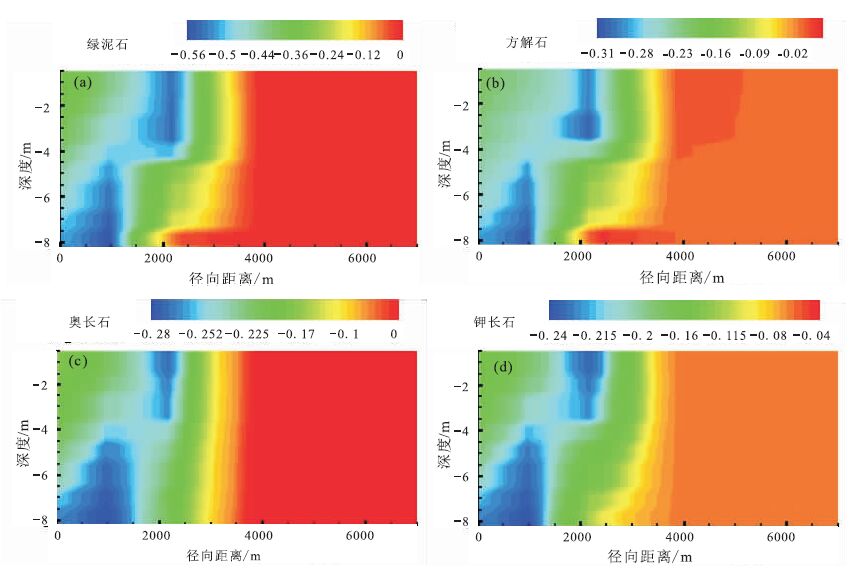
1000年时,矿物达到最大溶解范围约为2500 m。此时,绿泥石最大溶解掉0.5%(图 2a); 方解石溶解掉0.3%(图 2b); 长石类矿物均溶解掉0.25%(图 2c,2d)。
|
负号表示溶解,正号表示沉淀; 图例单位为%,表示矿物体积分数的变化量 图 2 1000 a时溶解矿物体积分数变化 Figure 2 The variation of volume fractions of dissolved minerals after 1000 a |
随着绿泥石、方解石和长石类矿物的溶解,含水层中的Mg2+、Na+、Ca2+等离子浓度改变,发生沉淀反应:
20HCO3-+10Ca2++3Mg2++7Fe2+→10CaMg0.3Fe0.7(CO3)2(铁白云石)+20H+
2.3K++2.3Al3++6.9H4SiO4+0.25Mg2++H++H2O→K0.6Mg0.25Al1.8(Al0.5Si3.5O10)(OH)2(伊利石)+1.7K++3.4SiO2(aq)
0.26Mg2++0.29Na++1.77Al(OH)3+3.97H4SiO4→Na0.29Mg0.26Al1.77Si3.97O10(OH)2(钠蒙脱石)+0.81H++9.19H2O
0.26Mg2++0.145Ca2++1.77Al(OH)3+3.97H4SiO4→Ca0.145Mg0.26Al1.77Si3.97O10(OH)2(钙蒙脱石)+0.81H++9.19H2O
HCO3-+Mg2+→MgCO3(菱镁矿)+H+
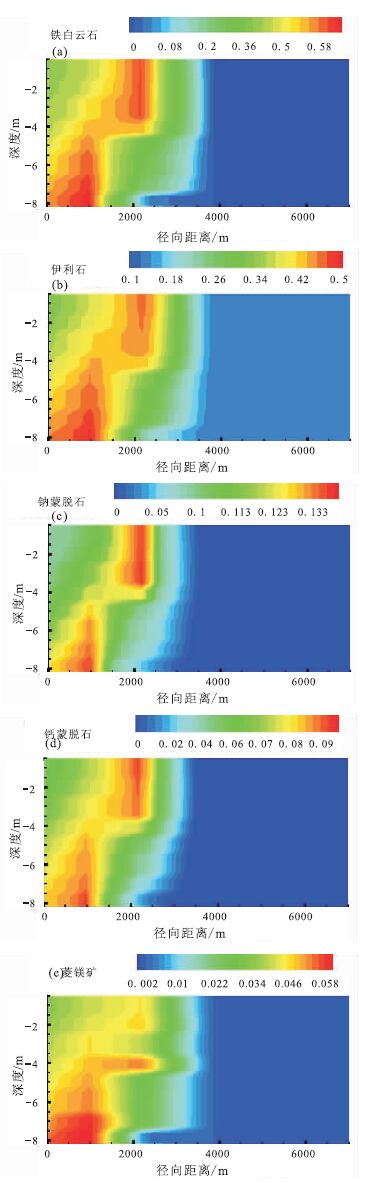
1000年时,矿物达到沉淀的最大范围约2500 m。此时,铁白云石最大沉淀0.6%(图 3a); 伊利石最大沉淀0.5%(图 3b); 钠蒙脱石最大沉淀0.12%(图 3c),钙蒙脱石最大沉淀0.09%(图 3d); 菱镁矿最大沉淀0.06%(图 3e)。其中,铁白云石是最主要的固碳矿物。
|
负号表示溶解,正号表示沉淀; 图例单位为%,表示矿物体积分数的变化量 图 3 1000年时主要沉淀矿物体积分数变化 Figure 3 The variation of volume fractions of precipitated minerals after 1000 years |
根据基础方案的结果,以刘家沟组岩石露头样品的测试数据作为矿物体积含量变化范围的依据,改变奥长石、钾长石、方解石、绿泥石4种溶解矿物的初始体积分数(表 4)进行数值模拟,来分析矿物初始含量对CO2矿物储存量的影响。
|
|
表 4 参数敏感性分析模拟方案 Table 4 Simulation program for analyzing sensibilities of parameters |
石英在酸性环境中性质较为稳定,故其他矿物体积分数变化时,均通过改变石英体积含量来平衡总矿物的体积分数。同时,为了更好的分析矿物转化过程及最终形式,选取了位于集中发生矿物溶解沉淀区域的网格11T 5(网格坐标: X=960.9,Y=398.0,Z=-4.5)进行监测。
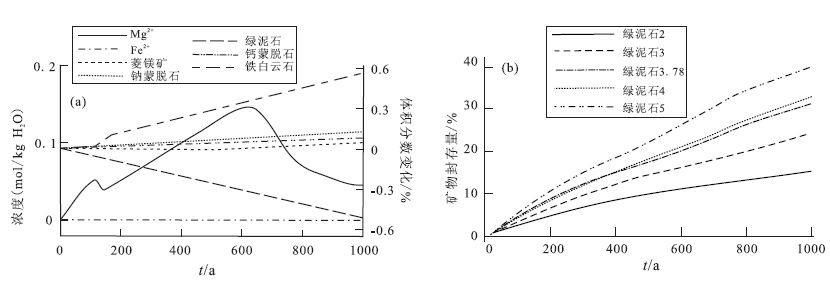
3.1 绿泥石初始含量对CO2矿物储存量的影响由 图 4a,CO2注入初期,钙、钠蒙脱石沉淀消耗的Mg2+小于绿泥石溶解产生的Mg2+,所以绿泥石溶解使地层水中Mg2+含量呈增加趋势。150年,铁白云石开始沉淀,消耗Mg2+,因此150~200年Mg2+浓度减少。200年后,铁白云石沉淀速率较之前减小,而绿泥石溶解速率未发生变化,因此地层水中Mg2+浓度又不断增加。到600年时,菱镁矿也开始发生沉淀,与铁白云石共同消耗Mg2+,使得Mg2+浓度开始下降。而绿泥石溶解产生的Fe2+基本全部提供给铁白云石,Fe2+是控制铁白云石沉淀的关键离子,因此在绿泥石溶解和铁白云石沉淀的平衡下,地层水中Fe2+浓度保持稳定。
|
(a)Mg2+、Fe2+及相关矿物随时间变化图;(b)绿泥石对矿物储存量的影响 图 4 离子、矿物及矿物储存量随时间变化图 Figure 4 The variations of ions,minerals and mineral sequestration over time |
铁白云石是固定CO2的重要矿物,而铁白云石沉淀需要的Fe2+受控于绿泥石溶解,由 图 4b可以看出,绿泥石的初始体积分数与固碳矿物的含量明显呈正相关关系。随着绿泥石初始体积分数的增加,CO2地质储存量也相应增大。
3.2 其他矿物对CO2矿物储存的影响分析结果表明,另外3种矿物初始含量变化对结果影响不显著,因此将方解石、钾长石和奥长石初始含量变化造成的影响放在一起讨论。
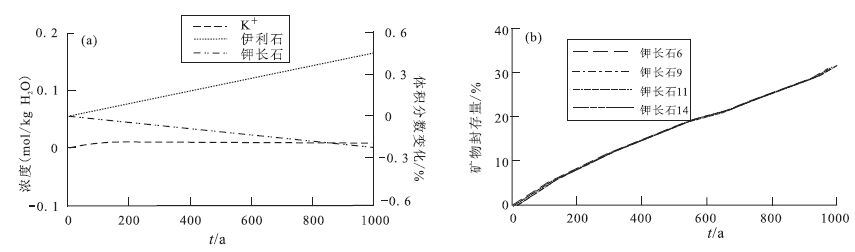
钾长石在酸性条件下发生溶解,产生K+。由 图 5a,钾长石的溶解和伊利石的沉淀同时进行,结合质量关系可以得到钾长石基本完全转化为伊利石的结论。因此,钾长石溶解产生K+,同时被伊利石沉淀消耗,K+浓度不会出现大范围的增加或减少,在地层水中比较稳定,结合 图 5b可以看到,钾长石基本不具备矿物捕获CO2的能力,改变钾长石初始体积,对CO2矿物捕获基本没有影响。
|
(a)K+及相关矿物随时间变化图;(b)钾长石对矿物储存量的影响 图 5 离子、矿物及矿物储存量随时间变化图 Figure 5 The variations of ions,minerals and mineral sequestration over time |
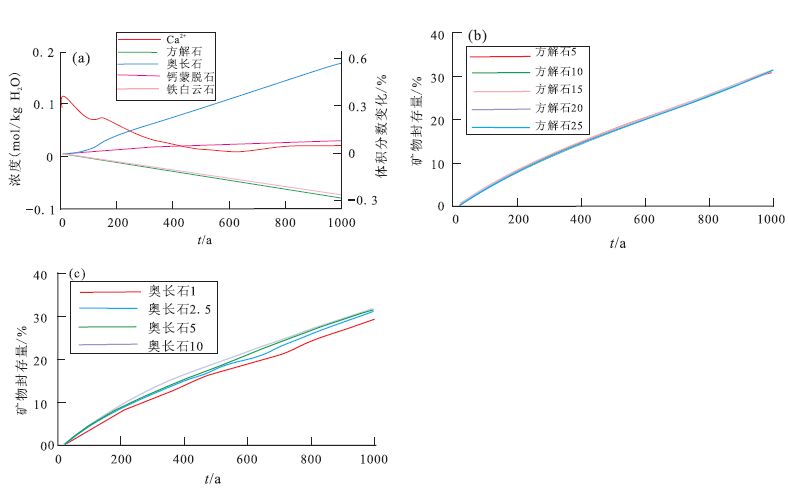
由 图 6a,注入CO2后,奥长石在酸性条件下首先发生溶解,产生的Ca2+提供给钙蒙脱石沉淀,此时地层水中Ca2+浓度减小; 随着CO2溶解反应的进行,地层水的pH值大幅减小,150年左右方解石开始溶解,初期溶解速率较大,导致150~200年间,Ca2+浓度稍有上升,此后,随着方解石和奥长石溶解逐渐稳定,铁白云石和钙蒙脱石也持续的消耗Ca2+,Ca2+浓度一直减小。
|
(a)Ca2+及相关矿物随时间变化图;(b)方解石对矿物储存量的影响;(c)奥长石对矿物储存量的影响 图 6 离子、矿物及矿物储存量随时间变化图 Figure 6 The variations of ions,minerals and mineral sequestration over time |
方解石本身作为一种含碳矿物,溶解后为铁白云沉淀提供Ca2+,以铁白云石的形式继续固定CO2,所以整体上固碳矿物的总量变化极小,只是固碳的矿物发生了变化。根据 图 6b可以看到,改变方解石的初始含量,对CO2矿物封存量影响极小。而铁白云石沉淀需要的Ca2+,不仅由奥长石提供,还可由其他矿物或者地层水中丰富的Ca2+提供,因此改变奥长石初始体积分数只在一定程度上对矿物封存量有影响(图 6c),效果并不显著。
4 结论(1) CO2注入储集层后发生复杂的水-岩-气的相互作用,导致各类矿物的溶解和沉淀。发生溶解的矿物主要是有长石类、方解石和绿泥石,发生沉淀的是钙钠蒙脱石、铁白云石和伊利石等; 其中固定CO2的矿物主要是铁白云石。
(2) 方解石和钾长石的初始含量变化对CO2矿物储存量影响极小; 随着奥长石含量的增加,矿物储存量在一定程度上逐渐增加; 而绿泥石初始含量变化显著影响矿物封存量,随着绿泥石初始体积分数的增加,矿物封存量显著增加。
(3) 含绿泥石和长石较多的地层具有较大的矿物封存CO2的潜力。因此,在进行CO2地质储存场地选取和储集层划分时应优先考虑绿泥石和奥长石含量较高的区域和层位。
| [1] | Bachu S. 2003. Screening and ranking of sedimentary basins for sequestration of CO2 in geological media in response to climate change. Environmental Geology , 44 (3) : 277–289. DOI:10.1007/s00254-003-0762-9 |
| [2] | Dalkhaa C, Shevalier M, Nightingale M, Mayer B. 2013. 2-D reactive transport modeling of the fate of CO2 injected into a saline aquifer in the Wabamun Lake Area, Alberta, Canada. Applied Geochemistry , 38 : 10–23. DOI:10.1016/j.apgeochem.2013.08.003 |
| [3] | De Silva G P D, Ranjith P G, Perera M S A. 2015. Geochemical aspects of CO2 sequestration in deep saline aquifers:A review. Fuel , 155 : 128–143. DOI:10.1016/j.fuel.2015.03.045 |
| [4] | Holloway S. 2001. Storage of fossil fuel-derived carbon dioxide beneath the surface of the Earth. Annual Review of Energy and the Environment , 26 (1) : 145–166. DOI:10.1146/annurev.energy.26.1.145 |
| [5] | IPCC. 2005. Carbon dioxide capture and storage. Geneva, Switzerland:IPCC |
| [6] | IPCC. 2007. Climate change 2007:The physical science basis. Summary for policy makers. IPCC Working Group 1 Fourth assessment report. Geneva, Switzerland:IPCC |
| [7] | Liu N, Liu L, Qu X Y, Yang H D, Wang L J, Zhao S. 2011. Genesis of authigene carbonate minerals in the Upper Cretaceous reservoir, Honggang Anticline, Songliao Basin:A natural analog for mineral trapping of natural CO2 storage. Sedimentary Geology , 237 (3-4) : 166–178. DOI:10.1016/j.sedgeo.2011.02.012 |
| [8] | Pruess K, Oldenburg C, Moridis G. 2012. TOUGH2 user's guide version2.0. Berkeley:Earth Science Division, Lawrence Berkeley National Laboratory. University of California . |
| [9] | Saadatpoor E, Bryant S L, Sepehrnoori K. 2010. New trapping mechanism in carbon sequestration. Transport in Porous Media , 82 (1) : 3–17. DOI:10.1007/s11242-009-9446-6 |
| [10] | Xu T F, Apps J A, Pruess K. 2003. Reactive geochemical transport simulation to study mineral trapping for CO2 disposal in deep arenaceous formations. Journal of Geophysical Research , 108 (B2) . DOI:10.1029/2002JB001979 |
| [11] | Xu T F, Apps J A, Pruess K. 2004. Numerical simulation of CO2 disposal by mineral trapping in deep aquifers. Applied Geochemistry , 19 (6) : 917–936. DOI:10.1016/j.apgeochem.2003.11.003 |
| [12] | Xu T F, Apps J A, Pruess K. 2005. Mineral sequestration of carbon dioxide in a sandstone-shale system. Chemical Geology , 217 (3-4) : 295–318. DOI:10.1016/j.chemgeo.2004.12.015 |
| [13] | Xu T F, Spycher N, Sonnenthal E L, Zhang G X, Zheng L G, Pruess K. 2011. TOUGHREACT Version 2. 0:A simulator for subsurface reactive transport under non-isothermal multiphase flow conditions. Computers & Geosciences , 37 (6) : 763–774. |
| [14] | 范基姣, 张森琦, 郭建强, 马致远, 李旭峰, 张徽. 2013. 水环境同位素技术在二氧化碳地质储存中的应用探讨. 水文地质工程地质 , 40 (1) : 106–109. |
| [15] | 郭建强, 文冬光, 张森琦, 许天福. 2014. 中国二氧化碳地质储存适宜性评价与示范工程. 北京: 地质出版社: 13 -19. |
| [16] | 李兰兰, 叶坤, 郭会荣, 吕万军, 卢波. 2013. 矿物封存二氧化碳实验研究进展. 资源与产业 , 15 (2) : 117–123. |
| [17] | 李小春, 刘延锋, 白冰, 方志明. 2006. 中国深部咸水含水层CO2储存优先区域选择. 岩石力学与工程学报 , 25 (5) : 963–968. |
| [18] | 莫绍星, 龙星皎, 李瀛, 郑菲, 施小清, 张可霓, 赵良. 2014. 基于TOUGHREACT-MP的苏北盆地盐城组咸水层CO2矿物封存数值模拟. 吉林大学学报(地球科学版) , 44 (5) : 1647–1658. |
| [19] | 孙枢. 2006. CO2地下封存的地质学问题及其对减缓气候变化的意义. 中国基础科学 , 8 (3) : 17–22. |
| [20] | 万玉玉. 2012. 鄂尔多斯盆地石千峰组咸水层CO2地质储存中CO2的迁移转化特征. 博士学位论文. 长春:吉林大学 http://cdmd.cnki.com.cn/Article/CDMD-10183-1012355019.htm |
| [21] | 王广华, 张静, 张凤君, 陶怡, 杨潇瀛, 王怀远. 2013. 砂岩储集层中CO2-地层水-岩石的相互作用. 中南大学学报(自然科学版) , 44 (3) : 1167–1173. |
| [22] | 杨潇瀛. 2012. CO2流体对储集层砂岩地质改造作用的实验研究. 硕士学位论文. 长春:吉林大学 http://cdmd.cnki.com.cn/Article/CDMD-10183-1012370385.htm |
| [23] | 杨志杰, 王福刚, 杨冰, 田海龙, 许天福. 2014. 砂岩中绿泥石含量对CO2矿物封存影响的模拟研究. 矿物岩石地球化学通报 , 33 (2) : 201–207. |
| [24] | 于炳松, 赖兴运. 2006. 成岩作用中的地下水碳酸体系与方解石溶解度. 沉积学报 , 24 (5) : 627–635. |
| [25] | 岳高凡. 2014. 典型二氧化碳地质储集层中二氧化碳不同形式储存量转化预测. 硕士学位论文. 长春:吉林大学 |
 2016, Vol. 35
2016, Vol. 35



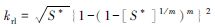 S*=(Sl-Slr)/(1-Slr)
S*=(Sl-Slr)/(1-Slr)