目前已经有300多种人乳头瘤病毒(human papillomavirus,HPV)被鉴定[1]。HPV可分为α属、β属等。其中,α属HPV也被称为黏膜HPV,主要感染生殖器和黏膜,导致良性皮肤疣和其他疾病;β属HPV主要侵染部位是皮肤[2]。HPV23是最常见的β属HPV,其基因组是由7.3 kb的环状双链DNA组成[3]。HPV主要衣壳蛋白L1是可自组装的病毒样颗粒(VLPs)[4],具有类似天然病毒的血凝活性,是预防性疫苗研究的主要靶点[5]。研究发现,HPV23与皮肤鳞状细胞癌、非黑色素瘤皮肤癌、眼汗管瘤、乳腺癌、基底细胞癌、疣状表皮发育不良、非生殖性脂溢性角化病等有关[6]。
目前,关于HPV23亚型L1蛋白的研究还比较少。本文尝试构建带有不同融合标签的原核表达载体,分析重组蛋白HPV23 L1的表达情况及活性,旨在筛选HPV23 L1蛋白高表达菌株,为HPV23亚型L1蛋白的结构和功能研究奠定基础。
1 材料和方法 1.1 菌种与载体pUC57-HPV23 L1由上海生工生物工程有限公司合成;大肠杆菌感受态细胞DH5α、BL21来自TaKaRa公司;原核表达载体pET28a、pET30a、pET32a和pESUMO均由郑州大学生命科学学院分子免疫实验室保存。
1.2 重组表达载体的构建 1.2.1 目的基因及引物的设计与合成根据NCBI网站公布的HPV23 L1蛋白序列(GenBank. ARA 71354.1)及大肠杆菌的密码子偏好性,利用生物信息学软件优化并送至上海生工生物工程有限公司合成HPV23 L1基因。分别在其5’末端与3’末端加入EcoR I、Bas I、Xho I限制性酶切位点,设计合成相应的引物,引物列表如表 1所示。
|
|
表 1 引物列表 Tab. 1 Primers list |
用DNASTAR软件对HPV23 L1蛋白二级结构及其亲水性和疏水性进行分析,选择pET28a(Kan+)、pET30a(Kan+)、pET32a(Amp+)和pESUMO(Amp+)用于构建原核表达载体。pET28a、pET30a和pET32a分别用EcoR I/Xho I进行双酶切,pESUMO用Bas I/Xho I进行双酶切,回收双酶切产物,与含对应酶切位点的引物进行目的基因PCR扩增,再进行双酶切回收后的产物连接,构建HPV23 L1蛋白重组表达载体,分别转化大肠杆菌感受态细胞DH5α,从经菌液PCR鉴定的阳性菌株中提取质粒,通过双酶切鉴定及测序,最终获得HPV23 L1蛋白的4种带有不同融合标签的重组表达载体。重组表达载体构建策略如图 1所示。
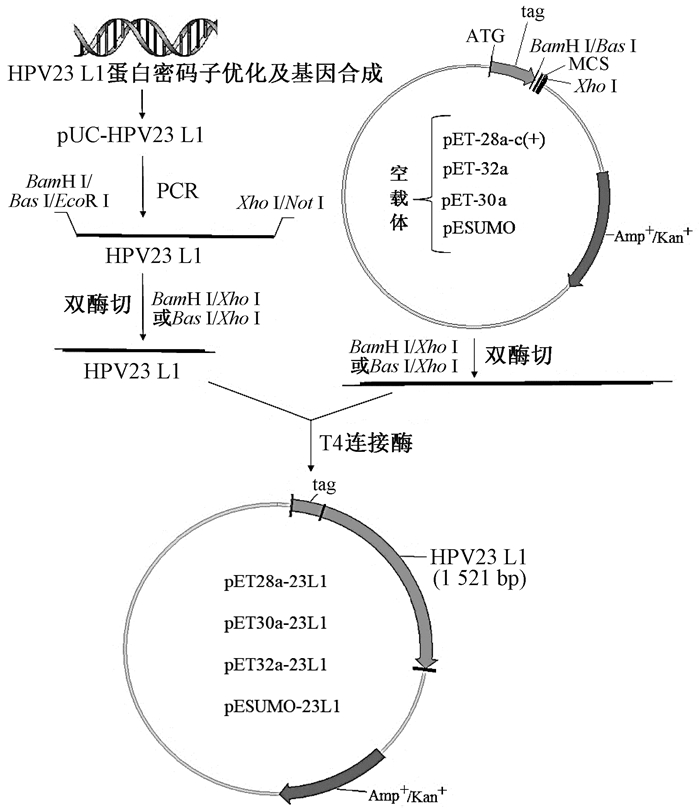
|
图 1 重组表达载体构建策略 Fig. 1 The construction strategy of recombinant expression vector |
将pET28a-23L1、pET30a-23L1、pET32a-23L1、pESUMO-23L1这4种重组表达载体阳性质粒转化大肠杆菌BL21(DE3)感受态细胞,挑取阳性克隆,经菌液PCR获得4种重组表达菌pET28a-23L1-BL21、pET30a-23L1-BL21、pET32a-23L1-BL21和pESUMO-23L1-BL21。将4种重组表达菌按1∶1 000接种在加有Amp+或Kan+抗性的5 mL LB液体培养基中,37 ℃摇床上220 r/min过夜培养,以活化菌种;过夜活化的菌种再按1∶100接种于相应抗性的5 mL LB液体培养基中,37 ℃、220 r/min培养至OD600约为0.6。加入0.3 mmol/L的诱导剂IPTG,16 ℃、220 r/min诱导18 h。经12% SDS-PAGE鉴定,分析重组蛋白的表达情况。
1.4 重组蛋白的可溶性分析诱导剂IPTG的浓度为0.3 mmol/L,16 ℃、220 r/min诱导表达18 h后收集表达菌体,4 ℃、12 000 r/min离心2 min,收集菌体,用5 mL pH 7.4的PBS重悬菌体。经超声破碎后4 ℃、12 000 r/min离心10 min,得到超声上清液和超声沉淀,通过12% SDS-PAGE分析重组目的蛋白的可溶性。
1.5 重组蛋白的纯化及鉴定根据1.4小节的结果,选择高表达菌株进行后续实验。诱导剂IPTG浓度为0.3 mmol/L,16 ℃诱导表达18 h后收集菌体,用pH 8.0的含有250 mmol/L NaCl的50 mmol/L Tris-HCl缓冲液重悬菌体后超声破碎,取上清液,选择Ni-NTA亲和层析法纯化重组蛋白。用咪唑浓度梯度法(Wash Buffer,pH 8.0的含有250 mmol/L NaCl的50 mmol/L Tris-HCl缓冲液+20 mmol/L咪唑;Elution Buffer,pH 8.0的含有250 mmol/L NaCl的50 mmol/L Tris-HCl缓冲液+200 mmol/L咪唑)进行洗脱,纯化后收集各组分,用12% SDS-PAGE和Western blot进行鉴定。
1.6 重组蛋白的活性分析与鉴定 1.6.1 同源建模利用SWISS-MODEL软件对HPV23 L1蛋白进行同源建模,预测HPV23 L1蛋白三维结构。
1.6.2 血凝实验取96孔微型血凝反应板,第1孔到第8孔均用25 μL PBS铺底。吸取25 μL纯化的HPV23 L1重组蛋白加入第1孔,充分混匀后进行2倍倍比稀释,一直倍比稀释至第5孔,在第6、7、8孔中分别加入25 μL PBS设置为阴性对照。将25 μL 1%小鼠红细胞悬液从第8孔倒加至第1孔,震荡混匀,室温静置40 min,拍照并记录实验结果。
2 实验结果分析 2.1 重组表达载体的构建重组表达载体的菌液PCR及双酶切鉴定结果如图 2所示。重组表达载体构建成功后,经菌液PCR鉴定发现,扩增产物条带出现在大约1 521 bp(图 2A、2B、2C);EcoR I/Xho I或Bas I/Xho I双酶切鉴定显示重组表达载体构建成功(图 2D)。将阳性质粒测序结果与合成的HPV23 L1序列进行比对分析,结果显示,两序列完全一致,说明pET28a-23L1、pET30a-23L1、pET32a-23L1、pESUMO-23L1这4种重组表达载体构建成功。
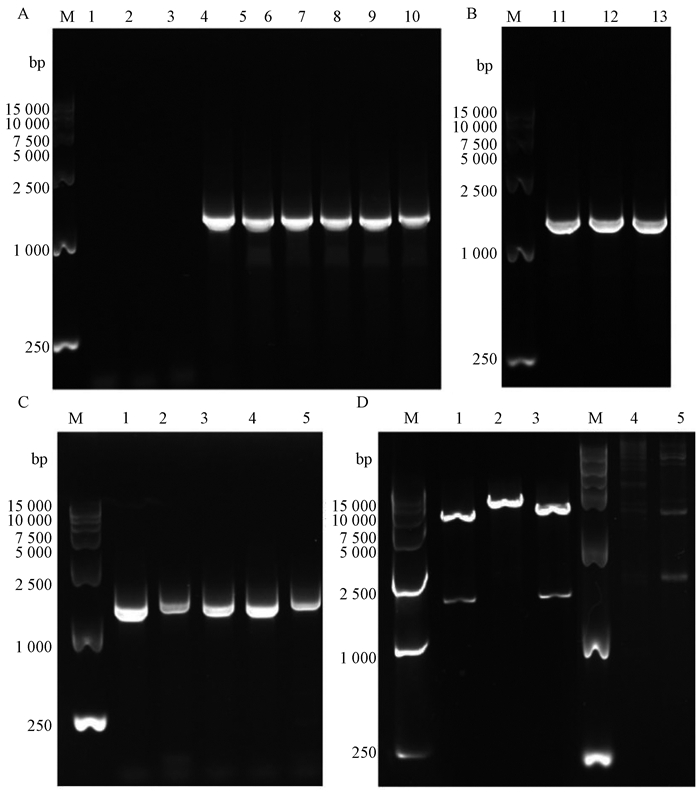
|
图 2 重组表达载体的菌液PCR及双酶切鉴定 Fig. 2 The identification of recombinant expression vector by PCR and double enzyme digestion A为pET28a-23L1、pET30a-23L1的菌液PCR鉴定(M:Marker;1~5:pET28a-23L1扩增产物;6~10:pET30-23L1扩增产物);B为pET32a-23L1的菌液PCR鉴定(M:Marker;11~13:pET32a-23L1扩增产物);C为pESUMO-23L1的菌液PCR鉴定(M:Marker;1~5:pESUMO-23L1扩增产物);D为重组表达载体的双酶切鉴定(M:Marker;1:pET30a-23L1;2:pET30a空载; 3:pET32a-23L1; 4:pET28a-23L1; 5:pESUMO-23L1)。 |
SDS-PAGE鉴定重组蛋白L1的表达情况如图 3所示。经生物信息学预测发现,重组HPV23 L1蛋白的相对分子质量约为57 400,具有较多亲水性区域(图 3A)。将4种重组表达菌pET28a-23L1-BL21、pET30a-23L1-BL21、pET32a-23L1-BL21和pESUMO-23L1-BL21进行诱导表达,经12% SDS-PAGE鉴定,结果显示,pET28a-23L1(HIS-23L1融合蛋白)和pET30a-23L1(HIS-S-23L1融合蛋白)几乎无目的蛋白表达,而pESUMO-23L1(SUMO-23L1)和pET32a-23L1(TRX-23L1)表达产物在大约80 kD处有目的条带(图 3B)。
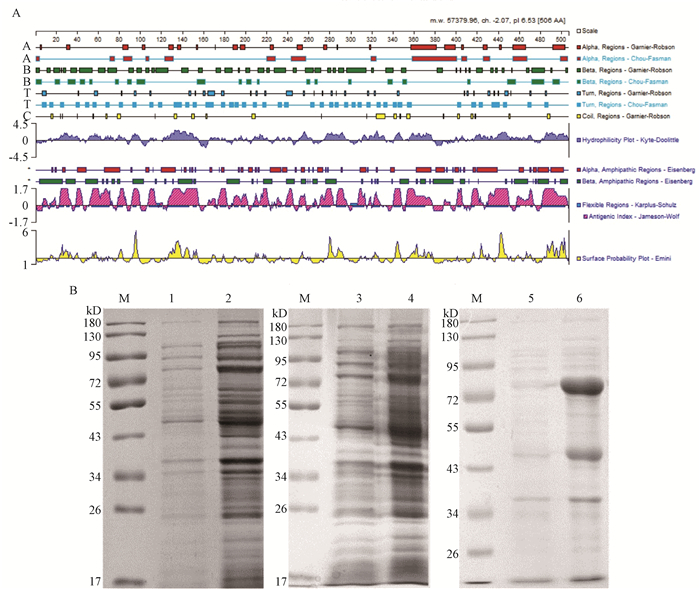
|
图 3 SDS-PAGE鉴定重组蛋白L1的表达情况 Fig. 3 The expression of recombinant protein L1 identified by SDS-PAGE A为HPV23 L1蛋白的二级结构;B为原核表达载体的诱导表达(M:Marker;1:pET32a-23L1未加诱导剂IPTG的对照;2:pET32a-23L1诱导表达产物;3:pET28a-23L1诱导表达产物;4:pET30a-23L1诱导表达产物; 5:pESUMO-23L1未加诱导剂IPTG的对照;6:pESUMO-23L1诱导表达产物)。 |
诱导剂IPTG浓度为0.3 mmol/L,16 ℃诱导表达18 h后收集pESUMO-23L1及pET32a-23L1的表达菌体,PBS重悬后经超声破碎处理,上清液和沉淀分别用12% SDS-PAGE进行鉴定。HPV23 L1重组蛋白的可溶性分析及Western blot鉴定结果如图 4所示。结果显示,pESUMO-23L1和pET32a-23L1的超声上清液和沉淀在大约80 kD的位置均存在蛋白条带(SUMO-23L1蛋白或TRX-23L1蛋白),而重组SUMO-23L1蛋白表达量整体高于TRX-23L1蛋白(图 4A、4B);重组SUMO-23L1蛋白或TRX-23L1蛋白均可与HIS单抗发生反应(图 4C、4D)。
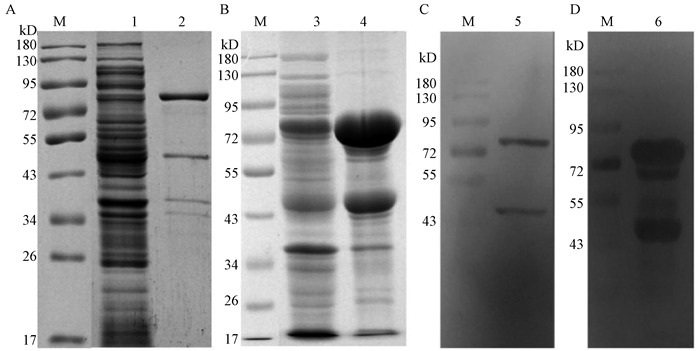
|
图 4 HPV23 L1重组蛋白的可溶性分析及Western blot鉴定 Fig. 4 Solubility analysis and Western blot identification of HPV23 L1 recombinant protein A~B为SDS-PAGE(M:Marker;1:pET32a-23L1超声上清液;2:pET32a-23L1超声沉淀;3:pESUMO-23L1超声上清液;4:pESUMO-23L1超声沉淀);C~D为Western blot(5:pET32a-23L1超声上清液;6:pESUMO-23L1超声上清液)。 |
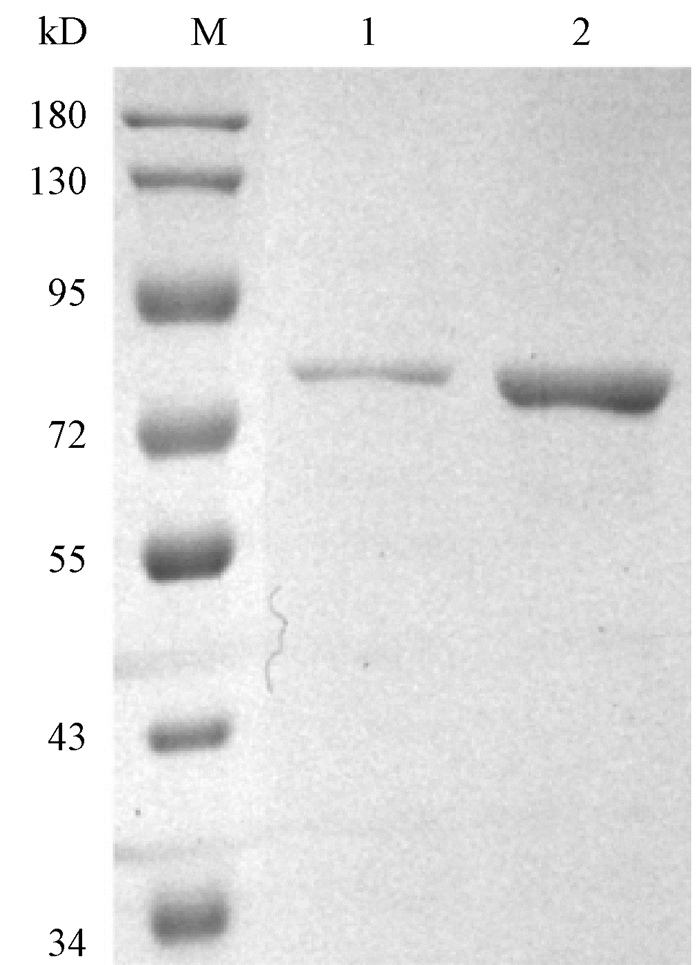
在pH 8.0的含有250 mmol/L NaCl的50 mmol/L Tris-HCl缓冲液条件下,用Ni-NTA亲和层析法纯化重组SUMO-23L1蛋白,经12% SDS-PAGE鉴定,重组蛋白的纯化结果如图 5所示。结果表明,纯化后目的蛋白的纯度约为90%。
|
图 5 SDS-PAGE鉴定重组蛋白的纯化结果 Fig. 5 The purification results of recombinant protein identified by SDS-PAGE M:Marker;1~2:纯化的SUMO-23L1蛋白。 |
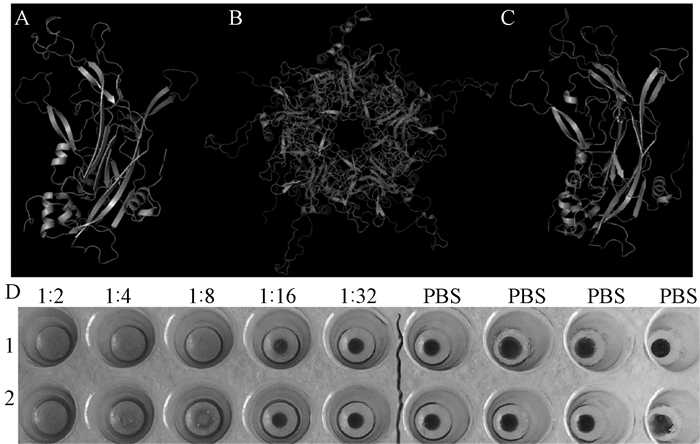
利用SWISS-MODEL软件对HPV23 L1蛋白进行同源建模,HPV23 L1蛋白同源建模及重组蛋白血凝活性鉴定结果如图 6所示。可以看出,HPV23 L1蛋白单体结构(图 6A)和五聚体结构(图 6B)与参考序列牛乳突瘤病毒(bovine papillomavirus type 1,BPV1)的L1蛋白(PDB:3iyj)结构相似(图 6C),二者序列同源性为49.39%。血凝实验结果显示,重组SUMO-23L1蛋白有凝集小鼠红细胞的能力(图 6D),说明本研究制备的重组HPV23 L1蛋白具有较高的活性。
|
图 6 HPV23 L1重组蛋白同源建模及血凝活性鉴定 Fig. 6 The homologous modeling and hemagglutination activity of HPV23 L1 recombinant protein A为HPV23 L1蛋白单体结构;B为HPV23 L1蛋白五聚体结构;C为BPV1 L1蛋白结构(PDB:3iyj);D为重组蛋白血凝活性鉴定(1和2为重复实验,其中1∶2~1∶32为纯化的SUMO-23L1蛋白2倍倍比稀释的结果;PBS为阴性对照)。 |
目前商品化的HPV疫苗主要基于用杆状病毒表达的HPV16、HPV18等α属高危型HPV的L1蛋白[7-8]。有许多研究者利用GST融合标签或者GST融合标签与伴侣蛋白共表达, 成功实现α属高危型HPV L1蛋白在大肠杆菌中的可溶性表达[9-10];也有研究者利用SUMO融合标签在原核表达系统中制备HPV16、HPV18等α属高危亚型HPV的L1蛋白[11-12]。
本研究主要通过构建4种原核重组表达载体pET28a-23L1、pET30a-23L1、pET32a-23L1和pESUMO- 23L1,分析不同融合标签对重组蛋白表达情况的影响。经SDS-PAGE分析发现,重组表达后,pET32a-23L1和pESUMO-23L1在大约80 kD处有一条明显的条带,比预测理论值(70 kD)偏大,推测可能是由于标签中6个连续的带正电荷的碱性氨基酸造成HIS-tag融合蛋白在SDS-PAGE中迁移速率变慢[12]。随后的Western blot鉴定结果也证实了80 kD处为重组目的蛋白。pET32a-23L1和pESUMO- 23L1均有可溶性表达,且pESUMO-23L1的可溶性表达量较高,这与本课题组前期研究结果[12]一致。
此外,用HIS单抗进行Western blot检测时发现,pET32a-23L1和pESUMO-23L1均在约45 kD处有一条明显的条带,推测可能是由于重组蛋白分子部分降解引起的。通过SWISS-MODEL软件同源建模发现,HPV23 L1蛋白与BPV1 L1蛋白的序列同源性为49.39%,并且HPV23 L1蛋白与参考序列BPV1 L1蛋白(PDB:3iyj)的结构极其相似,也可以形成五聚体结构。经血凝实验证实,该重组蛋白具有凝集小鼠红细胞的能力,说明所获得的HPV23 L1蛋白具有较高的活性,为进一步研究HPV23 L1蛋白的结构和功能奠定基础。
| [1] |
LI N, ZHANG G P, CHEN Y M, et al. Identification of the mimotopes within the major capsid protein L1 of human papillomavirus types 18 and 45, using neutralizing monoclonal antibodies[J]. International journal of biological macromolecules, 2021, 174: 587-595. DOI:10.1016/j.ijbiomac.2021.01.137 (  0) 0) |
| [2] |
KONING M N C, STRUIJK L, BAVINCK J N B, et al. Betapapillomaviruses frequently persist in the skin of healthy individuals[J]. Journal of general virology, 2007, 88(5): 1489-1495. DOI:10.1099/vir.0.82732-0 (  0) 0) |
| [3] |
ATKINSON K, BISHOP L, RHODES G, et al. Genome sequence of human papillomavirus 23 strain HPV-23/lancaster/2015[EB/OL]. [2020-12-21]. https://www.researchgate.net/publication/317074600.
(  0) 0) |
| [4] |
WANG D N, LIU X L, WEI M X, et al. Rational design of a multi-valent human papillomavirus vaccine by capsomere-hybrid co-assembly of virus-like particles[EB/OL]. [2020-12-21]. https://www.nature.com/articles/s41467-020-16639-1.
(  0) 0) |
| [5] |
CHEN Y M, LIU Y C, ZHANG G P, et al. Human papillomavirus L1 protein expressed in Escherichia coli self-assembles into virus-like particles that are highly immunogenic[J]. Virus research, 2016, 220: 97-103. DOI:10.1016/j.virusres.2016.04.017 (  0) 0) |
| [6] |
MVHR L S A, HULTIN E, DILLNER J. Transcription of human papillomaviruses in nonmelanoma skin cancers of the immunosuppressed[J]. International journal of cancer, 2021, 149(6): 1341-1347. DOI:10.1002/ijc.33683 (  0) 0) |
| [7] |
YANG Y, CHE Y X, ZHAO Y, et al. Prevention and treatment of cervical cancer by a single administration of human papillomavirus peptide vaccine with CpG oligodeoxynucleotides as an adjuvant in vivo[J]. International immunopharmacology, 2019, 69: 279-288. DOI:10.1016/j.intimp.2019.01.024 (  0) 0) |
| [8] |
MOREIRA E D, GIULIANO A R, DE HOON J, et al. Safety profile of the 9-valent human papillomavirus vaccine: assessment in prior quadrivalent HPV vaccine recipients and in men 16 to 26 years of age[J]. Human vaccines & immunotherapeutics, 2018, 14(2): 396-403. (  0) 0) |
| [9] |
BANG H B, LEE Y H, LEE Y J, et al. High-level production of human papillomavirus (HPV) type 16 L1 in Escherichia coli[J]. Journal of microbiology and biotechnology, 2016, 26(2): 356-363. DOI:10.4014/jmb.1511.11010 (  0) 0) |
| [10] |
PAN D, ZHA X, YU X H, et al. Enhanced expression of soluble human papillomavirus L1 through coexpression of molecular chaperonin in Escherichia coli[J]. Protein expression and purification, 2016, 120: 92-98. DOI:10.1016/j.pep.2015.12.016 (  0) 0) |
| [11] |
陈玉梅. 人乳头瘤病毒16亚型(HPV16)亚单位疫苗的初步研究[D]. 郑州: 郑州大学, 2017. CHEN Y M. Preliminary study on human papillomavirus subtype 16 (HPV16) subunit vaccine[D]. Zhengzhou: Zhengzhou University, 2017. (  0) 0) |
| [12] |
WANG A P, LI N, ZHOU J M, et al. Mapping the B cell epitopes within the major capsid protein L1 of human papillomavirus type 16[J]. International journal of biological macromolecules, 2018, 118: 1354-1361. DOI:10.1016/j.ijbiomac.2018.06.094 (  0) 0) |
 2022, Vol. 54
2022, Vol. 54


