2. 新疆农业职业技术学院园林科技学院,新疆昌吉 831100
2. Garden Science and Technology College, Xinjiang Agricultural Vocational Technical College, Changji, Xinjiang 831100, China
氮和硫都是植物的必需营养元素,氮是组成蛋白质、核酸、叶绿素、辅酶、植物激素和次生代谢物的必需组成元素[1–2]。硫对植物蛋白质合成、叶绿体构成和功能维持、辅酶,以及小分子物质合成、生长、抗逆调节等方面均有重要作用[3–5],更是含硫氨基酸 (半胱氨酸、甲硫氨酸等) 和次级代谢物 (十字花科的芥子油苷和葱属植物的风味前体物质 S-烃基半胱氨酸亚砜) 的组成成分[6]。硫的代谢与氮的代谢密切相关,如半胱氨酸的合成需要硫和氮同时参与,施用硫肥和氮肥可以提高 CSOs 的含量[7–8]。
研究证实小麦、玉米、大豆等作物生长过程中氮、硫元素间存在交互、协同作用[9–12],大蒜 (Allium sativum L.) 为百合科葱属植物,需硫量较大,氮、硫元素及交互作用对葱属植物生长与栽培品质均有重要的影响。孔灵君等[13],刘忠松等[14]分别研究了氮硫互作对大葱品质、主要元素吸收分配特性以及硫同化关键酶活性的影响,结果表明氮、硫水平及其互作效应对大葱 N、P、K、S 积累分配有显著影响,但硫的影响不及氮明显;低氮或者高氮条件下均抑制硫同化酶活性,而硫水平的提高则显著抑制 ATPS 和 OASS 活性。为此,本文研究了不同浓度氮、硫元素互作对大蒜不同生长期氮硫关键同化酶活性与植株氮、硫含量的影响,从生理角度阐述氮硫互作对大蒜氮、硫同化的影响机制,以期为大蒜栽培中氮、硫元素合理配施提供技术参考。
1 材料与方法 1.1 试验设计试验用大蒜品种为新疆白皮蒜,经地窖保藏越冬后,于 2015 年 4 月 18 日播种。栽培基质为蛭石、珍珠岩,配制比例 6∶4,蛭石粒度大小为 0.3~0.5 cm,栽培前先经蒸馏水充分淋洗。选用塑料栽培盆,盆高 20 cm,直径 15 cm,蛭石装载高度为盆高 4/5。每盆栽 2 株大蒜,置于塑料防雨棚下浇灌营养液培养。
营养液成分采用 Hoagland 营养配方,在大量元素、微量元素一致的基础上,采用缺素配方,分别设置 3 个氮素水平、3 个硫素水平,其中氮素水平调节使用硝酸铵,硫素水平调节使用硫酸钠。氮素水平分别为 5、10、20 mmol/L (记作 N1、N2、N3);硫素水平分别为 2、4、8 mmol/L (记作 S1、S2、S3),另设置空白对照组,即在其他营养元素一致基础上不施加氮素和硫素。采用二因素三水平完全随机区组设计,每组分别处理 30 盆。栽培期间,幼苗期每7天浇灌一次营养液,至花茎伸长期后每 3 天浇灌一次营养液。每浇灌 3 次营养液用蒸馏水清洗一次,清除积累的盐分。
分别在大蒜植株长至幼苗期 (6 月 1 日)、花茎伸长期 (6 月 29 日)、鳞茎膨大初期 (7 月 23 日)、鳞茎膨大中期 (8 月 28 日),随机选取 6 株植株,剪取最大功能叶,液氮处理后置于 –30℃ 冰箱中保存。
1.2 测定项目与方法硝酸还原酶 (NR) 活性参照李合生等方法,采用活体法测定[15],酶活单位为 μg/(g·h),FW。
谷氨酰胺合成酶 (GS) 活性参照赵世杰等方法[16],以 540 nm 处吸光值大小间接表示酶活性,单位为 OD/(mg·h),protein。
ATP 硫酸化酶 (ATPS) 活性测定参照 Ahmad 等方法[17],以 660 nm 处吸光值大小间接表示酶活性,单位为 OD/(mg·h),protein。
半胱氨酸合成酶 (OAS-TL) 活性测定参照 Demosthenis 等方法[18],以半胱氨酸做标曲,酶活单位为 μmol/(g·min),FW。
干样经超微粉碎后,过 100 目筛,准确称取 0.20 g 混合样分别用于测定全氮、全硫含量。其中全氮参照 GB50095–2010 采用分光光度法测定[19],全硫测定采用 BaSO4 比浊法[20]。
1.3 数据处理采用 DPS7.05 软件进行数据统计分析,方差分析采用 LSD (最小显著性差异) 进行差异显著性检验 (α=0.05),Pearson 系数采用 SPSS18.0 进行计算,采用 SigmaPlot12.5 制图。
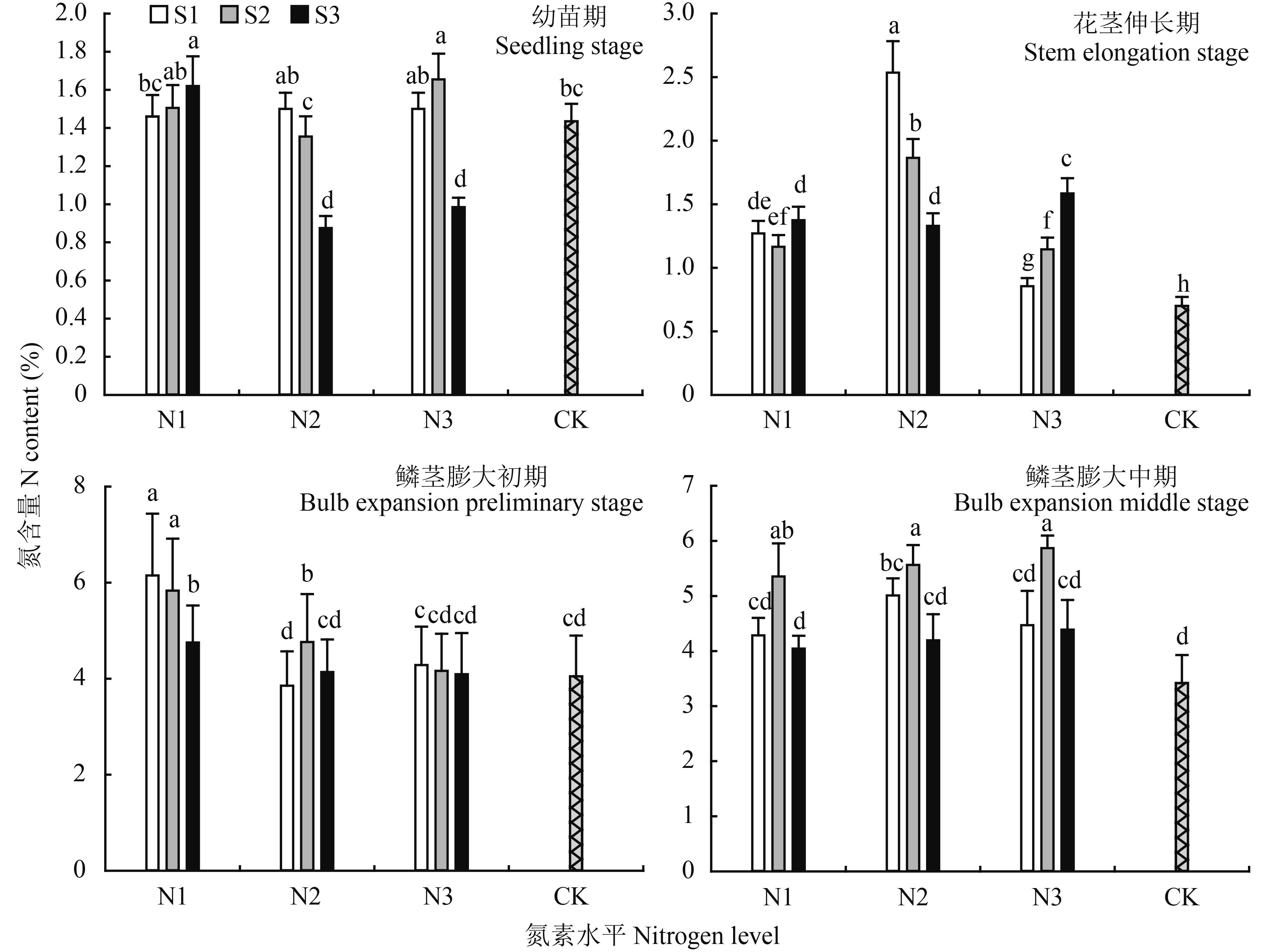
2 结果与分析 2.1 氮硫互作对大蒜植株氮、硫含量的影响2.1.1 氮素含量 由图 1可见,大蒜植株中氮素含量总体呈上升趋势,特别是在大蒜鳞茎膨大期,氮素含量显著升高。在幼苗期,氮素含量集中在 1.36%~1.66%,以 N2S3、N3S3 处理含量最低,分别为 0.98%、0.88%。在花茎伸长期,氮素含量以 N2 处理组最高,在此处理下随硫素浓度升高而降低;在 N3 条件下整体氮素含量较低,随硫浓度升高有显著升高,但以对照组最低,为 0.70%。鳞茎膨大初期大蒜植株以 N1 处理氮素含量最高,硫素增加则降低了植株氮素含量;N2 处理条件下,以 S2 处理最高,为 4.78%;N3 与 CK 处理氮素含量差异不显著。鳞茎膨大中期,不同氮素水平条件下均以 S2 水平处理氮素含量最高,随着硫素水平的升高而降低氮素吸收利用率,且 CK 最低,为 3.42%。
 |
|
图1
氮硫互作对大蒜植株氮含量的影响
Fig. 1
Influence of nitrogen and sulfur interaction on N contents of garlic plants
[注(Note):柱上不同小写字母表示不同处理间差异达到 0.05 显著水平 Different small letters above the bars mean significant difference among treatments at the 0.05 level.] |
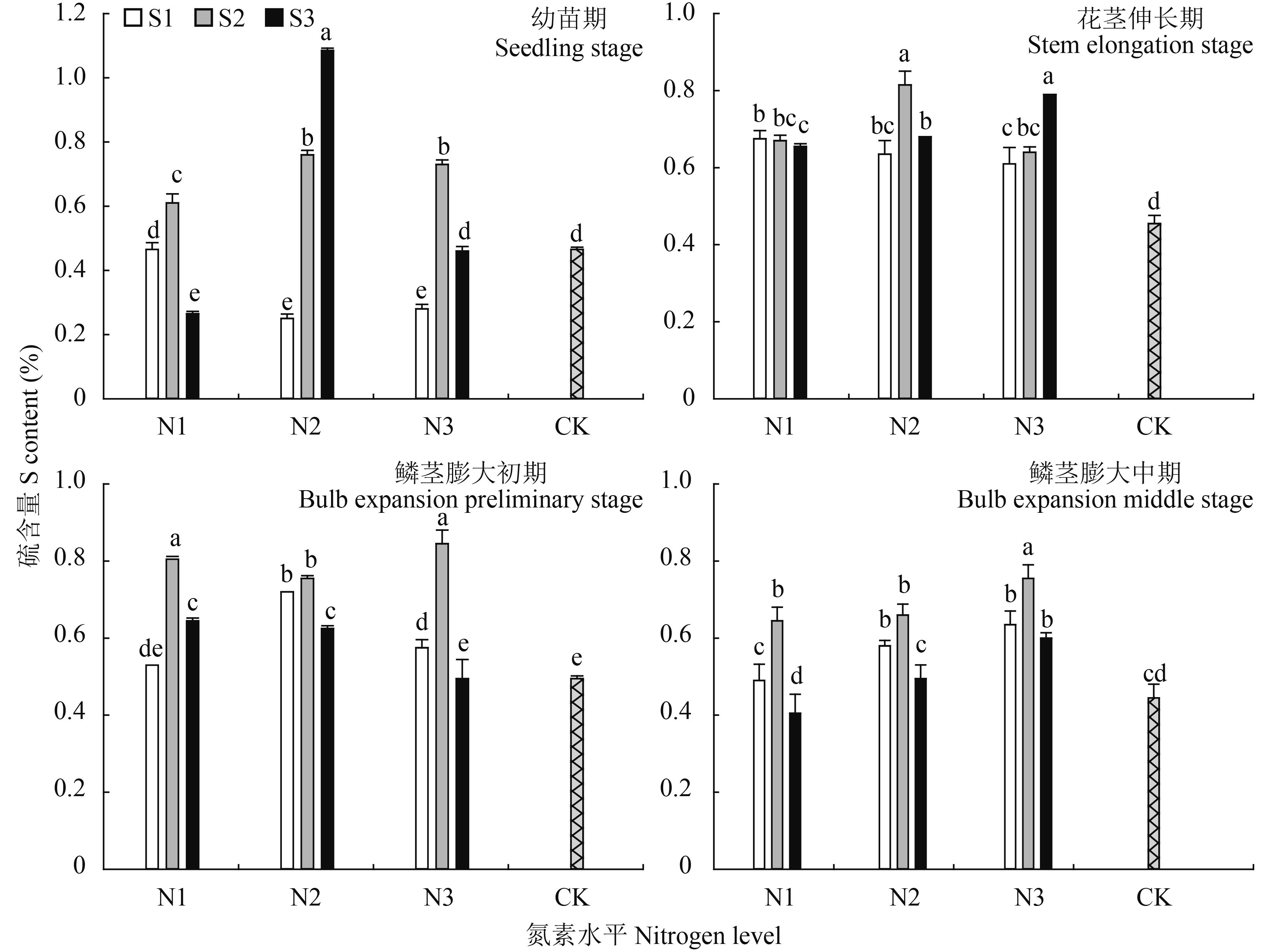
2.1.2 硫素含量 由图 2可见,大蒜植株硫含量总体呈先上升后平稳的趋势,且不同生长时期表现不一。幼苗期时在 N1、N3 条件下,随着硫素水平升高,植株硫素含量表现为先上升后下降,而在 N2 水平下则呈上升趋势,由 0.25% 升高到 1.08%。花茎伸长期 N1 处理组间差异较小,硫素施用越多则植株硫含量越小;随着氮水平的升高,硫素配施量的增加能够提高硫的吸收,而变化规律受到氮素水平影响,N2 条件下以 S2 最高,为 0.82%;N3 条件下以 S3 最高,为 0.79%。鳞茎膨大初期与中期,氮硫互作对植株硫含量的影响较为一致,在同一氮素水平下均以 S2 处理最高,且在鳞茎膨大中期增施氮素或硫素均能够促进植株硫含量。
 |
|
图2
氮硫互作对大蒜植株硫含量的影响
Fig. 2
Influence of nitrogen and sulfur interaction on S contents of garlic plants
[注(Note):柱上不同小写字母表示不同处理间差异达到 0.05 显著水平 Different small letters above the bars mean significant difference among treatments at the 0.05 level.] |
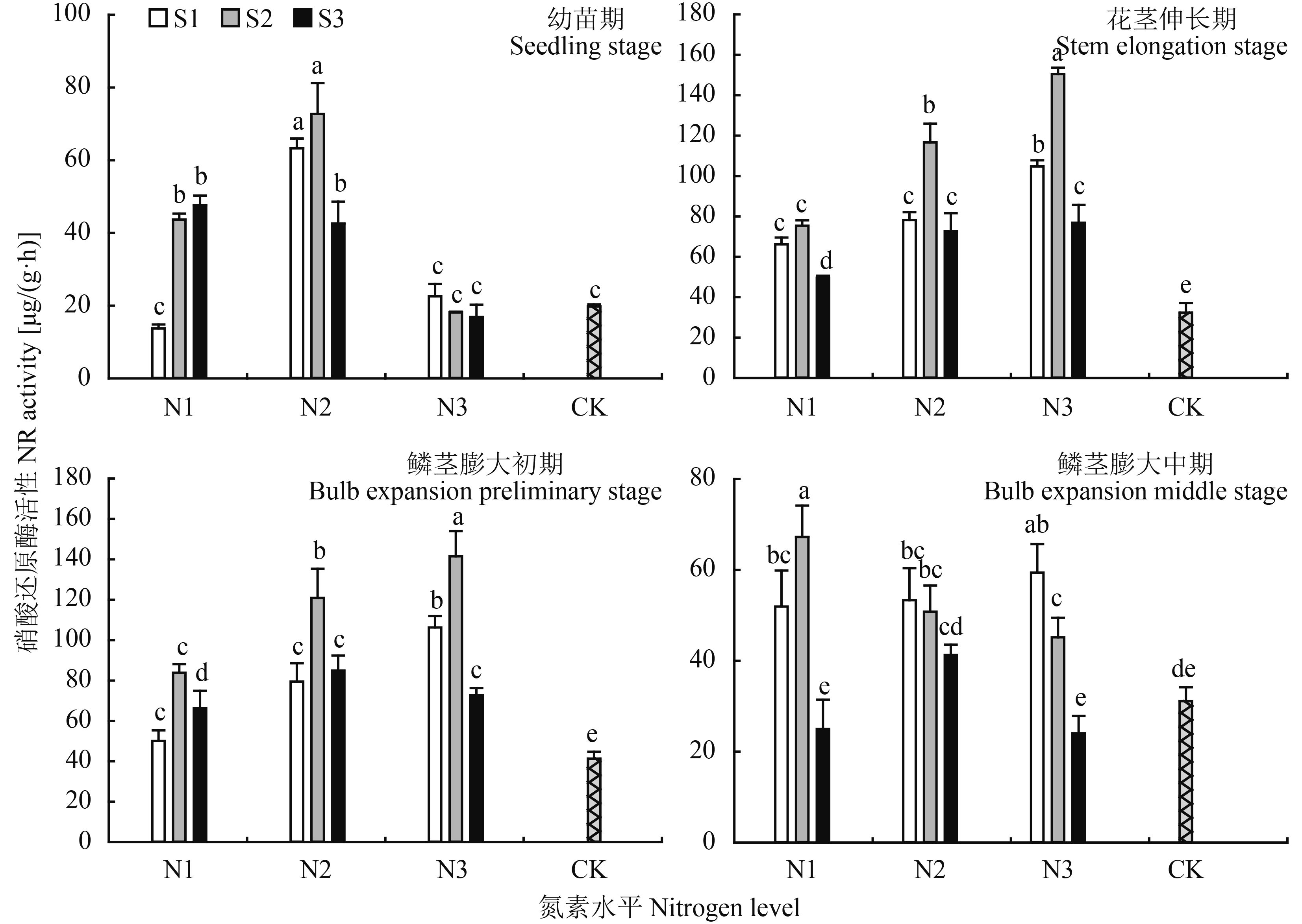
2.2.1 硝酸还原酶 (NR)图 3显示,不同生育时期大蒜叶片 NR 活性差异显著,整体呈先升高后降低趋势,处理组间差异显著。幼苗期,适当提高氮水平能够显著增加 NR 活性;低氮条件下 (N1) 硫的增施能够刺激酶活性升高,N2 时配施硫浓度达到 8 mmol/L 时则显著抑制该酶活性;而高氮 (N3) 条件下则显著抑制酶活性的升高,各处理组与 N2 组比较分别降低 40.74、54.57、25.64 μg/(g·h)。花茎伸长期与鳞茎膨大初期均以对照最低,为 32.31、41.31 μg/(g·h),随氮素水平升高 NR 活性整体呈上升趋势;各处理组酶活性均以 S2 处理最高,且该生长时期酶活性较稳定,变化趋势较一致。鳞茎膨大中期酶活性整体降低,硫施用量增加降低了酶活,以 N1S2 活性最高,为 67.21 μg/(g·h);N3S3 处理最低,为 24.04 μg/(g·h)。
 |
|
图3
氮硫互作对大蒜叶片中 NR 活性的影响
Fig. 3
Influence of nitrogen and sulfur interaction on NR activities of garlic leaves
[注(Note):柱上不同小写字母表示不同处理间差异达到 0.05 显著水平 Different small letters above the bars mean significant difference among treatments at the 0.05 level.] |
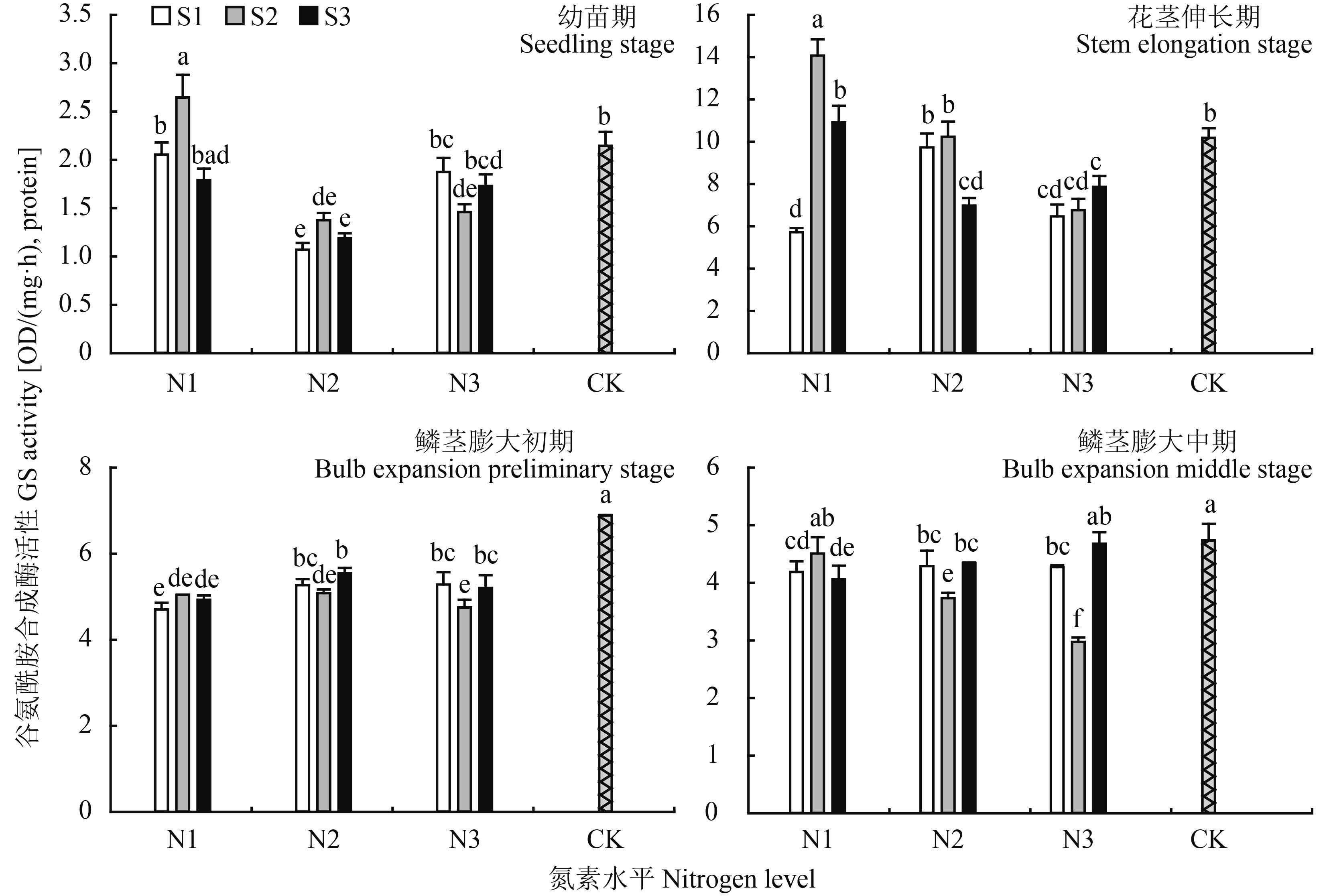
2.2.2 谷氨酰胺合成酶 (GS) 由图 4可见,在大蒜生长过程中,GS 活性整体呈先升高后降低趋势,在花茎伸长期该酶活性最高,随后各处理组的酶活性均有不同程度的降低。在大蒜不同生长时期,N1S2 处理在大蒜幼苗期、花茎伸长期 GS 活性最高,分别为 2.65、14.08 OD/(mg·h),protein。可见在该过程中酶活性急剧升高。幼苗期时,以 N2 水平下 GS 活性最低,在相同氮素水平条件下,随着硫素浓度升高 GS 活性呈先上升后下降趋势。花茎伸长期,以 N3 水平下 GS 活性最低,且处理组间差异不显著;随着氮素水平升高,在低硫 (S1) 条件下 GS 活性先升高后降低,在 S2、S3 条件下则呈下降趋势。在大蒜鳞茎膨大初期、中期,空白对照的酶活性则最高,分别为 6.89、4.74 OD/(mg·h),protein;鳞茎膨大初期除对照外,其它处理组间酶活性差异较小,介于 4.71~5.55 OD/(mg·h),protein;在鳞茎膨大中期,以 S2 水平下酶活性差异最大,随氮素水平升高 GS 活性显著降低,由 4.51 OD/(mg·h),protein 降至 2.98 OD/(mg·h),protein。
 |
|
图4
氮硫互作对大蒜叶片中 GS 活性的影响
Fig. 4
Influence of nitrogen and sulfur interaction on GS activities of garlic leaves
[注(Note):柱上不同小写字母表示不同处理间差异达到 0.05 显著水平 Different small letters above the bars mean significant difference among treatments at the 0.05 level.] |
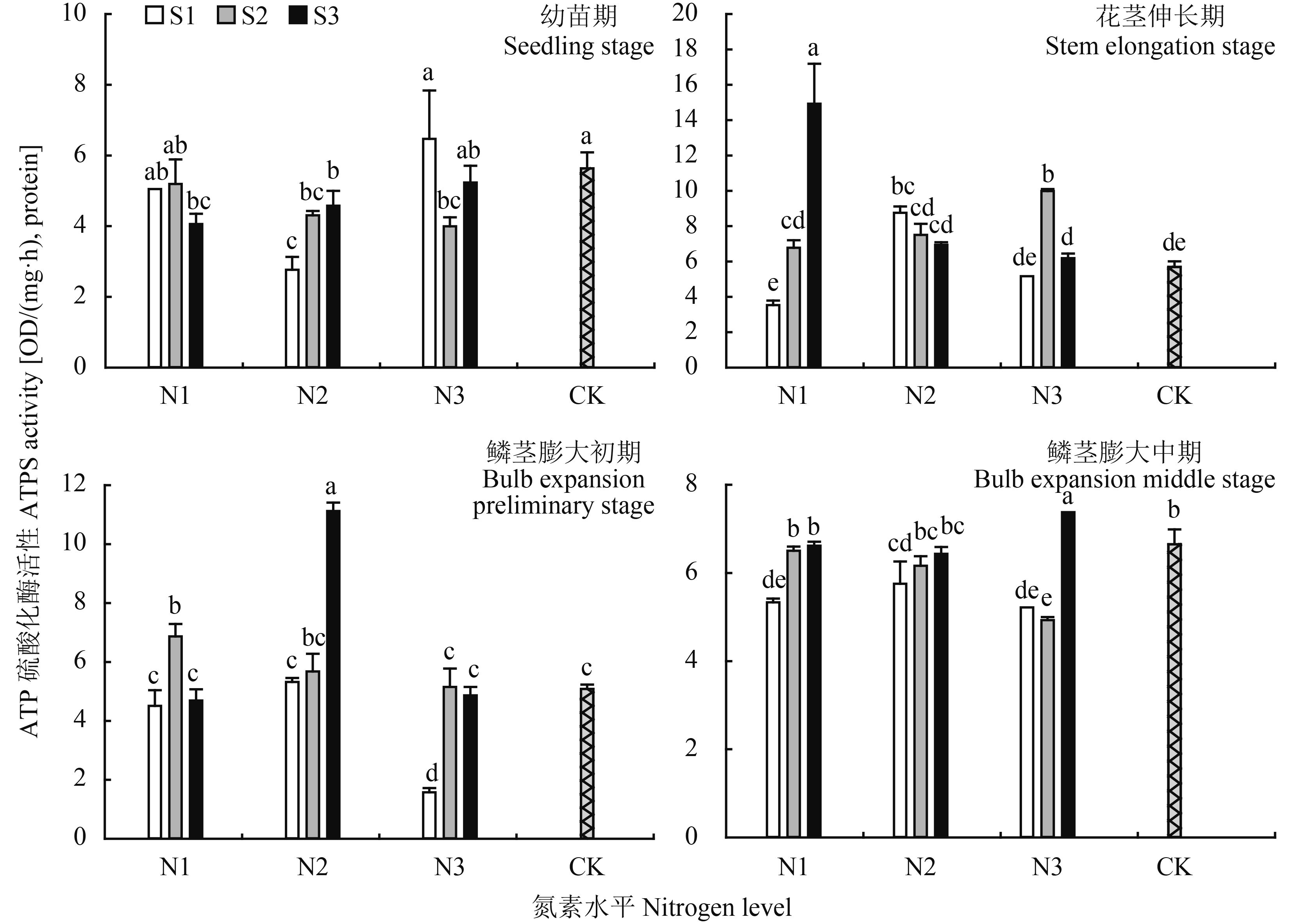
2.3.1 ATP硫酸化酶(ATPS) 由图 5可见,ATPS 活性在大蒜不同生长时期表现各不相同,总体呈先上升后下降趋势,且处理组间存在显著性差异。在大蒜幼苗期不同氮素水平下,N2 处理组酶活性整体偏低,其中 N2S1 最低,为 2.77 OD/(mg·h);在高氮 (N3) 条件下,S1 时酶活性最高,为 6.47 OD/(mg·h),S2 时酶活性最低,为 3.99 OD/(mg·h)。花茎伸长期,ATPS 活性较幼苗期整体升高;随氮素水平的提高,S1 时呈先上升后下降,S2 时呈上升趋势,而 S3 水平下呈下降趋势。可见硫素水平对 ATPS 的影响与氮素水平有密切关系,两元素之间有显著的互作关系。大蒜鳞茎膨大初期在高氮 (N3) 时 ATPS 活性较低,其中 N3S1 为 1.58 OD/(mg·h);在中度氮素 (N2) 条件下,酶活性较高,N2S3 为 11.13 OD/(mg·h),可见在此时期氮素的过量供给能够降低 ATPS 活性,而硫的增施能够相应刺激酶活性应答。鳞茎膨大中期,酶活性变化趋势较为一致,在试验氮素水平范围内,酶活性随硫素施用水平升高而升高;在高氮条件下,N3S3 酶活最高,为 7.38 OD/(mg·h)。
 |
|
图5
氮硫互作对大蒜叶片中 ATPS 活性的影响
Fig. 5
Influence of nitrogen and sulfur interaction on ATPS activities of garlic leaves
[注(Note):柱上不同小写字母表示不同处理间差异达到 0.05 显著水平 Different small letters above the bars mean significant difference among treatments at the 0.05 level.] |
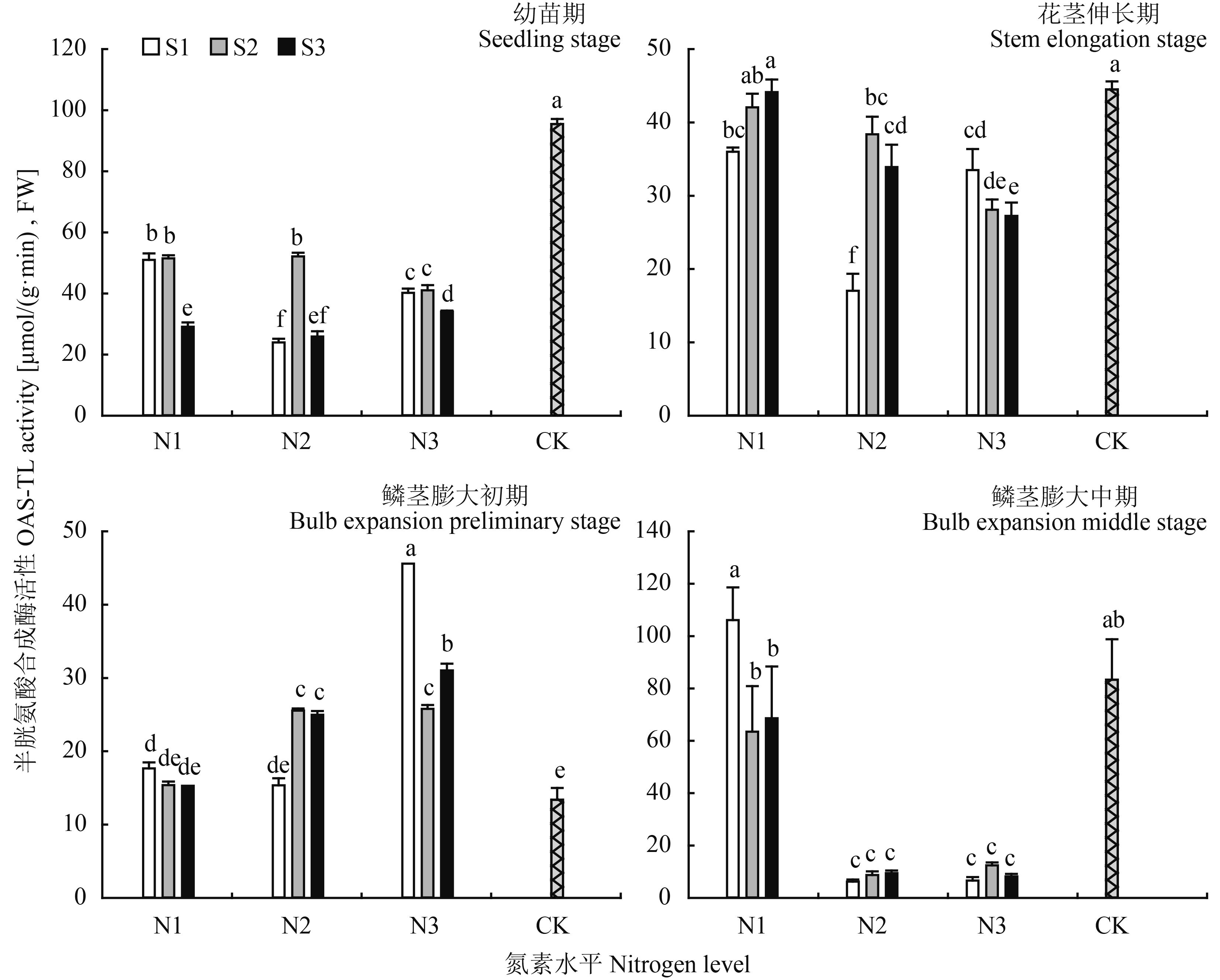
2.3.2 半胱氨酸合成酶 (OAS-TL) 乙酰丝氨酸裂解酶 (OAS-TL,又称半胱氨酸合成酶) 能够催化乙酰丝氨酸与硫化物反应,生成半胱氨酸,是硫同化的关键合成酶。由图 6可见,在幼苗期和花茎伸长期均以对照组 OAS-TL 活性最高,分别为 95.49、44.50 μmol/(g·min),FW。该时期 N、S 交互作用对酶活性影响有所差异,低氮条件下在幼苗期时,随着硫素水平增加酶活性呈下降趋势,而花茎伸长期则表现为上升趋势;N2 条件下,低硫 (S1) 与高硫 (S3) 对 OAS-TL 活性均有所抑制;N3 条件下,硫供给水平的升高则显著抑制该酶活性,分别比 S1 水平下降低 17.96%、22.89%。鳞茎膨大初期,N1 条件下 OAS-TL 活性对硫供给水平响应不显著,处理间差异不明显;随氮素水平升高,该酶活性呈升高趋势,但在 N3 水平下,硫水平提升反而抑制 OAS-TL 活性。鳞茎膨大中期,对照组与低氮处理组的 OAS-TL 活性显著升高,而 N2、N3 处理组叶片酶活性急剧降低。
 |
|
图6
氮硫互作对大蒜叶片中 OAS-TL 活性的影响
Fig. 6
Influence of nitrogen and sulfur interaction on OAS-TL activities of garlic leaves
[注(Note):柱上不同小写字母表示不同处理间差异达到 0.05 显著水平 Different small letters above the bars mean significant difference among treatments at the 0.05 level.] |
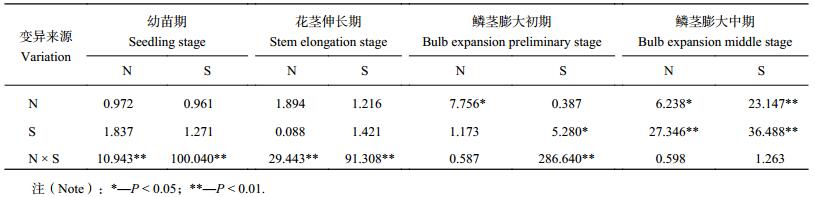
由表 1可见,大蒜植株氮、硫含量对氮硫互作水平的响应情况,大蒜在幼苗期、花茎伸长期 N、S 对大蒜植株氮含量没有显著影响,而 N × S (交互作用) 对其影响极显著;鳞茎膨大初期 N 对氮含量有显著影响,而 S、N × S 均无显著影响;在鳞茎膨大中期,N、S 对氮含量有显著或极显著影响,N × S 效应不明显。较氮含量而言,植株硫含量对氮硫互作响应有所差异,在幼苗期、花茎伸长期时仅 N × S 对其有显著影响;鳞茎膨大初期,S、N × S 分别有显著、极显著影响,而 N 无显著影响;鳞茎膨大中期时 N、S 均有极显著影响,而 N × S 作用不明显。
| 表1 氮硫互作对大蒜植株氮、硫含量影响的方差分析 (F 值) Table 1 ANOVA analysis of N and S interaction on activities of nitrogen and sulfur contents in garlic plants (F value) |
 |
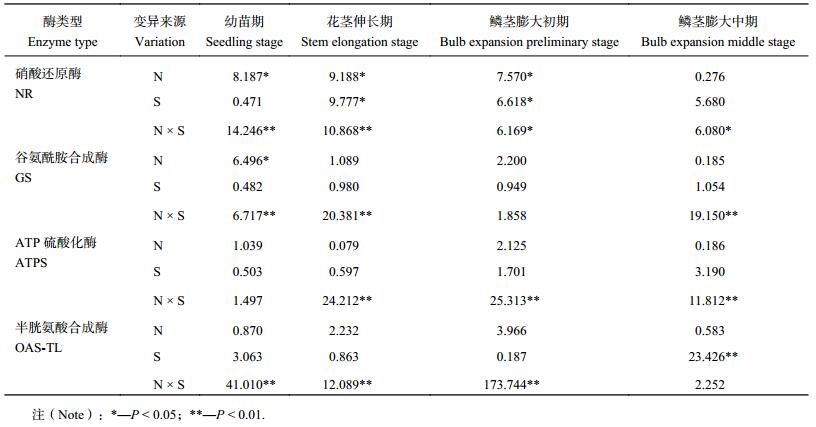
氮硫互作对不同生长期大蒜叶片中 NR、GS、ATPS、OAS-TL 活性影响的方差分析结果见表 2。对于氮合成关键酶分析可知,NR 与 GS 在不同生长时期对氮硫互作水平响应不一,NR 对氮素供应较为敏感,仅在鳞茎膨大中期氮素对其无显著影响,硫在花茎伸长期、鳞茎膨大初期对其也有显著影响;且 N × S 交互作用对 NR 活性有显著或极显著影响。GS 仅在幼苗期对氮素供给有显著响应,硫素对其影响不显著,而 N × S 交互作用对其多有极显著影响。
通过对 ATPS 与 OAS-TL 酶活性方差分析可知,单独施用氮肥或硫肥对提升这两种酶活性的影响不显著,在大蒜生长过程中 N × S 交互作用对幼苗期后大蒜叶片的 ATPS 活性,以及鳞茎膨大中期之前的 OAS-TL 活性均有极显著影响。
| 表2 不同处理对大蒜叶片中氮硫关键同化酶影响的方差分析 (F 值) Table 2 ANOVA analysis of the N and S treatments on activities of key enzymes in garlic leaves (F value) |
 |
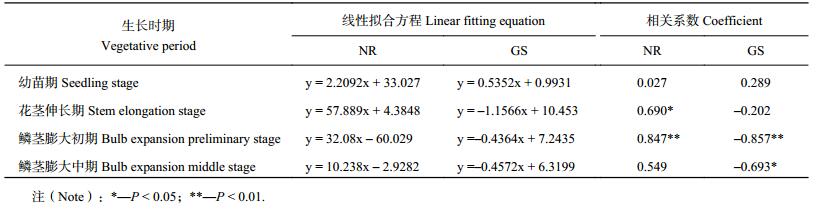
由表 3可见,大蒜生长过程中,NR 活性与氮含量呈正相关关系,而 GS 整体为负相关关系。幼苗期,NR 活性与植株氮含量相关性不显著,相关系数仅为 0.027,在花茎伸长期与鳞茎膨大初期为显著性相关,Pearson 系数分别为 0.690、0.847。在幼苗期和花茎伸长期,GS 活性与氮含量相关性不显著,鳞茎膨大初期、中期为显著性关系,相关系数分别为 –0.857、–0.693。由此可知,NR 对大蒜植株氮同化为正向调控,GS 表现为负向调控。
| 表3 不同生长时期 NR、GS 活性与植株氮含量线性拟合方程及其相关系数 Table 3 Liner fitting equation and Pearson correlation coefficient between the NR and GS activities and nitrogen contents |
 |
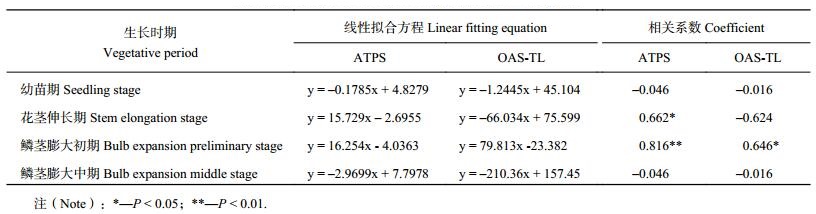
由表 4可见,大蒜幼苗期 ATPS、OAS-TL 与植株硫含量间无显著关系,ATPS 活性与硫含量整体呈正相关关系,而 OAS-TL 整体为负相关关系。ATPS 在花茎伸长期与鳞茎膨大初期为显著性相关,Pearson 系数分别为 0.662、0.816。OAS-TL 在鳞茎膨大初期为显著性关系,Pearson 系数为 0.646;虽然在花茎伸长期未呈现显著性关系,但相关性系数较高,且为负相关关系。
| 表4 不同生长时期 ATPS、OAS-TL 活性与植株硫含量的线性拟合方程及 Pearson 系数 Table 4 Linear fitting equation and Pearson correlation coefficient between the ATPS and OAS-TL activities and sulfur contents at different growth stages of garlic |
 |
硝酸还原酶 (NR) 作为氮同化的第一个步骤,是氮同化的关键限速酶之一[21]。植物硫素同化过程先由 ATP 提供能量,ATP 硫酸化酶催化 SO42- 生成 APS (5’-腺苷磷酸硫酸) 是硫同化的第一步[22]。OAS-TL 催化硫化物与乙酰丝氨酸 (OAS) 反应合成 Cys;半胱氨酸合成是硫同化的最后一个步骤[23–24]。
由结果分析已知,氮素总体呈上升趋势,以鳞茎膨大期上升幅度最大;而 NR 与 GS 活性在大蒜生长过程中均呈先上升后下降趋势,且在花茎伸长期、鳞茎膨大初期酶活性整体水平最高。硫含量整体呈先上升后平稳特征,ATPS 活性在花茎伸长期最大,而 OAS-TL 活性变化则相反,以该时期酶活性最低。分析认为 NR、ATPS 等酶活性的提高增加了植株氮、硫同化能力的提升,而 GS、OAS-TL 则可能是通过降低酶活性促进硫的同化。
氮硫的供应显著影响植株对氮、硫的同化,以及相关代谢酶活性。研究表明,硫素的施用不仅能够激活 ATP 硫化酶的活性,而且能够增强硝酸还原酶活性,同时增加叶片中的可溶性蛋白与叶绿素含量[25]。Fazili 等[26]研究氮硫交互作用对油菜氮同化的影响,认为与仅施用氮肥相比,增加硫的施用量能够通过提高 NR 活性而增强氮素同化能力。刘忠松等[14]认为,大葱在低硫和氮素充足供应条件下 ATPS 和 OAS-TL 活性最大,高硫条件下硫关键同化酶活性则相对减小。
在大蒜生长过程中,叶片中氮、硫关键同化酶活性整体呈先上升后下降趋势,且在各生长阶段,氮硫互作对酶活性影响不一。提高氮素供给量,可以提高 NR 活性,但在高氮条件下则抑制该酶活性;增加硫的供给,也提高 NR 活性。氮、硫单一元素对 GS 活性无显著影响,而两元素间交互作用影响甚为明显。氮、硫单一元素对硫关键同化酶无显著影响,而交互作用则起到显著作用。氮硫之间交互协同作用的分子机制尚不完全明晰。Koprivova 等[27]认为氮-硫同化途径存在密切交互作用,试验证实在营养液中增加 NH4+ 能够提高合成蛋白质的氨基酸合成量;OAS 是合成半胱氨酸限速步骤,被认为是联系氮硫互作关系路径的重要中间产物,OAS 在硫酸盐和硝酸盐同化过程中起到协调作用。OAS 增加不仅能够提升硫的吸收,而且提高 APR 活性以及 mRNA 水平,OAS 在此过程中具有重要作用[28]。
氮、硫两元素间互作关系复杂,若明晰这一机制,尚需从关键中间产物合成量、关键酶基因表达量着手,特别是转录水平与代谢组学方面进行系统阐述。综合分析可知,大蒜在鳞茎膨大期前,能够通过氮、硫配施的互作关系调控关键同化酶活性而影响氮、硫同化;而在鳞茎膨大期,可以通过单一施肥达到调控大蒜植株氮或硫含量的目的。
| [1] | Marschner H. Mineral nutrition of higher plants [M]. Amsterdam: Elsevier Press, 2012. |
| [2] |
吴魏, 赵军. 植物对氮素吸收利用的研究进展[J].
中国农学通报, 2010, 26(13): 75–78.
Wu W, Zhao J. Advances on plants’ nitrogen assimilation and utilization[J]. Chinese Agricultural Science Bulletin, 2010, 26(13): 75–78. |
| [3] |
李国强, 朱云集, 沈学善. 植物硫素同化途径及其调控[J].
植物生理学通讯, 2005, 41(6): 699–704.
Li G Q, Zhu Y J, Shen X S. Plants sulphur assimilation pathways and its regulation[J]. Plant Physiology Communications, 2005, 41(6): 699–704. |
| [4] |
吴宇, 高蕾, 曹民杰, 等. 植物硫营养代谢、调控与生物学功能[J].
植物学通报, 2007, 24(6): 735–761.
W u Y, Gao L, Cao M J, et al. Plant sulfur metabolism, regulation, and biological functions[J]. Chinese Bulletin of Botany, 2007, 24(6): 735–761. |
| [5] |
谢瑞芝, 董树亭, 胡昌浩. 植物硫素营养研究进展[J].
中国农学通报, 2002, 18(2): 65–69.
Xie R Z, Dong S T, Hu C H. Research progress in sulfur plant nutrient[J]. Chinese Agricultural Science Bulletin, 2002, 18(2): 65–69. |
| [6] |
许真, 严永哲, 卢钢, 等. 葱属蔬菜植物风味前体物质的合成途径及调节机制[J].
细胞生物学杂志, 2007, 29(4): 508–512.
Xu Z, Yan Y Z, Lu G, et al. The biosynthetic pathways of flavor precursors and its control in alliums[J]. Chinese Journal of Cell Biology, 2007, 29(4): 508–512. |
| [7] | Salvagiotti F, Julio M, Miralles D J, et al. Sulfur fertilization improves nitrogen use efficiency in wheat by increasing nitrogen uptake[J]. Field Crops Research, 2009, 113(2): 170–177. DOI:10.1016/j.fcr.2009.05.003 |
| [8] | Tatjana B, Zdenko R. Nitrogen and sulfur uptake and remobilization in canola genotypes with varied N- and S-use efficiency differ at vegetative and maturity stages[J]. Crop and Pasture Science, 2011, 62(4): 299–312. DOI:10.1071/CP10272 |
| [9] |
蔡铁, 王振林, 尹燕枰. 氮硫配施对小麦籽粒谷蛋白大聚合体含量及粒度分布的影响[J].
作物学报, 2011, 37(6): 1060–1068.
Cai T, Wang Z L, Yin Y P. Combined effects of nitrogen and sulphur fertilization on content and size distribution of glutenin macropolymer in wheat grain[J]. Acta Agronomica Sinica, 2011, 37(6): 1060–1068. DOI:10.3724/SP.J.1006.2011.01060 |
| [10] |
朱云集, 李国强, 郭天财, 等. 硫对不同氮水平下小麦旗叶氮硫同化关键酶活性及产量的影响[J].
作物学报, 2007, 33(7): 1116–1121.
Zhu Y J, Li G Q, Guo T C, et al. Effects of sulfur on key enzyme activities involved in nitrogen and sulphur assimilation in flag leaves and grain yield under different nitrogen levels in winter wheat (Triticum aestivum L.)[J]. Acta Agronomica Sinica, 2007, 33(7): 1116–1121. |
| [11] |
谢瑞芝, 董树亭, 胡昌浩, 等. 氮硫互作对玉米籽粒营养品质的影响[J].
中国农业科学, 2003, 36(3): 263–268.
Xie R Z, Dong S T, Hu C H, et al. Influence of nitrogen and sulfur interaction on grain quality of maize[J]. Scientia Agricultura Sinica, 2003, 36(3): 263–268. |
| [12] | Al-Redhaiman K N, Helal M I D, Shahin R R. Effect of sulfur blended N-fertilizers and nitrogen use efficiency and quality of lettuce yield[J]. Pakistan Journal of Biological Science, 2003, 6(16): 1408–1412. |
| [13] |
孔灵君, 徐坤, 何平, 等. 氮硫互作对大葱氮、磷、钾、硫吸收分配特性的影响[J].
植物营养与肥料学报, 2014, 20(1): 172–178.
Kong L J, Xu K, He P, et al. Influence of interaction between nitrogen and sulfur on N, P, K and S absorption and distribution of Chinese spring onion[J]. Journal of Plant Nutrition and Fertilizer, 2014, 20(1): 172–178. |
| [14] |
刘松忠, 陈清, 冯固, 等. 氮硫供应对大葱含硫有机物及其代谢关键酶活性的影响[J].
西北农业学报, 2010, 19(6): 148–152.
Liu S Z, Chen Q, Feng G, et al. Effects of nitrogen and sulfur supply on sulfur-containing compounds and activities of key enzymes for sulfur metabolism in Chinese spring onion[J]. Acta Agriculturae Boreali -occidentalis Sinica, 2010, 19(6): 148–152. |
| [15] |
李合生, 孙群, 赵世杰, 等. 植物生理生化实验原理和技术[M]. 北京: 高等教育出版社, 2000.
Li H S, Sun Q, Zhao S J,et al. The experiment principle and technology of plant physiology[M]. Beijing: Higher Education Press, 2000. |
| [16] |
赵世杰, 刘华山, 董新纯. 植物生理学实验指导[M]. 北京: 中国农业科技出版社, 1998.
Zhao S J, Liu H S, Dong X C. Techniques of plant physiological experiment [M]. Beijing: China Agricultural Science and Technology Press, 1998. |
| [17] | Ahmad S, Fazli I S, Jamal A, et al. Interactive effect of sulfur and nitrogen on nitrate reductase and ATP-sulfurylase activities in relation to seed yield fromPsoralea corylifolia L.[J]. Journal of Plant Biology, 2007, 50(3): 351–357. DOI:10.1007/BF03030666 |
| [18] | Demosthenis C, Krishnan B. Sulfur assimilation in soybean: Molecular cloning and character of O-acetylserine(thiol)lyase(cysteine synthase)[J]. Crop Science, 2003, 43(9): 1819–1827. |
| [19] |
GB50095-2010. 食品中蛋白质的测定[S].
GB50095-2010. Determination of protein in foods [S]. |
| [20] |
中国土壤学会农业化学专业委员会. 土壤农业化学常规分析方法[M]. 北京: 科学出版社, 1983.
Agricultural Chemistry Committee of Chinese Soil Society. Analysis methods of soil and agricultural chemistry [M]. Bejing: Science Press, 1983. |
| [21] | Hewitt R H. Crop physiology [M]. Wageningen, The Netherlands: Pudoc Press, 1980. |
| [22] | Leustek T, Martin M N, Bick J A, et al. Pathways and regulation of sulfur metabolism revealed through molecular and genetic studies. Annual Review of Plant Physiology and Plant[J]. Molecular Biology, 2000, 51: 141–159. |
| [23] | Saito K. Regulation of sulfate transport and synthesis of sulfur-containing amino acids[J]. Current Opinion in Plant Biology, 2000, 3: 188–195. |
| [24] | Luo J, Wu W J, Zhou B J, et al. Expression and purification of ATP sulfurylase from Saccharomyces cerevisias in Escherichia coli and its application in Pyro-sequencing[J]. Chinese Journal of Biotechnology, 2007, 23(4): 623–627. DOI:10.1016/S1872-2075(07)60042-9 |
| [25] | Arshad J, Inayat S F, Saif A, et al. Effect of sulfur on nitrate reductase and ATP sulfurylase activities in groundnut (Arachis hypogea L.)[J]. Journal of Plant Biology, 2006, 49(6): 513–517. DOI:10.1007/BF03031134 |
| [26] | Fazili I S, Jamal A, Ahmad S, et al. Interactive effect of sulfur and nitrogen on nitrogen accumulation and harvest in oilseed crops differing in nitrogen assimilation potential[J]. Journal of Plant Nutrition, 2008, 31(7): 1203–1220. DOI:10.1080/01904160802134905 |
| [27] | Koprivova A, Suter M, Opden C R, et al. Regulation of sulfate assimilation by nitrogen inArabidopsis[J]. Physiologia Plantarum, 2000, 122(3): 737–746. |
| [28] | Hesse H, Trachsel N, Suter M, et al. Effect of glucose on assimilatory sulphate reduction inArabidopsis thaliana roots[J]. Journal of Experiment Botany, 2003, 54(388): 1701–1709. |
 2017, Vol. 23
2017, Vol. 23  doi:
doi: 

