文章信息
- 呋喹替尼联合信迪利单抗治疗晚期微卫星稳定型结直肠癌疗效观察
- Efficacy and Safety of Fruquintinib Combined with Sintilimab in Treatment of Advanced Microsatellite Stable Colorectal Cancer
- 肿瘤防治研究, 2023, 50(12): 1227-1231
- Cancer Research on Prevention and Treatment, 2023, 50(12): 1227-1231
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2023.23.0578
- 收稿日期: 2023-05-30
- 修回日期: 2023-09-10
2. 430000 武汉,武汉科技大学附属普仁医院肿瘤科
2. Department of Oncology, Puren Hospital Affiliated to Wuhan University of Science and Technology, Wuhan 430000, China
结直肠癌(colorectal cancer, CRC)作为临床常见消化道恶性肿瘤之一,其发病率位列全球恶性肿瘤第三,病死率位列全球第二[1]。CRC发病隐匿,确诊时多为局部晚期或已发生远处转移,大部分患者失去了手术机会,5年总生存率(OS)不足15%[2-4]。近年来,免疫检查点抑制剂已广泛地应用于治疗各类肿瘤[5-7]。微卫星高度不稳定型(microsatellite height instability, MSI-H)CRC对免疫检查点抑制剂敏感,但这部分患者仅占CRC的5%;95%CRC为微卫星稳定型(microsatellite-stable, MSS)[8],这部分患者肿瘤淋巴细胞浸润水平和肿瘤突变负荷(tumor mutational burden, TMB)低[9],其免疫微环境特征为免疫豁免型及免疫荒漠型,对免疫检查点抑制剂治疗不敏感。REGONIVO研究显示,小分子酪氨酸激酶抑制剂瑞戈非尼联合抗程序性死亡受体1(programmed death 1, PD-1)免疫检查点抑制剂纳武利尤单抗治疗MSS型CRC患者客观缓解率(ORR)为33%[10],这为免疫检查点抑制剂治疗晚期MSS型结直肠癌患者提供了新思路。呋喹替尼是我国自主研发的小分子酪氨酸激酶抑制剂,FRESCO研究结果显示,呋喹替尼单药三线治疗转移性结直肠癌(metastatic colorectal cancer, mCRC)的ORR为4.7%,疾病控制率(DCR)为62.2%,显著高于安慰剂组的12.3%[11]。信迪利单抗是具有高亲和力、持久稳定、靶点占位率高等特点的抗PD-1免疫检查点抑制剂,在我国已获批用于淋巴瘤、肺癌、食管癌等癌种的治疗。
基于此,本研究旨在探讨呋喹替尼联合信迪利单抗相较呋喹替尼单药在晚期MSS型CRC患者临床疗效,为晚期MSS型CRC患者寻找新的治疗方案提供临床参考。
1 资料与方法 1.1 临床资料回顾性选择2020年10月—2022年1月武汉科技大学附属普仁医院肿瘤科收治的44例晚期MSS型结直肠癌患者作为研究对象,据治疗方案分为呋喹替尼单药组22例和信迪利单抗联合呋喹替尼组22例。诊断标准:依据《中国结直肠癌诊疗规范2019版》并通过影像学、组织病理检查、临床和实验室检查确诊。病例纳入标准:(1)年龄≥18岁;(2)影像学明确为转移性CRC且至少有1个可测量病灶;(3)体力状况依据美国东部肿瘤协作组(ECOG)评分为0~2分;(4)既往接受含氟尿嘧啶、奥沙利铂、伊立替康联合或不联合贝伐珠单抗、西妥昔单抗方案治疗失败或出现不可耐受毒性;(5)患者签署知情同意书。病例排除标准:(1)有严重肝肾功能异常、凝血功能障碍、心脏病及脑血管病者;(2)合并其他种类恶性肿瘤者;(3)患者存在精神或者认知障碍。
1.2 方法 1.2.1 治疗方法呋喹替尼单药组:口服呋喹替尼胶囊[和记黄浦医药(上海)有限公司,5毫克/片,国药准字H20180016],5毫克/天,1次/天,服用3周停药1周,4周为一个周期。呋喹替尼联合信迪利单抗组:静脉滴注信迪利单抗注射液[信达生物制药(苏州)有限公司,100毫克/支,国药准字S20180016],第一天200毫克,1次/3周,3周为一个周期;呋喹替尼服用方案同单药组。治疗直至疾病进展或因不可耐受不良反应停药或患者死亡。
1.2.2 客观疗效评价每8~12周通过影像学进行1次评估,包括计算机断层扫描(CT)或磁共振成像(MRI)扫描。根据实体瘤疗效评价标准1.1版(response evaluation criteria in solid tumors 1.1, RECIST 1.1)进行客观疗效评估。分为完全缓解(CR)、部分缓解(PR)、病情稳定(SD)和疾病进展(PD)。ORR=CR+PR。DCR为CR、PR和SD三者总和所占的比例。
1.2.3 生存分析无进展生存期(PFS)指首次用药至肿瘤进展的时间。
1.2.4 安全性评价根据美国国立癌症研究所常见毒性分级标准(4.0版)进行不良反应分级。将不良反应严重程度分为1~5级,1级表示轻度不良反应,2级表示中度不良反应,3级表示重度不良反应,4级表示危及生命、需紧急治疗的不良反应,5级表示死亡。
1.2.5 随访通过电话随访或查询住院记录对患者进行观察并记录相关资料,每月1次,随访时间截至2022年3月31日。
1.3 统计学方法应用SPSS27.0统计软件进行数据处理,计数资料以相对数表示,组间比较采用χ2检验或Fisher' s精确检验。运用Kaplan-Meier生存分析方法分析PFS,并采用Log rank法进行检验。P < 0.05为差异有统计学意义。
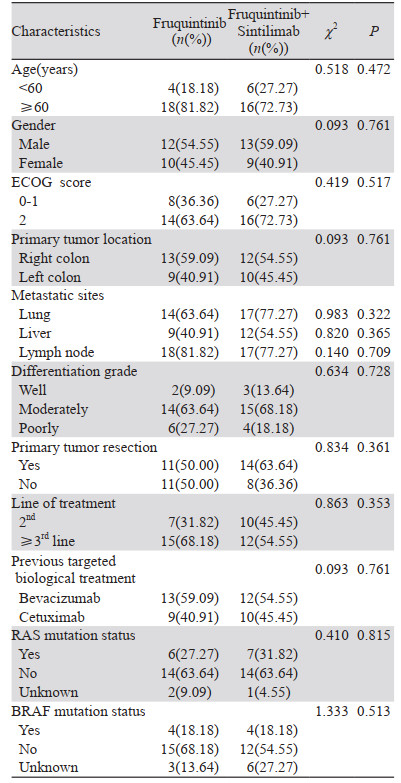
2 结果 2.1 临床特征本研究共纳入44例晚期MSS型CRC患者。比较两组患者年龄、性别、ECOG评分、转移部位、病理特征、原发肿瘤位置、原发病灶切除、既往化疗线数、既往靶向药使用、KRAS类型、BRAF类型比较,两组差异均无统计学意义(P > 0.05),具有可比性,见表 1。
|
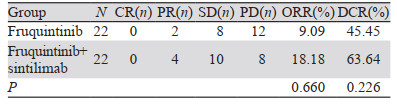
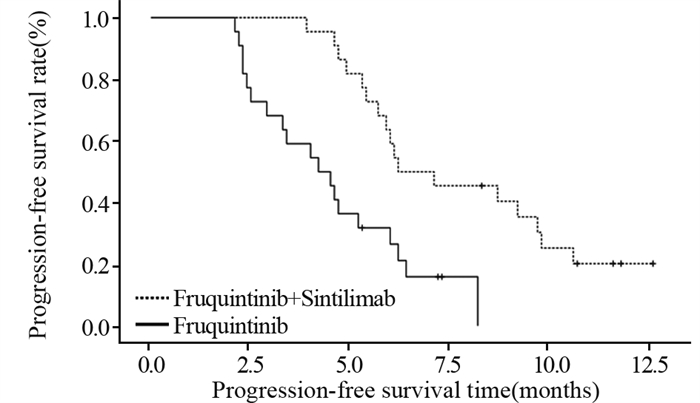
呋喹替尼单药组ORR为9.09%,DCR为45.45%。呋喹替尼联合信迪利单抗组ORR为18.18%,DCR为63.64%,两组差异无明显统计学意义,见表 2。呋喹替尼单药组中位PFS为4.4个月,呋喹替尼联合信迪利单抗组患者中位PFS为6.7个月,两组比较差异有统计学意义(χ2=4.372, P=0.037),见图 1。
|
|
| 图 1 呋喹替尼单药或联合信迪利单抗治疗晚期MSS型CRC患者无进展生存期Kaplan-Meier曲线图 Figure 1 Kaplan-Meier curves of PFS of patients with MSS CRC treated with fruquintinib alone or fruquintinib in combination with sintilimab |
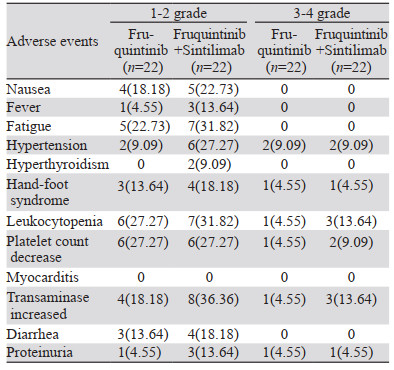
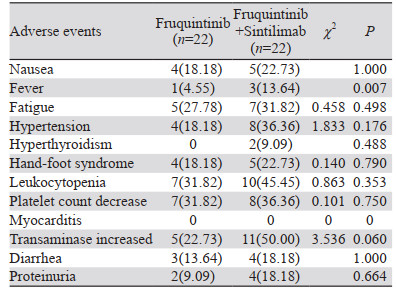
呋喹替尼联合信迪利单抗组患者治疗期间出现的主要不良反应是转氨酶升高、白细胞减少、血小板减少、高血压等。呋喹替尼单药组主要不良反应是白细胞减少、血小板减少、乏力、转氨酶升高等。两组患者中多数不良反应为1~2级,3~4级少见,见表 3。两组患者总不良反应发生率差异均无统计学意义(P > 0.05),所有不良反应经对症治疗均好转,见表 4。
|
|
MSS型结直肠癌约占mCRC的95%,其免疫微环境特征以免疫豁免型和免疫荒漠型为主,肿瘤淋巴细胞浸润水平和TMB低,抗PD-1/PD-L1免疫检查点抑制剂单药治疗基本无效,但如果联合放化疗、小分子酪氨酸激酶抑制剂,因后者可调节免疫原性,因此可能获得较好的治疗效果。
晚期结直肠癌经标准一线治疗失败后,对于体力状况较好的患者,临床多主张继续采取以靶向治疗+FOLFOX/FOLFIRI为主的二线治疗[12]。KEYNOTE 016研究表明,MSS型转移性结直肠癌对单一免疫检查点抑制剂基本无效[13],如何增强MSS型结直肠癌患者的免疫原性是临床重要研究方向。REGONIVO研究是探讨瑞戈非尼联合纳武利尤单抗治疗难治性MSS型结直肠癌和胃癌的探索性Ⅰb期研究,其中24例MSS晚期结直肠癌患者,ORR高达33%,mPFS为7.9个月,为今后晚期MSS型肿瘤的治疗提供新的思路。中国REGOTORI研究探讨了瑞戈非尼联合特瑞普利单抗治疗中39例患者的mOS为15.5个月,ORR为15.2%,DCR为36.4%[14],且不良反应可控。REGOMUNE研究探讨评价瑞戈非尼联合阿维鲁单抗在实体肿瘤患者中的疗效,结果显示mPFS为3.6个月,mOS为10.8个月[15]。根据CONCUR研究,瑞戈非尼单药治疗晚期结直肠癌mPFS为3.2个月,mOS为8.8个月[16],而FRESCO研究则显示呋喹替尼具有与瑞戈非尼相当的疗效。目前信迪利单抗已应用于食管癌、胃癌等消化道肿瘤的一线治疗,作为最早进入国家医保目录的抗PD-1免疫治疗药,信迪利单抗在价格和费用上具有明显的优势。
本研究显示呋喹替尼联合信迪利单抗治疗晚期MSS型结直肠癌的ORR为18.18%,DCR为63.64%,中位PFS为6.7个月,均好于呋喹替尼单药治疗组,但两组差异无统计学意义(P > 0.05),分析可能与两组患者基线特征不平衡、样本量较少等因素有关。联合组中位PFS显著高于单药组,提示小分子酪氨酸激酶抑制剂呋喹替尼与免疫检查点抑制剂信迪利单抗具有协同增效的作用,这也为抗血管生成药物联合免疫治疗改善肿瘤微环境中的免疫原性提供了证据支持。
相较于呋喹替尼单药治疗,呋喹替尼联合信迪利单抗治疗在为患者带来临床获益的同时也展现出良好的安全性。本研究与多项关于瑞戈非尼联合PD-1治疗晚期CRC患者的前瞻性研究[10, 14-15]结果相比,不良事件发生率类似,且手足综合征发生率更低。这可能与所使用小分子酪氨酸激酶抑制剂剂量及种类不同有关。
综上所述,本研究结果表明呋喹替尼联合信迪利单抗可给晚期MSS型CRC患者带来显著的临床获益,且具有良好的安全性。但由于本研究是回顾性研究,样本量较小,其结果有待大样本的前瞻性随机对照研究证实。
利益冲突声明:
所有作者均声明不存在利益冲突。
作者贡献:
李杉:选题设计、资料与数据收集、文章撰写和修改
柳艳飞:选题设计、数据收集
刘倩、何为、金红艳:指导选题设计、文章写作及修改
刘燕妮:数据收集
| [1] |
Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries[J]. CA Cancer J Clin, 2021, 71(3): 209-249. DOI:10.3322/caac.21660 |
| [2] |
Li X, Zhou Y, Luo Z, et al. The impact of screening on the survival of colorectal cancer in Shanghai, China: a population based study[J]. BMC Public Health, 2019, 19(1): 1016. DOI:10.1186/s12889-019-7318-8 |
| [3] |
Lee YH, Kung PT, Wang YH, et al. Effect of length of time from diagnosis to treatment on colorectal cancer survival: A population-based study[J]. PLoS One, 2019, 14(1): e0210465. DOI:10.1371/journal.pone.0210465 |
| [4] |
曹毛毛, 陈万青. 中国恶性肿瘤流行情况及防控现状[J]. 中国肿瘤临床, 2019, 46(3): 145-149. [Cao MM, Chen WQ. Epidemiology of cancer in China and the current status of prevention and control[J]. Zhongguo Zhong Liu Lin Chuang, 2019, 46(3): 145-149.] |
| [5] |
Maio M, Scherpereel A, Calabrò L, et al. Tremelimumab as second-line or third-line treatment in relapsed malignant mesothelioma (DETERMINE): a multicentre, international, randomised, double-blind, placebo-controlled phase 2b trial[J]. Lancet Oncol, 2017, 18(9): 1261-1273. DOI:10.1016/S1470-2045(17)30446-1 |
| [6] |
Galsky M, Arija J, Bamias A, et al. Atezolizumab with or without chemotherapy in metastatic urothelial cancer (IMvigor130): a multicentre, randomised, placebo-controlled phase 3 trial[J]. Lancet, 2020, 395(10236): 1547-1557. DOI:10.1016/S0140-6736(20)30230-0 |
| [7] |
André T, Shiu KK, Kim TW, et al. Pembrolizumab in Microsatellite-Instability-High Advanced Colorectal Cancer[J]. N Engl J Med, 2020, 383(23): 2207-2218. DOI:10.1056/NEJMoa2017699 |
| [8] |
南鹏, 李春晓, 孙芳洲, 等. 食管癌化疗耐药相关基因的初步筛选及其临床意义[J]. 解放军医学杂志, 2019, 44(3): 222-227. [Nan P, Li CX, Sun FZ, et al. Preliminary screening of chemotherapy-resistant genes in esophageal cancer and its clinical significance[J]. Jiefangjun Yi Xue Za Zhi, 2019, 44(3): 222-227.] |
| [9] |
Ganesh K, Stadler ZK, Cercek A, et al. Immunotherapy in colorectal cancer: rationale, challenges and potential[J]. Nat Rev Gastroenterol Hepatol, 2019, 16(6): 361-375. DOI:10.1038/s41575-019-0126-x |
| [10] |
Fukuoka S, Hara H, Takahashi N, et al. Regorafenib Plus Nivolumab in Patients With Advanced Gastric or Colorectal Cancer: An Open-Label, Dose-Escalation, and Dose-Expansion Phase Ib Trial (REGONIVO, EPOC1603)[J]. J Clin Oncol, 2020, 38(18): 2053-2061. DOI:10.1200/JCO.19.03296 |
| [11] |
Li J, Qin S, Xu RH, et al. Effect of Fruquintinib vs. Placebo on Overall Survival in Patients With Previously Treated Metastatic Colorectal Cancer: The FRESCO Randomized Clinical Trial[J]. JAMA, 2018, 319(24): 2486-2496. DOI:10.1001/jama.2018.7855 |
| [12] |
Heinemann V, von Weikersthal LF, Decker T, et al. FOLFIRI plus cetuximab versus FOLFIRI plus bevacizumab as first-line treatment for patients with metastatic colorectal cancer (FIRE-3): a randomised, open-label, phase 3 trial[J]. Lancet Oncol, 2014, 15(10): 1065-1075. DOI:10.1016/S1470-2045(14)70330-4 |
| [13] |
Le DT, Uram JN, Wang H, et al. PD-1 Blockade in Tumors with Mismatch-Repair Deficiency[J]. N Engl J Med, 2015, 372(26): 2509-2520. DOI:10.1056/NEJMoa1500596 |
| [14] |
Wang F, He MM, Yao YC, et al. Regorafenib plus toripalimab in patients with metastatic colorectal cancer: a phase Ⅰb/Ⅱ clinical trial and gut microbiome analysis[J]. Cell Rep Med, 2021, 2(9): 100383. DOI:10.1016/j.xcrm.2021.100383 |
| [15] |
Cousin S, Cantarel C, Guegan JP, et al. Regorafenib-Avelumab Combination in Patients with Microsatellite Stable Colorectal Cancer (REGOMUNE): A Single-arm, Open-label, PhaseⅡTrial[J]. Clin Cancer Res, 2021, 27(8): 2139-2147. DOI:10.1158/1078-0432.CCR-20-3416 |
| [16] |
Li J, Qin S, Xu R, et al. Regorafenib plus best supportive care versus placebo plus best supportive care in Asian patients with previously treated metastatic colorectal cancer (CONCUR): a randomised, double-blind, placebo-controlled, phase 3 trial[J]. Lancet Oncol, 2015, 16(6): 619-629. DOI:10.1016/S1470-2045(15)70156-7 |
 2023, Vol. 50
2023, Vol. 50


