文章信息
- LASP1基因对人结直肠癌LOVO细胞增殖、迁移和凋亡的影响及其机制
- Effects and Mechanism of LASP1 on Proliferation, Migration, and Apoptosis of Human Colorectal Cancer LOVO Cells
- 肿瘤防治研究, 2023, 50(10): 955-959
- Cancer Research on Prevention and Treatment, 2023, 50(10): 955-959
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2023.23.0301
- 收稿日期: 2023-03-22
- 修回日期: 2023-06-05
2. 310018 杭州,浙江中医药大学附属第一医院(浙江省中医院)肛肠科
2. Department of Anorectal Diseases, The First Affiliated Hospital of Zhejiang Chinese Medicine University (Zhejiang Provincial Hospital of Chinese Medicine), Hangzhou 310018, China
结直肠癌(colorectal cancer, CRC)是全球常见的消化道恶性肿瘤之一,国际癌症研究机构统计数据显示,CRC发病率在所有肿瘤中位居第三,死亡率仅次于肺癌位居第二[1]。远处侵袭和转移是CRC相关死亡发生的重要原因之一,尽管CRC治疗手段不断发展,转移性结直肠癌患者的疗效和预后仍不理想[2-3]。因此,开发新的分子诊疗手段,防治结直肠癌的转移,对于提高结直肠癌患者长期生存和改善预后意义重大。上皮细胞-间充质转化(EMT)指上皮细胞获得间充质表型的细胞重编程过程,在结直肠癌转移侵袭过程中发挥重要作用[3]。LIM和SH3蛋白1(LASP1)是CRC发展过程中一种转移相关蛋白,可通过介导EMT、诱导癌细胞侵袭性表型影响结直肠癌进展[4]。粘附斑激酶(focal adhesion kinase, FAK)/蛋白激酶B(AKT)可介导结直肠癌细胞EMT促进细胞迁移、侵袭能力[5]。研究报道LASP1可通过诱导FAK/AKT信号通路促进非小肺细胞癌的增殖和侵袭能力[6]。LASP1能否通过FAK/AKT信号通路促进结直肠癌发展、转移还未明确。本研究拟通过体外实验探究LASP1介导FAK/AKT在结直肠癌细胞增殖、迁移侵袭中的作用,以期完善CRC转移的作用机制,为其防治带来新办法。
1 材料与方法 1.1 主要试剂LOVO人结肠癌细胞(赛百慷(上海)生物技术股份有限公司,iCell-h126);pCMV6-ddk-myc、pCMV6-ddk-myc-LASP1、LASP1-siRNA、NC-siRNA(上海吉玛公司合成提供);Lipofectamine 3000试剂(美国Invitrogen抗体公司,L3000-008);DMEM高糖培养基(美国Hyclone试剂公司,SH30243.01);Transwell小室、Basement Membrane Matrix基质胶(美国康宁试剂公司,3422、356234);BCA蛋白定量试剂盒(北京索莱宝科技公司,pc0020);FAK、p-FAK、AKT、p-AKT蛋白抗体(美国Affinity抗体公司,AF6397、AF3398、AF6261、AF0016);LASP1蛋白抗体(美国Abcam抗体公司,ab117806);RIPA裂解液、Tunel细胞凋亡检测试剂盒(上海碧云天生物公司,P0013D、C1090);反转录试剂盒(江苏康为世纪生物公司,CW2569);MTT试剂盒、总RNA提取试剂TRIzol(生工生物工程(上海)公司,E606334-0500、B511311)。
1.2 实验仪器BB150细胞培养箱、Micro17R低温高速离心机(美国Thermo公司);610020-9Q化学发光仪(中国上海勤翔仪器公司);CMaxPlus酶标仪(美国MD公司);CFX Connect实时荧光定量PCR仪(美国BIO RAD公司)。
1.3 细胞转染LOVO细胞使用含10%胎牛血清、1%的青霉素改良的DMEM培养基,置于37℃、5%CO2培养箱中培养。使用Lipofectamine 3000试剂将pCMV6-ddk-myc(空白质粒)、pCMV6-ddk-myc-LASP1(LASP1过表达质粒)、NC-siRNA(sc-37007)(空白沉默质粒)、LASP1-siRNA(sc-105607)(LASP1沉默质粒)转染至LOVO细胞,并根据转染的质粒进行相应分组,分别为pCMV6-NC组、pCMV6-LASP1组、NC-siRNA组、LASP1-siRNA组。
1.4 qRT-PCR检测LASP1基因表达提取各组细胞RNA,反转录PCR进行DNA扩增,实时荧光定量PCR检测LASP1表达。反应条件为变性95℃ 10 min,扩增反应,95℃ 15 s,60℃ 60 s,40次,溶解曲线,95℃ 15 s,60℃ 60 s,95℃ 15 s。采用2-△△CT法对结果进行相对定量分析。引物序列见表 1。
取对数生长期细胞接种于平板。每孔加入10 μl MTT溶液与细胞混合,放回培养箱内孵育24 h后取出。酶标仪测定490 nm处吸光度值,进行细胞存活计算。
1.6 Tunel染色平板接种细胞后用4%多聚甲醛通透细胞。每平板细胞中加入50 μl Tunel检测液,室温下避光孵育1 h。PBS漂洗三次,制片、封片。荧光显微镜下观察拍照并计数Tunel阳性细胞数量。
1.7 Transwell实验Transwell小室放入24孔培养板,细胞加入上层小室,培养箱中培养24 h。取出后,棉签擦掉上室底层细胞。4%多聚甲醛固定下层小室细胞10 min,PBS洗3次,0.1%结晶紫染液染色计数迁移至下室中的细胞数量。30 μl Matrigel稀释液包被Transwell小室后4℃孵育过夜,上室加入细胞,培养箱中培养24 h,棉签擦掉上室底层细胞和剩余Matrigel稀释液,4%多聚甲醛固定10 min,PBS洗3次,0.1%结晶紫染液染色计数侵袭至下室中的细胞数量。
1.8 划痕实验各组细胞接种于平板,200 μl移液器吸头划线创建伤痕,分别24、48 h观察划线内细胞愈合情况,并拍照计数。
1.9 Western blot实验RIPA裂解收集细胞,离心收集底部细胞沉淀。BCA法测定细胞总蛋白浓度,随后转至PVDF膜,5%脱脂奶粉孵育,TBST清洗。加入检测的稀释后的FAK、p-FAK、AKT、p-AKT、LASP1一抗抗体,4℃下摇床振荡孵育过夜。隔天室温下振荡30 min,将上层液体轻轻吸出,TBST清洗3遍。5%脱脂奶粉封闭液稀释,稀释对应二抗抗体振荡孵育1.5 h,TBST清洗。ECL化学发光显影,计算各蛋白相对表达含量。
1.10 统计学方法采用SPSS16.0统计软件进行数据分析,多组间数据比较采用One-way-ANOAY单因素方差分析,组间两两比较采用Tukey检验。所有数据以均值±标准差(x±s)表示,P < 0.05为差异有统计学意义。
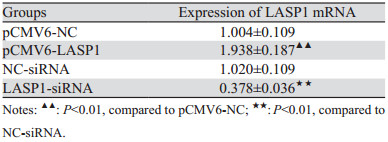
2 结果 2.1 转染结果鉴定与pCMV6-NC组相比,pCMV6-LASP1组细胞LASP1 mRNA表达显著上升(P=0.002)。与NC-siRNA组比较,LASP1-siRNA组细胞LASP1 mRNA表达显著下降(P=0.001),见表 2。结果显示细胞转染成功,可用于后续实验检测。
|
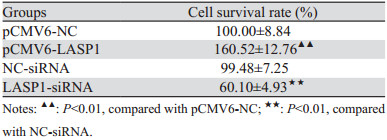
MTT实验结果显示,与pCMV6-NC组相比,pCMV6-LASP1组的细胞存活率显著上升(P=0.000),与NC-siRNA组比较,LASP1-siRNA组的细胞存活率显著下降(P=0.000),见表 3。
|
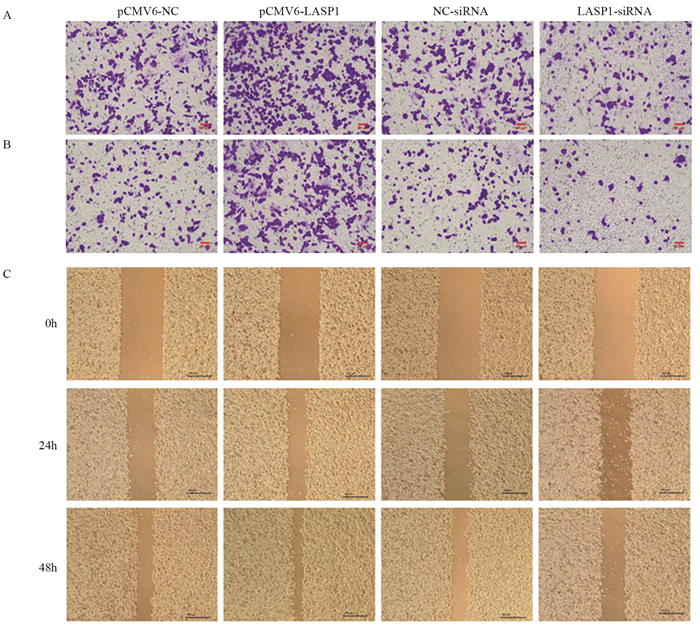
Transwell和划痕实验结果显示,与pCMV6-NC组相比,pCMV6-LASP1组细胞的迁移以及侵袭数量显著上升(分别P=0.003、P=0.000),24和48 h伤口愈合率均显著升高(分别P=0.004、P=0.009);与NC-siRNA组比较,LASP1-siRNA组细胞的迁移以及侵袭数量显著下降(分别P=0.002、P=0.001)、24 h和48 h伤口愈合率均显著降低(P=0.006、P=0.004),见图 1。
|
| A: transwell test detected migration ability of cells; B: transwell test detected invasion ability of cells; C: scratch healing test detected scratch migration ability of cells. 图 1 LASP1过表达或沉默对LOVO细胞迁移及侵袭能力的影响 Figure 1 Effects of LASP1 overexpression or silence on migration and invasion of LOVO cells |
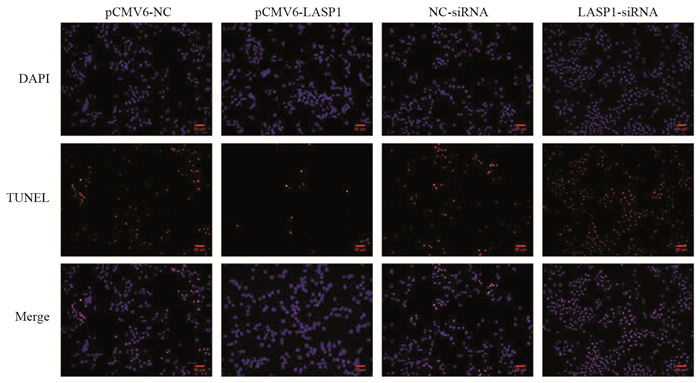
Tunel染色结果显示,与pCMV6-NC组相比,pCMV6-LASP1组细胞凋亡率显著降低(P=0.003);与NC-siRNA组比较,LASP1-siRNA组细胞凋亡率显著升高(P=0.000),见图 2。
|
| 图 2 LASP1过表达或沉默对LOVO细胞凋亡的影响(Tunel染色) Figure 2 Effects of LASP1 overexpression or silence on apoptosis of LOVO Cells (Tunel staining) |
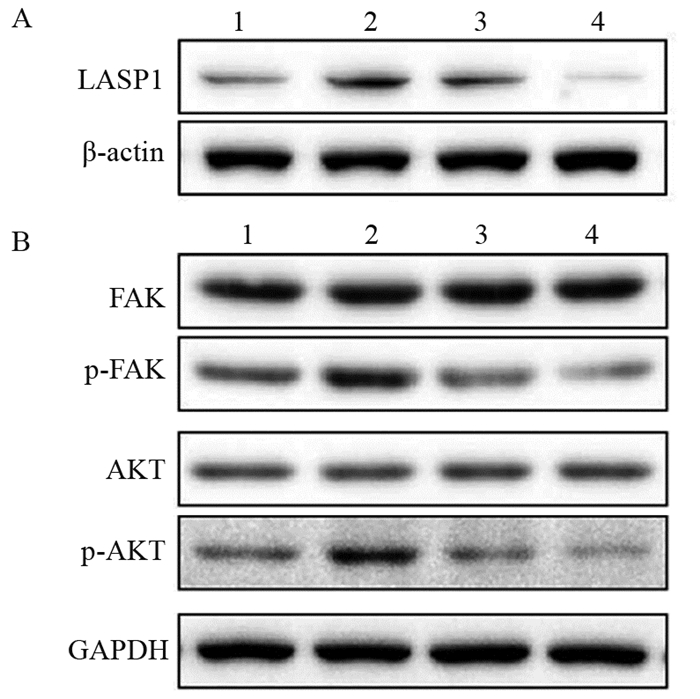
Western blot实验结果显示,与pCMV6-NC组相比,pCMV6-LASP1组细胞LASP1、p-FAK/FAK、p-AKT/AKT蛋白表达显著上升(分别P=0.002、P=0.010、P=0.004);与NC-siRNA组比较,LASP1-siRNA组细胞LASP1、p-FAK/FAT、p-AKT/AKT蛋白表达显著下降(分别P=0.000、P=0.005、P=0.002),见图 3。
|
| 1: pCMV6-NC; 2: pCMV6-LASP1; 3: NC-siRNA; 4: LASP1-siRNA; A: Western blot result of LASP1 protein expression; B: Western blot result of p-FAK/FAK and p-AKT/AKT protein expression. 图 3 LASP1过表达或沉默对LOVO细胞相关蛋白表达的影响 Figure 3 Effects of LASP1 overexpression or silence on related protein expression in LOVO cells |
LASP1基因位于染色体17q11-21.3,属于大肌动蛋白结合神经蛋白家族成员,在人体大部分组织内低表达[7-8]。LASP1的两端为LIM和SH3结构区域,可分别与肌动蛋白和其他信号受体发生作用,参与细胞运动、侵袭等过程[8]。LASP1在晚期结直肠癌组织中表达显著高于早期,可介导EMT促进CRC迁移,而敲除LASP1表达可以抑制CRC的转移侵袭[9]。而在体模型表明,LASP1过表达促进了小鼠结直肠原位肿瘤生长和进展[10]。本研究通过构建LASP1过表达质粒和干扰质粒转染人结肠癌LOVO细胞,通过细胞功能实验检测LASP1不同表达对LOVO细胞的影响,结果与朱龙海等[11]研究相符,表明LASP1基因的表达与结肠癌细胞迁移侵袭相关。
FAK为促转移功能蛋白,磷酸化表达增加可促进CRC细胞EMT及迁移和侵袭能力[12-13]。研究表明,FAK表达降低可抑制CRC细胞与胞外基质粘连作用,进而抑制CRC细胞迁移[14]。AKT相关通路为调节细胞生长、增殖和抗凋亡的重要通路,结直肠癌出现淋巴结转移、浆膜层浸润以及肿瘤低分化患者其癌组织p-AKT表达显著升高,p-AKT表达与CRC发展、预后相关[15]。Xu等研究表明FAK蛋白与AKT蛋白可相互作用,敲减CRC细胞FAK表达可抑制p-AKT表达,从而抑制CRC细胞干细胞样特性与转移能力[16]。其他相关研究表明,FAK/AKT信号通路激活,可增强CRC细胞迁移、侵袭能力和EMT[5, 17]。Zhou等研究结果表明LASP1可通过激活AKT促进CRC进展[18]。本研究结果表明,LASP1可调控CRC细胞中FAK/AKT信号通路的表达,由此推测LASP1可介导FAK/AKT信号通路参与CRC细胞增殖、迁移及侵袭过程。
综上,本研究结果表明LASP1基因表达促进了LOVO细胞增殖、迁移和侵袭能,而敲减LOVO细胞LASP1表达起相反作用,LASP1介导FAK/AKT通路表达是其促进CRC发展机制之一。由于本课题组条件有限,未能进行动物模型实验进一步研究LASP1介导FAK/AKT表达对CRC进展的影响。以后我们将继续探索LASP1介导FAK/AKT调控CRC进展的机制,为临床防治CRC转移提供新的方向。
利益冲突声明:
所有作者均声明不存在利益冲突。
作者贡献:
徐益平:数据分析及文章撰写与修改
尚韬:实验思路构思及指导
| [1] |
Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries[J]. CA Cancer J Clin, 2021, 71(3): 209-249. DOI:10.3322/caac.21660 |
| [2] |
田传鑫, 赵磊. 结直肠癌及结直肠癌肝转移流行病学特点[J]. 中华肿瘤防治杂志, 2021, 28(13): 1033-1038. [Tian CX, Zhao L. Epidemiological characteristics of colorectal cancer and colorectal liver metastasis[J]. Zhonghua Zhong Liu Fang Zhi Za Zhi, 2021, 28(13): 1033-1038.] |
| [3] |
唐潇潇, 汪源, 李婷婷. HOXB7对结直肠癌细胞侵袭、迁移和EMT作用及机制的研究[J]. 中国病理生理杂志, 2023, 39(1): 20-28. [Tang XX, Wang Y, Li TT. Effects of HOXB7 on migration, invasion and EMT of colorectal cancer cells and its mechanism[J]. Zhongguo Bing Li Sheng Li Za Zhi, 2023, 39(1): 20-28.] |
| [4] |
Yan P, Liu J, Zhou R, et al. LASP1 interacts with N-WASP to activate the Arp2/3 complex and facilitate colorectal cancer metastasis by increasing tumour budding and worsening the pattern of invasion[J]. Oncogene, 2020, 39(35): 5743-5755. DOI:10.1038/s41388-020-01397-7 |
| [5] |
Liu SQ, Xu CY, Wu WH, et al. Sphingosine kinase 1 promotes the metastasis of colorectal cancer by inducing the epithelial-mesenchymal transition mediated by the FAK/AKT/MMPs axis[J]. Int J Oncol, 2019, 54(1): 41-52. |
| [6] |
Zhang X, Liu Y, Fan C, et al. Lasp1 promotes malignant phenotype of non-small-cell lung cancer via inducing phosphorylation of FAK-AKT pathway[J]. Oncotarget, 2017, 8(43): 75102-75113. DOI:10.18632/oncotarget.20527 |
| [7] |
Butt E, Howard CM, Raman D. LASP1 in Cellular Signaling and Gene Expression: More than Just a Cytoskeletal Regulator[J]. Cells, 2022, 11(23): 3817. DOI:10.3390/cells11233817 |
| [8] |
Butt E, Raman D. New Frontiers for the Cytoskeletal Protein LASP1[J]. Front Oncol, 2018, 8: 391. DOI:10.3389/fonc.2018.00391 |
| [9] |
Chen N, Han X, Bai X, et al. LASP1 induces colorectal cancer proliferation and invasiveness through Hippo signaling and Nanog mediated EMT[J]. Am J Transl Res, 2020, 12(10): 6490-6500. |
| [10] |
林创. LASP1诱导巨噬细胞M2极化促进结直肠癌进展的分子机制研究[D]. 南方医科大学, 2022, 1-57. [Lin C. LASP1 promotes colorectal cancer progression by enhancing M2 polarization of macrophages[D]. Southern Medical University, 2022, 1-57.]
|
| [11] |
朱海龙, 朱旭友, 张龙, 等. miR-218-5p靶向LASP1对结直肠癌细胞侵袭和迁移影响的机制[J]. 中华肿瘤防治杂志, 2022, 29(1): 27-33. [Zhu HL, Zhu XY, Zhang L, et al. Mechanism of miR-218-5p targeting LASP1 affecting the invasion and migration of colorectal cancer cells[J]. Zhonghua Zhong Liu Fang Zhi Za Zhi, 2022, 29(1): 27-33.] |
| [12] |
Tan D, Zhang W, Tao Y, et al. PZR promotes metastasis of colorectal cancer through increasing FAK and Src phosphorylation[J]. Acta Biochim Biophys Sin (Shanghai), 2019, 51(4): 356-364. DOI:10.1093/abbs/gmz019 |
| [13] |
Huang YH, Chen HK, Hsu YF, et al. Src-FAK Signaling Mediates Interleukin 6-Induced HCT116 Colorectal Cancer Epithelial-Mesenchymal Transition[J]. Int J Mol Sci, 2023, 24(7): 6650. DOI:10.3390/ijms24076650 |
| [14] |
Amable G, Martínez-León E, Picco ME, et al. Metformin inhibition of colorectal cancer cell migration is associated with rebuilt adherens junctions and FAK downregulation[J]. J Cell Physiol, 2020, 235(11): 8334-8344. DOI:10.1002/jcp.29677 |
| [15] |
冯跃, 张永涛, 夏利锋, 等. PI3K/Akt/mTOR信号通路相关蛋白在结直肠癌中的表达及与临床病理特征和预后的关系[J]. 中国现代医学杂志, 2020, 30(24): 18-23. [Feng Y, Zhang YT, Xia LF, et al. Expression of protein associated with PI3K/Akt/mTOR pathway and its relationship with clinical pathology and prognosis in colorectal cancer[J]. Zhongguo Xian Dai Yi Xue Za Zhi, 2020, 30(24): 18-23.] |
| [16] |
Xu C, Zhang W, Liu C. FAK downregulation suppresses stem-like properties and migration of human colorectal cancer cells[J]. PloS One, 2023, 18(4): e0284871. |
| [17] |
Song G, Xu S, Zhang H, et al. TIMP1 is a prognostic marker for the progression and metastasis of colon cancer through FAK-PI3K/AKT and MAPK pathway[J]. J Exp Clin Cancer Res, 2016, 35(1): 148. |
| [18] |
Zhou R, Shao Z, Liu J, et al. COPS5 and LASP1 synergistically interact to downregulate 14-3-3σ expression and promote colorectal cancer progression via activating PI3K/AKT pathway[J]. Int J Cancer, 2018, 142(9): 1853-1864. |
 2023, Vol. 50
2023, Vol. 50



