文章信息
- 苦龙胆酯苷对热消融不全的残存肝癌干细胞的影响及机制初探
- Effects of Amarogentin on Residual Liver Cancer Stem Cells After Insufficient Thermal Ablation and Related Mechanism
- 肿瘤防治研究, 2023, 50(8): 760-766
- Cancer Research on Prevention and Treatment, 2023, 50(8): 760-766
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2023.22.1528
- 收稿日期: 2022-12-27
- 修回日期: 2023-02-13
2. 400010 重庆,重庆医科大学附属第二医院肝胆外科
2. Department of Hepatobiliary Surgery, the Second Affiliated Hospital of Chongqing Medical University, Chongqing 400010, China
肝癌是世界上恶性程度较高的肿瘤之一,每年数以万计的患者死于肝癌及其相关并发症[1-2]。近年来,射频消融术等热消融技术在临床上越来越多地被应用于肝癌的治疗[3-4]。有报道认为,对于小于5 cm的单发肝癌行射频消融术,患者5年总体生存率并不逊于肝切除术,且具有无创、并发症少和恢复快等优势[5-6]。然而,热消融不足导致残余肝癌的局部复发和远处转移仍然是一个难题。热消融不全的残存肝癌细胞被证实具有更强的增殖、侵袭、转移和耐药等能力,即肿瘤干细胞性蜕变[7-8]。研究报道,不完全射频消融术可促进肝癌细胞中CD133阳性干细胞的发育以及残余肝癌细胞的恶性进展[9-10]。因此,抑制肝癌干细胞生存可能是阻断热消融不全后残余肝癌进展的一种行之有效的方法。
p53作为机体内最重要的抑癌基因,通过激活多条效应通路来抑制肿瘤的发生[11-12]。据报道,过表达p53后可降低肝癌干细胞标志物CD133的表达,并抑制肿瘤的增殖[13-14]。而TBC1D15蛋白可通过影响p53的表达稳定,从而促进肝癌干细胞的分化和增殖[15-16]。可见,激活p53的抑癌作用可能是抑制肝癌干细胞致瘤最直接手段之一。
苦龙胆酯苷(Amarogentin),一种从中草药獐牙菜(Swertia davidiFranch)中提取的生物活性成分[17],不仅能通过提高p53的表达抑制肝癌细胞增殖和促进凋亡,还可作用于肝癌干细胞,抑制其快速增殖和分化,预防肝癌的发生[18-19]。然而,苦龙胆酯苷是否能抑制热消融不全后残余肝癌干细胞的发育及抑制其快速增殖,目前尚不清楚。因此,本研究将观察苦龙胆酯苷对体外热消融不全的残存肝癌干细胞的影响,并对其作用机制进行探索。
1 材料与方法 1.1 细胞肝癌细胞系(HepG2)为重庆市肝胆外科重点实验室保种细胞。
1.2 实验试剂苦龙胆酯苷(溶剂为100%二甲基亚枫)购自成都普思生物科技股份有限公司;兔抗CD133抗体(ab19898,比例1:1 000)、兔抗TBC1D15抗体(ab121396,比例1:1 000)和兔抗磷酸化p53抗体(ab76242,比例1:500)均购于美国Abcam公司;兔抗β-actin抗体(AF5003,比例1:2 000)、辣根过氧化物酶标记山羊抗兔IgG(A0208,比例1:1000)、BCA蛋白浓度测定试剂盒(P0010S)、彩色预染蛋白质分子量标准marker(P0069)和特超敏电化学发光试剂盒(P0018A)均购自江苏碧云天公司;CCK-8法细胞增殖检测试剂盒(KGA317)和Annexin V-FITC/PI双染细胞凋亡检测试剂盒(KGA107)均购自江苏凯基生物公司;组织总RNA提取试剂盒(DP431)、cDNA反转录试剂盒(KR103)和实时荧光定量聚合酶链式反应检测试剂盒(FP209-02)均购自北京天根生化科技公司。
1.3 实验仪器蛋白质垂直凝胶电泳槽系统、蛋白凝胶成像仪、荧光定量聚合酶链式反应仪为美国Bio-Rad公司产品,酶标仪为德国Eppendorf公司产品,流式细胞仪为美国BD公司产品。
1.4 方法 1.4.1 细胞培养HepG2细胞利用DMEM高糖培养基和10%胎牛血清培养于37℃、含5%CO2以及适合湿度的培养箱中。
1.4.2 肝癌细胞热消融不全的残存模型的建立参考Tan等[10]报道,利用水浴法建立HepG2肝癌细胞热消融不全的残存模型:将HepG2细胞(5×104个)置于6孔板中培养12 h,46℃水中孵育10 min后,继续在37℃培养箱中培养12、24和48 h,流式细胞仪检测CD133阳性细胞比例。
1.4.3 苦龙胆酯苷处理热消融不全的残存HepG2细胞模型建立24 h后,分别加入低(60 µg/ml)、中(120 µg/ml)、高(240 µg/ml)剂量的苦龙胆酯苷继续培养24 h。热消融不全的残存HepG2细胞模型对照组加入等体积的二甲基亚枫后,相同条件下培养24 h。
1.4.4 CCK-8结合酶标仪法检测细胞增殖每5 000个热消融不全的残存HepG2细胞加入到96孔板中,培养24 h后,每孔加入苦龙胆酯苷处理24 h。弃培养基后,每孔加入10 μl的CCK-8试剂和90 μl新鲜培养基,37℃暗室孵育1.5 h后用酶标仪检测吸光度值,检测波长为450 nm。
1.4.5 流式细胞术检测细胞凋亡每1×106个热消融不全的残存HepG2细胞用苦龙胆酯苷处理24 h后,加入500 μl结合缓冲液重悬。依次加入5 μl的Annexin V-FITC抗体和5 μl PI,4℃暗室孵育20 min后上流式细胞仪检测。
1.4.6 实时荧光定量聚合酶链式反应细胞总RNA提取参照试剂盒说明书操作:每1×107个HepG2细胞加入1 ml含有β-巯基乙醇的裂解液进行裂解,加入蛋白酶K消化(56℃ 20 min);12 000 r/min离心,离心5 min后转移至无酶EP管中;等体积无水乙醇溶解、祛除蛋白和DNA后,10 μl无酶水溶解。
cDNA合成:10 µl体系中含1 µl的10×RT Mix、1 µl的Supper pure dNTPs、1 µl的Oligo-(dT)15、0.5 µl的Quant Reverse Transcriptase、1 µg总RNA和无酶水补足至10 µl,反应条件为37℃ 60 min。
qRT-PCR反应,SYBR Green法:20 µl体系中含10 µl 2×Talent qPCR PreMix、0.6 µl正向引物、0.6 µl反向引物,100 ng cDNA和无酶水补足至20 µl;先进行预变性反应:95℃ 3 min,1个循环;然后进行扩增反应:95℃ 5 s和60℃ 15 s,总共40个循环。最后进行半定量分析(2-△△Ct=2-{(Ct目的-Ct内参)对照组-(Ct目的-Ct内参)实验组)。基因的引物序列大小如下:CD133的正义链:5-TTCTTGACCGACTGAGACCCA-3,反义链:5-TCATGTTCTCCAACGCCTCTT-3,大小99 bp;TBC1D15的正义链:5-TGGAAAGACCAATGACCAAGAC-3,反义链:5-TCCACTATTACTTCGGCATCCT-3,大小78 bp和β-actin的正义链:5-CATGTACGTTGCTATCCAGGC-3,反义链:5-CTCCTTAATGTCACGCACGAT-3,大小250 bp。
1.4.7 Western blot法检测蛋白表达细胞总蛋白提取:每1×107个HepG2细胞加入200 µl RIPA裂解,经离心(12 000 r/min×30 min)后获得蛋白上清。
凝胶电泳:采用BCA法测得蛋白浓度,设定每孔60 µg蛋白进行上样;8%~10%凝胶进行电泳(100 V,100~120 min)和转膜(250 mA,90~120 min);封闭后,一抗4℃孵育过夜;二抗室温孵育90 min;电化学发光试剂盒在凝胶成像系统成像。
蛋白表达半定量:Image Lab软件分别测量目的和内参蛋白的灰度值,目的蛋白与内参蛋白的灰度值比值,即为目的蛋白的相对表达量。
1.5 统计学方法本实验数据均为计量资料,以平均值±标准差(x±s)表示,并利用SPSS18.0软件进行统计分析。实验数据比较前均进行方差齐性检验,再采用2×2的析因设计分析。P < 0.05为数据间差异存在统计学意义。
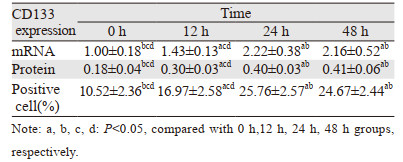
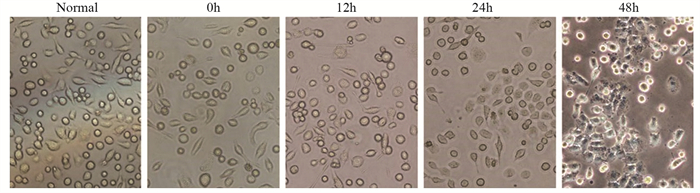
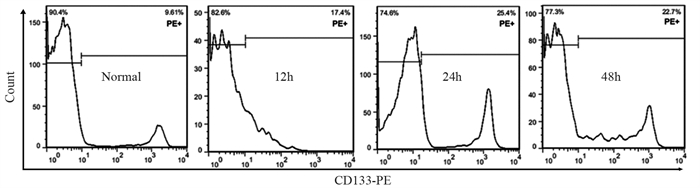
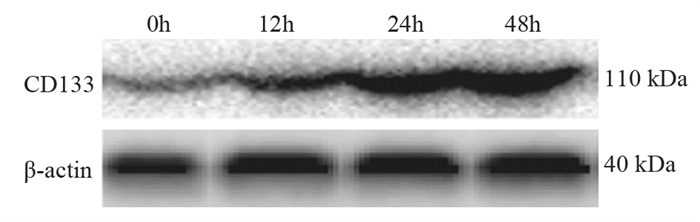
2 结果 2.1 热消融不全可提高残存肝癌干细胞的增生热消融不全残存的HepG2细胞继续培养12、24和48 h后,CD133阳性细胞的比例、CD133的mRNA和蛋白表达水平均显著高于正常的HepG2细胞,见表 1、图 1~3。此外,热消融不全残存的HepG2细胞培养12、24和48 h时,CD133阳性细胞的比例、CD133的mRNA和蛋白表达水平随着时间的延长而升高,但24 h组和48 h组无明显统计学差异,见表 1、图 2~3。说明热消融不全残存的HepG2细胞肝癌干细胞在24~48 h达到平台期。因此,后续热消融不全残存HepG2细胞模型实验均选择继续培养24 h后进行处理。
|
|
| 图 1 显微镜观察HepG2细胞建立热消融不全模型建模前后细胞形态 Figure 1 Morphology of HepG2 cells before and after insufficient thermal ablation |
|
| 图 2 流式细胞仪检测不同时间点热消融不全HepG2细胞模型中CD133阳性细胞的比例 Figure 2 Proportion of CD133-positive cells in insufficient thermal ablation HepG2 cellsat different time points determined by flow cytometry |
|
| 图 3 蛋白印迹法检测不同时间点热消融不全HepG2细胞中CD133蛋白的表达 Figure 3 Expression of CD133 protein in insufficient thermal ablation HepG2 cells at different time points detected by Western blot |
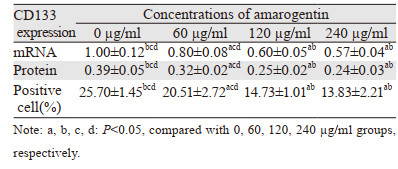
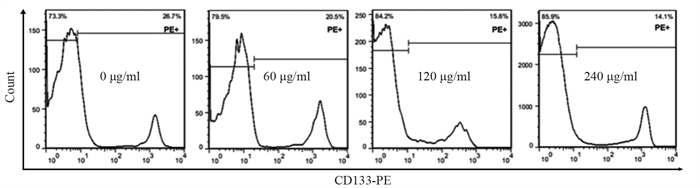
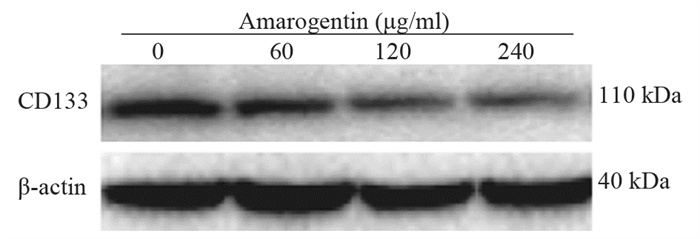
60 µg/ml、120 µg/ml和240 µg/ml的苦龙胆酯苷分别处理热消融不全残存的HepG2细胞24 h后,CD133阳性细胞的比例、CD133的mRNA和蛋白表达水平均显著低于对照组(均P < 0.05),见表 2、图 4~5。此外,随着苦龙胆酯苷作用浓度的升高,CD133阳性细胞的比例、CD133的mRNA和蛋白表达水平随之下降,但120 µg/ml和240 µg/ml组无明显统计学差异,见表 2、图 4~5。这说明,120~240 µg/ml的苦龙胆酯苷处理热消融不全残存的HepG2细胞时,肝癌干细胞的增生处于平台期。因此,后续苦龙胆酯苷处理热消融不全残存HepG2细胞模型的实验中,我们均选择120 µg/ml的浓度进行处理。
|
|
| 图 4 流式细胞仪检测不同浓度苦龙胆酯苷处理的热消融不全HepG2细胞中CD133的比例 Figure 4 Proportion of CD133 in the models of insufficient thermal ablation HepG2 cells after treatment with different concentrations of amarogentin detected by flow cytometry |
|
| 图 5 蛋白印迹法检测不同浓度的苦龙胆酯苷处理热消融不全HepG2细胞后CD133蛋白的表达 Figure 5 Protein expression of CD133 in the models of insufficient thermal ablation HepG2 cells after treatment with different concentrations of amarogentin detected by Western blot |
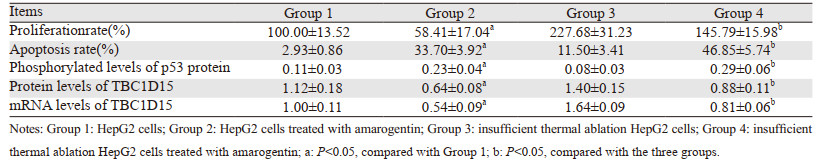
120 µg/ml的苦龙胆酯苷处理HepG2细胞和热消融不全残存的HepG2细胞24 h后,两组HepG2细胞的增殖率显著下降,但消融不全残存的HepG2细胞增殖率被抑制的幅度显著高于HepG2细胞组,见表 3。说明苦龙胆酯苷可抑制热消融不全的残存肝癌细胞的增殖。
|
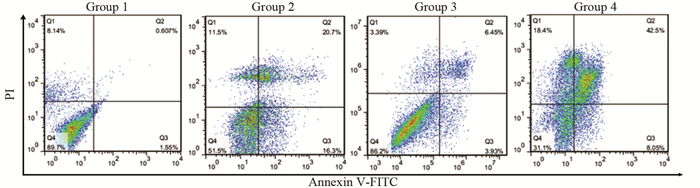
120 µg/ml的苦龙胆酯苷处理热消融不全残存的HepG2细胞24 h后,苦龙胆酯苷可显著促进两组处理后HepG2细胞的凋亡,但处理后消融不全残存的HepG2细胞凋亡率提高的幅度显著高于处理后HepG2细胞组,见表 3、图 6。
|
| 图 6 流式细胞仪检测苦龙胆酯苷对热消融不全HepG2细胞凋亡的影响 Figure 6 Effect of amarogentinon apoptosis of insufficient thermal ablation HepG2 cells determined by flow cytometry |
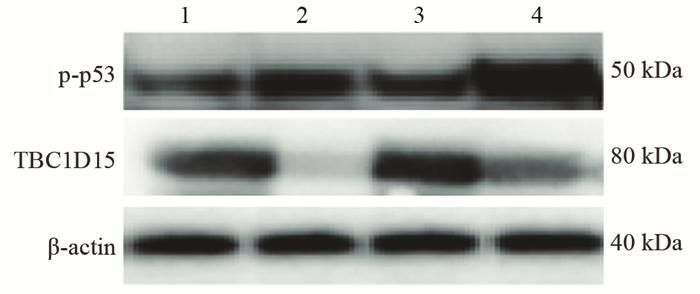
120 µg/ml的苦龙胆酯苷处理热消融不全残存的HepG2细胞24 h后,两组处理后HepG2细胞p53的磷酸化水平均显著提高,但处理后消融不全残存的HepG2细胞中p53磷酸化水平的提高幅度显著高于处理后HepG2细胞组;而两组处理后HepG2细胞中TBC1D15 mRNA和蛋白水平均显著下降,但处理后热消融不全残存的HepG2细胞中TBC1D15的mRNA和蛋白表达下降的幅度显著高于处理后HepG2细胞组,见表 3、图 7。
|
| 1: normal HepG2 cells; 2: normal HepG2 cells treated with amarogentin; 3: insufficient thermal ablation HepG2 cells; 4: insufficient thermal ablation HepG2 cells treated with amarogentin. 图 7 蛋白印迹法检测苦龙胆酯苷对热消融不全HepG2细胞中p53磷酸化水平和TBC1D15蛋白表达的影响 Figure 7 Effect of amarogentinon phosphorylation levels of p53 and protein expression of TBC1D15 in insufficient thermal ablation HepG2 cells determined by Western blot |
热消融不全残存的癌细胞仍是目前射频消融技术在临床上治疗肝癌的主要缺陷之一[20]。对肿瘤直径较大或者不规则生长的肝癌组织进行热消融处理时,热量不足或不均一将导致无法杀灭边缘或者过渡期的癌细胞[21]。相反,热消融不全残存的癌细胞反而会获得更恶性进展[22]。本实验中,亚致死热量处理肝癌细胞后,CD133阳性肝癌细胞的比例明显升高,且增殖率显著高于正常肝癌细胞。Tong等认为热消融不全残存的肝癌细胞表现出更高比例的干细胞样细胞,并具有较高的侵袭、转移和耐药性[23]。而下调肝癌细胞CD133的表达后可抑制热消融不全残存的肝癌细胞的增殖、侵袭和自噬。这可能是亚致死热量处理可促进肝癌细胞形成纺锤状形态并转化为CD133阳性的肝癌干细胞,即热消融不全使得更多的肝癌细胞转化为肝癌干细胞,从而更易局部复发和远处转移[24]。因此,有效地杀伤热消融不全残存的肝癌干细胞无疑是一种遏制残留肝癌恶性进展有效方法。
苦龙胆酯苷抗肿瘤的作用与阻滞肿瘤细胞周期有关,如Pal等报道苦龙胆酯苷通过调节G1/S细胞周期蛋白和诱导细胞凋亡抑制肝癌的生长[25];Zhao等报道苦龙胆酯苷通过阻滞G2/M细胞周期和抑制PI3K/Akt信号通路诱导胃癌细胞凋亡[26]。而Sur等证实苦龙胆酯苷过调控Wnt、hedgehog和表皮生长因子受体途径抑制小鼠体内肝癌干细胞的增殖,从而抑制肝癌细胞的自我更新和增殖能力[19]。这个研究是苦龙胆酯苷抑制肝癌增殖机制的另一种重要的解释,也为治疗热消融残余肝癌的复发和转移提供另一种可能。本研究发现苦龙胆酯苷抑制消融不全残存的HepG2细胞增殖的幅度显著高于正常HepG2细胞组,且促进凋亡的幅度也显著高于正常HepG2细胞组。苦龙胆酯苷抑制热消融不全的残存肝癌细胞的能力可能与减少残存细胞中肝癌干细胞的干性分化相关。
p53作为体内最重要的抑癌基因,可通过激活多种通路抑制肿瘤的发生和发展。Park等报道过表达CD133可拮抗p53的抑制肿瘤细胞增殖作用。此外,该研究还表明p53可通过抑制CD133的表达抑制肿瘤的生长[27]。Xu等报道p53突变型肺癌干细胞的比例远高于野生型[28],可能是突变的p53促进了肿瘤干细胞的增殖和不对称分裂。这些研究提示了p53基因在调控肿瘤干细胞分化及抑制肿瘤生长过程中发挥着重要的作用,提高p53表达可能影响肿瘤干细胞的干性表达。在本实验我们观察到,苦龙胆酯苷显著降低了热消融不全的残存肝癌细胞中CD133阳性细胞的比例,同时提高了p53磷酸化水平和肿瘤细胞的凋亡率。而CD133是肝癌干细胞公认的表面标志物,CD133阳性细胞被发现是一种具有更强增殖能力的祖细胞样癌细胞群。已有报道证实热消融不全会促进肝癌细胞纺锤状形态的改变,促进癌细胞转化为CD133阳性的肝癌干细胞。许多研究也将CD133表达水平作为判断肝癌干细胞的标记。因此,我们推测苦龙胆酯苷的抑瘤作用可能也是通过作用于肝癌干细胞而实现的。
上述研究表明,p53的表达和稳定可影响肿瘤干细胞分化和增殖过程,从而对肿瘤发生及发展进行调节。因此,研究抑制或破坏p53稳定表达的分子机制对靶向抑制肿瘤干细胞的分化和增殖尤其重要。Feldman等报道TBC1D15蛋白通过破坏NUMB内吞适配蛋白(NUMB endocytic adaptor protein, NUMB)与p53的复合物的稳定性来调控肝癌干细胞的自我更新[29];Machida等认为toll样受体4/NANOG途径磷酸化NUMB后,通过蛋白TBC1D15破坏p53的稳定结构而导致p53降解,从而促进肝癌干细胞不对称分裂和增加耐药性[30]。TBC1D15目前被证实主要有两条促肝癌发生的途径[31]:一是通过与人核有丝分裂器蛋白1(nuclear mitotic apparatus protein 1, NuMA1)相互作用干扰肿瘤干细胞不对称分裂机制;二是破坏NuMA1与EvC睫状复合体亚单位2(EvCciliary complex subunit 2, EvC2)形成。后者主要通过诱导的NUMB磷酸化和p53降解。可见,TBC1D15可作为中枢调节器通过降解p53和促进NANOG转录激活促进肝癌干细胞的自我更新、分化和增殖等。因此,TBC1D15可作为肝癌治疗的潜在靶点。本实验发现HepG2细胞中TBC1D15的表达水平与p53磷酸化水平呈相反的趋势,而且利用苦龙胆酯苷处理HepG2细胞后,两组细胞TBC1D15的mRNA和蛋白表达均显著下降,但热消融不全残存的HepG2细胞TBC1D15的mRNA和蛋白表达下降的幅度显著高于正常HepG2细胞组。这与前文观察到苦龙胆酯苷可显著降低热消融不全残存的HepG2细胞中肿瘤干细胞的比例是一致的。由此,我们推断苦龙胆酯苷抑制热消融不全残存肝癌细胞的增殖可能与下调TBC1D15表达,致使p53稳定表达上升,从而抑制肝癌干细胞的干性分化有关。
综上,本实验结果发现,苦龙胆酯苷处理后可显著降低热消融不全的残存肝癌细胞中CD133阳性细胞的比例以及细胞增殖率,并提高肝癌细胞的凋亡率。苦龙胆酯苷抑制热消融不全的残存肝癌干细胞的机制可能与下调TBC1D15表达以及提高p53稳定表达密切相关,这可为进一步在临床上探讨热消融不足导致残余肝癌的局部复发和远处转移的治疗提供新的思路。
利益冲突声明:
所有作者均声明不存在利益冲突。
作者贡献:
刘彦:实验实施、文稿撰写
秦凡博:实验实施
龚建平:数据整理及文章终审
张文锋:数据整理、文章终审及基金支持
| [1] |
Donne R, Lujambio A. The Liver Cancer Immune Microenvironment: Therapeutic Implications for Hepatocellular Carcinoma[J]. Hepatology, 2022, 77(5): 1773-1796. |
| [2] |
Huang AC, Dodge JL, Yao FY, et al. National Experience on Waitlist Outcomes for Down-staging of Hepatocellular Carcinoma: High Dropout Rate in "All-Comers"[J]. Clin Gastroenterol Hepatol, 2023, 21(6): 1581-1589. DOI:10.1016/j.cgh.2022.08.023 |
| [3] |
Deng Q, He M, Fu C, et al. Radiofrequency ablation in the treatment of hepatocellular carcinoma[J]. Int J Hyperthermia, 2022, 39(1): 1052-1063. DOI:10.1080/02656736.2022.2059581 |
| [4] |
Zhu S, Wu Y, Zhang X, et al. Targeting N7-Methylguanosine tRNA modification blocks hepatocellular carcinoma metastasis after insufficient radiofrequency ablation[J]. Mol Ther, 2023, 31(6): 1596-1614. DOI:10.1016/j.ymthe.2022.08.004 |
| [5] |
Zou YW, Ren ZG, Sun Y, et al. The latest research progress on minimally invasive treatments for hepatocellular carcinoma[J]. Hepatobiliary Pancreat Dis Int, 2023, 22(1): 54-63. DOI:10.1016/j.hbpd.2022.08.004 |
| [6] |
Chen L, Zhang W, Sun T, et al. Effect of Transarterial Chemoembolization Plus Percutaneous Ethanol Injection or Radiofrequency Ablation for Liver Tumors[J]. J Hepatocell Carcinoma, 2022, 9: 783-797. DOI:10.2147/JHC.S370486 |
| [7] |
Dong S, Li Z, Kong J, et al. Arsenic trioxide inhibits angiogenesis of hepatocellular carcinoma after insufficient radiofrequency ablation via blocking paracrine angiopoietin-1 and angiopoietin-2[J]. Int J Hyperthermia, 2022, 39(1): 888-896. DOI:10.1080/02656736.2022.2093995 |
| [8] |
Guo Y, Ren Y, Dong X, et al. An Overview of Hepatocellular Carcinoma After Insufficient Radiofrequency Ablation[J]. J Hepatocell Carcinoma, 2022, 9: 343-355. DOI:10.2147/JHC.S358539 |
| [9] |
Zhang Y, Zhang Y, Wang J, et al. Amarogentin Inhibits Liver Cancer Cell Angiogenesis after Insufficient Radiofrequency Ablation via Affecting Stemness and the p53-Dependent VEGFA/Dll4/Notch1 Pathway[J]. Biomed Res Int, 2020, 2020: 5391058. |
| [10] |
Wang S, Liu J, Wu H, et al. All-trans retinoic acid (ATRA) inhibits insufficient radiofrequency ablation (IRFA)-induced enrichment of tumor-initiating cells in hepatocellular carcinoma[J]. Chin J Cancer Res, 2021, 33(6): 694-707. DOI:10.21147/j.issn.1000-9604.2021.06.06 |
| [11] |
Zhang X, Zheng Q, Yue X, et al. ZNF498 promotes hepatocellular carcinogenesis by suppressing p53-mediated apoptosis and ferroptosis via the attenuation of p53 Ser46 phosphorylation[J]. J Exp Clin Cancer Res, 2022, 41(1): 79. DOI:10.1186/s13046-022-02288-3 |
| [12] |
Xiao Y, Chen J, Zhou H, et al. Combining p53 mRNA nanotherapy with immune checkpoint blockade reprograms the immune microenvironment for effective cancer therapy[J]. Nat Commun, 2022, 13(1): 758. DOI:10.1038/s41467-022-28279-8 |
| [13] |
Delman M, Avcı ST, Akçok İ, et al. Antiproliferative activity of (R)-4'-methylklavuzon on hepatocellular carcinoma cells and EpCAM+/CD133+ cancer stem cells via SIRT1 and Exportin-1 (CRM1) inhibition[J]. Eur J Med Chem, 2019, 180: 224-237. DOI:10.1016/j.ejmech.2019.07.024 |
| [14] |
Pustovalova M, Blokhina T, Alhaddad L, et al. CD44+ and CD133+ Non-Small Cell Lung Cancer Cells Exhibit DNA Damage Response Pathways and Dormant Polyploid Giant Cancer Cell Enrichment Relating to Their p53 Status[J]. Int J Mol Sci, 2022, 23(9): 4922. DOI:10.3390/ijms23094922 |
| [15] |
Choi HY, Siddique HR, Zheng M, et al. p53 destabilizing protein skews asymmetric division and enhances NOTCH activation to direct self-renewal of TICs[J]. Nat Commun, 2020, 11(1): 3084. DOI:10.1038/s41467-020-16616-8 |
| [16] |
Machida K. Cell fate, metabolic reprogramming and lncRNA of tumor-initiating stem-like cells induced by alcohol[J]. Chem Biol Interact, 2020, 323: 109055. DOI:10.1016/j.cbi.2020.109055 |
| [17] |
Song B, Zhou W. Amarogentin has protective effects against sepsis-induced brain injury via modulating the AMPK/SIRT1/NF-κB pathway[J]. Brain Res Bull, 2022, 189: 44-56. DOI:10.1016/j.brainresbull.2022.08.018 |
| [18] |
Pal D, Sur S, Roy R, et al. Hypomethylation of LIMD1 and P16 by downregulation of DNMT1 results in restriction of liver carcinogenesis by amarogentin treatment[J]. J Biosci, 2021, 46: 53. DOI:10.1007/s12038-021-00176-0 |
| [19] |
Sur S, Pal D, Banerjee K, et al. Amarogentin regulates self renewal pathways to restrict liver carcinogenesis in experimental mouse model[J]. Mol Carcinog, 2016, 55(7): 1138-1149. DOI:10.1002/mc.22356 |
| [20] |
Ma H, Li Z, Yuan J, et al. Extrapolating Prognostic Factors of Primary Curative Resection to Postresection Recurrences Hepatocellular Carcinoma Treatable by Radiofrequency Ablation[J]. Gastroenterol Res Pract, 2021, 2021: 8878417. |
| [21] |
Chen X, Huang Y, Chen H, et al. Augmented EPR effect post IRFA to enhance the therapeutic efficacy of arsenic loaded ZIF-8 nanoparticles on residual HCC progression[J]. J Nanobiotechnology, 2022, 20(1): 34. DOI:10.1186/s12951-021-01161-3 |
| [22] |
Wang F, Xu C, Li G, et al. Incomplete radiofrequency ablation induced chemoresistance by up-regulating heat shock protein 70 in hepatocellular carcinoma[J]. Exp Cell Res, 2021, 409(2): 112910. DOI:10.1016/j.yexcr.2021.112910 |
| [23] |
Tong Y, Yang H, Xu X, et al. Effect of a hypoxic microenvironment after radiofrequency ablation on residual hepatocellular cell migration and invasion[J]. Cancer Sci, 2017, 108(4): 753-762. DOI:10.1111/cas.13191 |
| [24] |
Zaimoku R, Miyashita T, Tajima H, et al. Monitoring of Heat Shock Response and Phenotypic Changes in Hepatocellular Carcinoma After Heat Treatment[J]. Anticancer Res, 2019, 39(10): 5393-5401. DOI:10.21873/anticanres.13733 |
| [25] |
Pal D, Sur S, Mandal S, et al. Prevention of liver carcinogenesis by amarogentin through modulation of G1/S cell cycle check point and induction of apoptosis[J]. Carcinogenesis, 2012, 33(12): 2424-2431. DOI:10.1093/carcin/bgs276 |
| [26] |
Pal D, Sur S, Roy R, et al. Epigallocatechin gallate in combination with eugenol or amarogentin shows synergistic chemotherapeutic potential in cervical cancer cell line[J]. J Cell Physiol, 2018, 234(1): 825-836. |
| [27] |
Park EK, Lee JC, Park JW, et al. Transcriptional repression of cancer stem cell marker CD133 by tumor suppressor p53[J]. Cell Death Dis, 2015, 6(11): e1964. DOI:10.1038/cddis.2015.313 |
| [28] |
Xu Y, Xu Z, Li Q, et al. Mutated p53 Promotes the Symmetric Self-Renewal of Cisplatin-Resistant Lung Cancer Stem-Like Cells and Inhibits the Recruitment of Macrophages[J]. J Immunol Res, 2019, 2019: 7478538. |
| [29] |
Feldman DE, Chen C, Punj V, et al. The TBC1D15 oncoprotein controls stem cell self-renewal through destabilization of the Numb-p53 complex[J]. PLoS One, 2013, 8(2): e57312. DOI:10.1371/journal.pone.0057312 |
| [30] |
Machida K, Feldman DE, Tsukamoto H. TLR4-dependent tumor-initiating stem cell-like cells (TICs) in alcohol-associated hepatocellular carcinogenesis[J]. Adv Exp Med Biol, 2015, 815: 131-144. |
| [31] |
Espinosa-Sánchez A, Suárez-Martínez E, Sánchez-Díaz L, et al. Therapeutic Targeting of Signaling Pathways Related to Cancer Stemness[J]. Front Oncol, 2020, 10: 1533. |
 2023, Vol. 50
2023, Vol. 50


