文章信息
- 抑制上游转录因子2的表达对胃癌BGC-823细胞增殖和凋亡的影响
- Effect of Inhibiting Upstream Transcription Factor 2 Expression on Proliferation and Apoptosis of Gastric Cancer BGC-823 Cells
- 肿瘤防治研究, 2022, 49(12): 1217-1222
- Cancer Research on Prevention and Treatment, 2022, 49(12): 1217-1222
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2022.22.0413
- 收稿日期: 2022-04-21
- 修回日期: 2022-09-18
2. 250021 济南,山东大学附属省立医院胃肠外科
2. Department of Gastrointestinal Surgery, Shandong Provincial Hospital, Cheeloo College of Medicine, Shandong University, Jinan 250021, China
我国胃癌的发病率和病死率均处于较高水平[1-3]。胃癌的早期症状不明显,确诊时大多已经发展到晚期阶段。目前,胃癌的治疗手段主要是手术和放化疗,患者症状有所改善但总体生存率仍然不高。近年来,癌症基因层面的检测和治疗应用越来越广。上游转录因子2(upstream transcription factor 2, USF2)已被证实在多种肿瘤中发挥作用[4-5],本课题组前期的研究已经发现USF2在胃癌组织中高表达[6],但USF2基因是否参与胃癌细胞的增殖和凋亡尚不明确。本研究旨在分析USF2与胃癌细胞增殖和凋亡的关系,因此我们通过敲低胃癌细胞中USF2的表达,观察胃癌细胞增殖和凋亡的变化,为寻找胃癌诊疗的新思路提供依据。
1 材料与方法 1.1 材料人胃癌细胞株GES-1、AGS、HGC-27、MKN-45、MGC-803、SGC-7901和BGC-823购自上海中国科学院生物化学与细胞生物学研究所。BGC-823细胞在RPMI1640完全培养液中常规培养,培养液中含10%胎牛血清。在温度37℃、含5%的CO2细胞培养箱中培养。RPMI1640培养基、胎牛血清和胰蛋白酶试剂购自美国Gibco公司;USF2 siRNA和阴性对照siRNA均购自上海吉满公司;PCR引物及试剂盒购自广州锐博公司,Lipofectamine™3000转染试剂和兔多克隆抗体(USF2)购自美国Invitrogen公司。兔抗人GAPDH抗体和二抗均购自武汉三鹰公司。
1.2 方法 1.2.1 细胞培养和siRNA转染细胞在含有10%胎牛血清的RPMI 1640培养基中于37℃、5%CO2的条件下培养。当细胞融合度达到70%时,用1×PBS(pH7.4)洗涤,然后使用Lipofectamine™3000将siRNA-USF2、siRNA-NC分别转染至BGC-823细胞中,空白对照组不转染。实验分为空白对照组、siRNA-NC组和siRNA-USF2组,细胞转染72 h后收集细胞用于后续实验操作。
1.2.2 实时荧光定量PCR法检测USF2 mRNA的表达细胞转染48 h后,使用TRIzol试剂提取细胞的总RNA,用紫外分光光度计测定RNA的浓度及纯度,使用反转录试剂盒将RNA反转录为cDNA,用cDNA进行PCR扩增检测mRNA的表达,β-actin用作内源对照。解链曲线用于评估非特异性扩增。实时荧光定量PCR反应程序如下:95℃持续30 s,95℃ 5 s和60℃ 30 s进行40个循环。使用2-ΔΔCt方法计算相对表达水平。引物序列如下:USF2:Forward-AAAGGAGGGATCCTGTCCAA,Reverse-CAGGGCGTTCTCATTCTTCA; β-actin:Forward-GCATCGTCACTGGGGAC,Reverse-ACCTGG CCGTCAGGCAGCTC。
1.2.3 Western blot检测USF2蛋白的表达细胞转染72 h后,用冷PBS冲洗细胞两次。吸干水分后用RIPA裂解液裂解细胞获取细胞总蛋白,然后用BCA(bicinchoninic acid)蛋白质浓度测定试剂盒计算蛋白质浓度,使用10%聚丙烯酰胺凝胶通过SDS-PAGE分离蛋白质(每个样品30 μg)。蛋白质通过电泳按分子量分离,然后通过转膜转移到NC膜上。用快速封闭液封闭NC膜,再与适当的一抗(抗USF2,抗GADPH)在4℃孵育过夜,所有抗体均在4℃按说明书稀释。第二天将NC膜用TBST洗涤3次,每次5~10 min,然后在室温下与HRP连接的二抗共同孵育1 h。GADPH用作内部对照。通过Amersham Imager 680,用增强的化学发光方法对蛋白质条带进行曝光。
1.2.4 CCK-8实验检测细胞增殖能力将上述转染24 h后的三组细胞以2×103个/孔接种于96孔板中,每组设3个复孔,置于37℃培养箱中继续培养,分别在24、48、72和96 h采用CCK-8法检测细胞的增殖能力,即在各时间点每孔分别加入10 μl CCK-8试剂,置于37℃细胞培养箱中孵育1 h,使用酶标仪检测波长在450 nm处的光密度值,细胞增殖活性=实验组光密度值-空白组光密度值。
1.2.5 平板克隆实验检测细胞克隆形成能力将上述转染24 h后的三组细胞以每个培养皿1 000个的密度重新铺板,每组设3个平皿。每3天更换一次培养基。培养14天后弃培养基,PBS洗涤细胞,4%多聚甲醛固定20 min,1%结晶紫染色20 min,冲洗干净后以进行可视化和计数,比较克隆形成率。
1.2.6 流式细胞术检测细胞凋亡率将上述转染24 h后的三组细胞常规消化后,用冷PBS洗涤细胞,然后离心收集细胞,重复1次,用1 ml的结合缓冲液重悬细胞,分别添加5 μl Annexin V-FITC和10 μl PI,轻轻摇匀细胞,室温(25℃)避光孵育15 min,然后每管再加入4 ml结合缓冲液,立即上流式细胞仪检测。分析各组细胞的凋亡率。
1.3 统计学方法所有实验独立重复3次。结果用平均值±标准误差平均值(SEM)表示。使用SPSS19.0软件执行两个独立的样本t检验或方差单向分析(ANOVA)。P < 0.05为差异有统计学意义。
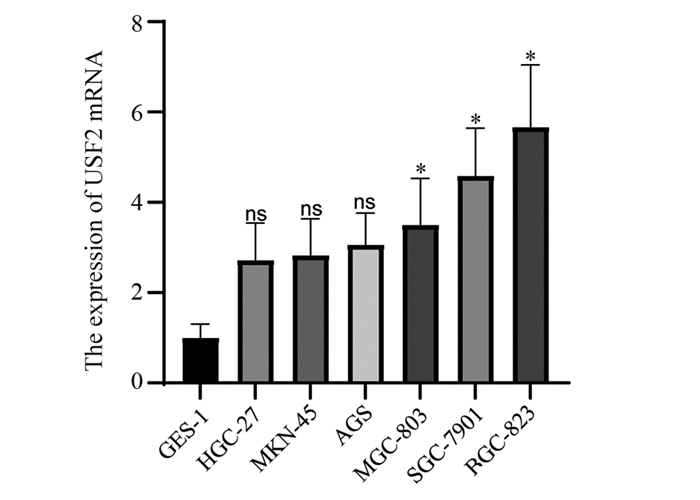
2 结果 2.1 胃癌细胞系和GES-1细胞中USF2 mRNA的表达实时荧光定量PCR法检测结果示,USF2 mRNA在各组细胞中的表达,见图 1。与GES-1细胞相比较,各组胃癌细胞系中USF2 mRNA的表达均升高(P值分别为0.1514,0.1206,0.0694,0.0230,0.0015,0.0001)。因此我们选择表达最高的BGC-823细胞敲低后进行后续实验。
|
| ns: P > 0.05, compared with GES-1 group; *: P < 0.05, compared with GES-1 group. 图 1 胃癌细胞系和GES-1细胞USF2 mRNA的表达 Figure 1 USF2 mRNA expression in gastric cancer cell lines and GES-1 cells |
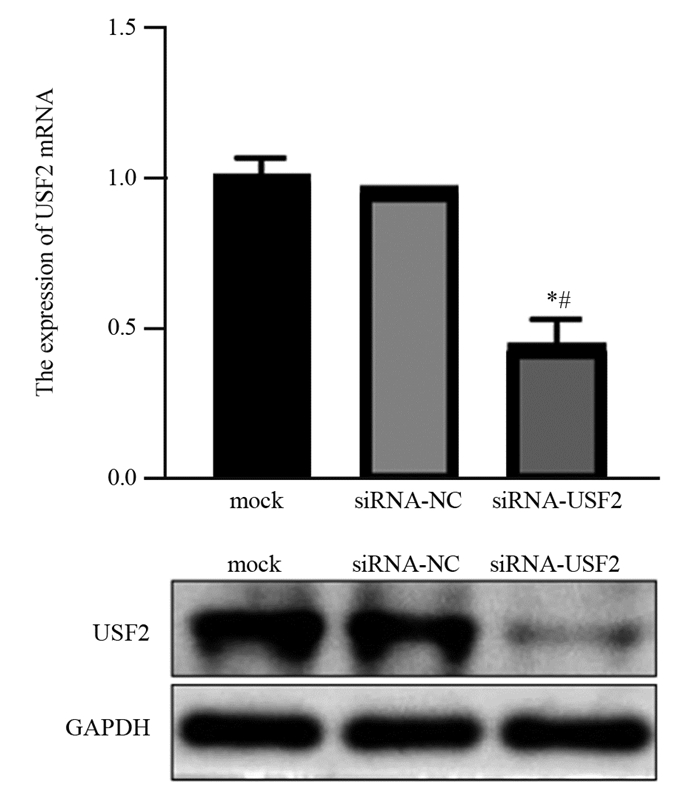
BGC-823细胞转染USF2 siRNA 48 h后,实时荧光定量PCR法检测结果示,空白对照组、siRNA-NC组和siRNA-USF2组BGC-823细胞中USF2 mRNA的表达水平分别为1.00±0.07、0.96±0.00和0.44±0.09,siRNA-USF2组BGC-823细胞中USF2 mRNA的表达水平明显降低,与空白对照组和siRNA-NC组相比差异具有统计学意义(P=0.0001、0.0002)。BGC-823细胞转染USF2 siRNA 72 h后,Western blot法检测结果示,空白对照组、siRNA-NC组和siRNA-USF2组BGC-823细胞中USF2蛋白的表达水平分别为0.25±0.01、0.26±0.00和0.08±0.00,siRNA-USF2组BGC-823细胞中USF2蛋白的表达水平明显降低,与空白对照组和siRNA-NC组相比差异具有统计学意义(均P < 0.0001),见图 2。
|
| *: P < 0.05, compared with mock group; #: P < 0.05, compared with siRNA-NC group. 图 2 各组BGC-823细胞中USF2 mRNA和蛋白的表达水平 Figure 2 The mRNA and protein expression levels of USF2 in BGC-823 cells |
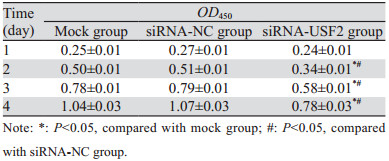
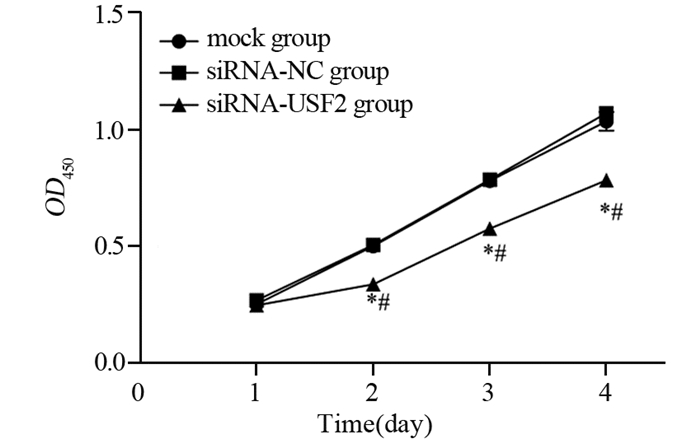
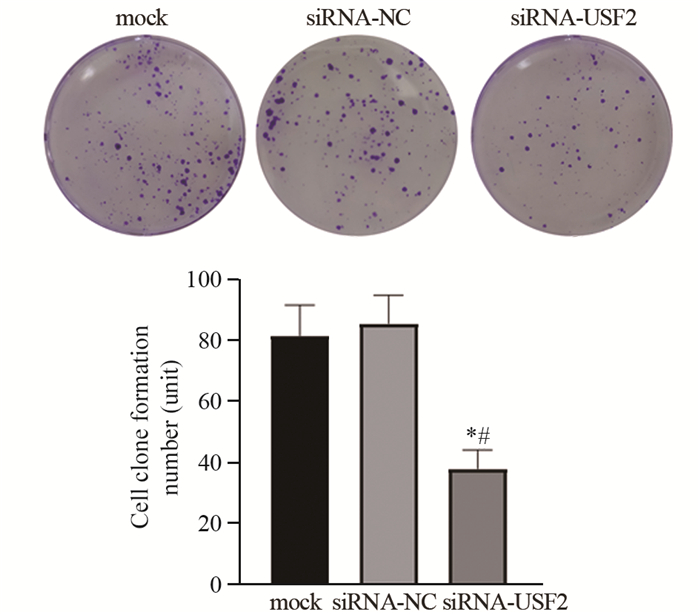
CCK-8检测结果显示,与空白对照组和siRNA-NC组相比,siRNA-USF2组BGC-823细胞在第1、2、3和4天时的吸光度值均明显降低(第1天:P=0.1224、0.0559;第2天:均P < 0.0001;第3天:均P < 0.0001;第4天:P=0.0001、< 0.0001),见表 1、图 3。平板克隆实验结果显示,空白对照组、siRNA-NC组和siRNA-USF2组的克隆形成数分别是81.67±10.02、85.67±9.30和38.00±6.25个。siRNA-USF2组BGC-823细胞的克隆数明显减少,与空白对照组和siRNA-NC组相比差异均具有统计学意义(P=0.0020、0.0013),见图 4。
|
|
| *: P < 0.05, compared with mock group; #: P < 0.05, compared with siRNA-NC group. 图 3 CCK-8法检测各组胃癌BGC-823细胞的增殖能力 Figure 3 Proliferation of BGC-823 cells in each group detected by CCK-8 method |
|
| A: mock group; B: siRNA-NC group; C: siRNA-USF2 group; *: P < 0.05, compared with mock group; #: P < 0.05, compared with siRNA-NC group. 图 4 平板克隆形成实验检测各组BGC-823细胞的克隆形成能力 Figure 4 Clonogenesis ability of BGC-823 cells in each group detected by plate clonogenesis assay |
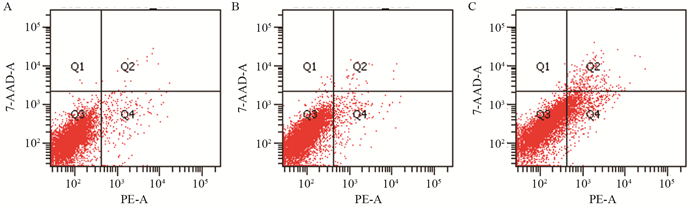
流式细胞术实验显示,空白对照组、siRNA-NC组和siRNA-USF2组的BGC-823细胞凋亡率分别是(3.67±1.58)%、(2.87±0.15)%和(11.27±0.65)%。siRNA-USF2组BGC-823细胞的凋亡率明显升高,与空白对照组和siRNA-NC组相比差异均具有统计学意义(P=0.0002、P=0.0001),见图 5。
|
| A: mock group; B: siRNA-NC group; C: siRNA-USF2 group. 图 5 USF2 siRNA对胃癌BGC-823细胞凋亡率的影响 Figure 5 Effect of USF2 siRNA on apoptosis rate of gastric cancer BGC-823 cells |
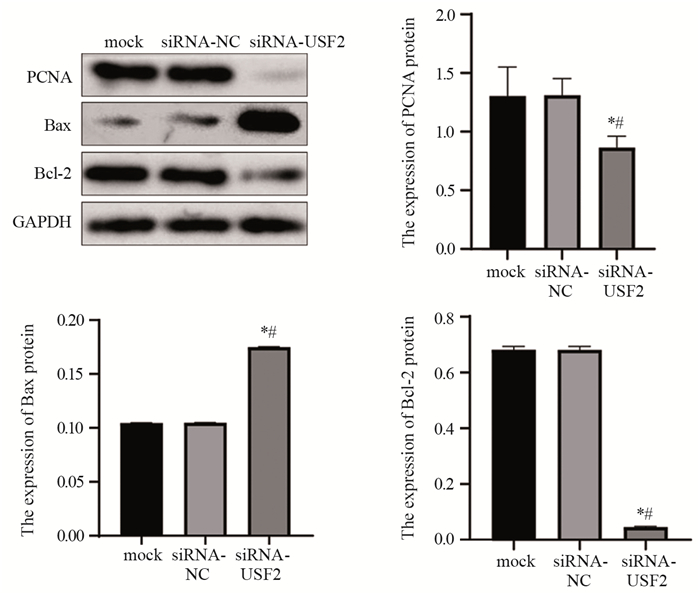
Western blot法检测显示,空白对照组、siRNA-NC组和siRNA-USF2组PCNA蛋白的表达量分别为1.30±0.25、1.21±0.14和0.86±0.10,siRNA-USF2组PCNA表达量明显降低,与空白对照组和siRNA-NC组相比差异均具有统计学意义(P=0.0487、P=0.0456)。空白对照组、siRNA-NC组和siRNA-USF2组Bax蛋白的表达量分别是1.10±0.00、0.10±0.00和0.18±0.00,siRNA-USF2组Bax蛋白的表达量明显升高,与空白对照组和siRNA-NC组相比差异均具有统计学意义(均P < 0.0001);空白对照组、siRNA-NC组和siRNA-USF2组Bcl-2蛋白的表达量分别是0.68±0.13、0.68±0.13和0.18±0.24,siRNA-USF2组Bcl-2蛋白的表达量明显下降,与空白对照组和siRNA-NC组相比差异均具有统计学意义(均P < 0.0001),见图 6。
|
| *: P < 0.05, compared with mock group; #: P < 0.05, compared with siRNA-NC group. 图 6 Western blot法检测各组胃癌BGC-823细胞中PCNA、Bax和Bcl-2蛋白的表达水平 Figure 6 Expression levels of PCNA, Bax and Bcl-2 proteins in GC BGC-823 cells of each group detected by Western blot |
胃癌是常见的消化系统恶性肿瘤之一,在我国癌症发病率中居第六位,致死率高居第二位,严重影响着人们的健康生活和生命安全[1-3]。目前胃癌的治疗仍以手术和放化疗为主。随着胃癌分子分型及发病机制研究的不断进展,胃癌治疗也逐渐进入靶向治疗、精准医疗及免疫治疗的新时代,基因靶向治疗的发展为临床提供了新思路。通过靶向抑制胃癌促癌基因或上调抑癌基因的表达,探讨其对胃癌细胞增殖、迁移和侵袭、凋亡等生物学特性的影响,已经成为了胃癌基因治疗研究的主要思路。人上游转录因子最初是从HeLa细胞中提取获得的两个表观分子量分别为43和44 kDa的USF多肽,分别称为USF1和USF2[6-8]。USF2是由异二聚体和重叠基因编码的碱性螺旋-环-螺旋转录因子。剪接产生的同型在特定的启动子环境中表现出不同的转录活性。尽管人们普遍认为不同组织中USF2的表达和相对丰度不同,但它在组织中与其他因子协同作用,并具有刺激特异性转录的调控作用[9-10]。USF2是一个蛋白编码基因,编码一个亮氨酸拉链转录因子家族的成员,编码的蛋白质可以通过富含嘧啶的启动子(Inr)元件和E-box基序激活转录,参与调节多种细胞过程。
已有研究表明,USF2在肺癌、前列腺癌、乳腺癌和结直肠癌的发展中起着重要作用[4-5, 11-17]。USF2与胃癌的关系尚不明确。本研究检测了USF2在不同胃癌细胞系和GES-1细胞中的表达,发现USF2在胃癌细胞系中的表达均高于GES-1细胞系,并选择将表达最高的BGC-823细胞敲低后进行后续实验。将USF2 siRNA转染至BGC-823细胞中,通过实时荧光定量PCR法和Western blot实验检验转染效果,显示转染后USF2 mRNA和蛋白的表达均明显下降,说明转染USF2 siRNA能够成功抑制BGC-823细胞中USF2的表达。抑制USF2的表达后,CCK-8实验和平板克隆实验结果均显示,BGC-823细胞的增殖能力和克隆形成能力明显减弱。流式细胞术检测显示,BGC-823细胞的凋亡率明显增加。这些结果说明USF2 siRNA能明显抑制胃癌BGC-823细胞的增殖,诱导细胞凋亡。
PCNA为DNA聚合酶的辅助蛋白,与细胞DNA合成关系密切,在细胞增殖的启动上起重要作用,是反映细胞增殖状态的良好指标。本研究发现,抑制BGC-823细胞中USF2的表达后,PCNA的表达水平明显降低,说明BGC-823细胞的增殖能力受到抑制。促凋亡蛋白Bax和抗凋亡蛋白Bcl-2是Bcl-2蛋白家族成员,Bax可以通过介导细胞膜的通透性来促进细胞色素C的释放,启动细胞凋亡级联反应。Bcl-2的功能则刚好相反,其抑制细胞色素C的释放,阻止细胞凋亡的级联反应。Bax和Bcl-2的比例决定细胞凋亡的启动与否。本研究Western blot实验结果表明,抑制USF2表达后,Bax的表达水平明显升高,Bcl-2的表达水平明显降低,提示BGC-823细胞的凋亡增加。这些结果表明USF2 siRNA能够抑制胃癌BGC-823细胞的增殖,诱导细胞凋亡,与下调细胞中PCNA和Bcl-2蛋白以及促进Bax蛋白的表达有关。
综上所述,转染USF2 siRNA抑制USF2的表达后,人胃癌BGC-823细胞的增殖受到抑制,凋亡增多,这一过程可能与下调细胞中PCNA和Bcl-2蛋白以及促进Bax蛋白的表达相关。本研究表明USF2在胃癌的增殖和凋亡中发挥重要作用,为胃癌的基因治疗提供了新的思路和靶点。
作者贡献:
王绪斌、高慎硕:论文撰写、细胞实验实施
张智凯、马岩:统计分析
郭晓波:课题设计、指导
| [1] |
Cao W, Chen HD, Yu YW, et al. Changing profiles of cancer burden worldwide and in China: a secondary analysis of the global cancer statistics 2020[J]. Chin Med J (Engl), 2021, 134(7): 783-791. DOI:10.1097/CM9.0000000000001474 |
| [2] |
Smyth EC, Nilsson M, Grabsch HI, et al. Gastric cancer[J]. Lancet, 2020, 396(10251): 635-648. DOI:10.1016/S0140-6736(20)31288-5 |
| [3] |
Sung H, Ferlay J, Siegel RL, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2021, 71(3): 209-249. DOI:10.3322/caac.21660 |
| [4] |
Situ Y, Gao R, Lei L, et al. System analysis of FHIT in LUAD and LUSC: The expression, prognosis, gene regulation network, and regulation targets[J]. Int J Biol Markers, 2022, 37(2): 158-169. DOI:10.1177/03936155221084056 |
| [5] |
Chen N, Szentirmay MN, Pawar SA, et al. Tumor-suppression function of transcription factor USF2 in prostate carcinogenesis[J]. Oncogene, 2006, 25(4): 579-587. DOI:10.1038/sj.onc.1209079 |
| [6] |
Gao S, Zhang Z, Wang X, et al. hsa-miR-875-5p inhibits tumorigenesis and suppresses TGF-beta signalling by targeting USF2 in gastric cancer[J]. J Transl Med, 2022, 20(1): 115. DOI:10.1186/s12967-022-03253-6 |
| [7] |
Wang J, Zhao S, He W, et al. A transcription factor ⅡA-binding site differentially regulates RNA polymeraseⅡ-mediated transcription in a promoter context-dependent manner[J]. J Biol Chem, 2017, 292(28): 11873-11885. DOI:10.1074/jbc.M116.770412 |
| [8] |
Chi TF, Horbach T, Götz C, et al. Cyclin-Dependent Kinase 5 (CDK5)-Mediated Phosphorylation of Upstream Stimulatory Factor 2 (USF2) Contributes to Carcinogenesis[J]. Cancers (Basel), 2019, 11(4): 523. DOI:10.3390/cancers11040523 |
| [9] |
Chi TF, Khoder-Agha F, Mennerich D, et al. Loss of USF2 promotes proliferation, migration and mitophagy in a redox-dependent manner[J]. Redox Biol, 2020, 37: 101750. DOI:10.1016/j.redox.2020.101750 |
| [10] |
Stögbauer L, Stummer W, Senner V, et al. Telomerase activity, TERT expression, hTERT promoter alterations, and alternative lengthening of the telomeres (ALT) in meningiomas - a systematic review[J]. Neurosurg Rev, 2020, 43(3): 903-910. DOI:10.1007/s10143-019-01087-3 |
| [11] |
Tan Y, Chen Y, Du M, et al. USF2 inhibits the transcriptional activity of Smurf1 and Smurf2 to promote breast cancer tumorigenesis[J]. Cell Signal, 2019, 53: 49-58. DOI:10.1016/j.cellsig.2018.09.013 |
| [12] |
Wang X, Xing L, Yang R, et al. The circACTN4 interacts with FUBP1 to promote tumorigenesis and progression of breast cancer by regulating the expression of proto-oncogene MYC[J]. Mol Cancer, 2021, 20(1): 91. DOI:10.1186/s12943-021-01383-x |
| [13] |
Li S, Zhang J, Qian S, et al. S100A8 promotes epithelial-mesenchymal transition and metastasis under TGF-beta/USF2 axis in colorectal cancer[J]. Cancer Commun (Lond), 2021, 41(2): 154-170. DOI:10.1002/cac2.12130 |
| [14] |
Zeng HB, Dong LQ, Huang YL, et al. USF2 reduces BMP3 expression via transcriptional activation of miR-34a, thus promoting osteogenic differentiation of BMSCs[J]. J Bone Miner Metab, 2021, 39(6): 997-1008. DOI:10.1007/s00774-021-01254-x |
| [15] |
Hou Y, Zhang Y, Lin S, et al. Protective mechanism of apigenin in diabetic nephropathy is related to its regulation of miR-423-5P-USF2 axis[J]. Am J Transl Res, 2021, 13(4): 2006-2020. |
| [16] |
Liu F, Wang X, Zheng B, et al. USF2 enhances the osteogenic differentiation of PDLCs by promoting ATF4 transcriptional activities[J]. J Periodontal Res, 2020, 55(1): 68-76. DOI:10.1111/jre.12689 |
| [17] |
Hu D, Tjon EC, Andersson KM, et al. Aberrant expression of USF2 in refractory rheumatoid arthritis and its regulation of proinflammatory cytokines in Th17 cells[J]. Proc Natl Acad Sci U S A, 2020, 117(48): 30639-30648. DOI:10.1073/pnas.2007935117 |
 2022, Vol. 49
2022, Vol. 49
