文章信息
- 血管内皮细胞中RhoC的表达对骨髓瘤RPMI8226细胞增殖和侵袭的影响
- Effect of RhoC Expression in Vascular Endothelial Cells on Proliferation and Invasion of Myeloma RPMI8226 Cells
- 肿瘤防治研究, 2022, 49(4): 299-303
- Cancer Research on Prevention and Treatment, 2022, 49(4): 299-303
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2022.21.0934
- 收稿日期: 2021-11-26
- 修回日期: 2022-01-14
2. 450007 郑州,郑州大学附属郑州中心医院病理科;
3. 476000 商丘,商丘工学院医学院;
4. 450000 郑州,郑州人民医院病理科
2. Department of Pathology, Zhengzhou Central Hospital Affiliated to Zhengzhou University, Zhengzhou 450007, China;
3. School of Medicine, Shangqiu Institute of Technology, Shangqiu 476000, China;
4. Department of Pathology, Zhengzhou People's Hospital, Zhengzhou 450000, China
多发性骨髓瘤(multiple myeloma, MM)是血液系统B淋巴细胞恶性增殖性疾病,发病率在血液系统恶性肿瘤中排列第二,其中65岁以上的老年人占发病人数的2/3[1-2]。随着我国人口老龄化,MM患病人数也逐年增多。尽管骨髓瘤靶向治疗和免疫调节剂的应用使预后有了很大改善,但至今仍无法治愈[3]。对于MM而言,单纯地以骨髓瘤细胞为靶点治疗,效果并不理想。
研究发现,同其他系统肿瘤一样,MM的发生和发展也需要血管生成[4]。肿瘤血管生成是一个多步骤、多种生物成分参与的复杂过程[5]。RhoC作为Rho GTP酶家族中重要成员,参与恶性肿瘤的浸润、转移及血管生成[6-7],是一个备受关注的肿瘤治疗潜在靶点。前期研究发现,RhoC在血管内皮中表达,可调节血管内皮细胞的生物学行为并影响血管的生成[8];下调骨髓瘤RPMI8226细胞中RhoC表达,不仅可抑制移植瘤的生长,对肿瘤血管的生成也有抑制作用[9]。肿瘤血管是肿瘤靶向治疗的重要目标,肿瘤细胞可分泌高水平的促血管生成因子形成异常的血管网络,反过来,肿瘤血管系统的异常化对肿瘤细胞的生物学行为也有重要影响[10]。
目前,已有研究主要以骨髓瘤细胞为靶点进行传统的抗血管生成治疗,但效果不能令人满意。本研究将探讨下调骨髓瘤血管内皮细胞(myeloma vascular endothelial cells, MVECs)中RhoC表达对骨髓瘤RPMI8226细胞增殖和侵袭能力的影响,进一步研究其可能机制,以期为临床骨髓瘤治疗和研究提供新的思路和理论依据。
1 材料与方法 1.1 材料及主要试剂RhoC shRNA慢病毒载体购自苏州吉玛基因公司;RhoC抗体购自英国Abcam公司;CDK、CyclinD1、AKT、PI3K、MMP2、MMP9抗体购自美国Proteintech公司;Transwell小室购自美国Corning公司;PI染色试剂盒购自江苏凯基生物科技有限公司;CCK-8试剂盒购自日本同仁化学研究所;Matrigel胶购自美国BD公司;Polybrene购自上海翊圣生物科技有限公司;本实验室保存的MVECs、人脐静脉内皮细胞(human umbilical vein endothelial cells, HUVECs)、骨髓瘤RPMI8226细胞;DMEM、RPMI1640培养基购自美国Gibco公司。
1.2 细胞培养与条件培养基收集MVECs和HUVECs使用含10%胎牛血清的DMEM培养基培养,骨髓瘤RPMI8226细胞使用含10%胎牛血清的RPMI1640培养基培养,置于37℃、5%CO2培养箱中培养,生长至对数期时用于后续实验。
将MVECs和HUVECs按照每孔5×104个细胞加入24孔板中培养,24 h后将阴性对照组(NC组)和RhoC shRNA组(S组)慢病毒载体原液与细胞培养液按1:10稀释,各孔加500 μl慢病毒稀释液;12 h后更换新的培养液,继续培养48 h后收集条件培养基,离心、过滤、浓缩后用于培养骨髓瘤RPMI8226细胞[11]。
1.3 RhoC shRNA慢病毒载体转染将NC组和S组慢病毒载体原液(2×108 TU/ml)与细胞培养液按1:10稀释后加入2.5 μg聚凝胺,用于培养MVECs和HUVECs细胞,12 h后更换新鲜培养液,48 h后观察慢病毒载体转染效率,并用Western blot法验证RhoC的表达变化[8]。
1.4 CCK-8试剂盒检测细胞增殖能力使用条件培养基培养骨髓瘤RPMI8226细胞48 h后,用含10%FBS的RPMI1640培养基重悬细胞,调整细胞浓度至每孔3×103个,每组3个复孔。CCK-8工作液与培养基按1:10稀释后加入待测孔中,置于细胞培养箱中培养。分别于培养24、48、72、96 h后,使用酶标仪在450 nm条件下检测各组细胞OD值。
1.5 流式细胞仪检测细胞周期将经条件培养基培养的各组RPMI8226细胞收集、离心,调整细胞浓度为每毫升2×106个,离心去上清液,使用70%的乙醇固定细胞,于4℃冰箱过夜。离心弃上清液,900 µl预冷PBS及50 µl RNA酶重悬细胞,37℃反应30 min,然后加入5 µl PI试剂,37℃染色30 min;将细胞悬液转入流式管,上机检测,每组细胞重复3次,根据Flow J软件分析数据,得出G0/G1期、S期、G2/M期细胞比例。
1.6 Transwell实验检测细胞侵袭能力经条件培养基培养的RPMI8226细胞用无血清培养基饥饿处理24 h,取50 µl稀释后的Matrigel胶加入小室,调整细胞密度为2×103个/孔后加入小室,向小室外加入含20%FBS的RPMI1640培养基,在37℃、5%CO2培养箱中培养24 h后取出小室固定染色。置于显微镜200倍视野下,随机选取5个视野,计数小室膜下细胞数量,每组设置3个复孔。
1.7 Western blot实验将各组细胞在冰上裂解并提取蛋白质,蛋白定量配平后,煮沸变性上样,每孔10 μl,设置电压80 V 30 min,120 V 60 min进行电泳。电泳完成后,设置转膜电压80 V,90 min转膜至PVDF膜。然后添加一抗(RhoC、CDK、CyclinD1、AKT、PI3K、MMP2、MMP9),4℃过夜,次日添加HRP标记的二抗,ECL化学发光显色,使用Image J软件进行灰度定量分析。检测慢病毒载体转染MVECs和HUVECs后RhoC蛋白表达水平,以及NC组和S组骨髓瘤RPMI8226细胞中CDK、CyclinD1、AKT、PI3K、MMP2、MMP9蛋白表达水平的差异,每组实验重复3次。
1.8 统计学方法采用SPSS21.0统计软件检验计量资料的正态性,将符合条件的计量资料以平均数±标准差(x±s)表示,两样本之间比较采用t检验,P < 0.05为差异有统计学意义。
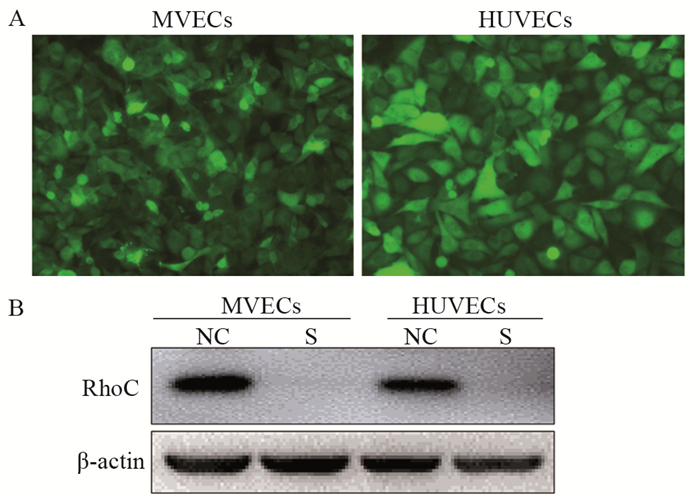
2 结果 2.1 RhoC shRNA慢病毒载体转染情况慢病毒载体转染48 h后,荧光显微镜下观察绿色荧光蛋白表达情况,MVECs和HUVECs细胞转染效率均可达到80%以上,见图 1A;Western blot法检测发现,慢病毒载体转染MVECs和HUVECs细胞后,与NC组相比,S组RhoC蛋白表达量明显降低(P=0.003、0.001),见图 1B。
|
| A: The transfection effect was observed under fluorescence microscope; B: The transfection effect was detected by Western blot. NC: negative control group; S: RhoC shRNA group. 图 1 RhoC shRNA慢病毒载体转染情况(×200) Figure 1 Transfection of RhoC shRNA lentivirus vector (×200) |
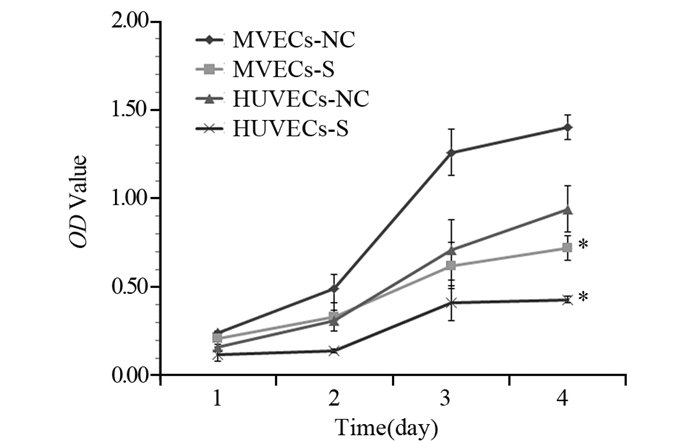
CCK-8结果显示:经条件培养基对骨髓瘤RPMI8226细胞连续培养4天后,与NC组相比,S组细胞增殖能力均明显降低(P=0.004、0.006),见图 2。
|
| *: P < 0.05, compared with NC groups. 图 2 骨髓瘤RPMI8226细胞增殖情况 Figure 2 Proliferation of myeloma RPMI8226 cells |
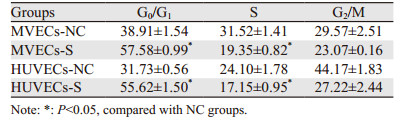
流式细胞仪检测各组细胞周期,见表 1。与NC组相比,S组骨髓瘤RPMI8226细胞的G0/G1期细胞数目明显增加、S期细胞数目减少,差异有统计学意义(MVECs: P=0.003、0.005; HUVECs: P=0.0.021、0.003)。
|
Transwell实验结果显示:与NC组相比,S组骨髓瘤RPMI8226细胞侵袭力明显降低(45.33±9.45 vs. 109.33±14.36, 67.67±9.71 vs. 122.33±7.09,P=0.003、0.001)。
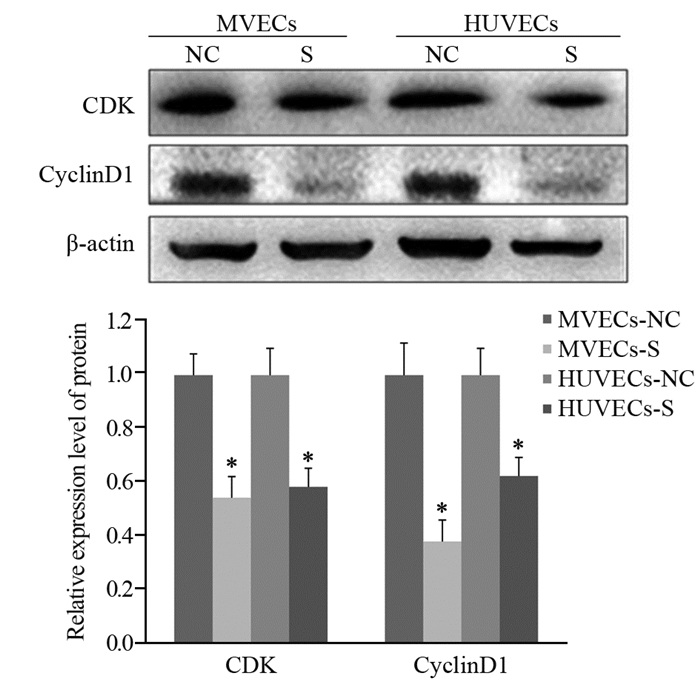
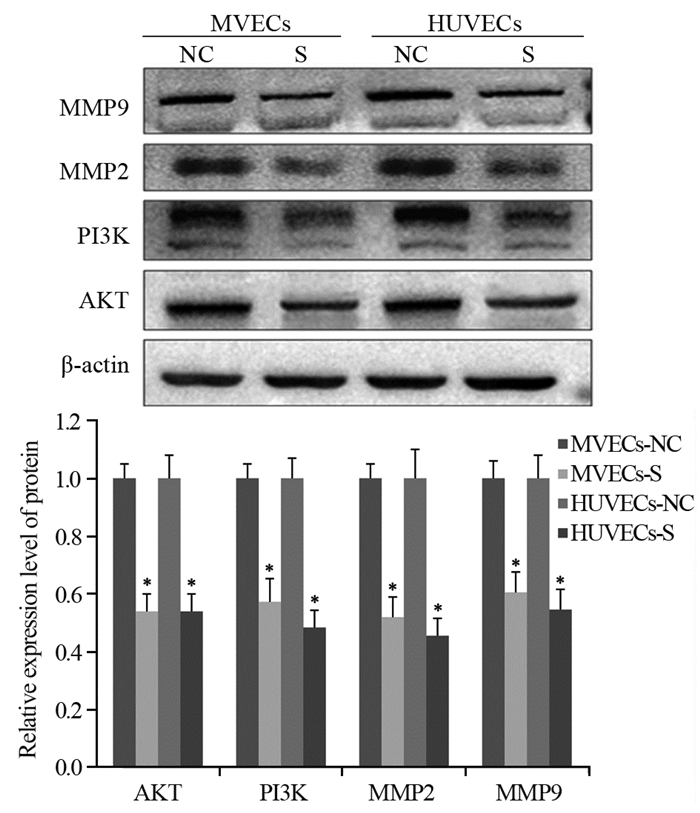
2.5 Western blot法检测骨髓瘤RPMI8226细胞中蛋白表达情况经条件培养基培养骨髓瘤RPMI8226细胞48 h后,Western blot法检测骨髓瘤RPMI8226细胞中CDK、CyclinD1、AKT、PI3K、MMP2、MMP9蛋白表达情况,与NC组相比,S组蛋白表达均降低(MVECs: P=0.0.023、0.003、0.015、0.001、0.034、0.021; HUVECs: P=0.0.035、0.005、0.021、0.002、0.025、0.032),见图 3、4。
|
| *: P < 0.05, compared with NC groups. 图 3 骨髓瘤RPMI8226细胞中CDK、CyclinD1蛋白表达情况 Figure 3 Expression of CDK and CyclinD1 proteins in myeloma RPMI8226 cells |
|
| *: P < 0.05, compared with NC groups. 图 4 骨髓瘤RPMI8226细胞中AKT、PI3K、MMP2、MMP9蛋白表达情况 Figure 4 Expression of AKT, PI3K, MMP2 and MMP9 proteins in myeloma RPMI8226 cells |
众所周知,Rho GTPase通过激活下游多种效应蛋白来调节细胞的生物学功能。RhoC作为Rho GTPase家族的重要成员,主要参与调节细胞骨架重组、细胞黏附与迁移、恶性肿瘤增殖、转移等生物学功能[6, 12-13]。RhoC高表达可促进结直肠癌细胞的增殖、侵袭和迁移,是预测结直肠癌复发风险的重要生物标志物[14]。研究发现,肿瘤细胞和血管内皮细胞之间可以相互作用,而RhoC在其中发挥重要作用[15]。肿瘤血管在肿瘤微环境中对肿瘤细胞的生长、增殖等过程起着重要作用,韩易等[16]研究发现,肿瘤血管不仅为肿瘤细胞提供营养,对肿瘤细胞的迁移能力也有重要影响。因此,本研究使用RhoC shRNA慢病毒载体下调血管内皮细胞中RhoC表达,收集条件培养基,观察对骨髓瘤RPMI8226细胞增殖和侵袭能力的影响。
恶性增殖是癌细胞的主要特征之一,细胞增殖与细胞周期依赖性激酶(Cyclin dependent kinase, CDK)和细胞周期蛋白D(CyclinD1)等基因表达有关[17],CDK和CyclinD1形成的蛋白激酶复合体共同推动了细胞周期的运行[18]。CyclinD1作为细胞周期蛋白家族成员,参与细胞周期的调控,使G1期细胞转变为S期,与细胞生长关系较为密切[19]。本实验结果显示,干扰血管内皮细胞中RhoC表达后,骨髓瘤RPMI8226细胞的增殖和侵袭能力均受到抑制,细胞周期阻滞在G0/G1期,同时细胞中CDK和CyclinD1蛋白表达也受到抑制,与陈佳琳等[20]研究结果相一致。程婧等[21]研究发现,乙酰辅酶A羧化酶1可通过调控CDK和CyclinD1表达促进肾透明细胞癌细胞增殖。然而本研究使用条件培养基调控骨髓瘤RPMI8226细胞增殖的机制是否与乙酰辅酶A羧化酶1的表达改变参与调控有关,还有待进一步研究。
癌细胞侵袭与转移的过程复杂,影响因素众多,其中基质金属蛋白酶(matrix metalloproteinases, MMPs),尤其MMP2、MMP9活性增高,降解基底膜中Ⅳ型胶原是引起肿瘤侵袭与转移的重要因素[22-23]。Wang等[24]研究发现,MMP2、MMP9在卵巢癌的侵袭和转移中具有重要作用,干扰MMP2、MMP9表达可抑制癌细胞侵袭和迁移。本研究Transwell实验结果显示,下调血管内皮细胞中RhoC表达后,骨髓瘤RPMI8226细胞侵袭细胞数目明显降低,侵袭能力受到抑制,与前者结论一致。此外,邓文松等[25]研究发现,微小RNA作为非编码RNA在骨髓瘤细胞中高表达不但促进骨髓瘤细胞侵袭,也参与调控骨髓瘤的发生发展。近年来,非编码RNA受到广泛关注,非编码RNA与恶性肿瘤生物学行为及作用机制研究或将成为新的研究方向。
研究显示,磷脂肌醇3-激酶(phosphoinositide-3 kinase, PI3K)/蛋白激酶B(AKT)通路作为细胞内最重要的信号通路之一,对调节细胞存活、生长、分化和细胞骨架重组等一系列信号做出反应;该通路的异常激活存在于多种恶性肿瘤中,主要与肿瘤生长和血管生成有关[26],且在不同癌种中RhoC对PI3K/AKT信号通路的影响不同,RhoC蛋白表达的变化可激活PI3K/AKT信号通路,引起癌细胞的增殖[27]。PI3K/AKT信号通路的异常激活可减少糖原的合成,增加糖酵解,通过N末端丝氨酸磷酸化抑制糖原合成酶激酶活性,增加CyclinD1的积累,从而促进细胞增殖[28],因此抑制PI3K活性可取得有益的临床治疗效果。胡桂芳等[29]研究显示,青蒿琥酯联合亚砷酸通过抑制PI3K/AKT信号通路的活化而抑制骨髓瘤细胞增殖。本实验结果表明,下调血管内皮中RhoC表达也可抑制骨髓瘤细胞增殖。
综上所述,下调血管内皮细胞中RhoC表达,对骨髓瘤RPMI8226细胞的增殖和侵袭能力具有抑制作用,其机制可能与CDK、CyclinD1、MMP2、MMP9、PI3K、AKT参与有关。本研究从血管内皮细胞角度对骨髓瘤细胞功能及可能机制进行了初步研究,下一步我们将对血管内皮细胞参与调节相关蛋白的作用机制进行深入研究,为骨髓瘤发生发展的分子机制提供理论依据,同时为以血管内皮细胞中RhoC为靶点进行骨髓瘤治疗奠定理论基础。
作者贡献:
孙淼淼:实验设计及操作、论文撰写
刘凯、王瞳、邱森:实验操作
赵志华:实验数据整理、分析
陈奎生:实验指导、修改论文
| [1] |
Barwick BG, Gupta VA, Vertino PM, et al. Cell of Origin and Genetic Alterations in the Pathogenesis of Multiple Myeloma[J]. Front Immunol, 2019, 10: 1121. DOI:10.3389/fimmu.2019.01121 |
| [2] |
Borad A, Saeed H, Toscani M, et al. Age demographics of subjects enrolled in interventional phase 3 multiple myeloma clinical trials[J]. J Oncol Pharm Pract, 2020, 26(6): 1475-1481. DOI:10.1177/1078155220934162 |
| [3] |
Minnie SA, Hill GR. Immunotherapy of multiple myeloma[J]. J Clin Invest, 2020, 130(4): 1565-1575. DOI:10.1172/JCI129205 |
| [4] |
Ribatti D, Vacca A. New Insights in Anti-Angiogenesis in Multiple Myeloma[J]. Int J Mol Sci, 2018, 19(7): 2031. DOI:10.3390/ijms19072031 |
| [5] |
Li T, Kang G, Wang T, et al. Tumor angiogenesis and anti-angiogenic gene therapy for cancer[J]. Oncol Lett, 2018, 16(1): 687-702. |
| [6] |
Guan X, Chen S, Zhao Y. The role of RhoC in malignant tumor invasion, metastasis and targeted therapy[J]. Histol Histopathol, 2018, 33(3): 255-260. |
| [7] |
Guo Y, Wang J, Zhou K, et al. Cytotoxic necrotizing factor 1 promotes bladder cancer angiogenesis through activating RhoC[J]. FASEB J, 2020, 34(6): 7927-7940. DOI:10.1096/fj.201903266RR |
| [8] |
Zhao Z, Liu K, Tian X, et al. Effects of RhoC downregulation on the angiogenesis characteristics of myeloma vascular endothelial cells[J]. Cancer Med, 2019, 8(7): 3502-3510. DOI:10.1002/cam4.2208 |
| [9] |
Liu K, Sun MM, Zhao ZH, et al. Effect of RhoC silencing on multiple myeloma xenografts and angiogenesis in nude mice[J]. J Biol Regul Homeost Agents, 2019, 33(5): 1387-1394. |
| [10] |
Viallard C, Larrivée B. Tumor angiogenesis and vascular normalization: alternative therapeutic targets[J]. Angiogenesis, 2017, 20(4): 409-426. DOI:10.1007/s10456-017-9562-9 |
| [11] |
Hergesheimer R, Lanznaster D, Bourgeais J, et al. Conditioned Medium from Cells Overexpressing TDP-43 Alters the Metabolome of Recipient Cells[J]. Cells, 2020, 9(10): 2198. DOI:10.3390/cells9102198 |
| [12] |
Xu M, Huang S, Dong X, et al. A novel isoform of ATOH8 promotes the metastasis of breast cancer by regulating RhoC[J]. J Mol Cell Biol, 2021, 13(1): 59-71. DOI:10.1093/jmcb/mjaa050 |
| [13] |
Xie SL, Wang M, Du XH, et al. miR-455 Inhibits HepG2 Cell Proliferation and Promotes Apoptosis by Targeting RhoC[J]. Mol Biol(Mosk), 2020, 54(1): 69-77. |
| [14] |
Ha YJ, Tak KH, Kim S, et al. Biological Characteristics and Clinical Significance of ITGB1 and RHOC in Patients With Recurrent Colorectal Cancer[J]. Anticancer Res, 2019, 39(9): 4853-4864. DOI:10.21873/anticanres.13671 |
| [15] |
Reymond N, Im JH, Garg R, et al. RhoC and ROCKs regulate cancer cell interactions with endothelial cells[J]. Mol Oncol, 2015, 9(6): 1043-1055. DOI:10.1016/j.molonc.2015.01.004 |
| [16] |
韩易, 郑夏林, 孙涛, 等. 肿瘤血管内皮细胞对胶质瘤细胞迁移能力影响的机制研究[J]. 蚌埠医学院学报, 2019, 44(3): 289-292. [Han Y, Zheng XL, Sun T, et al. Study on the mechanism of the tumor vascular endothelial cells influencing the migration ability of glioma cells[J]. Bengbu Yi Xue Yuan Xue Bao, 2019, 44(3): 289-292.] |
| [17] |
Sánchez-Martínez C, Lallena MJ, Sanfeliciano SG, et al. Cyclin dependent kinase (CDK) inhibitors as anticancer drugs: Recent advances (2015-2019)[J]. Bioorg Med Chem Lett, 2019, 29(20): 126637. DOI:10.1016/j.bmcl.2019.126637 |
| [18] |
Medda N, De SK, Maiti S. Different mechanisms of arsenic related signaling in cellular proliferation, apoptosis and neo-plastic transformation[J]. Ecotoxicol Environ Saf, 2021, 208: 111752. DOI:10.1016/j.ecoenv.2020.111752 |
| [19] |
Ding J, Xu K, Sun S, et al. SOCS1 blocks G1-S transition in hepatocellular carcinoma by reducing the stability of the CyclinD1/CDK4 complex in the nucleus[J]. Aging (Akbabt NY), 2020, 12(4): 3962-3975. |
| [20] |
陈佳琳, 林翠燕, 赖美燕, 等. 超声微泡介导Caprin-1-KO转染对人肝癌HepG2细胞增殖, 周期及cyclinD1, cyclinD2表达的影响[J]. 实用医学杂志, 2021, 37(10): 1250-1256. [Chen JL, Lin CY, Lai MY, et al. Effects of the proliferation, cycle and the expression of cyclinD1 and cyclinD2 in human hepatoma HepG2 cells after Caprin-1-KO transfection mediated by ultrasound-microbubbles[J]. Shi Yong Yi Xue Za Zhi, 2021, 37(10): 1250-1256. DOI:10.3969/j.issn.1006-5725.2021.10.004] |
| [21] |
程婧, 倪月莉, Luther AY, 等. 乙酰辅酶A羧化酶1通过调控CyclinD1/CDK4影响肾透明细胞癌细胞增殖[J]. 中国生物化学与分子生物学报, 2021, 37(6): 743-751. [Cheng J, Ni YL, Luther AY, et al. Acetyl-CoA Carboxylase 1(ACC1) Affects the Proliferation of Clear Cell Renal Cell Carcinoma (ccRCC) by Regulating Cyclin D1/CDK4[J]. Zhongguo Sheng Wu Hua Xue Yu Fen Zi Sheng Wu Xue Bao, 2021, 37(6): 743-751.] |
| [22] |
Cabral-Pacheco GA, Garza-Veloz I, Castruita-De la Rosa C, et al. The Roles of Matrix Metalloproteinases and Their Inhibitors in Human Diseases[J]. Int J Mol Sci, 2020, 21(24): 9739. DOI:10.3390/ijms21249739 |
| [23] |
Napoli S, Scuderi C, Gattuso G, et al. Functional Roles of Matrix Metalloproteinases and Their Inhibitors in Melanoma[J]. Cells, 2020, 9(5): 1151. DOI:10.3390/cells9051151 |
| [24] |
Wang X, Yang B, She Y, et al. The lncRNA TP73-AS1 promotes ovarian cancer cell proliferation and metastasis via modulation of MMP2 and MMP9[J]. J Cell Biochem, 2018, 119(9): 7790-7799. DOI:10.1002/jcb.27158 |
| [25] |
邓文松, 马巧玲, 张晓云, 等. miR-181a靶向RASSF1A促进多发性骨髓瘤U266细胞增殖、侵袭[J]. 临床检验杂志, 2020, 38(3): 191-195. [Deng WS, Ma QL, Zhang XY, et al. miR-181a targeting RASSF1A promotes the proliferation and invasion of multiple myeloma U266 cells[J]. Lin Chuang Jian Yan Za Zhi, 2020, 38(3): 191-195.] |
| [26] |
Noorolyai S, Shajari N, Baghbani E, et al. The relation between PI3K/AKT signalling pathway and cancer[J]. Gene, 2019, 698: 120-128. DOI:10.1016/j.gene.2019.02.076 |
| [27] |
Arisanty D, Harahap WA, Khambri D, et al. The Comparison of RhoC and PI3K Gene Expression on the Breast Cancer Tissue and Benign Tumour Tissue[J]. Open Access Maced J Med Sci, 2019, 7(12): 1911-1916. DOI:10.3889/oamjms.2019.543 |
| [28] |
Xie Y, Shi X, Sheng K, et al. PI3K/Akt signaling transduction pathway, erythropoiesis and glycolysis in hypoxia (Review)[J]. Mol Med Rep, 2019, 19(2): 783-791. |
| [29] |
胡桂芳, 董珂, 陆静峰, 等. 青蒿琥酯联合亚砷酸通过PI3K/AKT信号通路对多发性骨髓瘤细胞增殖及凋亡的影响[J]. 中国实验血液学杂志, 2021, 29(6): 1819-1824. [Hu GF, Dong K, Lu JF, et al. Effects of Artesunate Combined with Arsenious Acid on Proliferation and Apoptosis of Multiple Myeloma Cells via PI3K/AKT Signaling Pathway[J]. Zhongguo Shi Yan Xue Ye Xue Za Zhi, 2021, 29(6): 1819-1824.] |
 2022, Vol. 49
2022, Vol. 49


