文章信息
- PTENP1对结直肠癌细胞增殖和凋亡的影响及其分子机制
- Effect of PTENP1 on Proliferation and Apoptosis of Colorectal Cancer Cells and Its Molecular Mechanism
- 肿瘤防治研究, 2022, 49(3): 192-196
- Cancer Research on Prevention and Treatment, 2022, 49(3): 192-196
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2022.21.0819
- 收稿日期: 2021-07-19
- 修回日期: 2022-01-04
2. 450003 郑州,河南省人民医院,郑州大学人民医院,河南大学人民医院肿瘤中心
2. Department of Oncology, Henan Provincial People's Hospital, People's Hospital of Zhengzhou University, People's Hospital of Henan University, Zhengzhou 450003, China
结直肠癌是指从齿状线至直肠乙状结肠交界处之间的癌,是消化道最常见的恶性肿瘤之一,其发病率和致死率仅次于胃癌、食管癌和原发性肝癌等消化系统肿瘤,成为严重影响人类健康的疾病之一[1]。结直肠癌发病机制较为复杂,是遗传因素和外界环境共同作用的结果。探讨其发病机制对于结直肠癌的诊治具有重要价值。长链非编码RNA(LncRNA)是一类长度大于200 nt、不能编码蛋白质的RNA,其在表观遗传、细胞周期和细胞分化调控等生命活动中发挥重要作用[2]。PTENP1属于LncRNAs的一种,与PTEN高度同源,能与PTEN靶标miRNA特异性结合,进而调节PTEN蛋白的表达[3]。PTENP1在乳腺癌、肾癌、前列腺癌和肝癌等多种肿瘤组织中异常表达,并与患者临床病理特征和预后密切相关[4-7]。然而,有关PTENP1在结直肠癌中的表达和功能,目前报道尚少。本研究探讨了PTENP1在结直肠癌组织及细胞系中的表达及其生物学功能,旨在探讨其在结直肠癌发生发展中的可能机制,为结直肠癌的分子诊断提供新的靶点。
1 材料与方法 1.1 一般资料选取2017年3月—2019年3月在郑州人民医院手术切除的107例结直肠癌及对应的癌旁组织作为研究对象,术后均经病理学确诊。其中男70例,女37例;年龄39~79岁,平均年龄(60.25±9.38)岁;其中结肠癌69例,直肠癌38例;所有患者均为初治,临床资料完整。排除良性结直肠肿瘤患者和严重免疫缺陷疾病患者。癌旁组织经病理检测未出现病理学改变。本研究经本院医学伦理委员会许可和监督,所有患者均签署知情同意书。
1.2 实验材料HT29结肠癌细胞系购自美国ATCC公司;DMEM培养基、胰酶、青链霉素和胎牛血清等细胞培养试剂均购自南京维森特生物有限公司;CCK8试剂盒和Annexin V-FITC细胞凋亡检测试剂盒均购自上海碧云天生物科技有限公司;PTENP1和空载体慢病毒由山东维真生物有限公司构建及包装;PTEN兔多克隆抗体购自美国Abcam公司;双荧光素酶报告基因试剂盒购自北京Promega公司;miR-21 mimic和对照mimic购自上海吉玛生物有限公司;HRP标记羊抗兔二抗购自北京中山金桥生物有限公司。荧光定量PCR引物由上海生工生物合成。
1.3 细胞培养及稳定细胞系构建HT29结肠癌细胞系置于含10%FBS的DMEM培养基中培养至对数生长期后,接种于6孔板中,待细胞贴壁后,分别加入PTENP1和空载体慢病毒,感染12 h,更换含有2 μg/ml嘌呤霉素的新鲜完全培养基,继续培养24 h,存活细胞即为PTENP1过表达细胞系和空载体细胞系,实验分为两组:PTENP1组(PTENP1过表达细胞系)和对照组(空载体细胞系)。此外,生物信息学研究显示PTENP1 3’UTR与miR-21存在碱基配对。为了寻找PTENP1的下游靶基因,分别将野生型PTENP1(PTENP1-WT)、miR-21结合区域的突变体PTENP1(PTENP1-Mut)载体转染至mimics对照和miR-21 mimics过表达的细胞中,以检测荧光素酶活性。
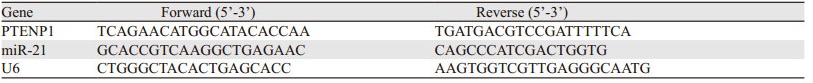
1.4 荧光定量PCR收集癌旁组织、结肠癌组织、对照组和PTENP1组细胞,采用TRIzol法提取总RNA,分光光度计测定总RNA浓度,并将1 μg总RNA反转录为cDNA,用于后续荧光定量PCR分析。为了计算PTENP1的相对表达水平,根据PTENP1和miR-21的序列信息,设计荧光定量PCR引物,其中U6为内参,见表 1。制备以下反应体系:SYBR Green PCR mix 10 µl,上游引物0.6 µl,下游引物0.6 µl,cDNA模板8.8 µl,总体积20 µl。按照下列条件进行PCR:95℃ 5 min,95℃ 5 s,60℃ 30 s,72℃ 30 s,共40个循环。相对mRNA表达水平采用2-ΔΔCT法表示。
待对照组和PTENP1组细胞生长至对数生长期,胰酶消化后将密度调整为每毫升1×105个细胞,96孔板每孔接种100 μl,每组设置3个复孔,待细胞贴壁后,分别在培养24、48、72 h时,加入10 μl CCK8溶液,37℃培养2 h,然后采用酶标仪在450 nm波长处测定细胞吸光度值。
1.6 流式细胞术分析对照组和PTENP1组细胞用不含EDTA的胰酶消化,每毫升1×106个细胞密度收集细胞,1 000 r/min离心5 min,弃上清液,PBS洗涤一次,细胞重悬于400 µl Annexin V-FITC结合液中,并加入5 µl Annexin V-FITC,混匀后室温避光孵育30 min,PBS洗涤未结合的Annexin V-FITC,重悬于结合缓冲液,加5 µl碘化丙锭染色液,冰上孵育5 min,采用流式细胞术分析两组细胞凋亡比例。实验重复3次。
1.7 双荧光素酶报告基因分析为了进一步确定PTENP1与miR-21是否存在碱基互补关系,分别将构建好的PTENP1-WT、PTENP1-Mut载体转染至mimics对照和miR-21 mimics过表达的细胞中,48 h后,采用双荧光素酶报告基因试剂盒检测荧光素酶活性。
1.8 Western blot检测对照组和PTENP1组细胞收集后,采用细胞裂解液提取总蛋白并变性,进行聚丙烯酰胺凝胶电泳,PTEN兔多克隆抗体和Tubulin抗体浓度采用1:300,其中Tubulin为内参对照,羊抗兔二抗的浓度为1:5 000,5%脱脂牛奶封闭后进行电化学发光自显影,通过生物图像处理软件计算蛋白条带灰度值,蛋白相对表达水平=目的条带灰度值/内参蛋白灰度值。
1.9 统计学方法所有数据均采用SPSS17.0统计学软件进行分析,计量数据采用平均值±标准差表示,计量数据比较采用t检验,P < 0.05为差异有统计学意义。
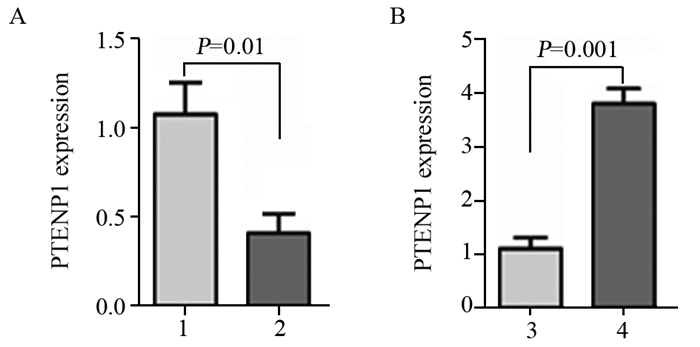
2 结果 2.1 肿瘤组织和细胞系PTENP1表达水平分析与癌旁组织比较,结肠癌组织中PTENP1表达水平显著下调,差异有统计学意义(P=0.01)。与对照组细胞比较,PTENP1组细胞PTENP1的表达水平显著增加,差异有统计学意义(P=0.001),表明转染成功,见图 1。
|
| 1: adjacent tissue; 2: colorectal cancer tissue; 3: control group; 4: PTENP1 group. 图 1 荧光定量PCR检测肿瘤组织(A)和细胞系(B)中PTENP1的表达水平 Figure 1 PTENP1 expression level in tumor tissues(A) and cell lines(B) detected by fluorescence quantitative PCR |
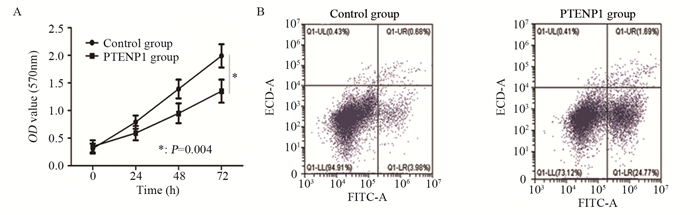
与对照组24、48和72 h细胞吸光度值比较,PTENP1组24、48和72 h吸光度值显著下降,差异有统计学意义(P=0.004),见图 2A。与对照组(5.01±1.25)%比较,PTENP1组凋亡细胞比率(34.12±5.79)%显著增加,差异有统计学意义(P=0.009),见图 2B。
|
| 图 2 CCK8和流式细胞术分别检测PTENP1对细胞增殖(A) 和凋亡(B)的影响 Figure 2 Effect of PTENP1 on cell proliferation(A) and apoptosis(B) detected by CCK8 and flow cytometry |
生物信息学结果显示:PTENP1与miR-21存在碱基互补,见图 3。双荧光素酶报告基因显示,野生型PTENP1(PTENP1-WT)转染至miR-21 mimics过表达的细胞后荧光素酶活性(0.44±0.04)明显低于转染mimics过表达的细胞(1.00±0.03),差异有统计学意义(P=0.001)。而PTENP1(PTENP1-Mut)质粒转染至mimics对照(1.02±0.11)和miR-21 mimics过表达的细胞后荧光素酶活性(0.98±0.09)比较差异无统计学意义(P=0.571)。与对照组细胞miR-21表达水平(0.61±0.06)比较,PTENP1组细胞miR-21表达水平(0.21±0.04)显著下降,差异有统计学意义(P=0.001)。
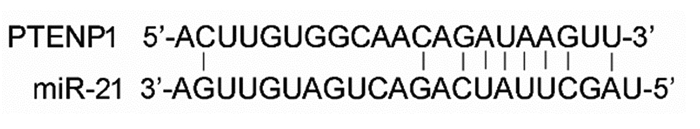
|
| 图 3 生物信息学分析PTENP1与miR-21相互关系 Figure 3 Relation between PTENP1 and miR-21 analyzed by bioinformatics |
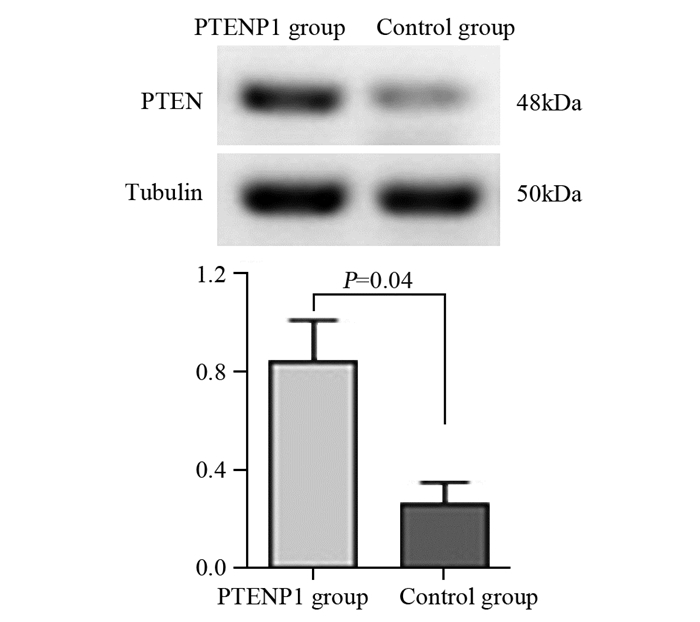
PTEN是miR-21的靶基因,Western blot分析显示,与对照组比较,PTENP1组细胞PTEN蛋白表达水平显著增加,差异有统计学意义(P=0.04),见图 4。
|
| 图 4 Western blot法检测PTENP1对靶蛋白PTEN的影响 Figure 4 Effect of PTENP1 on target protein PTEN analyzed by Western blot |
非编码RNA是一类不能编码蛋白质的RNA,包括长链非编码RNA(LncRNA)和微小RNA(microRNA)等,起初被认为是“垃圾RNA”[8]。但是,随着研究的不断深入,人们发现非编码RNA在细胞发育、细胞分化、基因表达调控等诸多方面发挥着重要作用。LncRNA作为一种非编码RNA,以癌基因和抑癌基因角色在肿瘤发生、发展和转移过程中发挥着重要作用。目前已经发现诸多LncRNA在肿瘤组织中异常表达,并与临床病理特征和预后密切相关[9-10]。PTENP1是LncRNA家族成员之一,研究显示其在膀胱癌、乳腺癌和胃癌中起着抑癌基因的作用,其表达紊乱与肿瘤的增殖、侵袭和凋亡密切相关[11-13]。本研究采用荧光定量PCR分析了癌旁组织和结肠癌组织中PTENP1表达水平,研究结果显示结肠癌组织中PTENP1表达水平较癌旁组织显著下降,说明PTENP1在结直肠癌中异常表达,可能参与了结直肠癌的发生和发展。
LncRNA PTENP1被认为是肿瘤抑制因子PTEN的假基因[14],而PTEN编码一种具有蛋白酪氨酸磷酸酶结构域的细胞质蛋白,并且PTEN在保持染色体完整性和细胞周期进程中发挥着重要作用[15]。前期研究发现,哺乳动物的假基因PTENP1可以作为竞争的内源RNA,通过竞争性结合祖先基因共享的miRNA而调节PTEN的表达[16]。然而,PTENP1如何调控PTEN的表达,其作用机制尚不清楚。为了分析PTENP1对结直肠癌细胞生物学行为的影响,本研究在结肠癌细胞系中建立了PTENP1过表达稳定细胞系,采用CCK8和流式细胞术分析了PTENP1对细胞增殖和凋亡的影响。研究结果显示,PTENP1过表达显著抑制结肠癌细胞的增殖,促进结肠癌细胞的凋亡,说明PTENP1可通过诱导细胞凋亡抑制肿瘤细胞的增殖,在结直肠癌中起着抑癌基因的作用。这一研究结果与PTENP1在其他肿瘤中的作用一致。LncRNA对靶基因的调控主要通过与靶基因相互作用的miRNA竞争性结合进而发挥生物学功能。因此,本研究采用生物信息学和双荧光素酶报告基因分析发现PTENP1与miR-21存在碱基互补,PTENP1与miR-21竞争性结合后,影响miR-21靶基因的表达水平进而调控肿瘤细胞的生物学行为。目前报道显示miR-21与PTEN 3’非编码区存在碱基互补,进而调控PTEN蛋白表达, PTEN是抑癌基因,其水平下调会导致细胞癌基因和抑癌基因平衡被打破,促进肿瘤的发生和发展[17-19]。本研究证实,PTENP1过表达细胞中,miR-21表达水平显著下调,导致PTEN蛋白表达水平上调,进而抑制肿瘤细胞增殖,促进肿瘤细胞凋亡。
总之,本研究结果证实,PTENP1在结肠癌组织中低表达,PTENP1通过miR-21/PTEN轴调节结直肠癌细胞增殖和凋亡,本研究为结直肠癌的早期诊断、开发新的治疗手段奠定良好的实验基础。
作者贡献:
胡晓舒:实验设计及操作、文章撰写
温一阳:确定研究方向、实验设计及文章修改
杨金花:实验操作、标本收集
| [1] |
Fidler MM, Soerjomataram I, Bray F. A global view on cancer incidence and national levels of the human development index[J]. Int J Cancer, 2016, 139(11): 2436-2446. DOI:10.1002/ijc.30382 |
| [2] |
Anastasiadou E, Jacob LS, Slack FJ. Non-coding RNA networks in cancer[J]. Nat Rev Cancer, 2018, 18(1): 5-18. DOI:10.1038/nrc.2017.99 |
| [3] |
Liu L, Liao JZ, He XX, et al. The role of autophagy in hepatocellular carcinoma: friend or foe[J]. Oncotarget, 2017, 8(34): 57707-57722. DOI:10.18632/oncotarget.17202 |
| [4] |
Yndestad S, Austreid E, Skaftnesmo KO, et al. Divergent Activity of the Pseudogene PTENP1 in ER-Positive and Negative Breast Cancer[J]. Mol Cancer Res, 2018, 16(1): 78-89. DOI:10.1158/1541-7786.MCR-17-0207 |
| [5] |
Qian YY, Li K, Liu QY, et al. Long non-coding RNA PTENP1 interacts with miR-193a-3p to suppress cell migration and invasion through the PTEN pathway in hepatocellular carcinoma[J]. Oncotarget, 2017, 8(64): 107859-107869. DOI:10.18632/oncotarget.22305 |
| [6] |
Yu G, Yao W, Gumireddy K, et al. Pseudogene PTENP1 functions as a competing endogenous RNA to suppress clear-cell renal cell carcinoma progression[J]. Mol Cancer Ther, 2014, 13(12): 3086-3097. DOI:10.1158/1535-7163.MCT-14-0245 |
| [7] |
Ou L, Xiang TY, Hao XY, et al. Reduced long non-coding RNA PTENP1 contributed to proliferation and invasion via miR-19b/MTUS1 axis in patients with cervical cancer[J]. Eur Rev Med Pharmacol Sci, 2020, 24(8): 4132-4144. |
| [8] |
Ning S, Li X. Non-coding RNA resources[J]. Adv Exp Med Biol, 2018, 1094: 1-7. |
| [9] |
Liu F, Gao H, Li S, et al. Long non-coding RNA ZFAS1 correlates with clinical progression and prognosis in cancer patients[J]. Oncotarget, 2017, 8(37): 61561-61569. DOI:10.18632/oncotarget.18633 |
| [10] |
Pang EJ, Yang R, Fu XB, et al. Overexpression of long non-coding RNA MALAT1 is correlated with clinical progression and unfavorable prognosis in pancreatic cancer[J]. Tumour Biol, 2015, 36(4): 2403-2407. DOI:10.1007/s13277-014-2850-8 |
| [11] |
Zheng R, Du M, Wang X, et al. Exosome-transmitted long non-coding RNA PTENP1 suppresses bladder cancer progression[J]. Mol Cancer, 2018, 17(1): 143. DOI:10.1186/s12943-018-0880-3 |
| [12] |
Gao X, Qin T, Mao J, et al. PTENP1/miR-20a/PTEN axis contributes to breast cancer progression by regulating PTEN via PI3K/AKT pathway[J]. J Exp Clin Cancer Res, 2019, 38(1): 256. DOI:10.1186/s13046-019-1260-6 |
| [13] |
Zhang R, Guo Y, Ma Z, et al. Long non-coding RNA PTENP1 functions as a ceRNA to modulate PTEN level by decoying miR-106b and miR-93 in gastric cancer[J]. Oncotarget, 2017, 8(16): 26079-26089. DOI:10.18632/oncotarget.15317 |
| [14] |
Wang L, Zhang N, Wang Z, et al. Pseudogene PTENP1 Functions as a Competing Endogenous RNA (ceRNA) to Regulate PTEN Expression by Sponging miR-499-5p[J]. Biochemistry(Mosc), 2016, 81(7): 739-747. |
| [15] |
Squatrito M, Holland EC. DNA damage response and growth factor signaling pathways in gliomagenesis and therapeutic resistance[J]. Cancer Res, 2011, 71(18): 5945-5949. DOI:10.1158/0008-5472.CAN-11-1245 |
| [16] |
Travis G, Haddadi N, Simpson AM, et al. Studying the oncosuppressive functions of PTENP1 as a ceRNA[J]. Methods Mol Biol, 2021, 2324: 165-185. |
| [17] |
Li X, Dai Y, Xu J. MiR-21 promotes pterygium cell proliferation through the PTEN/AKT pathway[J]. Mol Vis, 2018, 24: 485-494. |
| [18] |
Hao XJ, Xu CZ, Wang JT, et al. miR-21 promotes proliferation and inhibits apoptosis of hepatic stellate cells through targeting PTEN/PI3K/AKT pathway[J]. J Recept Signal Transduct Res, 2018, 38(5-6): 455-461. DOI:10.1080/10799893.2019.1585452 |
| [19] |
Zhao MY, Wang LM, Liu J, et al. MiR-21 suppresses anoikis through targeting PDCD4 and PTEN in human esophageal adenocarcinoma[J]. Curr Med Sci, 2018, 38(2): 245-251. DOI:10.1007/s11596-018-1872-7 |
 2022, Vol. 49
2022, Vol. 49