文章信息
- NAIF1对胃癌细胞中IFIT家族蛋白的影响
- Effect of NAIF1 on IFIT Family Proteins in Gastric Cancer
- 肿瘤防治研究, 2022, 49(2): 90-94
- Cancer Research on Prevention and Treatment, 2022, 49(2): 90-94
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2022.21.0551
- 收稿日期: 2021-05-17
- 修回日期: 2021-10-21
2. 100020 北京,国家癌症中心/国家肿瘤临床医学研究中心/中国医学科学院北京协和医学院肿瘤医院;
3. 510000广州,中国科学院广州生物医药与健康研究院
2. National Cancer Center/National Clinical Research Cencer for Cancer/Cancer Hospital, Chinese Academy of Medical Sciences and Peking Union Medical Colloge, Beijing 100020, China;
3. Guangzhou Institutes of Biomedicine and Health, Chinese Academy of Sciences, Guangzhou 510000, China
胃癌是我国常见的消化道肿瘤之一,是全球第五常见癌症,也是引起全球癌症死亡的重要原因之一。2018年全球统计显示,胃癌新发病例103万人,癌症死亡率中,胃癌位居第二[1]。尽管数十年来胃癌亚洲年龄标准化的发病率已经出现降低的趋势,但是随着人口老龄化的加剧,胃癌的发病率和死亡率正逐年增高[2-5]。在我国,胃癌已经成为第三常见癌症[6]。核诱导凋亡因子(nuclear apoptosis-inducing factor 1, NAIF1)作为凋亡因子首次在宫颈癌细胞中被发现[7],随后其被报道在包括胃癌[8-10]、肺癌[11]、前列腺癌[12]、神经胶质瘤[13]以及骨肉瘤[14]等多种人类癌症中起到抑瘤作用。其中,NAIF1在胃癌中的研究发现,NAIF1通过MAPK信号通路抑制癌细胞的迁移和侵袭[9],通过caspase-9信号通路促进胃癌细胞的凋亡[8]。不仅如此,NAIF1还可以通过阻滞细胞周期进而抑制胃癌细胞的生长[10]。探索胃癌细胞中NAIF1在基因及蛋白水平所引起的变化,为胃癌的治疗提供研究基础具有重要意义。本研究通过对过表达NAIF1的胃癌细胞进行基因表达谱芯片检测,寻找NAIF1的相关因子并探讨其相互作用,以期为胃癌的分子靶向治疗提供理论基础。
1 材料与方法 1.1 细胞培养胃癌细胞系MKN45培养于含10%胎牛血清、100 mg/ml青霉素和100 mg/ml链霉素的DMEM培养基中,上述材料均购自美国Gibco公司。置于37℃,5%CO2恒温培养箱培养。细胞系为本实验室保存。
1.2 细胞转染及处理将生长状态良好的MKN45细胞以1×106个每毫升浓度接种于6孔板,置常规37℃培养箱中培养,细胞生长约60%时转染。转染24 h后加入强力霉素(Dox)至终浓度为6 μg/μl,加药处理0、6、12、24 h后收集细胞进行观察,其中加药后0 h细胞记为空白对照组。
1.3 感受态菌株DH5: Genotype: supE44Δ lacU169 (Φ80 lacZΔM15) hsdR17 recAl endA1 gyrA96 thi-1 relA1和Turbo Competent E.coli: F' proA+B+lacIqΔlacZM15 /fhuA2 Δ (lac-proAB) glnV galK16 galE15 R (zgb-210 : : Tn10) TetS endA1 thi-1 Δ (hsdS-mcrB)5均为本实验室保存。
1.4 质粒Tet-on系统质粒pLVX-Tight-Flag-NAIF1-puro带有Flag标签,由本实验室保存。
1.5 实时荧光定量PCR(qRT-PCR)qRT-PCR技术用于IFIT1/2/3/5基因表达量的检测,PCR引物由Thermo北京分公司合成,其中IFIT1上游引物为:5'-GCGCTGGGTATGCGATCTC-3',下游引物为:5'-CAGCCTGCCTTAGGGGAAG-3';IFIT2上游引物为:5'-GACACGGTTAAAGTGTGGAGG-3',下游引物为:5'-TCCAGACGGTAGCTTGCTATT-3';IFIT3上游引物为:5'-AATGGAGATCTGCTGCAAGCAGC-3',下游引物为:5'-TGGCCCATTTCCTCACTACCATC-3';IFIT5上游引物为:5'-ACAAGTTGGAGTGTCCTGAGA-3'。以GAPDH为内参照,其上游引物为:5'-ACAACTTTGGTATCGTGGAAGG-3',下游引物为:5'-GCCATCACGCCACAGTTTC-3'。
1.6 表达谱芯片选取表达谱芯片采用Agilent公司的Human Gene Expression v3.0(8*60K),该款芯片包含约26 083条Entrez Gene RNAs(unique)及30 606条lncRNAs(unique)。mRNA探针设计参照数据库为:RefSeq Build 66、Ensemble Release 76、Unigene Build 236、GenBank(Aug 2014)。ncRNA探针设计主要来源数据库为:LNCipedia Version 2.1、Broad Institute Human lincRNA catalog(Nov 2011)、Broad Institute TUCP transcripts catalog(Nov 2011)。
1.7 Western blot检测蛋白表达适量细胞裂解液提取转染相应时间的细胞总蛋白,通过BCA法测定总蛋白浓度,以GAPDH蛋白为内参调平蛋白总量进行聚丙烯酰胺凝胶电泳,分离后的蛋白转PVDF膜,5%脱脂奶粉封闭30 min,洗膜,加入相应一抗,其中GAPDH抗体、IFIT1抗体和Flag抗体购自Cell Signaling Technology公司,IFIT2、IFIT3和IFIT5抗体则均为Abcam公司产品,孵育过夜,加入相对应的辣根过氧化物酶表达的二抗,显色后处理。
1.8 统计学方法采用SPSS19.0软件进行统计学分析,计量资料呈正态分布,多组间比较采用单因素方差分析,两两组间比较采用SNK检验,检验水准为α=0.05。
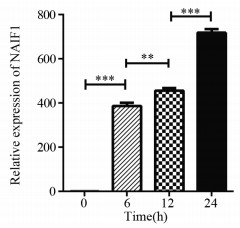
2 结果 2.1 MKN45细胞转染pLVX-Tight-Flag-NAIF1-puro后NAIFI的表达情况qRT-PCR结果显示,MKN45细胞系转染NAIF1后,0、6、12和24 h的NAIF1 mRNA相对表达量分别为1.0±0.007、386.8±8.338、456.3±7.130和718.0±9.705。与0 h相比,转染6、12、24 h后NAIFI mRNA水平明显增加,差异均有统计学意义(均P < 0.0001)。转染6、12、24 h后NAIF1 mRNA水平两两比较,差异均有统计学意义(均P < 0.01),见图 1。提示在MKN45细胞中转染NAIF1后能够在mRNA水平提高外源性NAIF1的水平。
|
| **: P < 0.01; ***: P < 0.0001. 图 1 qRT-PCR检测MKN45中NAIF1的表达 Figure 1 Expression of NAIF1 in MKN45 cells detected by qRT-PCR |
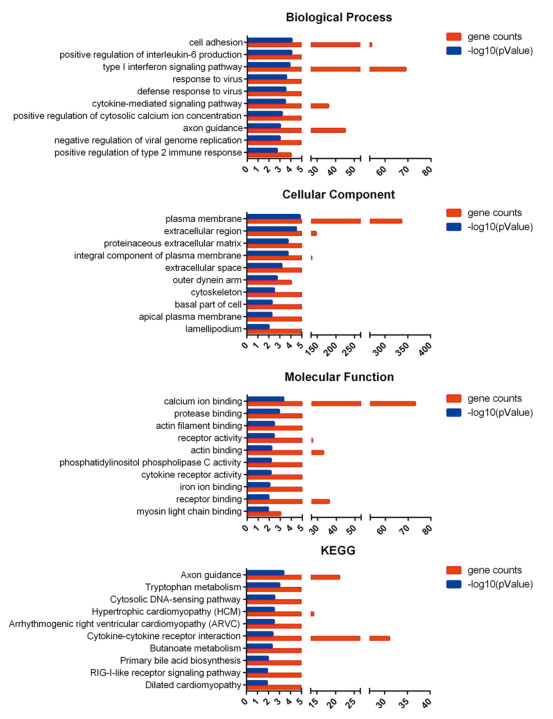
MKN45细胞系中转染NAIF1后,分别从GO方向的生物过程、细胞组成、分子功能及KEGG信号通路方向对差异基因进行注释,其中免疫相关生物过程差异基因有较多富集,见图 2。
|
| 图 2 过表达NAIF1的MKN45细胞系的基因表达谱分析 Figure 2 Gene expression profiling of MKN45 cells with NAIF1 overexpression |
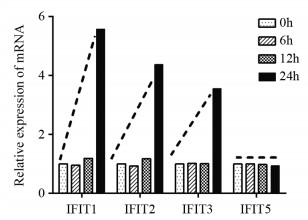
结果表明,与0 h对比,过表达NAIF1的MKN45细胞系中IFIT1、IFIT2、IFIT3的表达量在24 h时明显增大(斜率k分别为0.20、0.15、0.11),与NAIF1表达量呈正相关;IFIT5的表达量随时间的增加无明显变化,见图 3。结果提示MKN45细胞中转染NAIF1能够促进IFIT家族部分蛋白在mRNA水平的表达。
|
| 图 3 基因芯片检测MKN45细胞系中过表达NAIF1后IFIT家族基因的表达 Figure 3 Expression of IFIT family genes after NAIF1 overexpression in gastric cancer cells detected by gene microarray |
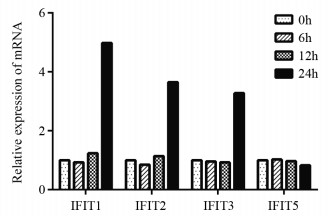
为了验证上述基因表达谱的结果,以相同方法收集0、6、12、24 h细胞,通过qRT-PCR技术验证IFIT家族蛋白的表达水平。结果显示:与芯片杂交结果相一致,IFIT1、IFIT2、IFIT3的基因mRNA水平24 h时有增加的趋势,且与12 h相比,24 h时,IFIT1、IFIT2、IFIT3 mRNA水平有明显增加(P < 0.0001),IFIT5家族mRNA水平表达则无明显变化,且与12 h相比,24 h的IFIT5表达水平反而降低,见图 4。
|
| 图 4 qRT-PCR法验证MKN45细胞系中过表达NAIF1后IFIT家族基因的表达 Figure 4 Expression of IFIT family genes after NAIF1 overexpression in MKN45 cells verified by qRT-PCR |
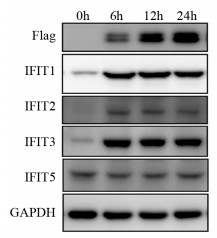
为了进一步验证上述结果,用Western blot检测其蛋白水平表达与否及其差异。胃癌细胞系MKN45中,以转染Flag-NAIF1的0 h为对照,以GAPDH蛋白为内参照,6、12和24 h后NAIF1蛋白表达水平增加,证明转染后蛋白表达成功。继而观察IFIT家族蛋白的变化,其中与转染0 h比较,转染6、12和24 h后IFIT1,IFIT2以及IFIT3蛋白表达量增加,而IFIT5蛋白表达量无变化,见图 5。
|
| 图 5 Western blot法检测MKN45细胞系中过表达NAIF1后的IFIT家族蛋白的表达 Figure 5 Expression of IFIT family proteins after NAIF1 overexpression in MKN45 cells detected by Western blot |
肿瘤的形成是在大量蛋白因子及信号通路的参与下引起细胞增殖与凋亡过程失衡的结果[15],在其形成过程中,许多基因起到了重要的调节作用,其中包括信号通路[16]、细胞周期与凋亡[17]及细胞增殖与凋亡基因[18]等。因此,探讨癌症的发生发展机制并寻找基于分子水平上的治疗靶点,促进癌症治疗领域的开发和应用,可为后续癌症基础机制研究和疾病治疗提供可能的指导方向。
本研究通过在胃癌细胞中过表达外源性NAIF1蛋白并做基因表达谱芯片检测,筛选与之作用的蛋白因子,进一步通过qRT-PCR和Western blot技术在mRNA和蛋白水平验证其对细胞生长相关的蛋白分子的影响,结果显示,过表达NAIF1蛋白能够促进细胞内源性干扰素诱导蛋白(IFIT)家族的部分蛋白的表达,提示NAIF1可能与IFIT家族蛋白有相互关联,根据上述结果推测NAIF1或许通过与IFIT蛋白相互作用起到调节癌症细胞发展的作用,此部分研究有待进一步的验证。
IFIT家族蛋白与癌症发展有重要的联系,NAIF1作为凋亡诱导因子,本研究结果表明,过表达NAIF1促进IFIT1、IFIT2及IFIT3内源性分子的转录和翻译过程,基于此结果,推测NAIF1通过促进IFIT家族蛋白的表达抑制癌症细胞发展。有研究表明,IFIT2的表达降低能够提高癌症转移率[19],高表达IFIT2蛋白与患者存活率呈正相关[20],在细胞水平的研究结果表明IFIT1和IFIT3具有促进肿瘤侵袭的作用[21],另外,IFIT家族不同蛋白之间是否有协同或者竞争的关联未见研究报道。因此,NAIF1在胃癌中细胞水平的作用机制仍需进一步的深入研究。此方向的研究可为NAIF1的分子靶向治疗提供一定的理论依据,有望成为胃癌患者治疗的一个新指标。
作者贡献:
张巧:实验研究、数据分析和论文撰写
黄常志、祝建疆、李燕、赵玫、李可心、李东东:参与论文写作和修订
戚红、黄声凯:研究设计及构思、提供基金资助
| [1] |
Bray F, Ferlay J, Soerjomataram I, et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2018, 68(6): 394-424. DOI:10.3322/caac.21492 |
| [2] |
Rahman R, Asombang AW, Ibdah JA. Characteristics of gastric cancer in Asia[J]. World J Gastroenterol, 2014, 20(16): 4483-4490. DOI:10.3748/wjg.v20.i16.4483 |
| [3] |
Hamashima C. Current issues and future perspectives of gastric cancer screening[J]. World J Gastroenterol, 2014, 20(38): 13767-13774. DOI:10.3748/wjg.v20.i38.13767 |
| [4] |
郑荣寿, 孙可欣, 张思维, 等. 2015年中国恶性肿瘤流行情况分析[J]. 中华肿瘤杂志, 2019, 41(1): 19-28. [Zheng RS, Sun KX, Zhang SW, et al. Report of cancer epidemiology in China, 2015[J]. Zhonghua Zhong Liu Za Zhi, 2019, 41(1): 19-28. DOI:10.3760/cma.j.issn.0253-3766.2019.01.005] |
| [5] |
孙秀娣, 牧人, 周有尚, 等. 中国胃癌死亡率20年变化情况分析及其发展趋势预测[J]. 中华肿瘤杂志, 2004, 26(1): 4-6. [Sun XD, Mu R, Zhou YS, et al. Analysis of mortality rate of stomach cancer and its trend in twenty years in China[J]. Zhonghua Zhong Liu Za Zhi, 2004, 26(1): 4-6. DOI:10.3760/j.issn:0253-3766.2004.01.002] |
| [6] |
Cao W, Chen HD, Yu YW, et al. Changing profiles of cancer burden worldwide and in China: a secondary analysis of the global cancer statistics 2020[J]. Chin Med J(Engl), 2021, 134(7): 783-791. |
| [7] |
Lv B, Shi T, Wang X, et al. Overexpression of the novel human gene, nuclear apoptosis-inducing factor 1, induces apoptosis[J]. Int J Biochem Cell Biol, 2006, 38(4): 671-683. DOI:10.1016/j.biocel.2005.11.007 |
| [8] |
Luo Q, Zhao M, Zhong J, et al. NAIF1 is down-regulated in gastric cancer and promotes apoptosis through the caspase-9 pathway in human MKN45 cells[J]. Oncol Rep, 2011, 25(4): 1117-1123. |
| [9] |
Yang M, Gu YY, Peng H, et al. NAIF1 inhibits gastric cancer cells migration and invasion via the MAPK pathways[J]. J Cancer Res Clin Oncol, 2015, 141(6): 1037-1047. DOI:10.1007/s00432-014-1865-2 |
| [10] |
Yang M, Zhong J, Zhao M, et al. Overexpression of nuclear apoptosis-inducing factor 1 altered the proteomic profile of human gastric cancer cell MKN45 and induced cell cycle arrest at G1/S phase[J]. PLoS One, 2014, 9(6): e100216. DOI:10.1371/journal.pone.0100216 |
| [11] |
Zhao G, Liu L, Zhao T, et al. Upregulation of miR-24 promotes cell proliferation by targeting NAIF1 in non-small cell lung cancer[J]. Tumour Biol, 2015, 36(5): 3693-3701. DOI:10.1007/s13277-014-3008-4 |
| [12] |
Fu Y, Cao F. MicroRNA-125a-5p regulates cancer cell proliferation and migration through NAIF1 in prostate carcinoma[J]. Onco Targets Ther, 2015, 8: 3827-3835. |
| [13] |
Wu X, Hu C, Long C, et al. MicroRNA-351 Promotes the Proliferation and Invasion of Glioma Cells through Downregulation of NAIF1[J]. J Mol Neurosci, 2020, 70(10): 1493-1499. DOI:10.1007/s12031-020-01582-z |
| [14] |
Kong D, Zhang Z. NAIF1 suppresses osteosarcoma progression and is regulated by miR-128[J]. Cell Biochem Funct, 2018, 36(8): 443-449. DOI:10.1002/cbf.3365 |
| [15] |
Hausman DM. What Is Cancer?[J]. Perspect Biol Med, 2019, 62(4): 778-784. DOI:10.1353/pbm.2019.0046 |
| [16] |
Li L, Tang P, Li S, et al. Notch signaling pathway networks in cancer metastasis: a new target for cancer therapy[J]. Med Oncol, 2017, 34(10): 180. DOI:10.1007/s12032-017-1039-6 |
| [17] |
Leal-Esteban LC, Fajas L. Cell cycle regulators in cancer cell metabolism[J]. Biochim Biophys Acta Mol Basis Dis, 2020, 1866(5): 165715. DOI:10.1016/j.bbadis.2020.165715 |
| [18] |
Vajaria BN, Patel PS. Glycosylation: a hallmark of cancer?[J]. Glycoconj J, 2017, 34(2): 147-156. DOI:10.1007/s10719-016-9755-2 |
| [19] |
Lai KC, Liu CJ, Chang KW, et al. Depleting IFIT2 mediates atypical PKC signaling to enhance the migration and metastatic activity of oral squamous cell carcinoma cells[J]. Oncogene, 2013, 32(32): 3686-3697. DOI:10.1038/onc.2012.384 |
| [20] |
Lai KC, Chang KW, Liu CJ, et al. IFN-induced protein with tetratricopeptide repeats 2 inhibits migration activity and increases survival of oral squamous cell carcinoma[J]. Mol Cancer Res, 2008, 6(9): 1431-1439. DOI:10.1158/1541-7786.MCR-08-0141 |
| [21] |
Pidugu VK, Yen AH, Chen YC, et al. Abstract 3933: Characterization of oncogenic activity of interferon-induced protein with tetratricopeptide repeats 1 and 3 in human oral squamous cell carcinoma progression[J]. Cancer Res, 2017, 77(13 Suppl): 3933. |
 2022, Vol. 49
2022, Vol. 49


