文章信息
- 血清PTX3在肝细胞癌中的表达及临床意义
- Expression and Clinical Significance of Serum PTX3 in Hepatocellular Carcinoma
- 肿瘤防治研究, 2021, 48(12): 1078-1081
- Cancer Research on Prevention and Treatment, 2021, 48(12): 1078-1081
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2021.21.0756
- 收稿日期: 2021-06-29
- 修回日期: 2021-10-19
肝细胞癌是全球第六大常见癌症,同时也是癌症相关死亡的第三大原因。数据显示2020年全球新增肝癌病例超过900000例[1]。目前,甲胎蛋白(alpha-fetoprotein, AFP)是临床上诊治肝细胞癌最常用的生物标志物,但其特异性较差,筛查和诊断价值并不高[2-4]。因此,寻找新的肝细胞癌早期诊断标志物是临床实践的迫切需要。穿透素-3(pentraxin-3, PTX3)是由8个亚基组成的同源多聚糖蛋白,属于正五聚蛋白家族[5]。功能上,PTX3在炎性反应、组织修复及肿瘤免疫中发挥重要作用[6-8]。近年来有研究表明,PTX3也与某些类型癌症的预后有关,比如结直肠癌[9]、肺癌[10]、胃癌[11]等。此外,PTX3已被证明能够促进肝癌的进展,且肿瘤组织PTX3高表达与肝癌患者的不良预后具有相关性[12]。但血清中PTX3水平在肝细胞癌中的作用仍待进一步研究,本研究旨在分析血清中PTX3水平在肝细胞癌中的诊断价值,以期为此类疾病的早期诊断提供参考。
1 资料与方法 1.1 一般资料选择2019年1月—2020年7月平顶山市第一人民医院收治的78例肝癌患者,其中27例病因与非酒精性脂肪肝有关、30例合并乙型肝炎病毒(hepatitis B virus, HBV)感染、8例酒精性肝病和13例隐源性肝癌。根据《原发性肝癌诊疗规范》[13]中所述中国肝癌的分期方案(China liver cancer staging, CNLC)进行分期:Ⅰ期20例(Ⅰa期13例、Ⅰb期7例)、Ⅱ期27例(Ⅱa期6例、Ⅱb期21例)、Ⅲ期31例(Ⅲa期4例、Ⅲb期27例)。纳入标准:(1)根据病史、临床症状、实验室、影像学及病理学检查确诊为原发性肝癌;(2)采集血液前未接受放化疗及免疫抑制剂治疗;(3)无家族遗传病和精神疾病史。排除标准:(1)有自身免疫性肝炎、系统性红斑狼疮等自身免疫性疾病及其他系统严重疾病者;(2)妊娠或哺乳期阶段妇女。同时选取本院健康体检者78例作为对照组。本研究获得医院伦理委员会批准,所有患者均签署知情同意书。
1.2 实验方法采集患者的清晨空腹静脉血5 ml,于4℃离心机中以3 000 r/min的速度离心15 min后将上清液置于-80℃冰箱保存待检。采用酶联免疫吸附法检测血清PTX3水平,试剂盒购自上海艾博抗贸易有限公司,操作步骤根据试剂盒中提供的说明书进行。
1.3 统计学方法采用SPSS21.0软件进行数据统计学分析,计量资料用(x±s)表示,两组间比较采用独立样本t检验,多组间比较采用方差分析。计数资料的组间比较采用卡方分析。采用MedCalc 20.009软件构建受试者工作特征(receiver operating characteristics, ROC)曲线。检验水准α设为0.05。
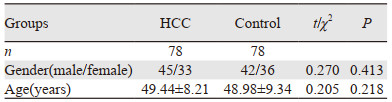
2 结果 2.1 两组研究对象的一般资料比较本研究共纳入肝癌患者78例,健康对照组78例。肝癌组男45例、女33例,平均年龄为(49.44±8.21)岁;健康对照组男42例、女36例,平均年龄为(48.98±9.34)。两组研究对象在年龄和性别资料上差异均无统计学意义(P > 0.05),见表 1。
肝癌组血清PTX3表达水平为14.88±2.13,健康对照组血清PTX3表达水平为5.24±0.49。两组间比较差异有统计学意义(t=25.631, P=0.002)。
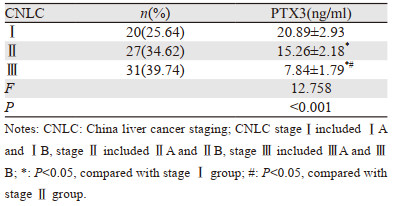
2.3 不同分期肝癌患者血清中PTX3表达的比较Ⅰ期肝癌组血清PTX3水平高于Ⅱ期组,Ⅱ期肝癌组血清PTX3水平高于Ⅲ期组,差异有统计学意义(P < 0.05),见表 2。
|
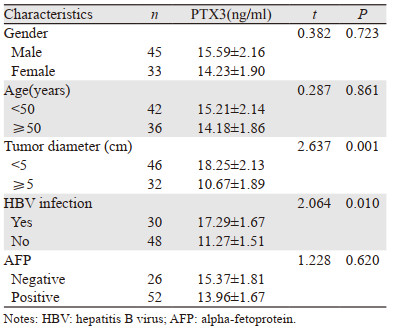
肿瘤直径≥5 cm患者血清中PTX3水平明显低于肿瘤直径 < 5 cm患者(P < 0.05)。合并HBV感染的肝癌患者血清中PTX3水平高于无HBV感染的患者(P < 0.05),见表 3。
|
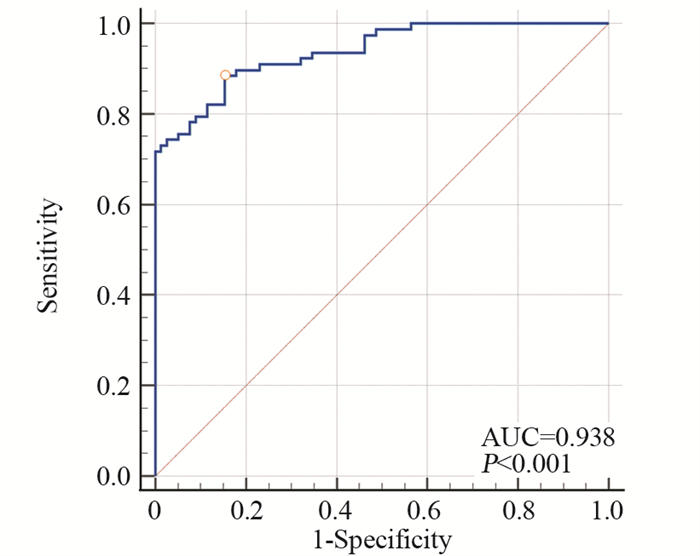
ROC曲线分析结果显示:血清PTX3水平辅助诊断肝癌ROC曲线的AUC为0.938,95%CI为0.888~0.970,敏感度为88.5%,特异性为84.6%,约登指数为0.731,可见其对肝癌诊断的预测能力具有较高的准确性,见图 1。
|
| 图 1 ROC曲线分析血清PTX3水平对肝癌的诊断价值 Figure 1 Prognostic value of serum PTX3 for hepatocellular carcinoma analyzed by ROC curve |
肝癌是一种发生于肝脏的常见恶性肿瘤[14],分为原发性和转移性肝癌,以原发性更多见。肝癌发病隐匿,患者早期无特异性症状,多数患者在中晚期寻求诊断和治疗,往往错过最佳的治疗时间[15]。因此,寻求一种操作简便、非介入性且重复性好的早期肝癌筛查诊断方法一直受到关注。近年来,研究表明多种血液标志物对肝癌的诊断具有良好的预测价值[16-18]。
PTX3又称肿瘤坏死因子刺激基因14(tumor necrosis factor-stimulated gene 14, TSG-14),与C反应蛋白(C reactive protei, CRP)同属于一种在进化中高度保守的正五聚蛋白家族[19-20]。结构上,PTX3有一个与其他已知蛋白无序列相似性的N端结构域和一个C端结构域,由8个亚基组成,含有381个氨基酸[19]。PTX3已在某些肿瘤中被证实是一种外在抑癌因子,通过调节巨噬细胞介导肿瘤进展[7]。然而,PTX3在癌症中是否起到保护或促进作用仍未完全明确。但有研究发现在肝细胞癌中PTX3高表达并通过驱动上皮-间充质转化加速肿瘤转移,提示其与预后不良相关[12]。这提示血清中PTX3水平可能与肝癌的发展相关。
肝癌的诊断主要依靠影像学,但由于影像学检查的放射性,降低了用于肝癌筛查的可能性;又由于影像学检查的敏感度,降低了早期诊断的可能性。相反,血清标志物由于简便快速且成本低廉的特点,普遍被患者所接受。目前,血清AFP水平的检测是最常用的诊断方法。有研究显示,血清AFP水平在部分良性肝病患者中也会处于高水平,但其并未出现肝癌的迹象,而在少数HCC患者AFP呈阴性或水平较低,这导致AFP对肝癌的误诊率较高[2, 21]。因此,临床实践迫切需要发现一种新的肝癌诊断生物标志物。
本研究将肝癌患者及健康体检者作为研究对象,分析血清中PTX3表达水平,并采用ROC曲线分析血清PTX3对肝癌的辅助诊断价值。结果显示,肝癌患者血清中PTX3水平显著升高,提示通过测定机体血清中PTX3水平可能有助于诊断肝细胞癌。Deng等[20]研究表明慢性HBV感染患者血清PTX3水平高于健康对照者,而HCC患者血清PTX3水平高于慢性HBV感染患者,与本研究结果相类似。通过构建裸鼠肝癌模型[12]发现PTX3与上皮间质转分化(epithelial-mesenchymal transition, EMT)相关,可能通过激活EMT加速肝癌细胞的增殖和生长,这提示PTX3可能通过EMT参与调控肝癌进展。有研究结果显示,随着肿瘤分期的增加,肝癌患者血清PTX3水平相应降低,Feder等[22]研究发现肝癌患者中血清PTX3水平并不随着TNM分期而相应增加,而Song等[12]应用免疫组织化学方法检测210例HCC患者肿瘤组织及癌旁组织中的PTX3水平,发现其在肿瘤组织中的表达异常升高,且与肝癌TNM分期显著相关。此外,现有研究证明在癌症中PTX3与补体C1q和H因子相互作用,激活并调节补体级联,从而在人体内作为外源性抑癌因子抑制肿瘤相关炎性反应[23]。不同研究相悖的结果提示PTX3控制肿瘤发展过程中可能有多种因素参与,或许存在一种还未阐明的复杂的调控网络,具体机制仍待进一步研究。
本研究进一步采用ROC曲线分析血清PTX3对肝癌(包括HBV感染者和非HBV感染者)的辅助诊断价值,AUC为0.938,说明血清PTX3表达水平对肝癌的诊断具有较高的准确性,但样本量较少,可能存在一定的偏移,需进一步扩大样本量进行深入研究。
作者贡献:
庞康清:研究设计、实施、数据收集分析、论文撰写及修改
马洪德:数据收集整理
杨汝磊:数据收集分析
庞国宏:研究设计指导、文章写作指导及校对
| [1] |
Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries[J]. CA Cancer J Clin, 2021, 71(3): 209-249. DOI:10.3322/caac.21660 |
| [2] |
Parikh ND, Mehta AS, Singal AG, et al. Biomarkers for the Early Detection of Hepatocellular Carcinoma[J]. Cancer Epidemiol Biomarkers Prev, 2020, 29(12): 2495-2503. DOI:10.1158/1055-9965.EPI-20-0005 |
| [3] |
曹丽荣. 肿瘤标志物联合甲胎蛋白检测方法在原发性肝癌患者中的诊断研究[J]. 中国药物与临床, 2017, 17(6): 909-911. [Chao LR. Study on the diagnosis of primary liver cancer patients with tumor markers combined with alpha-fetoprotein detection[J]. Zhongguo Yao Wu Yu Lin Chuang, 2017, 17(6): 909-911.] |
| [4] |
陈利君, 陈静琦, 曾波航. 肝癌组织中CD68+肿瘤相关巨噬细胞数量与Ki-67蛋白表达及原发性肝癌预后的关系[J]. 肿瘤防治研究, 2016, 43(9): 774-778. [Chen LJ, Chen JQ, Zeng BH, et al. Correlation of CD68+ Tumor-associated Macrophages Number with Ki-67 Expression and Prognosis of Patients with Primary Hepatocellular Carcinoma[J]. Zhong Liu Fang Zhi Yan Jiu, 2016, 43(9): 774-778. DOI:10.3971/j.issn.1000-8578.2016.09.009] |
| [5] |
Inforzato A, Doni A, Barajon I, et al. PTX3 as a paradigm for the interaction of pentraxins with the complement system[J]. Semin Immunol, 2013, 25(1): 79-85. DOI:10.1016/j.smim.2013.05.002 |
| [6] |
Rubino M, Kunderfranco P, Basso G, et al. Epigenetic regulation of the extrinsic oncosuppressor PTX3 gene in inflammation and cancer[J]. Oncoimmunology, 2017, 6(7): e1333215. |
| [7] |
Doni A, Stravalaci M, Inforzato A, et al. The Long Pentraxin PTX3 as a Link Between Innate Immunity, Tissue Remodeling, and Cancer[J]. Front Immunol, 2019, 10: 712. DOI:10.3389/fimmu.2019.00712 |
| [8] |
Daigo K, Inforzato A, Barajon I, et al. Pentraxins in the activation and regulation of innate immunity[J]. Immunol Rev, 2016, 274(1): 202-217. DOI:10.1111/imr.12476 |
| [9] |
Liu B, Zhao Y, Guo L. Increased serum pentraxin-3 level predicts poor prognosis in patients with colorectal cancer after curative surgery, a cohort study[J]. Medicine (Baltimore), 2018, 97(40): e11780. DOI:10.1097/MD.0000000000011780 |
| [10] |
Infante M, Allavena P, Garlanda C, et al. Prognostic and diagnostic potential of local and circulating levels of pentraxin 3 in lung cancer patients[J]. Int J Cancer, 2016, 138(4): 983-991. DOI:10.1002/ijc.29822 |
| [11] |
Choi B, Lee EJ, Park YS, et al. Pentraxin-3 Silencing Suppresses Gastric Cancer-related Inflammation by Inhibiting Chemotactic Migration of Macrophages[J]. Anticancer Res, 2015, 35(5): 2663-2668. |
| [12] |
Song T, Wang C, Guo C, et al. Pentraxin 3 overexpression accelerated tumor metastasis and indicated poor prognosis in hepatocellular carcinoma via driving epithelial-mesenchymal transition[J]. J Cancer, 2018, 9(15): 2650-2658. DOI:10.7150/jca.25188 |
| [13] |
中华人民共和国卫生和计划生育委员会医政医管局. 原发性肝癌诊疗规范(2017年版)[J]. 中华消化外科杂志, 2017, 16(7): 635-647. [Bureau of Medical Administration, Health and Family Planning Commission of the People's Republic of China. Standardization of diagnosis and treatment for hepatocellular carcinoma(2017 edition)[J]. Zhonghua Xiao Hua Wai Ke Za Zhi, 2017, 16(7): 635-647.]
|
| [14] |
叶冬雪, 刘芬, 杨茜, 等. Mina53与CBX8在肝细胞肝癌中的表达及其与临床病理特征和预后的关系[J]. 肿瘤防治研究, 2020, 47(6): 451-456. [Ye DX, Liu F, Yang Q, et al. Expression of Mina 53 and CBX8 in Hepatocellular Carcinoma and Their corelation with Clinicopathological Features and Prognosis[J]. Zhong Liu Fang Zhi Yan Jiu, 2020, 47(6): 451-456. DOI:10.3971/j.issn.1000-8578.2020.19.1341] |
| [15] |
赵荣荣, 邓永东, 袁宏. 236例原发性肝癌患者流行病学及临床特点分析[J]. 临床肝胆病杂志, 2016, 32(8): 1538-1542. [Zhao RR, Deng YD, Yuan H. Epidemiological and clinical features of primary liver cancer: an analysis of 236 patients[J]. Lin Chuang Gan Dan Bing Za Zhi, 2016, 32(8): 1538-1542. DOI:10.3969/j.issn.1001-5256.2016.08.021] |
| [16] |
程书平, 李明, 谭诗云. 血清AFP、PIVKA-Ⅱ、GGT、GGT/ALT检测对早期原发性肝癌的诊断价值[J]. 山东医药, 2021, 26(1): 61-65. [Cheng SP, Li M, Tan SY. The diagnostic value of serum AFP, PIVKA-Ⅱ, GGT, GGT/ALT for early primary liver cancer[J]. Shandong Yi Yao, 2021, 26(1): 61-65. DOI:10.3969/j.issn.1002-266X.2021.01.014] |
| [17] |
杨文聪, 魏统双. 血清miR-122-5p水平联合MSCT对肝癌的诊断价值[J]. 中国CT和MRI杂志, 2021, 19(4): 86-89. [Yang WC, Wei TS. Diagnostic value of serum miR-122-5p level combined with MSCT for liver cancer[J]. Zhongguo CT He MRI Za Zhi, 2021, 19(4): 86-89. DOI:10.3969/j.issn.1672-5131.2021.04.027] |
| [18] |
刘毓键, 马明洋. 血清标志物在肝细胞肝癌早期诊断中的研究进展及应用前景[J]. 医学综述, 2020, 26(7): 1325-1330, 1336. [Liu YJ, Ma MY. Research progress and application prospect of serum markers in early detection of hepatocellular carcinoma[J]. Yi Xue Zong Shu, 2020, 26(7): 1325-1330, 1336. DOI:10.3969/j.issn.1006-2084.2020.07.016] |
| [19] |
彭婉君, 赵彬彬, 武婧, 等. 可溶性识别分子PTX3的研究进展[J]. 中国比较医学杂志, 2020, 30(1): 115-121. [Peng WJ, Zhao BB, Wu J, et al. Research progress on soluble recognition molecule PTX3[J]. Zhongguo Bi Jiao Yi Xue Za Zhi, 2020, 30(1): 115-121. DOI:10.3969/j.issn.1671-7856.2020.01.020] |
| [20] |
Deng H, Fan X, Wang X, et al. Serum pentraxin 3 as a biomarker of hepatocellular carcinoma in chronic hepatitis B virus infection[J]. Sci Rep, 2020, 10(1): 20276. DOI:10.1038/s41598-020-77332-3 |
| [21] |
代伟伟, 刘正新, 徐宝宏. 肝硬化和肝癌患者血清CA125、CA199、AFP和CEA水平变化[J]. 实用肝脏病杂志, 2017, 20(1): 81-84. [Dai WW, Liu ZX, Xu BH. Serum CA125, CA199, AFP, CEA in patients with cirrhosis and primary liver cancer[J]. Shi Yong Gan Zang Bing Za Zhi, 2017, 20(1): 81-84. DOI:10.3969/j.issn.1672-5069.2017.01.021] |
| [22] |
Feder S, Haberl E M, Spirk M, et al. Pentraxin-3 is not related to disease severity in cirrhosis and hepatocellular carcinoma patients[J]. Clin Exp Med, 2020, 20(2): 289-297. DOI:10.1007/s10238-020-00617-4 |
| [23] |
Bonavita E, Gentile S, Rubino M, et al. PTX3 Is an Extrinsic Oncosuppressor Regulating Complement-Dependent Inflammation in Cancer[J]. Cell, 2015, 160(4): 700-714. DOI:10.1016/j.cell.2015.01.004 |
 2021, Vol. 48
2021, Vol. 48