文章信息
- miR-148a靶向STAT3对宫颈癌HeLa细胞顺铂化疗敏感度的增强作用
- Enhanced Effect of miR-148a Targeting STAT3 on Chemosensitivity of Cervical Cancer HeLa Cells to Cisplatin
- 肿瘤防治研究, 2021, 48(8): 762-768
- Cancer Research on Prevention and Treatment, 2021, 48(8): 762-768
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2021.21.0003
- 收稿日期: 2021-01-06
- 修回日期: 2021-06-22
2. 242000 宣城,宣城市中心医院妇产科;
3. 310000 杭州,浙江中医药大学附属新华医院妇产科
2. Department of Obstetrics and Gynecology, Xuancheng Central Hospital, Xuancheng 242000, China;
3. Department of Obstetrics and Gynecology, Xinhua Hospital Affiliated of Zhejiang Chinese Medicine University, Hangzhou 310000, China
宫颈癌是全球常见的妇科恶性肿瘤之一,近年来发病率逐渐升高,且呈年轻化趋势发展[1]。目前,手术前后辅助化疗被认为是治疗宫颈癌有效的治疗方法之一,顺铂作为化疗的常用药物,在宫颈癌新辅助化疗方案中作为基础药物被广泛应用,然而,顺铂具有的肾、耳、血液、胃肠道等不良反应限制了化疗效果[2-3]。因此,寻找可增强宫颈癌顺铂敏感度的基因靶点药物,对降低顺铂用量、减轻不良反应具有重要的应用价值。微小RNA(microRNA, miRNA)是一类小分子非编码单链RNA,通过从转录后水平调控靶基因表达,广泛参与细胞的生长、分化、增殖、凋亡等过程[4]。研究发现,肾癌、乳腺癌等多种类型癌细胞的化疗敏感度均与miR-148a表达相关[5-6],但miR-148a与宫颈癌顺铂耐药的关系尚不明确。信号转导和转录激活因子3(signal transducer and activator of transcription 3, STAT3)参与宫颈癌的发生发展,抑制STAT3通路可提高宫颈癌顺铂敏感度[7]。miRTarBase数据库预测发现,STAT3是miR-148a的潜在靶点,其靶向关系在非小细胞肺癌中已有研究,但在宫颈癌中尚无定论[8]。HeLa细胞是宫颈癌细胞中最为稳定且增殖迅速的细胞系,故本研究将通过调控miR-148a表达,探讨miR-148a靶向STAT3对宫颈癌HeLa细胞顺铂化疗敏感度的影响。
1 材料与方法 1.1 试剂与仪器人HeLa细胞(货号:HZ-H496)购自美国ATCC细胞库;胎牛血清(货号:0025)购自美国ScienCell公司;顺铂(货号:D8810)购自北京索莱宝科技有限公司;DMEM培养基(货号:KL-P0032)购自德国Merck/Sigma公司;Lipofectamine 2000转染试剂(货号:11668019)购自美国Invitrogen公司;实时荧光定量PCR(qRT-PCR)试剂盒(货号:K1002S)、pGL3-basic vector(货号:E1751)购自美国Promega公司;miR-control、miR-148a mimic、nonsense inhibitor、miR-148a inhibitor及miR-148a、STAT3、U6、β-actin引物均由生工生物工程(上海)股份有限公司设计合成;MTT溶液(货号:N/A-896)购自美国AMEKO公司;AnnexinV-FITC/PI细胞凋亡检测试剂盒(货号:S0185)购自哈尔滨新海基因检测有限公司;p-STAT3抗体、STAT3抗体、CyclinD1抗体、Bcl-2抗体、Bax抗体、Cleaved caspase-3抗体、GAPDH抗体、羊抗兔lgG(货号:ab76315、ab119352、ab226977、ab194583、ab81083、ab2302、ab59164、ab6717)均购自美国Abcam公司;双荧光素酶报告基因检测试剂盒(货号:SLDL-100)购自美国BioAssay Systems公司。培养箱(型号:MIR-162-PC/MIR-262-PC)购自日本松下公司;荧光定量PCR仪(型号:ABI 7500)购自美国Applied Biosystems公司;酶标仪(型号:Stat Fax-2100)购自美国Awareness公司;流式细胞仪(型号:Guauasoft 6L)购自美国Millipor公司。
1.2 实验方法 1.2.1 细胞培养用含10%胎牛血清、1%双抗的DMEM培养基培养HeLa细胞,并置于37℃、5% CO2培养箱中常规培养,细胞融合至80%左右时消化、传代,取对数生长期细胞进行实验。
分为对照组(细胞不进行转染)、mimic对照组、miR-148a mimic组、inhibitor对照组和miR-148a inhibitor组。除对照组外,其他组均使用Lipofectamine 2000转染试剂分别转染miR-control、miR-148a mimic、nonsense inhibitor和miR-148a inhibitor。转染步骤:细胞在转染前一天消化、计数铺24孔板,用含血清DMEM培养基培养,使之在转染日密度达90%,并替换为无血清培养基培养;分别取0.8~1.0 µg转染物miR-control、miR-148a mimic、nonsense inhibitor和miR-148a inhibitor并用50 µl DMEM培养基稀释;取2 µl转染试剂Lipofectamine 2000并用DMEM培养基稀释,5 min内与转染物稀释液混合,室温保温20 min后加入每孔中轻轻摇匀,置于37℃、5%CO2培养箱中培养48 h。
1.2.2 qRT-PCR法检测HeLa细胞中miR-148a和STAT3的表达将转染后的各组HeLa细胞以1×105个/毫升接种于96孔培养板,每孔100 μl,培养48 h后收集细胞,使用TRIzol试剂提取细胞总RNA,反转录试剂盒合成cDNA,qRT-PCR试剂盒检测细胞中miR-148a、STAT3 mRNA表达水平,U6、β-actin为内参基因。反应条件:95℃预变性30 s;95℃变性5 s,60℃退火35 s,循环40次。miR-148a上游引物:5'-TCTGAGACACTCCGACTCTGA-3',下游引物:5'-CTGGCGTCTGGAGCACTG-3';STAT3上游引物:5'-ACTCCATCGCTGACAAAA-3',下游引物:5'-CAGTGACCAGGCAGAAGA-3';U6上游引物:5′-CTCGCTTCGGCAGCACA-3′,下游引物:5′-AACGCTTCACGAATTTGCGT-3′;β-actin上游引物:5′-TCCCATCACCATCTTCCAG -3′,下游引物:5′-GGTATCCATCGCCATGCTC-3′。结果分析采用2-ΔΔCt法表示。
1.2.3 MTT法检测HeLa细胞增殖将未转染的HeLa细胞及转染后的各组HeLa细胞以1×105个/毫升接种于96孔培养板,每孔100 μl,未转染的HeLa细胞用不同浓度的顺铂(0、1、2、4、8、16、32、64、128 μmol/L)处理48 h,转染后的各组HeLa细胞用4 μmol/L顺铂处理48 h,每孔加50 μl 5 mg/ml的MTT溶液,置于培养箱继续培养4 h,弃培养液,每孔加入150 μl DMSO,充分溶解后终止反应,根据酶标仪450 nm处测定的各孔吸光度OD值,计算细胞增殖抑制率,增殖抑制率=(OD对照组- OD实验组)/OD对照组×100%。
1.2.4 流式细胞仪检测HeLa细胞凋亡情况将转染后的各组HeLa细胞以1×105个/毫升接种于96孔培养板,每孔100 μl,4 μmol/L顺铂处理48 h后收集细胞,胰酶消化后再次收集,加入400 μl Binding Buffer将细胞重悬,依次加入Annexin V-FITC、PI各5 μl,混匀,避光孵育15 min,流式细胞仪检测细胞凋亡情况。
1.2.5 流式细胞仪检测HeLa细胞周期分布将转染后的各组HeLa细胞以1×105个/毫升接种于96孔培养板,每孔100 μl,4 μmol/L顺铂处理48 h后收集细胞,PBS洗涤,每孔加900 μl 75%乙醇固定过夜,离心收集细胞,PBS洗涤后每孔加500 μl RNase A/PI(50 μg/ml RNase A,50 μg/ml PI)重悬,避光放置20 min,流式细胞仪检测细胞周期分布情况。
1.2.6 Western blot法检测HeLa细胞中STAT3通路相关蛋白表达将转染后的各组HeLa细胞以1×105个/毫升接种于24孔培养板,每孔300 μl,4 μmol/L顺铂处理48 h后收集细胞,加裂解液置于冰上裂解30 min,1200 r/min离心10 min后加200 μl Loading Buffer,100℃煮沸10 min,用BCA蛋白测定试剂盒测定蛋白浓度。10%SDS-PAGE电泳分离蛋白质,半干法转至PVDF膜上,用含5%脱脂奶粉的TBST封闭1.5 h,加入一抗(p-STAT3抗体、STAT3抗体、Cyclin D1抗体、Bcl-2抗体、Bax抗体、Cleaved caspase-3抗体、GAPDH抗体,1:1000)孵育过夜,TBST洗涤3遍,加二抗(羊抗兔,辣根过氧化物酶标记,1:2000)孵育1 h,TBST洗膜3遍,曝光显影,BandScan图像分析系统扫描图像并分析条带灰度,计算目的蛋白与内参蛋白的灰度值比值。
1.2.7 双荧光素酶报告基因实验验证miR-148a与STAT3的靶向作用关系利用miRTarBase网站预测miR-148a与STAT3的靶向关系及潜在结合位点。构建STAT3的野生型、突变型3'UTR-荧光素酶表达载体(STAT3-WT和STAT3-MUT),利用脂质体转染技术将其分别与miR-control、miR-148a mimic共同转入HeLa细胞中,48 h后用双荧光素酶报告基因检测试剂盒测定荧光素酶活性,以萤火虫与海肾荧光素酶活性比值表示荧光素酶相对活性。
1.3 统计学方法采用SPSS19.0版统计软件进行数据分析。所得数据以均数±标准差(x±s)表示,两组比较采用t检验,多组间比较采用单因素方差分析,组间两两比较采用SNK-q检验。P < 0.05为差异有统计学意义。
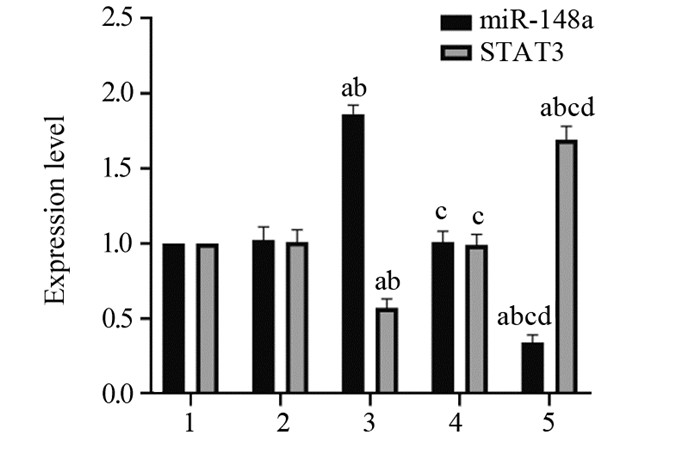
2 结果 2.1 转染后各组HeLa细胞中miR-148a和STAT3的表达转染后,与对照组相比,mimic对照组、inhibitor对照组HeLa细胞中miR-148a、STAT3表达水平差异无统计学意义(P=0.980、0.999,P=0.999、0.999);与mimic对照组相比,miR-148a mimic组HeLa细胞中miR-148a表达水平显著升高(P=0.000),STAT3表达水平显著降低(P=0.000);与inhibitor对照组相比,miR-148a inhibitor组HeLa细胞中miR-148a表达水平显著降低(P=0.000),STAT3表达水平显著升高(P=0.000),见图 1。
|
| a: P < 0.05, compared with control group; b: P < 0.05, compared with mimic control group; c: P < 0.05, compared with miR-148a mimic group; d: P < 0.05, compared with inhibitor control group; STAT3: signal transducer and activator of transcription 3; 1: control group; 2: mimic control group; 3: miR-148a mimic group; 4: inhibitor control group; 5: miR-148a inhibitor group. 图 1 转染后各组HeLa细胞中miR-148a、STAT3的表达水平 Figure 1 Expression level of miR-148a and STAT3 in HeLa cells after transfection |
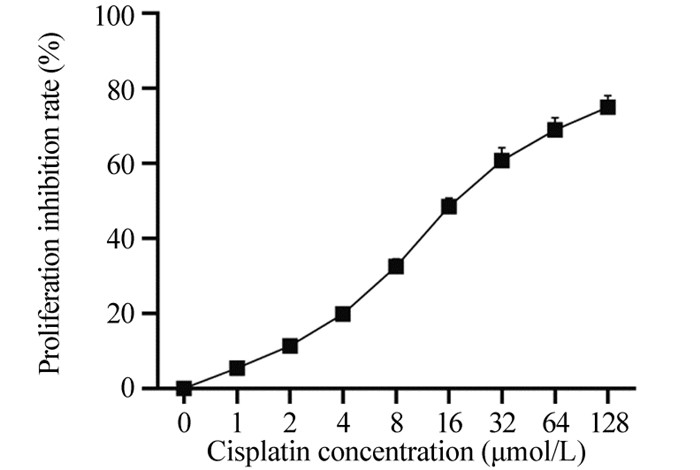
随着顺铂浓度的升高,HeLa细胞增殖抑制率逐渐升高;HeLa细胞的顺铂IC20约为4 μmol/L,见图 2。后续实验将以4 μmol/L为顺铂处理浓度。
|
| 图 2 不同浓度顺铂作用下HeLa细胞增殖抑制率(x±s, n=6) Figure 2 Proliferation inhibition rate of HeLa cells under different concentrations of cisplatin treatment (x±s, n=6) |
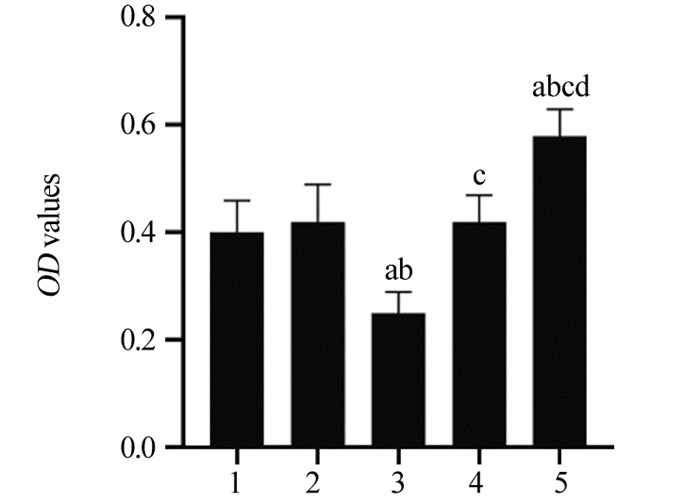
与对照组相比,mimic对照组、inhibitor对照组HeLa细胞OD值差异无统计学意义(P=0.969、0.969);与mimic对照组相比,miR-148a mimic组HeLa细胞OD值显著降低(P=0.000);与inhibitor对照组相比,miR-148a inhibitor组HeLa细胞OD值显著升高(P=0.000),见图 3。
|
| a: P < 0.05, compared with control group; b: P < 0.05, compared with mimic control group; c: P < 0.05, compared with miR-148a mimic group; d: P < 0.05, compared with inhibitor control group; 1: control group; 2: mimic control group; 3: miR-148a mimic group; 4: inhibitor control group; 5: miR-148a inhibitor group. 图 3 各组HeLa细胞OD值 Figure 3 OD values of HeLa cells in each group |
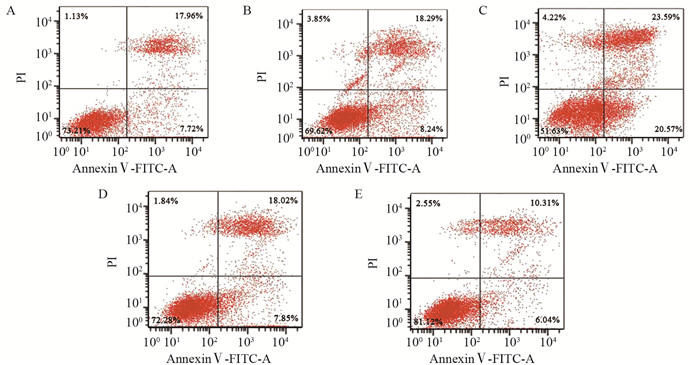
与对照组相比,mimic对照组、inhibitor对照组HeLa细胞凋亡率差异无统计学意义(P=0.952、0.981);与mimic对照组相比,miR-148a mimic组HeLa细胞凋亡率显著升高(P=0.000);与inhibitor对照组相比,miR-148a inhibitor组HeLa细胞凋亡率显著降低(P=0.000),见图 4。
|
| A: control group; B: mimic control group; C: miR-148a mimic group; D: inhibitor control group; E: miR-148a inhibitor group. 图 4 各组HeLa细胞凋亡情况 Figure 4 Apoptosis of HeLa cells in each group |
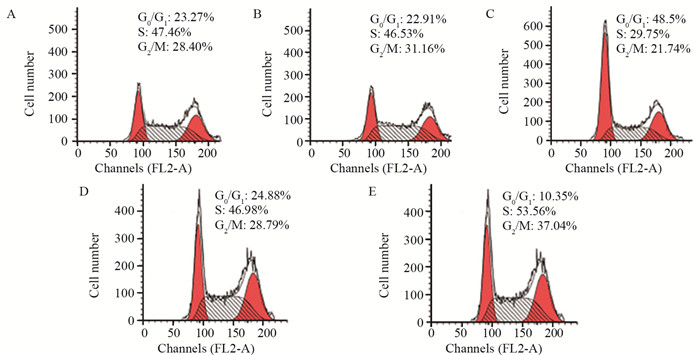
与对照组相比,mimic对照组、inhibitor对照组HeLa细胞G0/G1、S、G2/M期比例差异无统计学意义(P=0.999、0.828, P=0.980、0.998, P=0.437、0.999);与mimic对照组相比,miR-148a mimic组HeLa细胞G0/G1期比例显著升高(P=0.000),S、G2/M期细胞比例显著降低(P=0.000, P=0.000);与inhibitor对照组相比,miR-148a inhibitor组HeLa细胞G0/G1期比例显著降低(P=0.000),S、G2/M期细胞比例显著升高(P=0.005, P=0.002),见图 5。
|
| A: control group; B: mimic control group; C: miR-148a mimic group; D: inhibitor control group; E: miR-148a inhibitor group. 图 5 各组HeLa细胞周期分布情况 Figure 5 Distribution of HeLa cells cycle in each group |
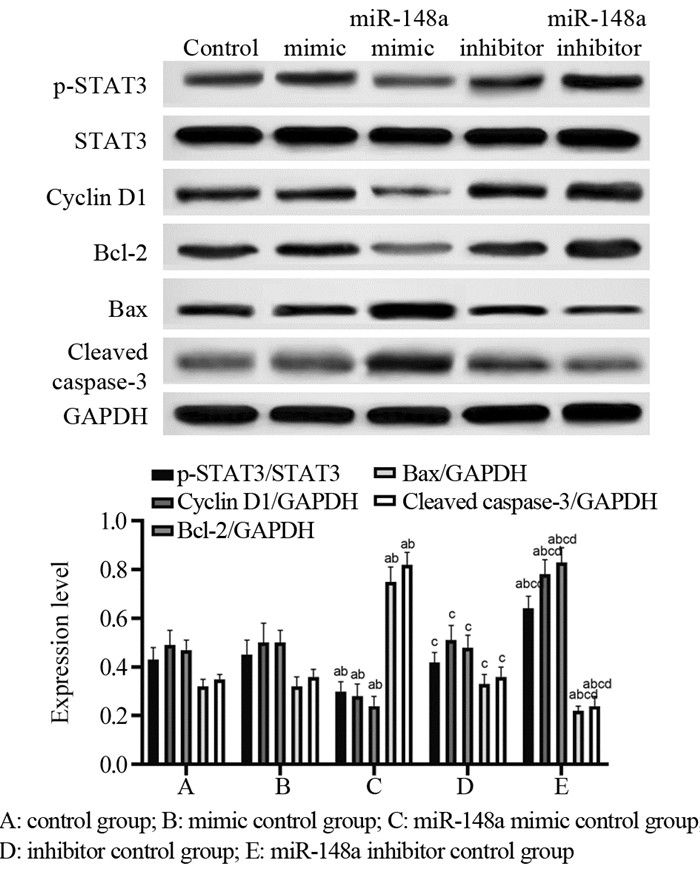
与对照组相比,mimic对照组、inhibitor对照组HeLa细胞中p-STAT3/STAT3、Cyclin D1、Bcl-2、Bax、Cleaved caspase-3蛋白表达水平差异无统计学意义(P=0.952、0.996, P=0.999、0.981,P=0.820、0.996, P=0.999、0.992, P=0.990、0.990);与mimic对照组相比,miR-148a mimic组HeLa细胞中p-STAT3/STAT3、Cyclin D1、Bcl-2蛋白表达水平显著降低(P=0.000, P=0.000, P=0.000),Bax、Cleaved caspase-3蛋白表达水平显著升高(P=0.000, P=0.000);与inhibitor对照组相比,miR-148a inhibitor组HeLa细胞中p-STAT3/STAT3、Cyclin D1、Bcl-2蛋白表达水平显著升高(P=0.000, P=0.000, P=0.000),Bax、Cleaved caspase-3蛋白表达水平显著降低(P=0.007, P=0.000),见图 6。
|
| a: P < 0.05, compared with control group; b: P < 0.05, compared with mimic control group; c: P < 0.05, compared with miR-148a mimic group; d: P < 0.05, compared with inhibitor control group. 图 6 各组HeLa细胞中STAT3通路相关蛋白表达 Figure 6 Expression level of STAT3 pathway-related protein in HeLa cells of each group |
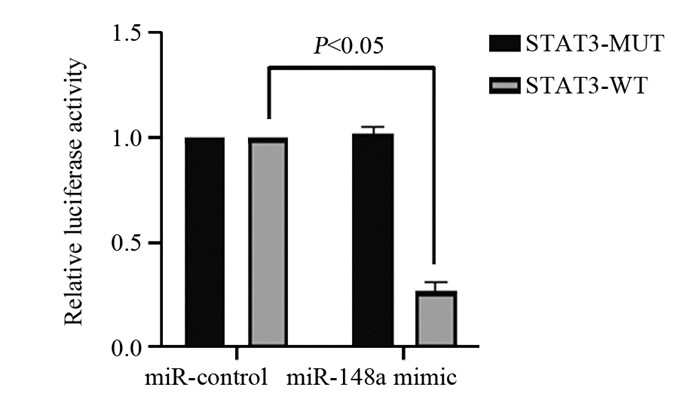
miRTarBase网站预测发现STAT3可能为miR-148a的下游靶基因。双荧光素酶报告基因实验结果显示,miR-148a对转染突变型STAT3 3'UTR-荧光素酶表达载体细胞的荧光素酶活性无明显影响(P=0.134),但可抑制转染野生型STAT3 3'UTR-荧光素酶表达载体细胞的荧光素酶活性(P=0.000),见图 7~8。

|
| 图 7 miRTarBase预测miR-148a与STAT3的靶向关系 Figure 7 Targeting relation between miR-148a and STAT3 predicted by miRTarBase |
|
| 图 8 各组HeLa细胞相对荧光素酶活性 Figure 8 Relative luciferase activity of HeLa cells in each group |
宫颈癌是女性常见恶性肿瘤之一,发病率、死亡率较高,严重威胁女性健康及生命安全。目前,已有包括手术切除、化疗、放疗、激素治疗在内的多种治疗措施被引入并应用于宫颈癌,但肿瘤复发仍是导致宫颈癌患者死亡的主要原因[9]。辅助化疗是减少肿瘤复发的传统治疗策略,可明显提高肿瘤局控率及改善患者生存率[10]。顺铂是化疗的基础药物,但患者在治疗过程中出现各种不良反应,不利于患者的治疗效果及身心健康[11]。临床上常通过联合治疗,在保证癌细胞敏感度不降低的前提下,降低顺铂用药剂量及频次,减轻不良反应[12]。因此,寻找在顺铂低剂量下,提高宫颈癌细胞顺铂化疗敏感度的方法具有重要意义。本研究通过设置顺铂浓度梯度,发现4 μmol/L顺铂最接近HeLa细胞的IC20,故后续实验均以4 μmol/L为顺铂处理浓度。
miRNA是一种非编码小RNA分子,通过与靶基因mRNA的3’未翻译区序列特异性结合,在肿瘤细胞的增殖、凋亡及放化疗敏感度等生物学行为方面发挥重要的调控作用[13-14]。李航等[15]研究表明,人为过表达miR-148a能降低肺癌A549、H1299细胞的增殖能力,并增强其放射敏感度。陈元元等[6]研究中亦发现,miR-148a-3p与乳腺癌的紫杉醇耐药性有关,可用于判断患者的紫杉醇耐药情况。Li等[16]研究认为,miR-148a-3p下调是胃癌患者化疗过程中产生顺铂耐药性的关键步骤,miR-148a-3p可能是克服胃癌顺铂耐药性的预后标志物或治疗候选物。Kim等[5]研究发现,miR-148a能通过靶向Rab14诱导肾癌细胞凋亡,降低肾癌细胞克隆形成性并增加顺铂敏感度。本研究显示,在4 μmol/L顺铂处理过程中,过表达miR-148a后,HeLa细胞OD值及S、G2/M期细胞比例显著降低,凋亡率及G0/G1期细胞比例显著升高;抑制miR-148a表达后,HeLa细胞OD值及S、G2/M期细胞比例显著升高,凋亡率及G0/G1期细胞比例显著降低,提示在顺铂诱导基础上,miR-148a可进一步诱导HeLa细胞,将细胞周期阻滞于G0/G1期,进而抑制HeLa细胞增殖并促进细胞凋亡,增强HeLa细胞的顺铂敏感度。
STAT3是转录信号转导子与激活子家族的重要成员,其持续激活会导致癌细胞中抗凋亡蛋白及细胞周期调控因子上调,促进肿瘤异常增殖及恶性转化[17]。Bcl-2和Bax为Bcl-2家族的重要成员,对细胞凋亡分别具有抑制和促进作用[18]。Caspase-3是各种细胞凋亡途径的共同执行蛋白,Cleaved caspase-3是其活性形式[19]。Cyclin D1是重要的细胞周期调控因子,在细胞从G0期进入G1期过程中发挥重要调控作用[20]。双荧光素酶报告基因实验显示,在HeLa细胞中,STAT3为miR-148a的下游靶基因。进一步通过蛋白检测显示,在4 μmol/L顺铂处理过程中,过表达miR-148a后,HeLa细胞中STAT3 mRNA及蛋白磷酸化水平、Cyclin D1、Bcl-2蛋白水平显著降低,Bax、Cleaved caspase-3蛋白水平显著升高;反之,抑制miR-148a表达后,HeLa细胞中STAT3 mRNA及蛋白磷酸化水平、Cyclin D1、Bcl-2蛋白水平显著升高,Bax、Cleaved caspase-3蛋白水平显著降低,提示在顺铂诱导基础上,miR-148a可能通过靶向抑制STAT3的表达与活化,影响Cyclin D1、Bcl-2、Bax、Cleaved caspase-3蛋白水平,进而调控HeLa细胞的增殖、凋亡、细胞周期进程,增强HeLa细胞的顺铂敏感度。
综上所述,miR-148a可靶向抑制STAT3,在顺铂处理宫颈癌HeLa细胞基础上,抑制HeLa细胞增殖、诱导细胞周期阻滞及细胞凋亡,对HeLa细胞顺铂化疗敏感度具有增强作用,在临床化疗中顺铂小剂量用药方向具有一定前景。
作者贡献:
汤良君:实验设计及实施,论文撰写
孙艳、张晓红:实验实施
盛少琴:实验评估
| [1] |
Li X, Zheng R, Li X, et al. Trends of incidence rate and age at diagnosis for cervical cancer in China, from 2000 to 2014[J]. Chin J Cancer Res, 2017, 29(6): 477-486. DOI:10.21147/j.issn.1000-9604.2017.06.02 |
| [2] |
Zhuang L, Liu F, Peng P, et al. Effect of Ku80 on the radiosensitization of cisplatin in the cervical carcinoma cell line HeLa[J]. Oncol Lett, 2018, 15(1): 147-154. |
| [3] |
Drögemöller BI, Brooks B, Critchley C, et al. Further investigation of the role of ACYP2 and WFS1 pharmacogenomic variants in the development of cisplatin-induced ototoxicity in testicular cancer patients[J]. Clin Cancer Res, 2018, 24(8): 1866-1871. DOI:10.1158/1078-0432.CCR-17-2810 |
| [4] |
Xu J, Zhang L, Shu G, et al. microRNA-16-5p promotes 3T3-L1 adipocyte differentiation through regulating EPT1[J]. BiochemBiophys Res Commun, 2019, 514(4): 1251-1256. DOI:10.1016/j.bbrc.2019.04.179 |
| [5] |
Kim EA, Kim TG, Sung EG, et al. miR-148a increases the sensitivity to cisplatin by targeting Rab14 in renal cancer cells[J]. Int J Oncol, 2017, 50(3): 984-992. DOI:10.3892/ijo.2017.3851 |
| [6] |
陈元元, 唐铁雷, 程永刚, 等. miR-148a-3p、miR-128、miR-588在乳腺癌中的表达情况及其与耐药性的关系[J]. 现代肿瘤医学, 2019, 27(12): 2108-2113. [Chen YY, Tang TL, Cheng YG, et al. The differential expression of miR-148a-3p, miR-128, miR-588 and their association with chemo-resistance in breast cancer[J]. Xian Dai Zhong Liu Yi Xue, 2019, 27(12): 2108-2113. DOI:10.3969/j.issn.1672-4992.2019.12.018] |
| [7] |
Yao T, Lu R, Zhang J, et al. Growth arrest-specific 5 attenuates cisplatin-induced apoptosis in cervical cancer by regulating STAT3 signaling via miR-21[J]. J Cell Physiol, 2019, 234(6): 9605-9615. DOI:10.1002/jcp.27647 |
| [8] |
He M, Xue Y. MicroRNA-148a suppresses proliferation and invasion potential of non-small cell lung carcinomas via regulation of STAT3[J]. Onco Targets Ther, 2017, 10: 1353-1361. DOI:10.2147/OTT.S123518 |
| [9] |
Sun H, Fan G, Deng C, et al. miR-4429 sensitized cervical cancer cells to irradiation by targeting RAD51[J]. J Cell Physiol, 2020, 235(1): 185-193. DOI:10.1002/jcp.28957 |
| [10] |
Jang SH, Jung YJ, Kim MG, et al. The prognostic significance of compliance with postoperative adjuvant chemotherapy in patients with stage Ⅲ gastric cancer: an observational study[J]. J Gastric Cancer, 2018, 18(1): 48-57. DOI:10.5230/jgc.2018.18.e4 |
| [11] |
Shahid F, Farooqui Z, Khan F. Cisplatin-induced gastrointestinal toxicity: an update on possible mechanisms and on available gastroprotective strategies[J]. Eur J Pharmacol, 2018, 827: 49-57. DOI:10.1016/j.ejphar.2018.03.009 |
| [12] |
文习之, 潘求忠, 翁德胜, 等. 聚乙二醇修饰脂质体阿霉素联合顺铂单次给药治疗晚期骨肉瘤的剂量递增试验[J]. 中山大学学报(医学科学版), 2020, 41(4): 582-588. [Wen XZ, Pan QZ, Weng DS, et al. Pegylated liposomal doxorubicin combined with cisplatin for advanced osteosarcoma: a single-dose dose-escalating trial[J]. Zhongshan Da Xue Xue Bao (Yi Xue Ke Xue Ban), 2020, 41(4): 582-588.] |
| [13] |
Potestà M, Roglia V, Fanelli M, et al. Effect of microvesicles from Moringa oleifera containing miRNA on proliferation and apoptosis in tumor cell lines[J]. Cell Death Discov, 2020, 6: 43. |
| [14] |
Du B, Wang X, Wu D, et al. MicroRNA expression profiles identify biomarkers for predicting the response to chemoradiotherapy in rectal cancer[J]. Mol Med Rep, 2018, 18(2): 1909-1916. |
| [15] |
李航, 姜勉, 樊赛军. MiR-148a对肺癌细胞放射敏感性的影响[J]. 国际放射医学核医学杂志, 2018, 42(3): 248-256. [Li H, Jiang M, Fan SJ. Effect of miR-148a on the radiosensitivity of lung cancer cells[J]. Guo Ji Fang She Yi Xue He Yi Xue Za Zhi, 2018, 42(3): 248-256. DOI:10.3760/cma.j.issn.1673-4114.2018.03.010] |
| [16] |
Li B, Wang W, Li Z, et al. MicroRNA-148a-3p enhances cisplatin cytotoxicity in gastric cancer through mitochondrial fission induction and cyto-protective autophagy suppression[J]. Cancer Lett, 2017, 410: 212-227. DOI:10.1016/j.canlet.2017.09.035 |
| [17] |
胡轶, 李雄, 蒋桂英, 等. 曲古抑菌素A下调STAT3增强卵巢癌细胞顺铂化疗敏感性的体外研究[J]. 华中科技大学学报(医学版), 2019, 48(3): 253-257. [Hu Y, Li X, Jiang GY, et al. Tragomycin A Enhances Chemosensitivity to Cisplatin in Ovarian Cancer Cell Lines by Down-regulating STAT3[J]. Hua Zhong Ke Ji Da Xue Xue Bao (Yi Xue Ban), 2019, 48(3): 253-257. DOI:10.3870/j.issn.1672-0741.2019.03.001] |
| [18] |
Wu B, Wang R, Li S, et al. Antifibrotic effects of Fraxetin on carbon tetrachloride-induced liver fibrosis by targeting NF-κB/IκBα, MAPKs and Bcl-2/Bax pathways[J]. Pharmacol Rep, 2019, 71(3): 409-416. DOI:10.1016/j.pharep.2019.01.008 |
| [19] |
Zhang Y, Yang X, Ge X, et al. Puerarin attenuates neurological deficits via Bcl-2/Bax/cleaved caspase-3 and Sirt3/SOD2 apoptotic pathways in subarachnoid hemorrhage mice[J]. Biomed Pharmacother, 2019, 109: 726-733. DOI:10.1016/j.biopha.2018.10.161 |
| [20] |
Zhong Q, Hu Z, Li Q, et al. Cyclin D1 silencing impairs DNA double strand break repair, sensitizes BRCA1 wildtype ovarian cancer cells to olaparib[J]. Gynecol Oncol, 2019, 152(1): 157-165. DOI:10.1016/j.ygyno.2018.10.027 |
 2021, Vol. 48
2021, Vol. 48


