文章信息
- 髓系抑制性细胞对神经母细胞瘤抗原特异性细胞毒性T淋巴细胞体外增殖和杀伤抑制作用
- yeloid-derived Suppressor Cells Inhibit Proliferation and Killing Activity of Neuroblastoma Antigen-specific Cytotoxic T Lymphocyte in vitro
- 肿瘤防治研究, 2017, 44(11): 728-732
- Cancer Research on Prevention and Treatment, 2017, 44(11): 728-732
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.17.0709
- 收稿日期: 2017-06-21
- 修回日期: 2017-09-26
神经母细胞瘤(neuroblastoma, NB)是小儿最常见的神经内分泌性肿瘤,恶性度高、早期易发生转移。临床上尽管采用了手术、放化疗、造血干细胞移植等多种治疗方法,但高危NB患儿的存活率仍低于40%,因此急需一种新的治疗方法来提高NB患儿疗效,减少其复发和转移[1]。免疫治疗在小儿实体肿瘤的应用虽起步较晚,但研究表明NB免疫疗法与传统疗法相比具有更高特异度和更小不良反应,可以有效清除肿瘤细胞,降低肿瘤复发和转移[2]。
然而在NB生存的微环境中存在着各种复杂的免疫抑制因素,包括肿瘤表面HLA-Ⅰ抗原表达下调、各种免疫抑制因子的表达和各种免疫抑制细胞,如髓系抑制性细胞(myeloid-derived suppressor cell, MDSC)、调节性T细胞和肿瘤相关巨噬细胞等的聚集[3-5]。Jales等[6]在研究中则发现NB表面由于特异性抗原抗-双唾液酸神经节苷脂(disialoganglioside, GD2)的高表达,使得肿瘤微环境中MDSC集聚明显增高,启动肿瘤免疫抑制而促进肿瘤发展和转移。所以在这些因素中,MDSC可能是影响NB免疫疗效的主要障碍,其具体作用机制尚不十分清楚。
因此,本研究中,我们拟以BALB/c小鼠为实验对象,在对MDSC体外分离培养的基础上,成功制备NB抗原特异性细胞毒性T淋巴细胞(cytotoxic T lymphocyte, CTL),探讨MDSC对CTL体外增殖及杀伤NB肿瘤细胞活性的影响,完善MDSC造成NB免疫耐受的机制,为NB免疫疗效提供新靶点。
1 材料与方法 1.1 实验动物与细胞株人神经母细胞瘤SK-N-SH细胞株,购自中国医学科学院上海细胞库,储存于含10%胎牛血清(美国Gibco公司)和2 ml谷氨酰胺(中国华北制药厂)的培养液中,在5%CO2加湿培养箱中37℃孵育。
健康6周龄雌性BALB/c小鼠,体重18~20 g,购自河北省实验动物中心(许可证编号SCXK冀2008-1-003),饲养于河北省实验动物中心(SPF级动物实验室,SYXK(冀)2008-0026)。饲养室温度控制在(25±1)℃,高效过滤器每小时换气10~15次,相对湿度保持在40%~60%,每日保持12 h光照、12 h无光的明暗周期。饲养笼具及饮用水均经过高压消毒,饲养笼具及垫料每 3 天更换1次,动物饲料以及垫料均应用60Co进行灭菌处理。
1.2 MDSC体外分离与纯化BALB/c小鼠脱颈处死后取骨髓细胞制成单细胞悬液,加入2 ml红细胞裂解液,用吸管轻轻吹打后静置3 min,以含10%胎牛血清的RPMI 1640培养液终止红细胞裂解反应,离心洗涤细胞,用培养液调整细胞浓度,置冰上备用。分别采用抗Gr-1-FITC、抗CD11b-PE、抗CD80-PE、抗F4/80-FITC、抗CD11c-PE以及抗MHC-Ⅱ-FITC抗体进行染色,流式细胞仪检测Gr-1+ CD11b+细胞的比例以及MDSC的分化程度。
采用Percoll密度梯度离心法初步分离MDSC。预先用PBS悬浮上述骨髓细胞,将一吸管插至15 ml离心管中,沿吸管壁依次缓缓注入PBS、50%、60%、70%和100%Percoll溶液悬浮的上述骨髓细胞各2 ml,2 900 r/min离心30 min,收集50%和60% Percoll溶液之间的细胞悬液,PBS洗3次,调整细胞浓度至2×107个每毫升,置冰上备用。上述细胞进一步以抗CD11b抗体染色,采用美天旎磁珠分离纯化CD11b阳性细胞,获得的细胞约90%为Gr-1+ CD11b+MDSC。
1.3 神经母细胞瘤抗原特异性CTL制备 1.3.1 BALB/c小鼠骨髓来源树突状细胞(dendritic cell, DC)的提取、培养和功能鉴定BALB/c小鼠脱颈处死,无菌状态下取股骨和胫骨,浸泡于RPMI 1640培养液中。1 ml注射器吸取培养液,刺入骨髓腔,冲洗骨髓至无菌培养皿中。收集骨髓细胞悬液,1 500 r/min,离心5 min。弃上清液,加入3 ml红细胞裂解液,室温静置3 min,加入培养液终止。离心后弃上清液,再用RPMI 1640洗2遍。悬浮细胞按1×106个每毫升浓度分至6孔培养板,每孔加入培养液至4 ml,再加入rmGM-CSF(20 ng/ml)、rmIL-4(20 ng/ml)。将培养板放入37℃、5%CO2培养箱培养48 h。第3天更换细胞因子和培养液,继续培养至第5天。半量换液,并补足rmGM-CSF。第6天加入rmTNF-α(15 ng/ml),继续培养至第7天,吸管吹打后收集悬浮细胞,即为富集的小鼠骨髓来源DC。相差显微镜下观察DC形态特征。细胞按每管1×106数量行流式细胞学检测,检测CD11c、MHC-Ⅱ和CD86表达水平。
1.3.2 肿瘤抗原负载DC对数生长期SK-N-SH细胞重悬,调整细胞浓度至2×107个/毫升,快速冷冻细胞至-80℃,然后于37℃水浴复温,循环4次,10 000 r/min离心15 min,收集上清液,于-80℃冻存备用。取培养6 d的DC,按每毫升培养液加入相当于2×106个肿瘤细胞的裂解物,4 h后再加入重组小鼠TNF-α,培养至第7天,收集悬浮细胞,即为负载肿瘤抗原DC。相差显微镜观察抗原刺激活化后DC细胞形态,流式细胞术检测细胞CD11c、CD86和MHC-Ⅱ表达率。
1.3.3 小鼠脾脏CD3+T细胞的提取、鉴定及培养利用小鼠CD3+T细胞磁珠分选试剂盒分选小鼠脾脏淋巴细胞悬液提取CD3+T细胞,可重复磁铁筛选操作若干次,每只小鼠脾脏可提取约3×106个T淋巴细胞。收集分离纯化的细胞,取部分细胞流式检测鉴定T细胞纯度。细胞调整浓度至5×106个每毫升,加入含rmIL-2(20 ng/ml)的全培养液中原代培养2天后相差显微镜观察细胞形态,锥虫蓝检测细胞活力。
1.3.4 SK-N-SH细胞抗原特异性CTL制备及细胞因子释放检测在CD3+T细胞培养2天后,在培养瓶中按DC:T=1:20比例加入已负载肿瘤抗原的成熟DC,同时补充rmIL-2(20 ng/ml)混合培养3~4天后,倒置显微镜下观察T细胞形态。留取激活的T细胞72 h后产生的各组CTL上清液,根据酶标仪测量的样本吸光度OD450值和标准曲线计算IL-2和IFN-γ浓度。比较各组上清液中IL-2和IFN-γ差异。
1.4 MDSC对SK-NK-SH抗原特异性CTL增殖的抑制实验活化后的CTL用CFSE(终浓度5μmol/L[7])进行染色,分为两组,一组与磁珠分选后Gr-1+CD11b+MDSC(4:1)混合,以CD3/CD28抗体刺激CTL增殖;另一组不加MDSC,其他条件相同。每一组均设置平行对照组,对照组处理方式与实验组完全相同。培养4 d后,荧光显微镜观察,流式细胞术检测细胞增殖情况。
1.5 MDSC对抗原特异性CTL体外杀伤SK-N-SH细胞效应的影响将CTL和MDSC+CTL(4:1)分别同SK-N-SH肿瘤细胞混合共孵育(E:T=20:1),同时设空白对照、靶细胞(SK-N-SH)对照、效应细胞(抗原特异性CTL)对照组。培养孵育后加入CCK-8 20微升每孔,用酶标仪在450 nm波长处测定实验孔A值。每孔数值减去空白孔对照,求出3个复孔的平均A值,按下面公式计算效应细胞的细胞毒活性,以杀伤率表示:杀伤率(%)=[靶细胞对照A值-(实验孔A值-效应细胞对照A值)]/靶细胞对照A值×100%。对比各组间CTL对SK-N-SH细胞的杀伤率。ELISA检测对比各组上清中IL-2、IFN-γ的分泌量。
1.6 统计学方法所有资料采用SPSS 22.0进行统计分析,计量资料采用(x±s)表达。CTL对SK-N-SH杀伤率的比较采用成组设计资料的t检验。各组上清液中IFN-γ和IL-2比较采用重复测量方差分析。P≤0.05为差异有统计学意义。
2 结果 2.1 MDSC的分离、提取和鉴定MDSC细胞Gr-1、CD11b、CD11c、CD80、F4/80、MHC-Ⅱ的表达率分别为70.4%、3.5%、4.8%、1.2%、0.3%、2.1%,而Gr-1+CD11b+MDSC的表达率为27.5%。
Percoll密度梯度离心法分离后的MDSC细胞悬液进行CD11b磁珠分选,流式检测显示磁珠分选纯化后Gr-1+ CD11b+MDSC比例为84.6%。
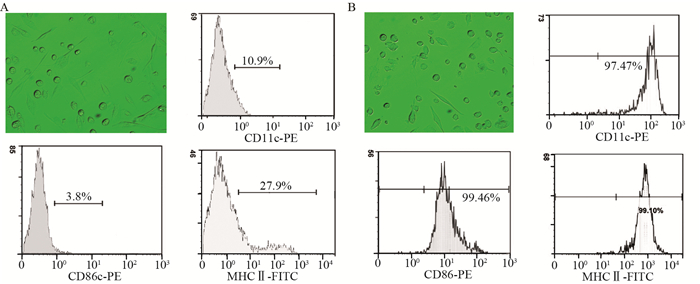
2.2 SK-N-SH细胞抗原特异性CTL制备和细胞因子释放检测结果活化前,DC培养第6天相差显微镜观察,可见大部分细胞贴壁生长,形态大小不等,有突起,呈星型或梭型,部分细胞表面粗糙,呈半贴壁状态。流式细胞术检测CD11c、CD86和MHC-Ⅱ的表达率分别为10.9%、3.8%和27.9%,抗原提呈能力较弱,见图 1A。
|
| A: most of dendritic cells without antigen loaded could be seen adherent growth with different size, star or spindle shape and stretching tubers, but part of the cells seemed half adherent state with rough surface (× 200). The expressive rates of CD11c, CD86 and MHC-Ⅱ on DCs were 10.9%, 3.8% and 27.9% respectively by flow cytometry; B: at the 7th day, DCs were stimulated and activated by tumor antigen. DCs in half adherent state increased obviously with radial spike and bigger shape (× 200). The expression rates of CD11c, CD86 and MHC-Ⅱ were 97.47%, 99.46% and 99.10% respectively by flow cytometry 图 1 活化前、后DC形态学变化及CD11c、CD86和MHC-Ⅱ表达 Figure 1 Morphological variation of DCs and expression of CD11c, CD86 and MHC-Ⅱ before and after activation |
第7天肿瘤抗原刺激活化后DC细胞,可见半贴壁细胞明显增多,形态较大且刺突明显,部分细胞悬浮生长,带有放射状刺突,形态较大。流式细胞术检测CD11c、CD86和MHC-Ⅱ表达率分别为97.47%、99.46%和99.10%,提示DC已经成熟,具备了高效提呈抗原的能力,见图 1B。
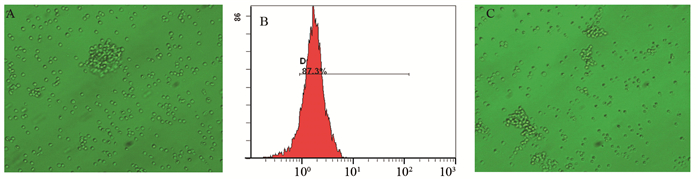
磁珠分选提取CD3+T细胞,流式细胞术检测鉴定T细胞纯度达87.3%。原代培养2天后出现了很多大小不一的细胞集落,提示T细胞扩增活化。锥虫蓝细胞活力检测活细胞率达96.38%。在CD3+T细胞中加入负载肿瘤抗原的成熟DC,倒置显微镜下观察可见T细胞的形态逐渐变得不规则,在DC集落的附近又出现了很多小的T细胞集落,见图 2。DC将负载的抗原提呈给T细胞后,上清液中IL-2[(1.092±0.010)ng/L]和IFN-γ[(0.855±0.038)ng/L]含量明显较单纯培养T细胞上清液中[(0.962±0.007)ng/L、(0.765±0.010)ng/L]含量高,差异有统计学意义(F=27.144, P=0.001; F=620.231, P=0.000)。
2.3 MDSC对SK-NK-SH抗原特异性CTL增殖的抑制
|
| A: CD3+T cells were extracted from mice spleen lymphocytes suspension by MACS (× 200); B: purity of CD3+T cells reached to 87.3% by flow cytometry; C: after two days' cultivation, T cell showed amplification and activation with many cell colonies in the view (× 200) 图 2 CD3+T细胞的纯度鉴定和扩增活化 Figure 2 Extraction, identification and cultivation of CD3+T cells |
培养4 d后荧光显微镜观察两组CFSE染色后的CTL,发现培养前两组CTL细胞数相同,而培养后未加MDSC组细胞密度明显增大,染色强度变弱;与MDSC共培养组细胞数目却未见增多,染色强度仍较强,见图 3A。

|
| Neuroblastoma antigen-specific CTLs in the two groups were stained by CFSE. A: under fluorescence microscopy, the number of CTLs was same in the two groups before cultivation (×200); B: after cultivation for four days, cell fluorescent intensity was weakened but cell density was increased obviously in CTL group. However, in CTL+MDSC group, cell fluorescent intensity remained strong and cell number was increased slightly (×200); C: flow cytometry results showed the consistent results with the view under microscopy. After cultivation, in CTL+MDSC group, the rate of CTLs with strong fluorescence was 87.6%. However, only 47.5% of CTLs with strong fluorescence were found in CTL group 图 3 MDSC对SK-NK-SH抗原特异性CTL增殖的抑制 Figure 3 MDSC inhibited proliferation of neuroblastoma antigen-specific CTL |
流式细胞术检测结果显示:与MDSC共培养CTL在强荧光处细胞数量多(87.6%),弱荧光处细胞数量较少;而单独培养CTL正好相反,强荧光处细胞数量较少(47.5%),弱荧光处细胞数量很多,见图 3B。
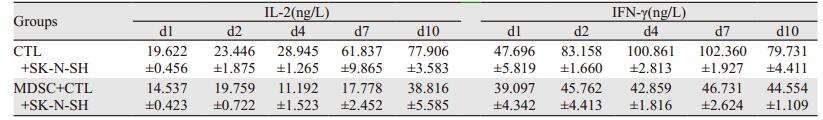
2.4 MDSC对抗原特异性CTL体外杀伤SK-N-SH细胞效应的影响CTL+SK-N-SH组和MDSC+CTL+SK-N-SH组的杀伤率分别为(42.58±7.09)%和(14.63±12.36)%,两组比较差异有统计学意义(t=6.506, P=0.000)。ELISA检测上清液中IL-2、IFN-γ的分泌量,结果显示,CTL+SK-N-SH组和MDSC+CTL+SK-N-SH组上清液中IL-2(F=429.272, P < 0.01)和IFN-γ(F=782.804, P < 0.01)分泌量差异均有统计学意义,见表 1。
|
目前NB免疫治疗的最有效手段之一是过继赋予嵌合GD2抗原受体的CTL[8]。但是临床Ⅲ期试验发现,利用嵌合GD2抗原受体的CTL回输治疗,虽然生存率有所提高,但部分高危NB患儿仍出现复发和转移,提示这种被动免疫治疗可能需要调整免疫抑制微环境介导的免疫系统激活来提高其疗效[3, 8]。
肿瘤生存的免疫微环境中,包括MDSC在内的各种免疫抑制细胞的聚集,形成了主要的免疫抑制因素,导致肿瘤免疫耐受发生[3-5]。MDSC是一群髓系来源具有抑制功能的天然免疫细胞,当机体在肿瘤、各种感染性疾病、骨髓移植等疾病应激状态下时,MDSC的分化过程受阻而被单纯扩增和活化。研究证实[3, 9-10],一方面MDSC通过增高IL-10水平抑制DC功能,或加速巨噬细胞向M2型极化,白细胞介素-12产生减少,降低NK细胞功能,抑制机体天然免疫;另一方面,通过高表达精氨酸酶-1、诱生型一氧化氮合酶、活性氧簇ROS、吲哚胺-2,3-双加氧酶以及TGF-β和IL-10诱发的调节性T细胞扩增等,抑制T细胞过继性免疫。因此,MDSC在肿瘤进展中发挥负向免疫调控作用,是造成肿瘤免疫耐受而影响疗效的主要障碍[11]。靶向抑制病理状态下异常扩增的MDSC不会对正常免疫功能造成影响,反而能控制MDSC造成的免疫耐受,有助于机体免疫系统发挥作用。
尽管国内外有关MDSC在其他肿瘤中的作用和机制已有较多阐述,但是MDSC对神经母细胞瘤的作用尚未得到完整的阐释。本组研究中,利用CFSE对神经母细胞瘤抗原特异性CTL进行染色,当细胞继续分裂增殖时,具有荧光的胞质蛋白被平均分配到下一代细胞中,其荧光强度便会减弱一半,以此类推,分裂得到的细胞代次越高其可以检测到的荧光强度会越弱。研究中发现CTL培养后,单独培养的CTL的增殖没有受到影响,可以在弱荧光处检测到数量较多的细胞。而与MDSC共培养的CTL细胞无明显分裂增殖,细胞仍以强荧光为主,这充分说明MDSC对神经母细胞瘤抗原特异性CTL的增殖发生了明显的抑制作用。
近年来研究已明确CTL对靶细胞产生细胞毒性有两条彼此独立途径,即穿孔蛋白(Perforin)途径和依赖Fas抗原分子介导的PCD途径[12-13]。其中Perforin途径是一条主要途径,在抗病毒、细胞内细菌、肿瘤、免疫病理等方面起重要作用[13-14]。CTL通过Perforin途径发挥肿瘤杀伤作用时会分泌释放出细胞因子IL-2和IFN-γ,作用越明显,细胞因子浓度会越高,反之则越低。本组进一步研究中,将抗原特异性CTL与SK-N-SH细胞混合孵育,检测效应细胞的杀伤率,发现与MDSC共孵育的CTL对SK-N-SH细胞杀伤率明显降低,而MDSC+CTL组上清液中IL-2、IFN-γ的分泌量比CTL组也明显减少。说明MDSC可以通过减少细胞因子IL-2和IFN-γ的分泌来抑制CTL活性,从而抑制Perforin途径对NB肿瘤细胞的杀伤效应。
由于对肿瘤免疫的负向调控作用,针对MDSC的靶向治疗成为目前研究热点。当前以MDSC为靶点的治疗包括:(1)促进MDSC分化。全反式维甲酸可在体内、外诱导MDSC分化成DC和巨噬细胞。(2)抑制MDSC免疫抑制功能。肾癌患者应用舒尼替尼(Sunitinib)后可以逆转MDSC介导的免疫抑制作用[15]。(3)消除MDSC。动物实验证明应用5-Fu、吉西他滨后MDSC数量明显降低,5-Fu可以选择性诱导MDSC凋亡而不影响T、NK、DC细胞[16]。
尽管可以作为肿瘤治疗新靶点,但MDSC的异质性及调控通路的复杂性等因素,给针对MDSC的免疫治疗带来较大障碍。MDSC对免疫系统抑制机制及正、负向调控MDSC信号通路仍未完全明晰;针对MDSC的免疫靶向治疗机制和临床疗效更有待探索。总之,本研究在对MDSC体外分离培养和成功制备NB抗原特异性CTL的基础上,论证了体外环境下MDSC的集聚对NB抗原特异性CTL的增殖和杀伤肿瘤细胞活性的抑制作用,完善了MDSC集聚造成NB免疫耐受的机制,为改善NB的免疫疗效提供了新的靶点,其具体机制有待进一步的体内实验深入研究。
| [1] | 侯渊涛, 刘璐, 王常林. 神经母细胞瘤的免疫学治疗进展[J]. 临床小儿外科杂志, 2011, 10(4): 290–3. [ Hou YT, Liu L, Wang CL. Advances in immunotherapy of neuroblastoma[J]. Lin Chuang Xiao Er Wai Ke Za Zhi, 2011, 10(4): 290–3. ] |
| [2] | Seeger RC. Immunology and immunotherapy of neuroblastoma[J]. Semin Cancer Biol, 2011, 21(4): 229–37. DOI:10.1016/j.semcancer.2011.09.012 |
| [3] | Pistoia V, Morandi F, Bianchi G, et al. Immunosuppressive microenvironment in neuroblastoma[J]. Front Oncol, 2013, 3: 167. |
| [4] | Long AH, Highfill SL, Cui Y, et al. Reduction of MDSCs with All-trans Retinoic Acid Improves CAR Therapy Efficacy for Sarcomas[J]. Cancer Immunol Res, 2016, 4(10): 869–80. DOI:10.1158/2326-6066.CIR-15-0230 |
| [5] | Komohara Y, Takeya M. CAFs and TAMs: maestros of the tumourmicroenvironment[J]. J Pathol, 2017, 241(3): 313–5. DOI:10.1002/path.4824 |
| [6] | Jales A, Falahati R, Mari E, et al. Ganglioside-exposed dendritic cells inhibit T-cell effector function by promoting regulatory cell activity[J]. Immunology, 2011, 132(1): 134–43. DOI:10.1111/j.1365-2567.2010.03348.x |
| [7] | Xu W, Cai J, Li S, et al. Improving the in vivo persistence, distribution and function of cytotoxic T lymphocytes by inhibiting the tumor immunosuppressive microenvironment[J]. Scand J Immunol, 2013, 78(1): 50–60. DOI:10.1111/sji.2013.78.issue-1 |
| [8] | Cheung NK, Dyer MA. Neuroblastoma: developmental biology, cancer genomics and immunotherapy[J]. Nat Rev Cancer, 2013, 13(6): 397–411. DOI:10.1038/nrc3526 |
| [9] | Gabrilovich DI. Myeloid-Derived Suppressor Cells[J]. Cancer Immunol Res, 2017, 5(1): 3–8. DOI:10.1158/2326-6066.CIR-16-0297 |
| [10] | Chen J, Ye Y, Liu P, et al. Suppression of T cells by myeloid-derived suppressor cells in cancer[J]. Hum Immunol, 2017, 78(2): 113–9. DOI:10.1016/j.humimm.2016.12.001 |
| [11] | Jordan KR, Kapoor P, Spongberg E, et al. Immunosupp-ressive myeloid-derived suppressor cells are increased in splenocytes from cancer patients[J]. Cancer Immunol Immunother, 2017, 66(4): 503–13. DOI:10.1007/s00262-016-1953-z |
| [12] | Hassin D, Garber OG, Meiraz A, et al. Cytotoxic T lymphocyte perforin and Fas ligand working in concert even when Fas ligand lytic action is still not detectable[J]. Immunology, 2011, 133(2): 190–6. DOI:10.1111/imm.2011.133.issue-2 |
| [13] | Martínez-Lostao L, Anel A, Pardo J. How Do Cytotoxic Lymphocytes Kill Cancer Cells?[J]. Clin Cancer Res, 2015, 21(22): 5047–56. DOI:10.1158/1078-0432.CCR-15-0685 |
| [14] | Voskoboinik I, Whisstock JC, Trapani JA. Perforin and granzymes: function, dysfunction and human pathology[J]. Nat Rev Immunol, 2015, 15(6): 388–400. DOI:10.1038/nri3839 |
| [15] | Kumar R, Avagyan S, Snoeck HW. A quantitative trait locus on chr.4 regulates thymic involution[J]. J Gerontol A Biol Sci Med Sci, 2010, 65(6): 620–5. |
| [16] | Lustig A, Carter A, Bertak D, et al. Transcriptome analysis of murine thymocytes reveals age-associated changes in thymic gene expression[J]. Int J Med Sci, 2009, 6(1): 51–64. |
 2017, Vol. 44
2017, Vol. 44
