文章信息
- 胸腹腔镜联合与传统开胸术治疗高龄食管癌患者(≥70岁)的临床比较
- Clinical Comparison of Minimally Invasive Esophagectomy Versus Open Esophagectomy on Elderly Esophageal Carcinoma Patients (≥70 Years Old)
- 肿瘤防治研究, 2017, 44(11): 740-744
- Cancer Research on Prevention and Treatment, 2017, 44(11): 740-744
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.17.0666
- 收稿日期: 2017-06-12
- 修回日期: 2017-07-13
2. 215008 苏州, 南京医科大学附属苏州市立医 院北区胸外科
2. Department of Thoracic Surgery, Suzhou Municipal Hospital North District, Nanjing Medical University, Suzhou 215008, China
我国为食管癌高发地区,其发病率占全球发病的49.5%[1]。食管癌根治术为治疗食管癌的有效手段,但传统开胸术(open esophagectomy, OE)存在手术创伤大、切口疼痛较剧烈及术后康复较慢等问题,尤其对于高龄食管癌患者(年龄≥70岁),其心肺功能及营养状况相对年轻患者差,术后易出现心肺相关并发症[2],因而高龄食管癌围手术期风险相应增加。我们对苏州大学附属第一人民医院及苏州市立医院北区胸外科2013年2月—2016年8月间所实施胸腹腔镜联合微创食管癌根治术(minimally invasive esophagectomy, MIE)及OE手术的高龄患者进行回顾性分析及总结,探讨全腔镜微创手术对比传统开放手术方式治疗高龄食管癌患者的疗效,为临床应用微创手术治疗高龄食管癌提供相关理论依据。
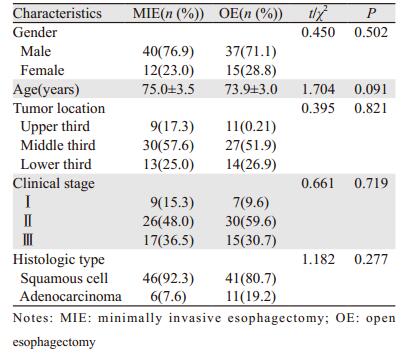
1 资料与方法 1.1 一般资料对苏州大学附属第一人民医院和南京医科大学附属苏州市立医院胸外科2013年2月至2016年8月所实施MIE及OE手术的高龄患者分两组:MIE组(Ivor-Lewis或McKeown术式)、OE组(Sweet、Ivor-Lewis或McKeown术式),每组分别随机挑选52例,两组患者一般临床资料见表 1。入组标准:(1)患者行MIE或OE术;(2)年龄≥70岁,性别不限;(3)术前胃镜及病理检查明确诊断;(4)术前行胸部CT及腹部B型超声排除远处转移,常规评估心肺功能排除手术禁忌证;(5)术前未进行新辅助化疗或放疗;(6)剔除姑息性手术切除患者。
|
入组病例中35例为McKeown式,17例为Ivor-Lewis式。(1)McKeown式:全身麻醉单腔管插管。患者左侧卧位,取胸部右侧腋前线第7肋间为腔镜孔,右腋前线第4肋间为主操作孔,腋后线第7、第9肋间为副操作孔。进胸后予以注入1.064 Kpa左右CO2气体行人工气胸以利暴露。游离奇静脉弓,Hem-o-lok夹闭其两侧后离断。向上游离食管至胸膜顶,临近右锁骨下动脉时注意游离暴露右喉返神经以避免损伤,同时钝性加锐性清扫右喉返神经旁淋巴结。五爪拉钩牵压右肺暴露左侧喉返神经行其旁淋巴结清扫。向下游离食管至膈肌裂孔处,同时清扫余下纵隔内淋巴结(隆突下、食管旁等处)。留置胸管后逐层关胸,放平体位常规消毒铺巾后行腹部操作。取脐下为腔镜观察孔,注入1.729 Kpa左右CO2气体行人工气腹。分别取左右锁骨中线肋弓下缘、剑突下、两侧腹直肌外缘平脐处为操作孔。沿大弯侧分别向上游离网膜,离断胃网膜左、胃短动脉至膈肌裂孔处,向下游离至幽门处,注意保留胃网膜右动脉。于小弯侧游离小网膜,分别离断胃左、胃右动脉(血管近端Hem-o-lok夹闭),同时行肝动脉旁、胃左动脉旁及贲门周围淋巴结清扫。左颈部胸锁乳突肌前为手术切口,逐层切开暴露游离并拉出食管,离断食管后其近端荷包缝合上抵钉座,食管远端缝闭并连一留置皮管。取腹部剑突下5 cm切口取出食管及胃,制作管胃并取出食管手术标本。通过留置皮管牵拉管胃至颈部,强生吻合器行胃食管机械吻合。(2)Ivor-Lewis式:胸腔食管及腹腔胃游离同上。胸内吻合方式如下:距肿块上缘5 cm以上予以上荷包钳并完成荷包缝合。于荷包线以下3~4 cm处切开食管置入抵钉座,收紧荷包线打结,于其下0.5 cm切除食管。将管胃提入胸腔,胃壁开窗后置入吻合器与抵钉座相连行机械吻合。胃残端闭合器闭合。吻合口处常规镜下加强缝合。
1.2.2 OE组手术方法入组病例中36例为Sweet式,12例为Ivor-Lewis式,4例为McKeown式。(1)Sweet式:取左胸第六肋后外侧切口,游离食管并行纵隔内淋巴结清扫。于肝脾交界处打开膈肌,游离胃大小弯侧并清扫周围淋巴结。制作管胃并切除肿瘤段食管,于胸腔内行胃食管机械吻合。(2)Ivor-Lewis、McKeown式:取右胸第五肋间为胸部切口,剑突下至脐正中连线为腹部切口。胸内及腹腔内手术操作同微创手术。Ivor-Lewis、McKeown各自行右胸内、左颈部胃食管机械吻合。
1.3 观察指标观察两组手术时间、术中出血、淋巴结清扫数目。对术后白细胞计数(white blood cell, WBC)、C反应蛋白(C-reactive protein, CRP)炎性反应指标进行分析及对术后疼痛予以视觉模拟评分法(visual analogue scale/score, VAS)进行评估。同时观察吻合口瘘、肺部感染、心肺相关并发症以及住院时间等指标。
1.4 统计学方法对数据应用SPSS22.0统计软件进行分析与处理。计量资料正态分布以(x±s)表示,予以独立样本t检验,非正态分布以中位数(最小值-最大值)表示,予以非参数秩和检验。计数资料予以χ2或Fisher精确检验。应用Kaplan-Meier法绘制生存曲线,生存率比较采用Log rank检验。P < 0.05为差异具有统计学意义。
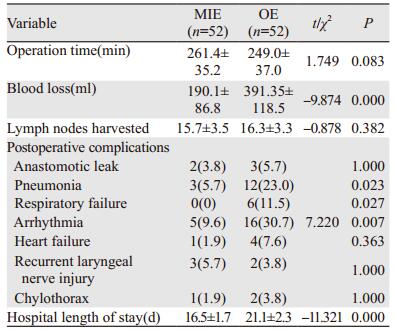
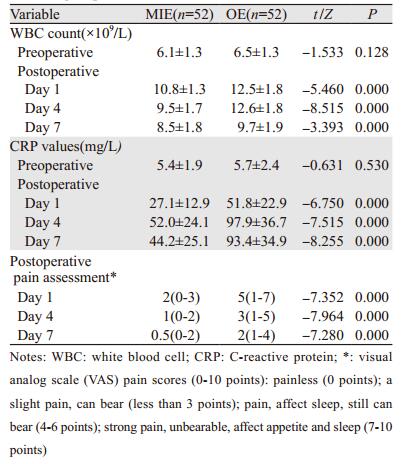
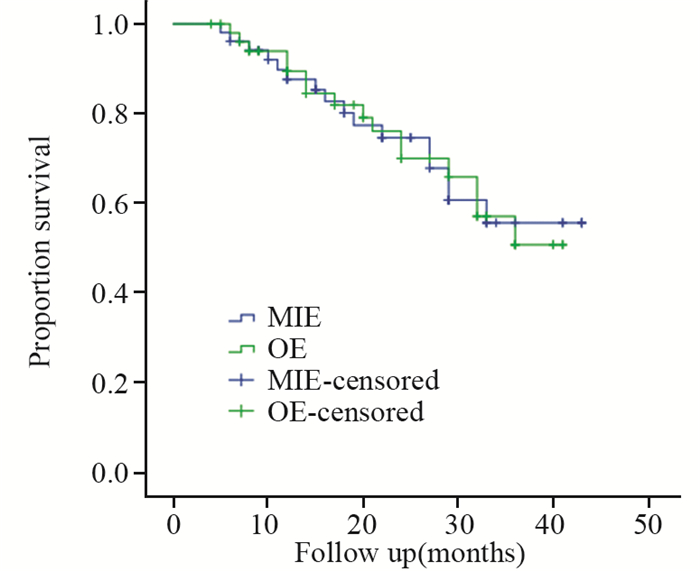
2 结果MIE全组均在全腔镜下顺利完成,无中转开胸。其手术时间与OE组相比差异无统计学意义(P > 0.05)。MIE组术中出血少于OE组(P < 0.05)。术后并发症:两组吻合口瘘、喉返神经损伤及乳糜胸无差异,但肺部感染及心律失常发生率MIE组低于OE组(P < 0.05),MIE组术后呼吸及心脏功能衰竭明显低于OE组(P < 0.05)。MIE组住院时间少于OE组(P < 0.05)。术后吻合口瘘共5例,予以禁食、营养支持以及抗感染、换药后痊愈。喉返神经损伤共5例,予以营养神经等保守治疗后好转,见表 2。观测术后WBC、CRP指标及疼痛程度,MIE组指标均优于OE组(P < 0.05),见表 3。术后平均随访(22.1±11.1)月,依照生存时间作Kaplan-Meier生存曲线,见图 1。两组术后1、2年生存率:MIE组:87.6%、77.4%,OE组:89.5%、79.1%,两组比较差异无统计学意义(P=0.985)。
|
|
|
| 图 1 MIE与OE组高龄食管癌患者术后生存时间比较 Figure 1 Comparison of postoperative survival time of elderly esophageal cancer patients between MIE group and OE group |
食管癌为我国常见恶性肿瘤之一,其发病率占我国恶性肿瘤发病第五位,同时食管癌发病率与年龄密切相关,在40岁之前发病率处于较低水平,70~80岁年龄组达到高峰[3]。尽管没有统一的标准确定高龄食管癌的年龄,但多数文献普遍以年龄≥70岁作为观察及研究的年龄界线[4-5]。
近年来化疗与放疗等手段在治疗食管癌方面得以发展[6-7],但手术仍是治疗食管癌最为有效的方式,食管癌根治术为治疗Ⅰ、Ⅱ期及部分Ⅲ期食管癌的首选[8]。传统开胸为手术治疗食管癌常规方式,从对位于食管下端的肿瘤采用经左胸单切口Sweet术式,以及对肿瘤位于食管中、上段所采用胸腹部两切口胸内吻合Ivor-Lewis术式,或经颈胸腹三切口颈部吻合的McKeown式可根除食管癌变组织。然而传统开胸手术操作时需切断胸壁重要肌肉组织,手术切口需肋骨撑开器撑开暴露,若需联合多切口时腹部同时行较大手术切口,致患者术后疼痛较为剧烈、炎性反应综合征较重以及术后早期肺功能较术前显著下降[9]。尤其对于高龄患者,心肺功能较年轻患者普遍下降,围手术期风险相应增加,尽管麻醉、外科手术技巧以及围手术期处理较以往明显改善与提高,但传统开胸术式患者手术风险仍然较高[10。
电视辅助胸部微创手术(video-assisted thoracic surgery, VATS)方式的出现与革新极大改变了胸部手术的治疗方式。随着腔镜技术及器械的迅速发展,胸腹腔镜联合微创行食管癌根治术(MIE)得到广泛应用[11-12]。MIE通过胸、腹壁微小手术切口进行手术操作,从而避免胸腹壁切断较长肌肉组织、肋骨撑开,减轻肋间神经及胸腹腔内邻近组织器官的损伤,从而显著减轻术后疼痛以及手术后创伤应激。通过对两组术后WBC、CRP的监测及术后疼痛评估进行比较,结果显示MIE组与OE组有显著性差异,从而证实MIE可明显减轻高龄患者术后疼痛,并显著降低手术创伤及应激所导致的全身炎性反应。
相关文献报道微创食管癌根治术其术后呼吸系统并发症显著低于传统开胸术[13-14]。我们观察结果亦提示MIE组患者术后肺部感染概率显著低于OE组。考虑因素为微创手术创伤明显减少,术后疼痛及炎性反应显著降低(MIE组术后WBC、CRP及疼痛评分均显著低于OE组),有利患者术后咳嗽排痰及降低全身炎性反应综合症的发生,因而减少肺部相关并发症的发生。观察两组术后呼吸衰竭发生率,MIE组明显少于OE组,相关文献显示传统剖胸患者术后肺功能术后第一天肺功能降低到术前的(39±14)%,术后第8天恢复到术前的(62±10)%[9],高龄食管癌患者传统剖胸术后因其肺功能损失、肺部易继发感染以及高龄所致自身肺功能减退,术后更易出现呼吸功能衰竭,而微创手术治疗可显著降低术后发生呼吸衰竭的概率。
比较两组术后心衰的发生率,MIE组与OE组差异无统计学意义,但MIE组心律失常发生率显著少于OE组,两者差异具有统计学意义。考虑食管癌术后伴发心律失常,通常为手术创伤应激及术后低氧血症、酸碱失衡及水电解质紊乱等因素诱发。微创手术治疗食管癌因其手术创伤小、术后肺功能损伤较小以及肺部感染概率低[14-15],而降低了术后创伤应激、低氧血症及肺功能不全的发生概率,从而使MIE组术后心律失常发生率显著降低。尤其对于心肺功能普遍降低的老年患者,微创手术治疗可显著降低患者术后伴发心肺系统相关并发症的发生。观察的住院时间MIE组较OE组明显减少,结果显示微创手术使高龄食管癌术后相关并发症降低,有利于患者术后早期康复。
MIE组术中失血显著少于开胸组,主要因为腔镜下手术操作时,其手术视野因经视频成像系统局部放大,因而手术操作更为精细、视野暴露更清晰,故显著减少术中失血量。通过对两组的手术时间及淋巴结清扫数目的比较,两组间差异无统计学意义,认为在行食管癌根治术时,左右喉返神经旁淋巴结的清扫为手术的重点与难点,尤其对左喉返神经旁的淋巴结扫除,术中采取单腔插管麻醉行人工气胸方式,可减少暴露左喉返神经旁时气管插管的干扰,因而方便清扫左喉返神经旁淋巴结手术操作。通过出院后随访,比较两组生存时间,两者无显著差异,与相关文献报道类似[16-18],提示微创手术方式至少可以取得与传统开胸相同的外科肿瘤学效应。
通过胸腹腔镜联合微创食管癌根治术在治疗高龄食管癌临床中的应用,显著减少术中出血,减轻高龄患者术后疼痛以及全身炎性反应,从而降低心肺系统等相关并发症的发生率,缩短住院时间,有利于其术后快速康复,使高龄食管癌患者获得了良好的治疗效果。因而MIE手术方式值得在高龄食管癌临床治疗中加以推广。
| [1] | International Agency for Research on Cancer. GLOBOCAN 2012: Estimated cancer incidence, mortality and prevalence worldwide in 2012[EB/OL]. [2017-04-26]. http://globocan.iarc.fr |
| [2] | Liu HC, Chen YC, Chen CH, et al. Esophagectomy in elderly patients with esophageal cancer[J]. Int J Gerontol, 2015, 48(4): 121–7. |
| [3] | 左婷婷, 郑荣寿, 曾红梅, 等. 中国食管癌发病状况与趋势分析[J]. 中华肿瘤杂志, 2016, 38(9): 703–8. [ Zuo TT, Zheng RS, Zeng HM, et al. The incidence status and trends analysis of esophageal carcinoma in China[J]. Zhonghua Zhong Liu Za Zhi, 2016, 38(9): 703–8. ] |
| [4] | Furlong H, Bass G, Breathnach O, et al. Targeting therapy for esophageal cancer in patients aged 70 and over[J]. J Geriatr Oncol, 2013, 4(2): 107–13. DOI:10.1016/j.jgo.2012.12.006 |
| [5] | Tapias LF, Muniappan A, Wright CD, et al. Short and Long-Term Outcomes After Esophagectomy for Cancer in Elderly Patients[J]. Ann Thorac Surg, 2013, 95(5): 1741–8. DOI:10.1016/j.athoracsur.2013.01.084 |
| [6] | Aridgides PD, Janik A, Bogart JA, et al. Radiotherapy for stage Ⅲ non-small-cell lung carcinoma in the elderly (age≥70 years)[J]. Clin Lung Cancer, 2013, 14(6): 674–9. DOI:10.1016/j.cllc.2013.05.001 |
| [7] | Ohba A, Kato K, Ito Y, et al. Chemoradiation therapy with docetaxel in elderly patients with stage Ⅱ/Ⅲ esophageal cancer: A phase 2 trial[J]. Adv Radiat Oncol, 2016, 1(4): 230–6. DOI:10.1016/j.adro.2016.07.002 |
| [8] | 胡胜寿. 心胸外科学[M]. 第1版. 北京: 人民卫生出版社, 2014: 107-9.] [ Hu SS. Thoracic and Cardiothoracic Surgey[M]. 1nd ed.. Beijing: People's Medical Publishing House, 2014: 107-9. ] |
| [9] | 崔玉尚, 张志庸, 阿伊都·阿布都热伊木. 开胸术后早期肺功能的变化规律及影响因素分析[J]. 中华外科杂志, 2003, 41(12): 909–12. [ Cui YS, Zhang ZY, Ayidu·ABDRYM, et al. Analysis of early lung function changes and influencing factors after thoracotomy[J]. Zhonghua Wai Ke Za Zhi, 2003, 41(12): 909–12. DOI:10.3760/j:issn:0529-5815.2003.12.008 ] |
| [10] | Battafarano RJ. Minimally invasive esophagectomy is there an advantage?[J]. Adv Surg, 2016, 50(1): 17–28. DOI:10.1016/j.yasu.2016.03.002 |
| [11] | Palazzo F, Rosato EL, Chaudhary A, et al. Minimally invasive esophagectomy provides significant survival advantage compared with open or hybrid esophagectomy for patients with cancers of the esophagus and gastroesophageal junction[J]. J Am Coll Surg, 2014, 220(4): 672–9. |
| [12] | Perry Y, Fernando HC. Three-field minimally invasive esophagectomy: current results and technique[J]. J Thorac Cardiovasc Surg, 2012, 144(3): S63. DOI:10.1016/j.jtcvs.2012.06.002 |
| [13] | Biere SS, van Berge Henegouwen MI, Maas KW, et al. Minimally invasive versus open oesophagectomy for patients with oesophageal cancer: a multicentre, open-label, randomized controlled trial[J]. Lancet, 2012, 379(9829): 1887–92. DOI:10.1016/S0140-6736(12)60516-9 |
| [14] | Shen Y, Zhong M, Wu W, et al. The impact of tidal volume on pulmonary complications following minimally invasive esophagectomy: A randomized and controlled study[J]. J Thorac Cardiovasc Surg, 2013, 146(5): 1267–74. DOI:10.1016/j.jtcvs.2013.06.043 |
| [15] | Bakhos CT, Fabian T, Oyasiji TO, et al. Impact of the surgical technique on pulmonary morbidity after esophagectomy[J]. Ann Thorac Surg, 2012, 93(1): 221–7. DOI:10.1016/j.athoracsur.2011.07.030 |
| [16] | Yerokun BA, Sun Z, Yang CJ, et al. Minimally invasive versus open esophagectomy for esophageal cancer:a population-based analysis[J]. Ann Thorac Surg, 2016, 102(2): 416–23. DOI:10.1016/j.athoracsur.2016.02.078 |
| [17] | Mitzman B, Lutfi W, Wang CH, et al. Minimally invasive esophagectomy provides equivalent survival to open esophagectomy:An analysis of the national cancer database[J]. Semin Thoracic Surg, 2017, 29(2): 244–53. |
| [18] | 杜泽森, 傅俊惠, 郑春鹏, 等. 胸腹腔镜联合食管癌切除术与传统开胸术式的临床对比研究[J]. 肿瘤防治研究, 2013, 41(4): 431–3. [ Du ZA, Fu JH, Zheng CP, et al. Clinical comparison between minimally invasive esophagectomy and Open esophagectomy[J]. Zhong Liu Fang Zhi Yan Jiu, 2013, 41(4): 431–3. ] |
 2017, Vol. 44
2017, Vol. 44


