文章信息
- 芦丁联合奥沙利铂激活FKN/SYK/p38通路促进胃癌细胞凋亡
- Effect of Rutin Combined with Oxaliplatin on Activation of FKN/SYK/p38 Pathway to Promote Apoptosis of Gastric Cancer Cells
- 肿瘤防治研究, 2017, 44(11): 719-723
- Cancer Research on Prevention and Treatment, 2017, 44(11): 719-723
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.17.0603
- 收稿日期: 2017-05-31
- 修回日期: 2017-07-12
2. 121000 锦州, 锦州医科大学附属第三医院病理科;
3. 130021 长春, 吉林大学药学院实验药理与 毒理学教研室
2. Department of Pathology, The Third Affiliated Hospital of Jinzhou Medical University, Jinzhou 121000, China;
3. Department of Experimental Pharmacology and Toxicology, School of Pharmaceutical Sciences, Jilin University, Changchun 130021, China
芦丁(rutin, RT)异名芸香苷、路丁、维生素p、紫槲皮苷,是具有多种生物活性的黄酮类化合物,广泛存在于多种天然植物如槐米、苦荞麦、尤曼桉中,在医药、日化、食品等领域有广泛的应用。芦丁具有多种生理功能,对人体各个器官进行保护,如清除自由基、抗氧化、抗衰老、抑菌、抗炎、促进成骨细胞的生长、降低血糖等作用[1-2]。近年来其抗肿瘤方面作用成为研究的热点,具有价格低廉、几乎无毒副作用等优点[3]。已有研究表明芦丁对结肠癌、肝癌等消化道肿瘤细胞有抑制增殖作用[4]。本研究将芦丁联合奥沙利铂作用于人胃癌细胞SGC-7901,观察其对SGC-7901细胞增殖及凋亡的影响,并探讨其增殖抑制作用是否通过FKN/SYK/p38通路,为胃癌的治疗提供更多的理论和实验依据。
1 材料与方法 1.1 材料 1.1.1 细胞株人胃癌SGC-7901细胞株由吉林大学白求恩医学院生命科学院实验室馈赠,本实验室冻存储备。
1.1.2 药品与试剂芦丁(南京景竹生物科技有限公司,纯度98%),注射用奥沙利铂(Oxaliplatin, OXA)(江苏恒瑞医药股份有限公司,批号H20000337),p38抑制剂(SB203580;美国Sigma公司),高糖培养液(美国Hyclone公司),优级胎牛血清(天津灏洋生物制品科技有限责任公司),噻唑蓝(MTT)(美国Sigma公司),二甲基亚砜(DMSO)(美国Sigma公司),Annexin V-FITC/PI凋亡检测试剂盒(美国Sigma公司),鼠抗人FKN多克隆抗体(武汉博士德生物工程有限公司),兔抗人SYK、P38、p-P38、pro-caspase-3、cleaved-caspase3、7、8和9单克隆抗体(北京中杉金桥生物技术有限公司),辣根过氧化物酶标记的山羊抗兔/鼠二抗(北京中杉金桥生物技术有限公司),TRIzol(美国Invitrogen公司),吐温-20、SDS、过硫酸铵、丙烯酰胺、Tris-HCl、Glycine(北京鼎国昌盛公司),N, N’亚甲双丙烯酰胺、四甲基乙二胺(TEMED)(美国Sigma公司),总蛋白提取试剂盒(北京普利莱基因技术有限公司)。
1.1.3 仪器倒置相差显微镜、生物显微镜(日本Nikon公司),DG5031型酶联免疫检测仪(南京华东电子集团医疗装备有限责任公司),电泳槽、流式细胞仪、CO2恒温培养箱、JJ260型精密电子天平(美国BD公司)。
1.2 方法 1.2.1 细胞体外培养SGC-7901细胞生长于含10%胎牛血清的DMEM高糖培养液,置于37℃、5%CO2饱和湿度的恒温密闭培养箱中进行常规培养并传代,0.25%胰蛋白酶消化,每2~3 d消化传代1次。
1.2.2 药物处理与分组芦丁用DMSO配成1 mol/L的储液,-20℃保存,实验当日用无血清培养液稀释,其中DMSO的浓度均控制在0.1%以下;p38抑制剂及奥沙利铂均现配现用。实验设:(1)阴性对照组(药物浓度为0 μmol/L)、(2)p38抑制剂组(15 μmol/L)、(3)RT组(300 μmol/L)、(4)OXA组(33 μmol/L)、(5)联合组(RT 300 μmol/L+OXA 33 μmol/L)。作用24 h后观察细胞形态及密度的变化情况。利用中效原理计算给药浓度及联合给药剂量,抑制率(fa)=1-(实验组平均OD值/对照组平均OD值),根据中效方程式fa/fu=(D/Dm)m,计算出各药物单用及合用时各自的中效浓度Dm,作为以上药物浓度分组及联合给药剂量的依据,两药合用时在各种效应时的合用指数(CI)=D1/Dx1+D2/Dx2+αD1D2/Dx1Dx2,CI < 1为两药有协同作用。在药物作用12 h细胞凋亡并不明显,作用36、48 h细胞过度凋亡,几乎看不见存活的细胞,作用24 h观察细胞凋亡的状态最为理想,凋亡细胞形态清晰可见。
1.3 实验检测指标 1.3.1 MTT法测定细胞活力取对数生长期的SGC-7901细胞,胰蛋白酶消化,用含10%胎牛血清的DMEM高糖培养液制成浓度为5×104个/毫升的单细胞悬液,接种于96孔细胞培养板中,每孔200 μl,每组设6个复孔,37℃、5%CO2、饱和湿度的恒温密闭培养箱中孵育至细胞单层铺满孔底时,将实验组中加入相应的药物。实验分组设阴性对照组、p38抑制剂组、RT组、OXA组、联合作用组。阴性对照组加入无血清培养液,p38抑制剂组的终浓度为15 μmol/L,RT组的终浓度为300 μmol/L,OXA组终浓度为33 μmol/L,联合作用组的RT和OXA的终浓度分别为300 μmol/L和33 μmol/L,培养至24 h,每孔加MTT溶液(5 mg/ml)20 μl,继续培养4 h,终止培养,小心吸弃孔内上清液,每孔加入150 μl DMSO,振荡10 min,使结晶物充分溶解。选择490 nm波长,以空白孔(无细胞,只含培养液)调零,酶标仪测定各孔光吸收值,实验重复3次,计算药物对细胞的存活率,细胞存活率=(实验组D490/对照组D490)×100%,结果取平均值。
1.3.2 流式细胞仪检测细胞周期取对数生长期SGC-7901细胞,制成1×106个/毫升的细胞悬液,按每孔1 ml接种于6孔板内,按1.3.1方法操作、分组及给药后,收集细胞,1 000 r/min离心5 min,弃培养液,1 ml PBS洗涤后,加入预冷的70%乙醇溶液4℃固定12 h,离心弃去固定液,PBS洗涤2遍,弃PBS,加入1 ml PI染液37℃避光孵育30 min后重悬细胞,30 min内上流式细胞仪检测。实验重复3次。
1.3.3 Western blot检测相关分子蛋白表达水平细胞种板及药物分组与流式细胞仪检测细胞周期分组相同,药物作用24 h后,按总蛋白提取试剂盒说明书提取各组总蛋白,BCA法检测蛋白浓度,每孔蛋白上样10 μl,进行SDS-PAGE凝胶电泳,湿转法转膜至PVDF膜上,Western blot封闭液封闭2 h,Western blot一抗稀释液稀释,一抗(FKN 1:500,SYK 1:200,p38 1:400、p-p38 1:400、pro-caspase-3 1:400、cleaved-caspase3 1:400、cleaved-caspase7 1:400、cleaved-caspase8 1:400和cleaved-caspase9 1:400)4℃孵育过夜,次日用Western blot二抗稀释液稀释,二抗(1:5 000)室温孵育摇床2 h,于暗室按高敏感度化学发光检测试剂盒说明书滴加发光工作液,暗盒中胶片曝光,显影、定影后用电脑扫描拍照,采用Image-proplus6.0软件进行灰度分析。
1.4 统计学方法采用SPSS23.0统计软件处理数据,数据符合正态分布并经方差齐性检验,数据以(x±s)表示,组间比较采用单因素方差分析(One-way ANOVA),两两之间比较采用LSD检验,P < 0.05为差异有统计学意义。
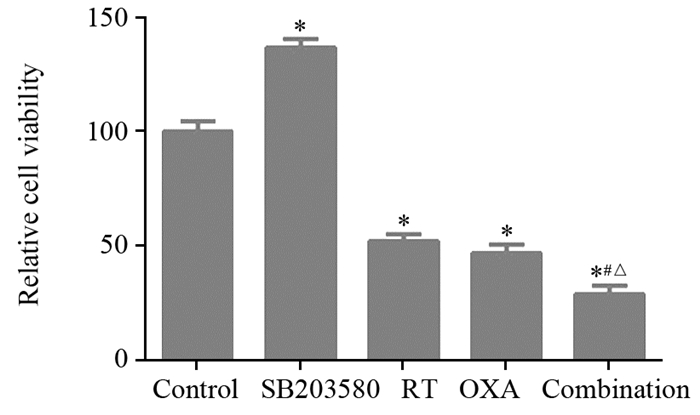
2 结果 2.1 不同药物对胃癌细胞增殖的影响与阴性对照组相比,p38抑制剂组对胃癌细胞SGC-7901有促进增殖的作用,可提升细胞存活率至(136.84±2.03)%(P=0.016),芦丁、奥沙利铂对胃癌细胞SGC-7901有明显的抑制作用,存活率降至(50.34±1.89)%、(46.37±2.01)%(P=0.001, P=0.001),联合组作用更显著,抑制率为(31.01±1.73)%(P=0.000),见图 1。
|
| *: P < 0.05, compared with Control group; #: P < 0.05, compared with RT group at the same concentration; △: P < 0.05, compared with OXA group at the same concentration; Control: SGC-7901; SB203580: 15μmol/L; RT: 300μmol/L; OXA:33μmol/L; Combination: RT+OXA (300μmol/L+33μmol/L); RT: rutin; OXA: oxaliplatin 图 1 MTT法检测不同药物对胃癌细胞增殖的影响(x±s, n=6) Figure 1 Effect of different drugs on gastric cancer cell proliferation assessed by MTT (x±s, n=6) |
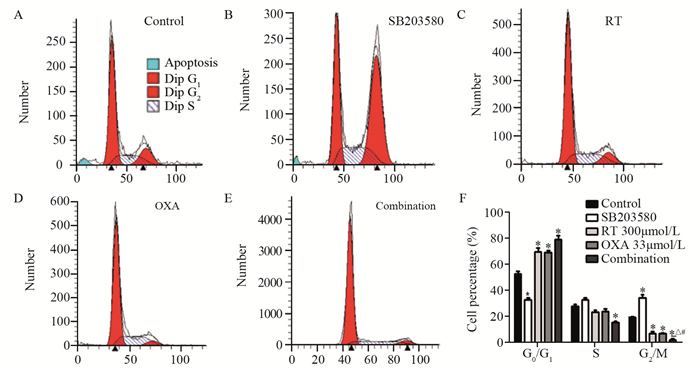
各药物干预SGC-7901细胞24 h后,收集细胞,检测细胞周期情况。结果显示与阴性对照组相比,p38抑制剂组SGC-7901细胞G0/G1期细胞百分率明显减少(P=0.008);芦丁、奥沙利铂及联合组SGC-7901细胞G0/G1期细胞百分率不同程度增加(P=0.010, P=0.010),以芦丁与奥沙利铂联合组最为明显(P=0.006),见图 2。结果表明p38抑制剂组可通过加快G0/G1期的进程促使细胞增殖,而芦丁、奥沙利铂及联合组可使细胞阻滞于G0/G1期,诱导细胞凋亡。
|
| *: P < 0.05, compared with control group; #: P < 0.05, compared with RT group; △: P < 0.05, compared with OXA group 图 2 流式细胞术检测不同药物处理后对细胞周期的影响(x±s, n=3) Figure 2 Effect of different drugs on gastric cancer cell cycle assessed by FCM after different drugs treatment (x±s, n=3) |
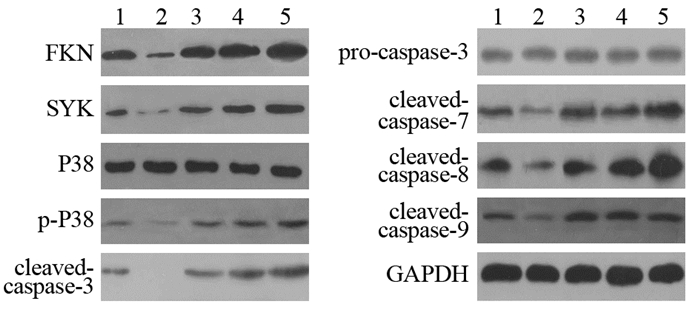
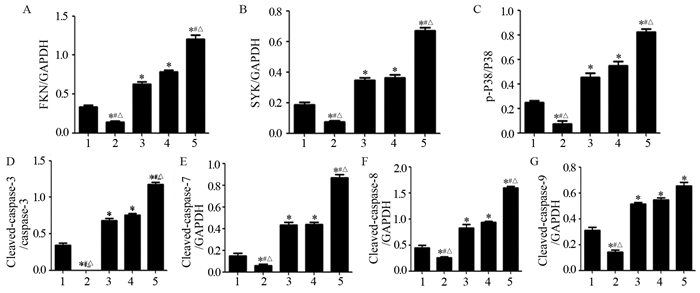
Western blot结果灰度分析表明:p38抑制剂作用后可明显下调FKN、SYK、p-p38、cleaved-caspase3、7、8、9的蛋白表达水平(均P=0.001);芦丁与奥沙利铂作用后均可不同程度的上调FKN、SYK、p-P38、cleaved-caspase3、7、8、9的蛋白表达水平,而联合组作用时变化更加明显(均P=0.018),见图 3~4。
|
| 1: Control group; 2: SB203580 15μmol/L; 3: RT 300μmol/L; 4: OXA 33μmol/L; 5: RT+OXA (300μmol/L+33μmol/L) 图 3 Western blot检测不同药物处理后胃癌细胞蛋白的表达(x±s, n=3) Figure 3 Effect of different drugs on gastric cancer cell proteins expressions assessed by Western blot (x±s, n=3) |
|
| 1: Control; 2: SB203580; 3: RT; 4: OXA; 5: Combination; *: P < 0.05, compared with control group; #: P < 0.05, compared with RT group; △: P < 0.05, compared with OXA group 图 4 Western blot检测不同药物处理后胃癌细胞蛋白表达的统计图(x±s, n=3) Figure 4 Statistical diagrams of gastric cancer cell proteins expressions detected by Western blot after different drugs treatment (x±s, n=3) |
胃癌是全世界最常见的恶性肿瘤之一,是一个多因素、多步骤、多阶段的发展过程,涉及癌基因、抑癌基因、凋亡相关基因与转移相关基因等的改变。虽然外科手术和放、化疗技术有明显提高,但胃癌治疗效果仍欠佳,导致胃癌预后不良原因主要在于胃癌的复发转移,其中,肿瘤血管生成与其生长、转移密切相关,如肿瘤没有局部血管新生,其将无法生长到2 mm3以上[5]。
FKN(fractalkine)是一种膜结合型趋化因子,具有黏附、促进血管平滑肌迁移、刺激炎症因子表达等功能。CX3CR1为G-蛋白耦联受体,分泌型可与受体CX3CR1结合,启动细胞内信号转导机制,导致血管内皮细胞损伤以及肿瘤细胞的黏附和侵袭,在炎性反应、疼痛、血管生成、肿瘤转移等病理生理过程中发挥重要作用[6]。FKN还可以通过调控Bcl-2和Bax的表达抑制细胞的增殖从而发挥促进细胞凋亡的作用[7-8]。据文献报道,在结肠癌患者中,肿瘤局部FKN的表达和淋巴细胞浸润及预后密切相关,小鼠肺癌模型和神经母细胞瘤荷瘤模型也证实FKN可以趋化NK细胞起到抗肿瘤作用。酪氨酸激酶(SYK)是SYK基因的蛋白产物,作为信号转导过程中一个影响因子[9],可能有抑制恶性肿瘤转移的作用。目前,国内外研究发现SYK基因在卵巢癌[10]、结直肠癌[11]、乳腺癌[12]、肺癌[13]、喉癌[14]、淋巴瘤[15]、胃癌[16]等多种肿瘤中广泛存在表达缺失的现象。SYK在肿瘤发生过程中发挥抑制性调节作用,其机制可能与影响血管内皮细胞功能、影响细胞信号转导通路,肿瘤细胞的成瘤能力等有关[17]。p38信号转导通路是MAPK家族中参与细胞凋亡的一条重要通路,可与其他信号转导通路有交叉作用,如活性氧类诱导p38信号转导通路介导caspase-3激活的FA-C淋巴细胞凋亡。p38可能参与芦丁与奥沙利铂对肿瘤细胞凋亡的调节,本实验前期研究表明,芦丁与奥沙利铂能通过上调Bax/Bcl-2比值,诱导胃癌细胞SGC-7901的凋亡(待发表)。本研究在前期实验的基础上进一步探讨芦丁与奥沙利铂促进SGC-7901细胞凋亡是否通过调控FKN/SYK/p38信号通路完成的。
本研究探讨p38抑制剂、芦丁、奥沙利铂的药物作用,以及p38信号转导通路和caspase家族在药物作用过程中蛋白表达的变化。caspase半胱氨酸蛋白酶家族在诱导细胞凋亡的分子机制中起着至关重要作用,是多条凋亡通路的汇聚点,是执行凋亡的最终途径。通过体外培养胃癌细胞SGC-7901,采用p38抑制剂、芦丁、奥沙利铂及两药联合进行干预。结果显示p38抑制剂可以促进细胞增殖,芦丁及奥沙利铂对胃癌SGC-7901细胞的生长有明显的抑制作用,两者联合应用明显增强对SGC-7901细胞抑制率。流式细胞周期检测进一步证明以上结果。Western blot结果显示p38抑制剂作用后可下调FKN、SYK、p-p38、cleaved-caspase3、7、8、9的蛋白表达水平;芦丁和奥沙利铂作用后均可上调FKN、SYK、p-p38、cleaved-caspase8、9蛋白表达,进而使cleaved-caspase3、7的蛋白表达水平增加,从而发挥诱导细胞凋亡的作用,而芦丁联合奥沙利铂作用时变化更加明显,其中caspase8、9作为第一类凋亡始动因子可通过转活化作用激活第二类凋亡效应子caspase3、7[18]。活化的caspase3又进一步切割不同的底物,导致蛋白酶级联切割放大,最终使细胞走向死亡。
综上所述,芦丁联合奥沙利铂可能通过激活FKN/SYK/p38通路诱导胃癌细胞的凋亡,且FKN/SYK可以抑制胃癌的血管内皮细胞,通过p38的激活引发caspase家族一系列的级联反应,进而促进胃癌细胞的凋亡,而加入p38抑制剂后可以抑制以上蛋白的表达,说明芦丁与奥沙利铂可能通过此通路发挥促凋亡的作用。但FKN/SYK/p38具体如何发挥抗胃癌的作用机制目前尚不清楚,在体内是否可能发挥抗胃癌的机制以及对胃癌细胞侵袭,转移是否具有抑制作用,这些问题有待进一步深入探究。
| [1] | 李玉山. 芦丁的资源、药理及主要剂型研究进展[J]. 氨基酸和生物资源, 2013, 35(3): 13–6. [ Li YS. Progress on resources, pharmacological effect and major forms of Rutin[J]. An Ji Suan He Sheng Wu Zi Yuan, 2013, 35(3): 13–6. ] |
| [2] | 马溶, 庞广昌. 芦丁对现代文明病的作用[J]. 食品科学, 2013, 34(7): 307–11. [ Ma R, Pang GC. Role of Rutin in modern Civilization diseases[J]. Shi Pin Ke Xue, 2013, 34(7): 307–11. DOI:10.7506/spkx1002-6630-201307065 ] |
| [3] | Orfali Gd, Duarte AC, Bonadio V, et al. Review of anticancer mechanisms of isoquercitin[J]. World J Clin Oncol, 2016, 7(2): 189–99. DOI:10.5306/wjco.v7.i2.189 |
| [4] | Li Y, Duan S, Jia H, et al. Flavonoids from tartary buckwheat induce G2/M cell cycle arrest and apoptosis in human hepatoma HepG2 cells[J]. Acta Biochim Biophys Sin (Shanghai), 2014, 46(6): 460–70. DOI:10.1093/abbs/gmu023 |
| [5] | 郑亚梅. FKN/CX3CR1对小细胞肺癌系H446迁移迁移和侵袭能力的影响及其机制初探和侵袭能力的影响及其机制初探[D]. 武汉: 华中科技大学, 2013. [ Zheng YM. Recombinant human FKN enhances the migration and invasion in H446 and the potential factors on CX3CR1 gene expression of H446[D]. Wuhan: Huazhong University of Science and Technology, 2013. ] |
| [6] | Boag SE, Das R, Shmeleva EV, et al. T lymphocytes and fractalkine contribute to myocardial ischemia/reperfusion injury in patients[J]. J Clin Invest, 2015, 125(8): 3063–76. DOI:10.1172/JCI80055 |
| [7] | Rennert K, Heisig K, Groeger M, et al. Recruitment of CD16(+) monocytes to endothelial cells in response to LpS-treatment and concomitant TNF release is regulated by CX3CR1 and interfered by soluble fractalkine[J]. Cytokine, 2016, 83: 41–52. DOI:10.1016/j.cyto.2016.03.017 |
| [8] | Li FQ, Zeng DK, Jia CL, et al. The effects of sodium tanshinone IIa sulfonate pretreatment on high glucose-induced expression of fractalkine and apoptosis in human umbilical vein endothelial cells[J]. Int J Clin Exp Med, 2015, 8(4): 5279–86. |
| [9] | Mohr S, Doebele C, Comoglio F, et al. Hoxa9 and Meis1 Cooperatively Induce Addiction to Syk Signaling by Suppressing miR-146a in Acute Myeloid Leukemia[J]. Cancer Cell, 2017, 31(4): 549–62. DOI:10.1016/j.ccell.2017.03.001 |
| [10] | Park GB, Chung YH, Kim D. Induction of galectin-1 by TLR-dependent pI3K activation enhances epithelial-mesenchymal transition of metastatic ovarian cancer cells[J]. Oncol Rep, 2017, 37(5): 3137–45. DOI:10.3892/or.2017.5533 |
| [11] | Ni B, Hu J, Chen D, et al. Alternative splicing of spleen tyrosine kinase differentially regulates colorectal cancer progression[J]. Oncol Lett, 2016, 12(3): 1737–44. |
| [12] | Naldi A, Larive RM, Czerwinska U, et al. Reconstruction and signal propagation analysis of the Syk signaling network in breast cancer cells[J]. PLoS Comput Biol, 2017, 13(3): e1005432. DOI:10.1371/journal.pcbi.1005432 |
| [13] | Chuanliang P, Yunpeng Z, Yingtao H, et al. Syk expression in non-small-cell lung cancer and its relation with angiogenesis[J]. J Cancer Res Ther, 2016, 12(2): 663–6. DOI:10.4103/0973-1482.154082 |
| [14] | Li Z, Cai Z, Tao B, et al. Full-length spleen tyrosine kinase inhibits the invasion and metastasis of human laryngeal squamous cell carcinoma[J]. Int J Clin Exp Pathol, 2015, 8(12): 15786–93. |
| [15] | Szydlowski M, Kiliszek P, Sewastianik T, et al. FOXO1 activation is an effector of SYK and AKT inhibition in tonic BCR signal-dependent diffuse large B-cell lymphomas[J]. Blood, 2016, 127(6): 739–48. DOI:10.1182/blood-2015-06-654111 |
| [16] | 洪华章, 周凯, 傅平, 等. 抑癌基因脾酪氨酸激酶和人类Runt相关转录因子3基因启动子甲基化与胃癌术后复发转移的关系[J]. 中华肿瘤杂志, 2012, 36(5): 341–5. [ Hong HZ, Zhou K, Fu P, et al. Relationship between promoter methylation of Syk and Runx3 genes and postoperative recurrence and metastasis in gastric carcinoma[J]. Zhonghua Zhong Liu Za Zhi, 2012, 36(5): 341–5. ] |
| [17] | Cui Y, Steagall WK, Lamattina A, et al. Aberrant SYK kinase signaling is essential for tumorigenesis induced by TSC2 inactivation[J]. Cancer Res, 2017, 77(6): 1492–502. DOI:10.1158/0008-5472.CAN-16-2755 |
| [18] | Dabrowska C, Li M, Yun F. Apoptotic caspases in promoting cancer: implications from their roles in development and tissue homeostasis[J]. Adv Exp Med Biol, 2016, 930: 89–112. DOI:10.1007/978-3-319-39406-0 |
 2017, Vol. 44
2017, Vol. 44


