文章信息
- 维吾尔族乳腺癌患者JAG1基因甲基化的临床意义
- Clinical Significance of JAG1 Gene Methylation in Uygur Breast Cancer Patients
- 肿瘤防治研究, 2017, 44(11): 734-739
- Cancer Research on Prevention and Treatment, 2017, 44(11): 734-739
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.17.0501
- 收稿日期: 2017-05-03
- 修回日期: 2017-08-15
2. 441100 襄阳, 襄阳市中心医院病理科;
3. 832003 石河子, 石河子市公安局刑侦支队法医中心;
4. 830000 乌鲁木齐, 新疆维吾尔自治区人民医院病理科
2. Department of Pathology, Xiangyang Central Hospital, Xiangyang 441100, China;
3. Forensic Centre, Criminal Investigation Department of Public Security Bureau, Shihezi 832003, China;
4. Department of Pathology, Xinjiang Uygur Municipal People's Hospital, Urumqi 830000, China
乳腺癌是女性最常见的恶性肿瘤[1-2],新疆维吾尔族乳腺癌的发病率近年呈明显上升趋势,且发病趋向年轻化[3]。不同民族乳腺癌具有不同的遗传易感性[4],因此这种遗传背景上的差异对阐明维吾尔族女性乳腺癌发生发展具有重要意义。
Notch1信号转导通路与乳腺癌相关性有大量文献报道[5-9],课题组前期实验结果发现Notch1信号通路中的配体JAG1分子与新疆汉族女性乳腺癌发生发展密切相关[10],并且JAG1基因甲基化是调控汉族乳腺癌的重要机制之一[11-12]。甲基化是表观遗传学修饰,不同种族人群中的基因甲基化谱及甲基化率可能存在差异[13-16]。新疆汉族与维吾尔族这两个民族具有不同的遗传背景,推测其乳腺癌患者的DNA甲基化水平存在不同的民族差异性,关于JAG1基因的甲基化状态与维吾尔族乳腺癌发生发展的相关性,目前尚未见相关报道。
因此,本研究以维吾尔族乳腺癌为研究对象,应用MALDI-TOF MS和免疫组织化学技术检测JAG1基因总体水平及单个CpG位点定量甲基化率以及JAG1蛋白表达,以探讨JAG1分子在维吾尔族乳腺癌变进展过程中的作用。
1 资料与方法 1.1 资料 1.1.1 样本和临床资料收集新疆维吾尔自治区人民医院1989年1月至2009年4月手术切除、石蜡包埋的维吾尔族女性乳腺标本,经过伦理委员会批准和受试者知情同意。其中,乳腺普通型导管增生(usual ductal hyperplasia, UDH)15例、非典型性导管增生(atypical ductal hyperplasia, ADH)15例、导管原位癌(ductal carcinoma in situ, DCIS)15例、浸润性导管癌(invasive ductal carcinoma, IDC)50例。收集乳腺癌患者的年龄、组织学分级、淋巴结转移、临床分期、雌孕激素受体水平、HER2表达等临床病理参数。
1.1.2 主要试剂和仪器EZ-96甲基化试剂盒购自美国Zymo Research公司,JAG1抗体购自美国Santa Cruz公司,SP试剂盒购自福建迈新生物开发有限公司,DAB显色液购自北京中杉金桥生物技术有限公司,MassCLEAVE试剂盒和SAP试剂购自美国Sequenom公司,Mass ARRAY质谱仪购自Sequenom公司。
1.2 方法 1.2.1 乳腺组织JAG1基因甲基化的检测检测JAG1基因单个CpG位点定量甲基化水平,该基因CpG位点位于启动子上游-1 396 bp~-1 083 bp之间的CpG岛区域,包括28个CpG位点即15个CpG单位,CpG位点示意图参照文献[11]。首先应用显微切割技术将乳腺组织中UDH和ADH分离出来,提取总DNA,应用MALDI-TOF MS法定量检测单个CpG位点DNA甲基化值。提取出的DNA经亚硫酸氢盐处理,未发生甲基化的胞嘧啶转变为尿嘧啶而甲基化的胞嘧啶保持不变,PCR扩增,引物序列见文献[11],虾碱性磷酸酶处理,处理后的产物体外转录最终成为腺嘌呤,然后再利用特异性的T切酶将甲基化和非甲基化区域剪切成不同的小片段,使发生甲基化CpG位点和非甲基化CpG位点之间相差16 Da,区分甲基化与非甲基化,放入基质芯片中检测,MassARRAY质谱仪收集质谱图,用Epityper TM software v1.0.5软件进行分析。
1.2.2 免疫组织化学SP染色方法检测JAG1蛋白表达石蜡包埋乳腺组织切片脱蜡至水,内源性抗原修复,3%双氧水室温孵育30 min阻断过氧化物酶,JAG1抗体(稀释度1:300)孵育过夜,加二抗,DAB溶液显色,苏木精对比染色,中性树胶封片。人肺癌组织为阳性对照,PBS替代一抗作为阴性对照[17]。
1.2.3 结果判定乳腺癌细胞或正常上皮细胞胞质出现黄色颗粒为阳性表达,阳性细胞所占比例≤5%为0分,5%~25%为1分,> 25%~50%为2分,> 50%~75%为3分,> 75%~100%为4分。细胞染色无着色为0分,浅黄色颗粒为1分,棕黄色颗粒为2分,棕褐色颗粒为3分。阳性评分由阳性细胞百分数和阳性强度相乘。总分小于4分为低表达,总分大于或等于4分为高表达[10]。
1.3 统计学方法实验数据采用SPSS 20.0软件分析,Kruskal-Wallis H检验分析JAG1基因总体和单个位点甲基化率在乳腺四组组织之间的比较、两组之间的甲基化率比较以及甲基化率与分级和分期之间的相关性。非参数U检验比较甲基化与ER、PR、HER2之间的关系。卡方检验或Fisher精确检验分析JAG1蛋白和临床病理特征的相关性。Spearman秩和检验分析JAG1蛋白表达和甲基化的相关性。所有检验均以P < 0.05为差异有统计学意义。
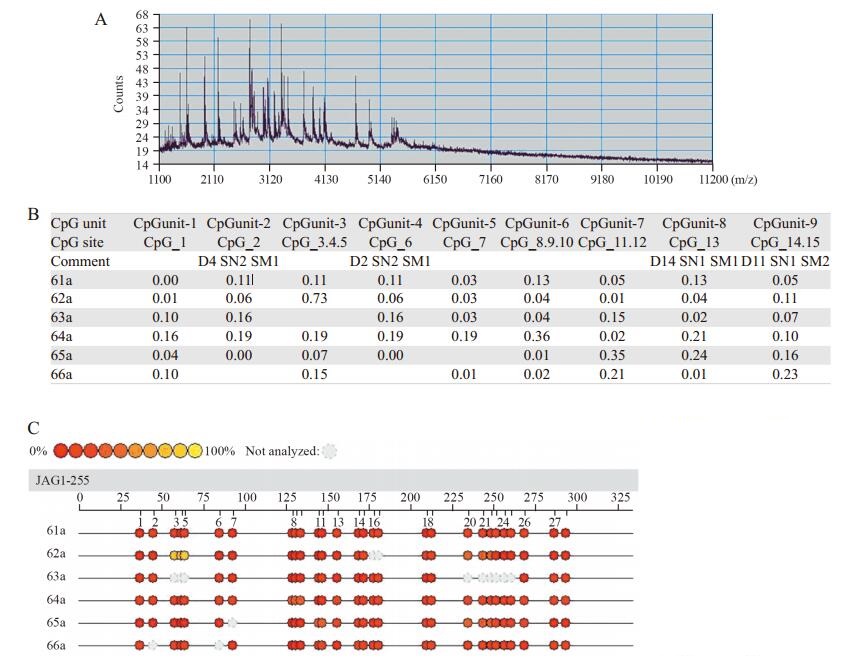
2 结果 2.1 JAG1基因在维吾尔族乳腺UDH、ADH、DCIS和IDC组中的甲基化水平MassARRAY质谱仪收集JAG1基因样本甲基化质谱图,见图 1A,EpiTYPERv1.0.5软件对其15个CpG单位进行甲基化定量分析,包括甲基化率图,见图 1B~1C。
|
| A : MALDI-TOF-MS mass spectrum of a sample from IDC; B: methylation percentage of CpG site in IDC group; C: methylation levels of CpG loci in IDC group 图 1 JAG1基因甲基化质谱图及定量分析 Figure 1 Mass spectrometry and quantitative analysis of JAG1 gene methylation |
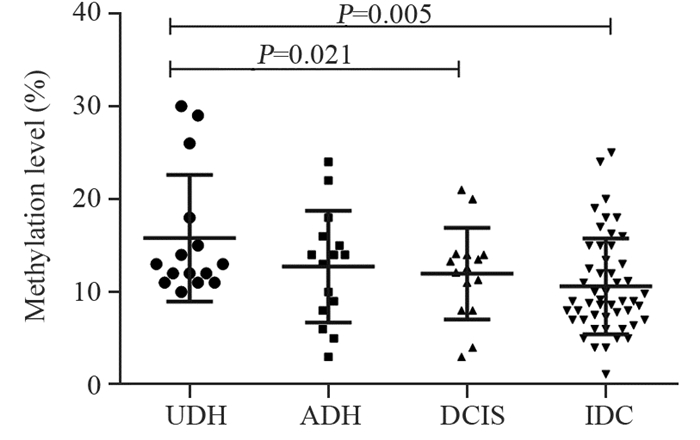
JAG1基因在维吾尔族乳腺UDH、ADH、DCIS和IDC组织样本中甲基化变化见图 2。JAG1基因总甲基化水平为该基因15个CpG单位甲基化平均值,这15个CpG单位位于该基因CpG岛丰富的启动子区,虽然不能准确代表总的甲基化水平,但可以作为该基因总甲基化定量水平的一个简单有用的参考指标。JAG1基因总甲基化水平从UDH、ADH、DCIS到IDC逐渐降低,四组之间差异有统计学意义(P=0.003),四组之间两两比较,IDC与DCIS组分别与UDH组之间差异有统计学意义,其余各组之间差异不明显。
|
| UDH: usual ductal hyperplasia; ADH: atypical ductal hyperplasia; DCIS: ductal carcinoma in situ; IDC: invasive ductal carcinoma 图 2 JAG1基因总甲基化率在乳腺UDH、ADH、DCIS、IDC组中的变化 Figure 2 Overall methylation rates of JAG1 gene in usual ductal hyperplasia(UDH), atypical ductal hyperplasia(ADH), ductal carcinoma in situ (DCIS), and invasive ductal carcinoma (IDC) groups of breast tissues |
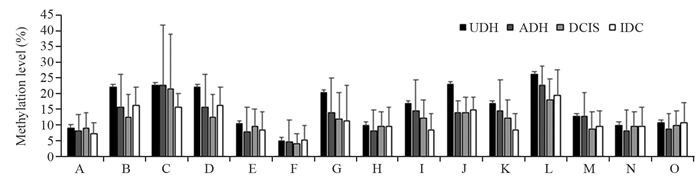
JAG1基因单个CpG单位的甲基化值在乳腺不同病变组中呈现不同的水平。JAG1大部分CpG单位的甲基化率在IDC组中均低于DCIS、ADH及UDH,并且CpG_11.12、CpG_14.15、CpG_18.19位点的甲基化率在四组之间比较差异有统计学意义(均P < 0.05)。CpG_3.4.5位点甲基化率在IDC和UDH中分别为15.7%和23.7%,CpG_20.21.22位点甲基化率在IDC和UDH分别为21.9%和26.0%,甲基化水平相对较高,CpG_8.9.10位点甲基化率在IDC和UDH组中均为4.9%,甲基化水平较低,见图 3。
|
| A: CpG_1; B: CpG_2; C: CpG_3.4.5; D: CpG6; E: CpG_7; F: CpG_8.9.10; G: CpG_11.12; H: CpG_13; I: CpG_14.15; J: CpG_16.17; K: CpG_18.19; L: CpG_20.21.22; M: CpG_23.24.25; N: CpG_26; O: CpG_27.28 图 3 JAG1基因单个CpG位点甲基化值在乳腺UDH、ADH、DCIS、IDC组中的变化 Figure 3 Single CpG site methylation values of JAG1 gene in UDH, ADH, DCIS, IDC groups of breast tissues |
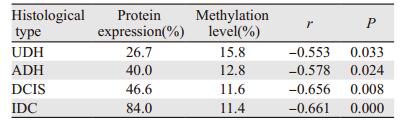
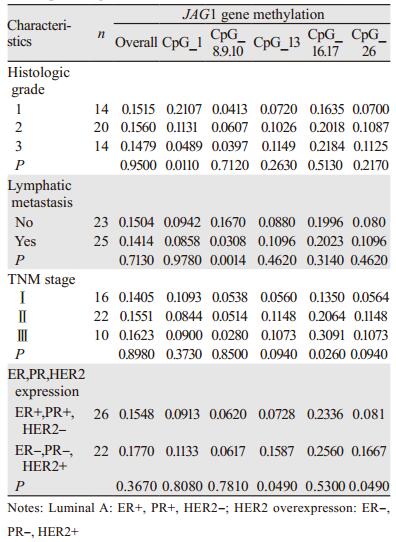
在48例乳腺癌组织中,JAG1基因总甲基化水平在乳腺癌高分级、淋巴结转移、低分期和Luminal A型(ER+,PR+,HER2-)组中是降低的,但没有统计学意义。然而就单个CpG位点而言,CpG_1甲基化水平从1级到2级至3级逐渐降低且差异有统计学意义(P=0.011);CpG_8.9.10位点甲基化率在无腋窝淋巴结转移组显著高于有腋窝淋巴结转移组(P=0.0014);CpG_16.17位点甲基化率从Ⅰ期到Ⅱ期至Ⅲ期呈逐渐升高趋势且差异有统计学意义(P=0.026);CpG_13、CpG_26位点甲基化在Luminal A型组明显低于HER2过表达组(ER-,PR-,HER2+)(均P=0.049),见表 1。
|
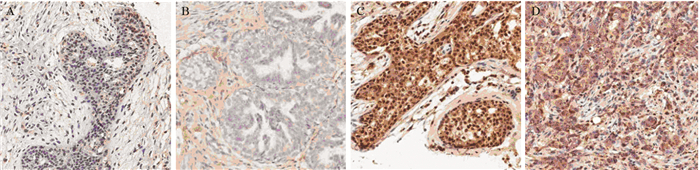
JAG1蛋白在维吾尔族乳腺UDH、ADH、DCIS及IDC组中的表达见图 4。JAG1分子的阳性表达定位于乳腺上皮细胞或癌细胞的细胞质和胞膜,从UDH到IDC这一癌变过程中的表达逐渐增强。
|
| A: UDH; B: ADH; C: DCIS; D: IDC 图 4 JAG1蛋白在乳腺UDH、ADH、DCIS、IDC组中的表达(SP×200) Figure 4 Expression of JAG1 protein in UDH, ADH, DCIS and IDC groups of breast tissues (SP×200) |
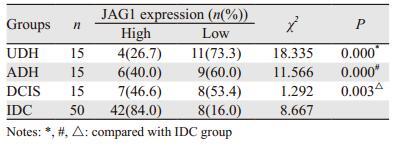
分析JAG1蛋白在四组中的表达,结果发现JAG1蛋白在四组中的表达逐渐升高,差异有统计学意义(P=0.015)。四组之间两两比较,UDH、ADH和DCIS组分别与IDC组比较差异有统计学意义,见表 2。
|
从UDH到IDC这一癌变过程中的JAG1蛋白表达率逐渐升高,同时相对应组中的甲基化水平逐渐降低,JAG1蛋白在四组中的总表达水平与基因总甲基化水平之间呈显著负相关(r=-0.674, P < 0.001),并且每一组中蛋白表达和甲基化水平也呈显著负相关,见表 3。
JAG1基因在维吾尔族女性乳腺UDH、ADH、DCIS和IDC组中的甲基化水平逐渐降低,以CpG_11.12、CpG_14.15、CpG_18.19位点甲基化率降低为明显,并且乳腺普通型上皮增生组分别与原位癌组和浸润癌组之间差异有统计学意义,提示JAG1基因低甲基化有可能促进乳腺上皮细胞的癌变和浸润,此结果与前期课题组研究汉族乳腺癌的结论相一致[12]。维吾尔族中CpG_11.12、CpG_14.15、CpG_18.19位点低甲基化可能在乳腺癌变早期阶段和晚期浸润阶段发挥了更加重要的作用,而汉族乳腺组织中CpG_27.28和CpG_23.24.25位点在促进乳腺癌变过程中发挥了重要作用[12],说明JAG1甲基化与乳腺癌的发生在维吾尔族和汉族中存在民族异质性。
JAG1甲基化和维吾尔族乳腺癌患者临床病理特征之间的相关性显示,CpG_1甲基化率在低分化组中显著降低,说明JAG1基因CpG_1位点低甲基化在乳腺癌的恶性进展过程中可能发挥了关键的作用;CpG_8.9.10在有腋窝淋巴结转移组中的甲基化率明显下降,提示JAG1基因CpG_8.9.10位点低甲基化提高了乳腺癌转移的能力;而CpG_16.17却在晚期乳腺癌组织中的甲基化率明显升高,说明JAG1基因特异性位点的低甲基化率在维吾尔族乳腺癌不同分期阶段可能发挥不同的作用;并且CpG_13和CpG_26甲基化率还与ER、PR、HER2的表达状态显著相关,提示JAG1基因CpG_13、CpG_26低甲基化水平可能与女性激素水平及预后有关。由此提示JAG1基因位点可能是影响乳腺癌发生进展的不同关键DNA区段,但要证实这一结论,有必要进一步检测该DNA区段甲基化水平是否调控基因的表达进而影响乳腺癌的生物学行为。我们前期结果发现汉族乳腺癌患者中JAG1基因低甲基化率促进乳腺癌进展[12],与本研究结果相一致,同时也与其他的研究结论相符合[18-19],本研究发现了JAG1基因在维吾尔族乳腺癌中有特异性甲基化位点,在其地区和民族中未见相关报道。
JAG1蛋白在维吾尔族乳腺癌变过程的组织(即从UDH、ADH、DCIS到IDC)中的表达逐渐升高,浸润癌中表达最强,提示JAG1分子在乳腺癌中扮演一个癌基因角色,并且与其甲基化水平呈显著负相关,推测JAG1基因低甲基化促进其蛋白表达,进而促进乳腺癌的发生发展。这与我们在汉族乳腺癌中的研究结果相一致[12]。
本研究表明,JAG1基因低甲基化率可能促进了维吾尔族女性乳腺癌的发生发展,并且可能通过JAG1蛋白高表达而实现,但其具体机制还需进一步研究。
| [1] | 王媛媛, 董惠玲, 吴炳义, 等. 2010-2012年山东省监测点居民恶性肿瘤死亡及减寿分析[J]. 肿瘤防治研究, 2016, 43(11): 980–3. [ Wang YY, Dong HL, Wu BY, et al. Death of malignant tumors and potential years of life lost among residents in shandong province, 2010-2012[J]. Zhong Liu Fang Zhi Yan Jiu, 2016, 43(11): 980–3. DOI:10.3971/j.issn.1000-8578.2016.11.012 ] |
| [2] | 庹吉妤, 张敏, 常江, 等. 2012年湖北省肿瘤登记地区恶性肿瘤发病与死亡情况分析[J]. 肿瘤防治研究, 2016, 43(11): 974–9. [ Tuo JY, Zhang M, Chang J, et al. Cancer incidence and mortality in cancer registries in Hubei province, 2012[J]. Zhong Liu Fang Zhi Yan Jiu, 2016, 43(11): 974–9. DOI:10.3971/j.issn.1000-8578.2016.11.011 ] |
| [3] | 李双武, 鲁英, 杨晓燕, 等. 新疆地区不同民族乳腺癌患者临床特征及相关因素分析[J]. 新疆医科大学学报, 2012, 35(7): 895–8. [ Li SW, Lu Y, Yang XY, et al. Analysis of clinical characteristics and related factors of breast cancer patients with different nationalities in Xinjiang areas[J]. Xinjiang Yi Ke Da Xue Xue Bao, 2012, 35(7): 895–8. ] |
| [4] | 钟芳芳, 张巍, 王成辉, 等. 上海汉族和新疆维吾尔族女性乳腺癌临床病理征的比较[J]. 中国癌症杂志, 2014, 24(1): 21–8. [ Zhong FF, Zhang W, Wang CH, et al. Comparison of clinicopathologic features of breast carcinoma in Shanghai Han and Xinjiang Uygur women[J]. Zhongguo Ai Zheng Za Zhi, 2014, 24(1): 21–8. ] |
| [5] | Speiser J, Foreman K, Drinka E, et al. Notch-1 and Notch-4 biomarker expression in triple-negative breast cancer[J]. Int J Surg Pathol, 2012, 20(2): 139–45. |
| [6] | 张娜, 孙振柱, 李锋, 等. 乳腺癌和乳腺导管内增生性病变Notchl基因甲基化的检测及临床意义[J]. 中华病理学杂志, 2011, 40(5): 324–9. [ Zhang N, Sun ZZ, Li F, et al. Detection and clinical significance of Notchl methylation in breast cancer and intraductal proliferative breast lesions[J]. Zhonghua Bing Li Xue Za Zhi, 2011, 40(5): 324–9. ] |
| [7] | Shan S, Zhao X, Zhang X, et al. Notch1 signaling regulates the epithelial-mesenchymal transition and invasion of breast cancer in a Slug-dependent manner[J]. Mol Cancer, 2015, 14: 28. DOI:10.1186/s12943-015-0295-3 |
| [8] | Reedijk M, Odorcic S, Chang L, et al. High level coexpression of JAG1 and NOTCH1 is observed in human breast cancer and is associated with poor overall surviva[J]. Cancer Res, 2005, 65(18): 8530–7. DOI:10.1158/0008-5472.CAN-05-1069 |
| [9] | Artavanis-Tsakonas S, Rand MD, Lake RJ. Notch signaling: cell fate control and signal integration in development[J]. Science, 1999, 284(5415): 770–6. DOI:10.1126/science.284.5415.770 |
| [10] | 曹玉文, 杜小明, 李文琴, 等. Jagged-1基因在乳腺癌和正常乳腺组织中的表达及临床意义[J]. 中国妇幼保健, 2014, 29(34): 5661–3. [ Cao YW, Du XM, Li WQ, et al. Expressions and significance of Jagged-1 in breast cancer and normal breast tissue[J]. Zhongguo Fu You Bao Jian, 2014, 29(34): 5661–3. ] |
| [11] | Cao Y, Li Y, Zhang N, et al. Quantitative DNA hypomethylation of ligand Jagged1 and receptor Notch1 signifies occurrence and progression of breast carcinoma[J]. Am J Cancer Res, 2015, 5(5): 1621–34. |
| [12] | 李怡晓, 李锋, 张娜, 等. Jagged1基因甲基化与乳腺癌发生发展相关性探讨[J]. 中华肿瘤防治杂志, 2015, 22(11): 846–50. [ Li YX, Li F, Zhang N, et al. Significance of jagged1 methylation status in breast carcinogenesis[J]. Zhonghua Zhong Liu Fang Zhi Za Zhi, 2015, 22(11): 846–50. ] |
| [13] | 缑文斌, 郭媛媛, 张巍. 维吾尔族和汉族散发性乳腺癌患者BRCA1基因启动子区基化的对比研究[J]. 新疆医科大学学报, 2015, 38(11): 1354–6. [ Gou WB, Guo YY, Zhang W. Comparative study methylation in sporadic breast cancer BRCA1 gene promoter region of Uygurs and Han women[J]. Xinjiang Yi Ke Da Xue Xue Bao, 2015, 38(11): 1354–6. DOI:10.3969/j.issn.1009-5551.2015.11.007 ] |
| [14] | Conway K, Edmiston SN, Tse CK, et al. Racial Variation in Breast Tumor Promoter Methylation in the Carolina Breast Cancer Study[J]. Cancer Epidemiology Biomarkers Prev, 2015, 24(6): 921–30. DOI:10.1158/1055-9965.EPI-14-1228 |
| [15] | Song MA, Brasky TM, Marian C, et al. Racial differences in genome-wide methylation profiling and gene expression in breast tissues from healthy women[J]. Epigenetics, 2015, 10(12): 1177–87. DOI:10.1080/15592294.2015.1121362 |
| [16] | Galanter JM, Gignoux CR, Oh SS, et al. Differential methylation between ethnic sub-groups reflects the effect of genetic ancestry and environmental exposures[J]. Elife, 2017, 6: e20532. |
| [17] | 姜昕, 周建华, 邓征浩, 等. Notch1, Jagged1和VEGF蛋白在非小细胞肺癌的表达及其意义[J]. 中南大学学报(医学版), 2007, 32(6): 1031–6. [ Jiang X, Zhou JH, Deng ZH, et al. Expression and significance of Notch1, Jagged1 and VEGF in human non-small cell lung cancer[J]. Zhongnan Da Xue Xue Bao(Yi Xue Ban), 2007, 32(6): 1031–6. ] |
| [18] | Shargh SA, Sakizli M, Khalaj V, et al. Down regulation of E-cadherin expression in breast cancer by promoter hypermethylation and its relation with progression and prognosis of tumor[J]. Med Oncol, 2014, 31(11): 250. DOI:10.1007/s12032-014-0250-y |
| [19] | Moarii M, Pinheir A, Sigal-Zafrani B, et al. Epigenomic alteration in breast carcinoma from primary tumor to locoreginal recurrences[J]. PLoS One, 2014, 9(8): e103986. DOI:10.1371/journal.pone.0103986 |
 2017, Vol. 44
2017, Vol. 44