文章信息
- Ubiquilin1蛋白在乳腺癌组织中的表达与预后意义
- Expression of Ubiquilin1 Protein in Breast Cancer Tissues and Its Prognostic Significance
- 肿瘤防治研究, 2017, 44(8): 535-539
- Cancer Research on Prevention and Treatment, 2017, 44(8): 535-539
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.17.0153
- 收稿日期: 2017-02-16
- 修回日期: 2017-05-08
2. 100050 北京,首都医科大学友谊医院干部医疗科
2. Department of Senior Official Ward, Beijing Friendship Hospital, Capital University of Medical Sciences, Beijing 100050, China
乳腺癌是全球女性中最常见的恶性肿瘤,在女性癌症相关死亡中居第二,严重威胁着女性的健康[1-2]。但目前对其发生、发展的精确分子机制尚不完全清楚。因此,探索可用于预测乳腺癌复发风险、评估预后的分子生物学标志极其重要。UBQLN1是一种泛素样蛋白质,在调节蛋白酶体降解过程中发挥核心作用[3]。近些年来研究发现其通过促进错误折叠蛋白质降解、参与内质网应激相关降解(ERAD)[4]、自噬[5-6]、细胞凋亡[7]和受体转运[8]等多种机制对肿瘤的迁移和侵袭等生物学特性产生重要影响。国内有关UBQLN1与乳腺癌方面的研究罕见报道。本研究通过检测UBQLN1在乳腺癌中的表达,探讨其与临床病理特征及预后的相关性,分析UBQLN1在乳腺癌浸润、转移中的重要作用,以期为判定乳腺癌预后及指导临床治疗提供新的思路。
1 资料与方法 1.1 临床资料收集首都医科大学附属北京世纪坛医院2009年1月—2012年9月间存档的石蜡包埋乳腺癌标本108例进行回顾性分析,并取得医学伦理学相关部门同意。患者均为女性,术前均未接受治疗(包括放疗、化疗及内分泌治疗)、无远处转移。平均年龄58岁(32~88岁)。另设对照组:对应癌旁正常乳腺组织108例(距癌缘 > 2.0 cm)。
1.2 乳腺癌病理学指标及诊断标准乳腺癌病理学指标包括:年龄、绝经状态、病理类型、组织学分级、肿瘤大小、TNM分期、淋巴结转移个数、ER、PR、HER2/neu表达、基因分型、淋巴浆细胞浸润、脉管浸润、神经侵犯、Ki-67及P53等,数据收集自存档病例的病理报告中。病理组织学诊断依据2003年《WHO乳腺及女性生殖器官肿瘤病理学和遗传学》中乳腺癌的诊断标准,由两位高级病理医生进行诊断、分级及分期。肿瘤分期根据AJCC TNM分期(第7版)分为Ⅰ期、Ⅱ期和Ⅲ期。基因分型的划分标准为[8]:Luminal A型(ER/PR+、HER2-、Ki-67低表达);Luminal B型(HER2阴性型:ER+/PR+、HER2-、Ki-67高表达;HER2阳性型:ER+/PR+、HER2 +、任何状态的Ki-67);ERBB2+型(HER2+、ER-/PR-);基底样型/三阴性:(HER2-、ER-/PR-)。Ki-67表达的划分标准为[9]:≥14%为高表达,< 14%为低表达。
1.3 方法 1.3.1 免疫组织化学法鼠抗人单克隆抗体UBQLN1购自英国Abcam公司(ab128011,稀释度1:50),免疫组织化学试剂盒购自北京中杉金桥生物技术有限公司。用已知肺腺癌肿瘤组织阳性切片作阳性对照,用磷酸盐缓冲液代替一抗作阴性对照。DAB显色,苏木精对比染色,梯度乙醇脱水,二甲苯透明,明胶封片后镜检。
1.3.2 结果判定采用双盲法,由两位病理医生独立观察。实验结果判断参照Remmele和Stegner[10]提出的免疫反应积分打分法,综合考虑阳性细胞的染色强度和所占比例。染色强度分为:无着色为0分,浅着色为1分,中等着色为2分,强着色为3分。阳性细胞所占比例分为:< 1%为0分,1%~ < 10%为1分,10%~ < 50%为2分,50%~ < 80%为3分,80%~100%为4分。阳性强度和阳性细胞所占比例得分相乘为最后得分:< 4分为阴性,≥4为阳性。
1.4 随访采用电话咨询结合临床病例资料查询方式,随访所有病例的生存时间、复发、转移、死亡等情况,随访截至2016年6月30日。
1.5 统计学方法统计数据采用SPSS17.0软件进行分析,P < 0.05为差异有统计学意义。采用χ2检验和Fisher’s精确检验分析UBQLN1表达和各临床病理指标之间的相关性。UBQLN1与P53及Ki-67间的相关性采用非参数Spearman检验;单因素生存分析采用Kaplan-Meier检验;乳腺癌的预后采用Cox多因素回归分析。
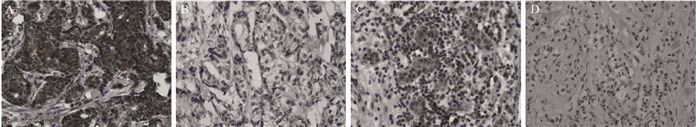
2 结果 2.1 免疫组织化学检测结果非特殊型浸润性导管癌90例,浸润性小叶癌18例,UBQLN1在两种类型的乳腺癌中表达方式差异无统计学意义。在乳腺癌组织中,UBQLN1的阳性染色定位于细胞质和(或)细胞核中,呈棕黄色或棕褐色,表达具有异质性;在癌旁正常乳腺组织中未见明显阳性表达,见图 1。UBQLN1在108例乳腺癌标本中有55例中高表达,阳性率为50.9%(55/108)。
|
| Strongly positive expression of UBQLN1 in invasive ductal(A) and invasive lobular breast cancer tissues(C) and weakly positive expression of UBQLN1 in invasive ductal(B) and invasive lobular breast cancer tissues(D) 图 1 乳腺癌组织中UBQLN1的染色结果(IHC ×400) Figure 1 Expression of UBQLN1 in breast cancer tissues (IHC ×400) |
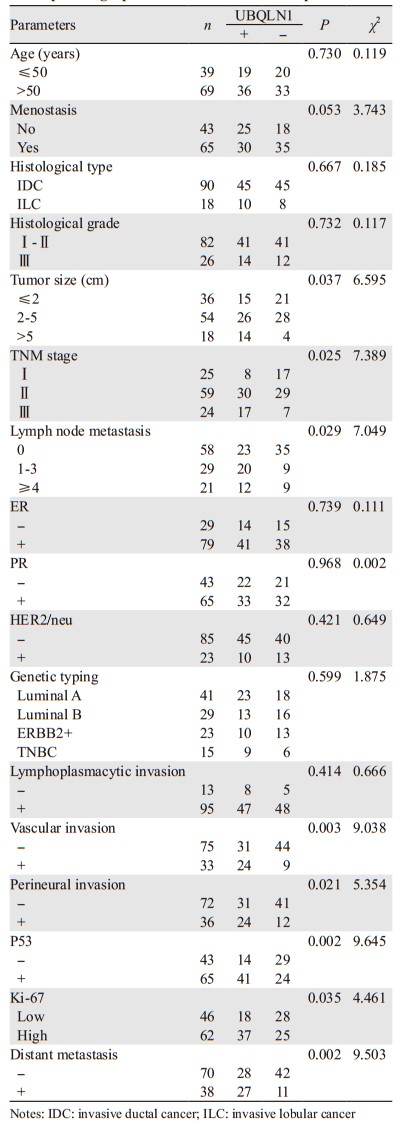
UBQLN1表达与肿瘤大小、临床TNM分期、淋巴结转移个数、脉管浸润、神经侵犯、Ki-67、P53及远处转移均呈正相关(P < 0.05),与患者年龄、绝经状态、病理类型、组织学分级、ER、PR、HER2/neu表达、基因分型、淋巴浆细胞浸润等无相关性(P > 0.05),见表 1。
 |
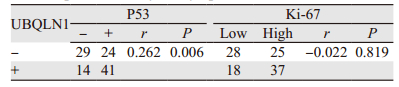
经Spearman秩相关检验得出UBQLN1的表达与P53的表达呈正相关(r=0.262,P=0.006);与Ki-67的表达不相关(r=-0.022,P=0.819),见表 2。
 |
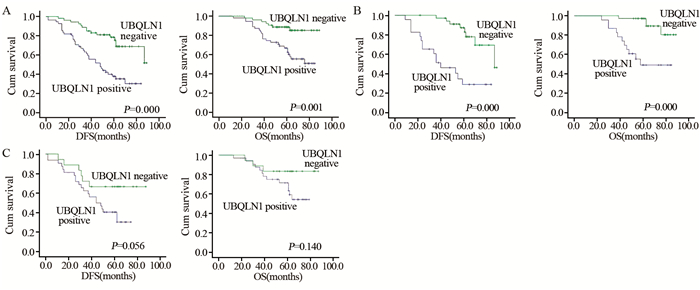
UBQLN1在淋巴结阳性组中阳性表达率为64%(32/50),在淋巴结阴性组中阳性表达率为39.7%(23/58),差异有统计学意义(χ2=6.368, P=0.012);UBQLN1在有远处转移组中阳性表达率为71.7%(27/38),在无远处转移组为40%(28/70),差异有统计学意义(χ2=9.503, P=0.002)。进一步行生存分析,在淋巴结阳性组,UBQLN1阳性组与阴性对照组间预后差异无统计学意义(DFS: P=0.056; OS: P=0.140)。然而,在淋巴结阴性组,UBQLN1阳性组与阴性对照组相比,DFS和OS显著降低(DFS: P=0.000; OS: P=0.000),见图 2。
|
| A: Kaplan-Meier curves of 108 breast cancer patients stratified by UBQLN1 (n=108); B: Kaplan-Meier curves of 58 breast cancer patients without lymph node metastasis stratified by UBQLN1 (n=58); C: Kaplan-Meier curves of 50 breast cancer patients with lymph node metastasis stratified by UBQLN1 (n=50) 图 2 UBQLN1表达与乳腺癌生存期的关系 Figure 2 Correlation of UBQLN1 expression with survival of breast cancer patients |
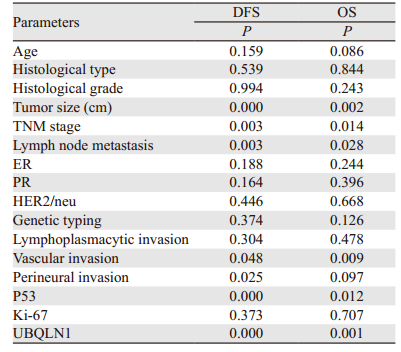
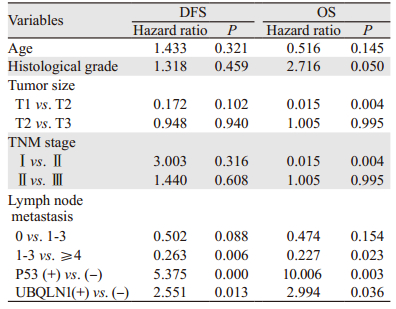
随访时间13~89月(平均60月)。108例乳腺癌患者中12例局部复发,38例远处转移,死亡31例,失访6例。Kaplan-Meier生存曲线分析显示,UBQLN1表达、肿瘤大小、临床TNM分期、淋巴结转移个数、脉管浸润、神经侵犯、P53与乳腺癌患者的DFS显著相关(P < 0.05)。UBQLN1表达、肿瘤大小、临床TNM分期、淋巴结转移、脉管浸润、P53与患者的OS显著相关(P < 0.05),见表 3。Cox回归模型进行多因素分析结果显示,UBQLN1是影响患者DFS和OS的独立不良预后因素(P < 0.05),UBQLN1表达阳性的患者复发转移风险比阴性患者增加2.551倍,死亡风险比阴性患者增加2.994倍。此外,P53也是乳腺癌患者独立的预后因素,见图 2、表 4。
 |
 |
UBQLN1是一种核小体表面蛋白,属于高度保守的泛素样蛋白家族(UBQLN1、UBQLN2、UBQLN3、UBQLN4和UBQLNL)中的一员,其编码基因位于人类9号染色体(9q22),编码589氨基酸序列或561氨基酸序列,在组织中广泛表达[11]。UBQLN1全长由11个外显子组成,具有3个功能结构域:N-末端泛素样区域(UBL),C-末端泛素相关的区域(UBA)和中间的STI伴侣样区域[12-13]。这些区域的存在表明,UBQLN1的功能类似于一个传递蛋白,它可将多泛素化目标提供给特定的蛋白,促进蛋白酶体降解。Beverly等[14]发现UBQLN1在肺癌中高表达,且与患者的生存期降低相关。Shah等[4]研究显示UBQLN1能诱导肺腺癌细胞的迁移、侵袭和上皮间质化。Guidi等[15]研究发现卵巢癌细胞系对顺铂的耐药性与UBQLN1的高表达有关。
自噬是一种进化上保守的溶酶体降解途径,对于维持细胞完整性至关重要[16]。作为维持内环境稳定的机制,自噬调节的失调与许多病理生理过程有关,包括神经退行性疾病、心血管疾病和癌症[17]。其可能会破坏细胞的完整性,并促进肿瘤的发生。作为一种促生存机制,乳腺癌细胞受到射线辐射后会增加自噬从而保护癌细胞免受损伤[18]。2015年由Sun等[19]发表的首篇关于UBQLN1与乳腺癌的研究显示,在乳腺癌组织中,miR-200c通过靶向抑制UBQLN1的表达抑制了辐射诱导的自噬反应,从而提高乳腺癌的放射敏感度。进一步研究发现UBQLN1的过表达可逆转miR-200c对乳腺癌细胞的放疗增敏及对放疗诱导自噬抑制的效果。另外2014年Bai等[20]研究中也发现,miR-200c表达降低与HER2阳性乳腺癌曲妥珠单抗耐药相关。
本研究中UBQLN1阳性表达与乳腺癌肿瘤大小、临床TNM分期、淋巴结转移个数等临床病理学指标明显正相关,这也进一步证实UBQLN1的表达与乳腺癌的侵袭和转移密切相关。乳腺癌中UBQLN1与P53的表达呈正相关,提示P53与UBQLN1基因的异常共同参与了乳腺癌的发生,两者在乳腺癌发展过程中可能起协同作用。这与Guidi等[15]发现在卵巢癌细胞系中,UBQLN1蛋白可抑制P53蛋白降解,可能与介导卵巢癌的顺铂耐药一致。但两者在乳腺癌中的具体作用机制尚未见报道,有待于进一步的实验研究证实。此外UBQLN1表达与淋巴结转移和远处转移具有更密切的关系,免疫组织化学及单因素生存分析等结果也证实了这一点。Kaplan-Meier单因素生存分析和Cox多因素回归分析均表明,UBQLN1阳性表达患者较阴性表达者的DFS和OS明显下降,UBQLN1是乳腺癌独立的预后因素。
综上所述,本研究提示UBQLN1蛋白表达与乳腺癌密切相关,且其阳性表达与乳腺癌预后不良有关,可作为乳腺癌的独立预后因子,对评估乳腺癌生物学行为及进展程度可能具有一定的临床价值。
| [1] | DeSantis C, Ma J, Bryan L, et al. Breast cancer statistics[J]. CA Cancer J Clin, 2014, 64(1): 52–62. DOI:10.3322/caac.21203 |
| [2] | 庹吉妤, 张敏, 常江, 等. 2012年湖北省肿瘤登记地区恶性肿瘤发病与死亡情况分析[J]. 肿瘤防治研究, 2016, 43(11): 974–9. [ Tuo JY, Zhang M, Chang J, et al. Cancer Incidence and Mortality in Cancer Registries in Hubei Province, 2012[J]. Zhong Liu Fang Zhi Yan Jiu, 2016, 43(11): 974–9. DOI:10.3971/j.issn.1000-8578.2016.11.011 ] |
| [3] | Haapasalo A, Viswanathan J, Bertram L, et al. Emerging role of Alzheimer's disease-associated ubiquilin-1 in protein aggregation[J]. Biochem Soc Trans, 2010, 38(Pt 1): 150–5. |
| [4] | Shah PP, Lockwood WW, Saurabh K, et al. Ubiquilin1 represses migration and epithelial-to-mesenchymal transition of human non-small cell lung cancer cells[J]. Oncogene, 2015, 34(13): 1709–17. DOI:10.1038/onc.2014.97 |
| [5] | N'Diaye EN, Kajihara KK, Hsieh I, et al. PLIC proteins or ubiquilins regulate autophagy-dependent cell survival during nutrient starvation[J]. EMBO Rep, 2009, 10(2): 173–9. DOI:10.1038/embor.2008.238 |
| [6] | Lee DY, Arnott D, Brown EJ. Ubiquilin4 is an adaptor protein that recruits Ubiquilin1 to the autophagy machinery[J]. EMBO Rep, 2013, 14(4): 373–81. DOI:10.1038/embor.2013.22 |
| [7] | Lu A, Hiltunen M, Romano DM, et al. Effects of ubiquilin 1 on the unfolded protein response[J]. J Mol Neuro Sci, 2009, 38(1): 19–30. DOI:10.1007/s12031-008-9155-6 |
| [8] | Zhang Y, Li Z, Gu J, et al. Plic-1, a new target in repressing epileptic seizure by regulation of GABAAR function in patients and a rat model of epilepsy[J]. Clin Sci, 2015, 129(12): 1207–23. DOI:10.1042/CS20150202 |
| [9] | 中国抗癌协会乳腺癌诊治指南与规范(2015版)[J]. 中国癌症杂志, 2015, 25(9): 692-754. [ Clinical Practice Guidelines in Breast Cancer by Chinese Anti-Cancer Association(2015 version)[J]. Zhongguo Ai Zheng Za Zhi, 2015, 25(9): 692-754. ] |
| [10] | Remmele W, Stegner HE. Recommendation for uniform definition of an immunoreactive score (IRS) for immunohistochemical estrogen receptor detection(ER-ICA)in breast cancer tissue[J]. Pathologe, 1987, 8(3): 138–40. |
| [11] | Kleijnen MF, Shih AH, Zhou P, et al. The hPLIC proteins may provide a link between the ubiquitination machinery and the proteasome[J]. Mol Cell, 2000, 6(2): 409–19. DOI:10.1016/S1097-2765(00)00040-X |
| [12] | Kurlawala Z, Shah PP, Shah C, et al. The STI and UBA Domains of UBQLN1 are Critical Determinants of Substrate Interaction and Proteostasis[J]. Cell Biochem, 2017, [Epub ahead of print]. http://onlinelibrary.wiley.com/doi/10.1002/jcb.25880/full |
| [13] | Lehmann G, Udasin RG, Livneh I, et al. Identification of UBact, a ubiquitin-like protein, along with other homologous components of a conjugation system and the proteasome in different gram-negative bacteria[J]. Biochem Biophys Res Commun, 2017, 483(3): 946–50. DOI:10.1016/j.bbrc.2017.01.037 |
| [14] | Beverly LJ, Lockwood WW, Shah PP, et al. Ubiquitination, localization, and stability of an anti-apoptotic BCL2-like protein, BCL2L10/BCLb, are regulated by Ubiquilin1[J]. Proc Natl Acad Sci U S A, 2012, 109(3): E119–26. DOI:10.1073/pnas.1119167109 |
| [15] | Guidi F, Puglia M, Gabbiani C, et al. 2D-DIGE analysis of ovarian cancer cell responses to cytotoxic gold compounds[J]. Mol Biosyst, 2012, 8(4): 985–93. DOI:10.1039/C1MB05386H |
| [16] | Levine B, Kroemer G. Autophagy in the pathogenesis of disease[J]. Cell, 2008, 132(1): 27–42. DOI:10.1016/j.cell.2007.12.018 |
| [17] | Choi AM, Ryter SW, Levine B. Autophagy in human health and disease[J]. N Engl J Med, 2013, 368(19): 1845–6. DOI:10.1056/NEJMc1303158 |
| [18] | Bristol ML, Di X, Beckman MJ, et al. Dual functions of autophagy in the response of breast tumor cells to radiation: cytoprotective autophagy with radiation alone and cytotoxic autophagy in radiosensitization by vitamin D3[J]. Autophagy, 2012, 8(5): 739–53. DOI:10.4161/auto.19313 |
| [19] | Sun Q, Liu T, Yuan Y, et al. MiR-200c inhibits autophagy and enhances radiosensitivity in breast cancer cells by targeting UBQLN1[J]. Int J Cancer, 2015, 136(5): 1003–12. DOI:10.1002/ijc.29065 |
| [20] | Bai WD, Ye XM, Zhang MY, et al. MiR-200c suppresses TGF-β signaling and counteracts trastuzumab resistance and metastasis by targeting ZNF217 and ZEB1 in breast cancer[J]. Int J Cancer, 2014, 135(6): 1356–68. DOI:10.1002/ijc.v135.6 |
 2017, Vol. 44
2017, Vol. 44


