文章信息
- SPARC在胃癌发生机制中作用的研究进展
- Research Progress on SPARC in Pathogenesis of Gastric Cancer
- 肿瘤防治研究, 2017, 44(10): 694-697
- Cancer Research on Prevention and Treatment, 2017, 44(10): 694-697
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.17.0124
- 收稿日期: 2017-02-09
- 修回日期: 2017-03-25
富含半胱氨酸的酸性分泌蛋白(secreted protein, acidic and rich in cysteine, SPARC),是一种32 kDa细胞外基质糖蛋白,也曾称为骨连接蛋白、43K蛋白或BM-40,最早由美国Termine等人于1981年在人和胎牛骨中分离提纯[1]。起初的认识仅仅限于它是一种能与钙离子结合的非胶原成分。随后的研究逐渐发现,SPARC在人体中广泛分布,尤其是重建组织中,其生物学行为随着环境不同也呈现出不同的特性。人类的SPARC基因位于5q31-33,是一种在进化上高度保守的单拷贝基因,编码由298~304个氨基酸构成的蛋白质。SPARC蛋白主要包括三个结构和功能不同的模块,分别具有抗原决定、抑制内皮细胞增殖和血管形成以及去细胞黏附等功能特性[2]。因此,不同于其他细胞基质蛋白,SPARC的主要功能在于调节细胞和基质之间的相互作用,参与组织修复、血管新生、细胞迁移等多个过程。近年来随着研究深入,人们发现SPARC与多种恶性肿瘤有十分密切的联系。肿瘤类型不同、微环境不同,SPARC在肿瘤形成进程中所起的作用也不尽相同。目前研究较多的恶性肿瘤主要有恶性黑色素瘤、卵巢癌、结肠癌、胰腺癌、前列腺癌等,而在胃癌中的研究仍处于起步阶段[3-4]。现就当前SPARC在胃癌中的研究进展进行综述。
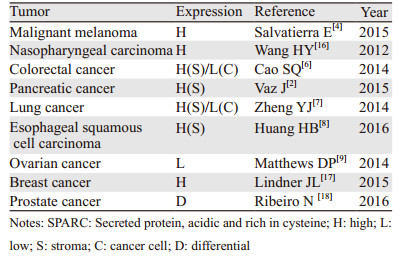
1 SPARC在胃癌中的表达情况目前针对SPARC的检测主要围绕核酸和蛋白水平,方法有反转录聚合酶链式反应(reverse transcription-polymerase chain reaction, RT-PCR)、蛋白免疫印迹法(Western blot)和免疫组织化学法(immunohistochemistry, IHC)等[5]。肿瘤类型不同,SPARC表达情况也不一致。在恶性黑色素瘤中,SPARC随肿瘤的进展而表达增加;结肠癌中,SPARC主要表达于结肠癌组织周围的间质细胞,而在结肠癌细胞中表达较正常组织低;胰腺癌、肺癌及食管鳞癌中同样出现间质过表达而肿瘤低表达的现象;而在卵巢癌中,SPARC出现低表达[4, 6-9]。在胃癌组织和常用的几种胃癌细胞系中,SPARC的表达呈现多样性。
Sato等[10]用RT-PCR的方法检测227名胃癌患者的癌与癌旁组织SPARC mRNA的表达情况,发现癌组织中SPARC表达明显高于癌旁正常组织。Wang等[11]通过对手术切除的80例胃癌以及30例正常癌旁组织IHC检测发现,SPARC高表达于胃癌细胞周围间质中,而癌细胞本身及正常胃黏膜细胞表达较低。SPARC的表达与肿瘤TNM分期以及局部淋巴结转移情况呈负相关;Lauren分型中,肠型胃癌的SPARC表达强于弥漫型胃癌;而性别、年龄、肿瘤大小、分化程度等与SPARC表达无明显相关性[12-13]。在常用的胃癌细胞系中,内源性SPARC mRNA仅在MGC-803和HGC-27两种胃癌细胞系呈现高表达,SGC-7901细胞系表达水平较低,而在NCI-N87、BGC-823、AGS、MKN-45、KATOⅢ、SUN-1以及SUN-16细胞系中均表达缺失,正常胃上皮细胞系GES中可见表达[14-15]。由此可见,胃癌组织中SPARC的表达高于正常胃黏膜组织,且主要表达于胃癌间质细胞;而在大多数胃癌细胞系中,内源性SPARC呈现表达抑制或缺失状态,在蛋白水平上也印证了此结论。癌巢间质细胞的SPARC异常表达在多种恶性肿瘤中均见报道,进一步研究有助于揭示SPARC在肿瘤微环境中的相关作用机制,见表 1。
已有的研究表明,SPARC蛋白在肿瘤进展的多个环节都发挥了一定作用,且存在组织特异性。对胃癌的研究主要集中在以下几个方面。
2.1 SPARC与胃癌细胞增殖SPARC对胃癌细胞的增殖作用目前尚无一致性的结论。Yin等[14]利用siRNA对SPARC高表达的MGC-803和HGC-27两种细胞进行SPARC干扰抑制后,发现相对于对照组,SPARC抑制组的胃癌细胞增殖和存活能力明显下降。随后的裸鼠体内成瘤实验也证实了这一观点[19]。然而,Zhang等[20]对SPARC表达缺失的胃癌细胞系BGC-823进行SPARC cDNA转染后发现,过表达SPARC的BGC细胞相比于对照组生长明显受限;而对HGC-27进行shRNA干扰SPARC后出现细胞增殖能力轻度升高。对于出现的不一致现象,笔者推测可能与细胞系的异质性及转染载体来源、实验条件、技术手段等多种因素相关,未来有待于多细胞系重复以及体内实验进一步验证。
SPARC对胃癌增殖的作用机制目前研究较少。已有的研究发现,血管内皮生长因子(vascular endothelial growth factor, VEGF)可能参与癌细胞增殖的过程。胃癌细胞过表达SPARC后可能干扰VEGF与VEGF受体2(VEGF-2)结合,抑制受体及其下游的ERK1/2激活,细胞周期停滞于G0/G1期,从而减弱癌细胞的增殖能力[11]。一项对前列腺癌的研究显示,在前列腺癌细胞中加入外源性SPARC可以引起整合素β1的增加并使AKT磷酸化水平降低,推测SPARC可能通过此种途径抑制癌细胞的增殖;相反SPARC的缺失能够促进癌细胞的生长[21]。另有对胰腺癌的研究发现,外源性的SPARC可使成纤维细胞生长因子1(fibroblast growth factor-1, FGF-1)介导的增殖作用减弱[22]。SPARC对恶性肿瘤增殖的作用可能是多因素、多通路共同参与的,综合效应网络的构建应是未来研究的新思路。
2.2 SPARC与胃癌侵袭、转移恶性肿瘤的侵袭、转移能力主要与肿瘤本身的增殖活性及肿瘤细胞微环境相关,其中比较重要的一个机制是上皮-间充质细胞转化(epithelial-mesenchymal transition, EMT)。肿瘤增殖能力活跃,肿瘤细胞间黏附作用减弱以及细胞外基质(extracellular matrix, ECM)的降解都是肿瘤发生侵袭和转移的重要环节。研究发现,在SPARC低表达的BGC-823和SGC-7901胃癌细胞系中过表达SPARC后可使癌细胞的侵袭和迁移能力明显降低;此外,在尾静脉注射胃癌细胞的裸鼠肺组织活检发现,SPARC过表达组中肺组织转移细胞数和转移灶数目都明显下降[12]。进一步的机制研究发现,SPARC过表达会引起胃癌细胞MMP-7、MMP-9、N-cadherin、Sp1分子的表达以及ERK1/2的激活受到抑制,这些分子均是EMT过程中的重要因子,表达受到抑制后,肿瘤的侵袭及转移能力也会受限。可见SPARC对胃癌的侵袭、转移可能存在负性调节的作用。
然而,对不同种属、不同组织的研究发现SPARC在侵袭、转移方面的作用有差异。一项对秀丽隐杆线虫(C. elegans)的研究发现,线虫体内过表达SPARC后,侵袭力较弱的锚细胞突破基底膜的能力显著增加,其部分原因是SPARC能够与ECM基底膜的重要组分Ⅳ型胶原结合,干扰其在基底膜的沉积,从而削弱基底膜的屏障功能,且这种功能是相对独立的[23]。而较早的研究也认为,SPARC的表达在多种恶性肿瘤中与MMP及整合素的信号表达成正相关,能够促进基底膜打破,提高恶性细胞的侵袭能力[24-25]。侵袭和转移是细胞自身与微环境相互作用、共同参与的过程,存在多因素之间的相互促进和制衡,SPARC在胃癌中侵袭和转移的作用机制仍需进一步探讨。
2.3 SPARC与肿瘤微血管的形成肿瘤的发生和转移扩散与血管形成关系密切,新生血管为肿瘤提供营养,对肿瘤的生长至关重要。而肿瘤微血管的形成由多种因子共同调控,如VEGF、血小板源性生长因子(platelet derived growth factor, PDGF)、FGF、转化生长因子β(transforming growth factor-β, TGF-β)、基质金属蛋白酶(matrix metalloproteinases, MMP)等。SPARC能够与多种生长因子相互作用,在不同微环境中,SPARC对恶性肿瘤血管形成的作用也不尽相同。PDGF能够促进有丝分裂,引起内皮细胞增殖。SPARC可以特异性地与PDGF结合,抑制其与PDGF受体相互作用或间接干扰PDGF通路,从而阻抑血管内皮细胞增殖。VEGF与PDGF在氨基酸序列上有20%的相似性。SPARC可以和VEGF结合,抑制其对VEGF受体1(VEGFR1)的磷酸化激活作用,从而减弱VEGF对人微血管内皮细胞的促增殖作用。FGF-2作为血管新生过程中的另一重要因子,也受到SPARC蛋白类似的调控,此外,SPARC还可降低FGF受体1(FGFR1)的磷酸化水平。
Zhang等[20]发现,过表达SPARC的胃癌细胞中VEGF和MMP-7水平降低,在体内成瘤实验中发现种植过表达SPARC胃癌细胞的裸鼠相比对照组肿瘤体积较小,肿瘤组织VEGF和MMP-7表达水平降低,微血管密度(microvascular density, MVD)相比对照组下降54.8%,认为SPARC可能通过降调节VEGF和MMP-7抑制血管新生。
2.4 SPARC甲基化与胃癌在肿瘤发展的进程中,原癌基因激活和抑癌基因失活扮演着重要角色。近年来,表观遗传学的改变如甲基化带来的抑癌基因失活问题逐渐受到关注[26-27]。DNA的甲基化主要发生于CpG二核苷酸聚集的CpG岛中。而在人类基因启动子中,约有70%的序列存在CpG岛,启动子在DNA甲基转移酶(DNA methyltransferase, DNMT)的作用下异常甲基化将导致基因沉默,抑癌基因的沉默成为导致肿瘤发生的重要环节[28]。研究发现,胃癌中许多抑癌基因启动子均存在不同程度的甲基化,如hMLM1、CDH1、COX-2、RUNX3、TIMP-3、RASSF以及SOX2等[29]。DNA核心启动子的甲基化能够影响SPARC表达[30]。Chen等[15]对10个常用胃癌细胞系进行检测发现,8个存在SPARC启动子异常甲基化,而其中7个呈现SPARC表达缺失;在经去甲基化试剂5-氮杂-2' -脱氧胞嘧啶核苷处理后,所有的细胞系SPARC都恢复了表达,且在多个细胞系中发现胃癌细胞的增殖、迁移能力都有所下降。在220例胃癌组织中检测发现,甲基化发生率高达74%,而正常胃黏膜组织甲基化发生率仅为5%。SPARC甲基化在胃癌中的发生率较高,而启动子的甲基化导致胃癌细胞中SPARC表达沉默,其功能受到抑制。
此外,甲基化对肿瘤辅助治疗的影响也成为当今学术热点。有研究发现,在结直肠癌中SPARC甲基化可能造成肿瘤对化疗的敏感度降低,影响患者总体生存率[31]。SPARC甲基化的现象为胃癌预后分析以及治疗靶点的选择提供了新的方向。
3 总结与展望SPARC作为一种细胞外基质糖蛋白,能够通过多种途径调节细胞和周围基质之间的相互作用,对多种恶性肿瘤的发生发展进程产生影响,且具有较高的组织特异性。在胃癌中,目前研究发现,SPARC主要表达于癌组织的间质细胞中,癌细胞本身表达较少,可能与SPARC基因启动子甲基化等因素相关。SPARC表达的缺失对胃癌细胞的侵袭、转移、血管新生等多种生物学行为都产生负性调节作用,对增殖方面的影响目前仍存在争议;而胃癌间质细胞中SPARC的异常表达对于肿瘤进程的意义目前仍是未知。未来的研究应着眼于SPARC在微环境中作用机制的进一步探索以及SPARC对胃癌影响的综合效应网络构建,以期为胃癌发生机制的研究及靶向治疗提供新思路。
| [1] | Termine JD, Kleinman HK, Whitson SW, et al. Osteonectin, a bone-specific protein linking mineral to collagen[J]. Cell, 1981, 26(1 Pt 1): 99. |
| [2] | Vaz J, Ansari D, Sasor A, et al. SPARC:A Potential Prognostic and Therapeutic Target in Pancreatic Cancer[J]. Pancreas, 2015, 44(7): 1024–35. DOI:10.1097/MPA.0000000000000409 |
| [3] | Rossi MK, Gnanamony M, Gondi CS. The 'SPARC' of life:Analysis of the role of osteonectin/SPARC in pancreatic cancer (Review)[J]. Int J Oncol, 2016, 48(5): 1765–71. DOI:10.3892/ijo.2016.3417 |
| [4] | Salvatierra E, Alvarez MJ, Leishman CC, et al. SPARC Controls Melanoma Cell Plasticity through Rac1[J]. PLoS One, 2015, 10(8): e0134714. DOI:10.1371/journal.pone.0134714 |
| [5] | Sinn M, Sinn BV, Striefler JK. SPARC expression in resected pancreatic cancer patients treated with gemcitabine:results from the CONKO-001 study[J]. Ann Oncol, 2014, 25(5): 1025–32. DOI:10.1093/annonc/mdu084 |
| [6] | 曹仕琼, 吴杰. 富含半胱氨酸的酸性分泌蛋白在人大肠癌、大肠腺瘤的表达及其临床意义[J]. 临床消化病杂志, 2014, 26(1): 15–8. [ Cao SQ, WU J. Relationship between expression of SPARC and its clinical significance in human colorectal carcinoma and colorectal adenoma[J]. Lin Chuang Xiao Hua Bing Za Zhi, 2014, 26(1): 15–8. ] |
| [7] | 郑英娟, 汤建华, 张志林, 等. 肺癌中SPARC和TGFβ1的表达及意义[J]. 肿瘤防治研究, 2014, 41(6): 596–7. [ Zheng YJ, Tang JH, Zhang ZL, et al. Significance of SPARC and TGFβ1 expression in lung cancer[J]. Zhong Liu Fang Zhi Yan Jiu, 2014, 41(6): 596–7. ] |
| [8] | 黄海波, 刘凯, 赵燕, 等. 酸性富含半胱氨酸分泌型蛋白表达与食管鳞癌术后预后的相关性[J]. 肿瘤防治研究, 2016, 43(1): 35–8. [ Huang HB, Liu K, Zhao Y, et al. Relationship of secreted protein acidic and rich in cysteine protein expression with prognosis of postoperative patients with esophageal squamous cell carcinoma[J]. Zhong Liu Fang Zhi Yan Jiu, 2016, 43(1): 35–8. ] |
| [9] | Matthews DP, Taylor S, Said NA. Epigenetic regulation of SPARC in ovarian cancer[J]. Cancer Res, 2014, 74(19 Suppl): 1364. |
| [10] | Sato T, Oshima T, Yamamoto N, et al. Clinical significance of SPARC gene expression in patients with gastric cancer[J]. J Surg Oncol, 2013, 108(6): 364–8. DOI:10.1002/jso.23425 |
| [11] | Wang L, Yang M, Shan L, et al. The role of SPARC protein expression in the progress of gastric cancer[J]. Pathol Oncol Res, 2012, 18(3): 697–702. DOI:10.1007/s12253-012-9497-9 |
| [12] | Zhang J, Wang P, Zhu J, et al. SPARC expression is negatively correlated with clinicopathological factors of gastric cancer and inhibits malignancy of gastric cancer cells[J]. Oncol Rep, 2014, 31(5): 2312–20. DOI:10.3892/or.2014.3118 |
| [13] | Franke K, Carl-Mcgrath S, Röhl FW, et al. Differential Expression of SPARC in Intestinal-type Gastric Cancer Correlates with Tumor Progression and Nodal Spread[J]. Transl Oncol, 2009, 2(4): 310–20. DOI:10.1593/tlo.09169 |
| [14] | Yin J, Chen G, Liu Y, et al. Downregulation of SPARC expression decreases gastric cancer cellular invasion and survival[J]. J Exp Clin Cancer Res, 2010, 29: 59. DOI:10.1186/1756-9966-29-59 |
| [15] | Chen ZY, Zhang JL, Yao HX, et al. Aberrant methylation of the SPARC gene promoter and its clinical implication in gastric cancer[J]. Sci Rep, 2014, 4: 7035. |
| [16] | Wang HY, Li YY, Shao Q, et al. Secreted protein acidic and rich in cysteine (SPARC) is associated with nasopharyngeal carcinoma metastasis and poor prognosis[J]. J Transl Med, 2012, 10: 27. DOI:10.1186/1479-5876-10-27 |
| [17] | Lindner JL, Loibl S, Denkert C, et al. Expression of secreted protein acidic and rich in cysteine (sparc) in breast cancer and response to neoadjuvant chemotherapy[J]. Ann Oncol, 2015, 26(1): 95–100. DOI:10.1093/annonc/mdu487 |
| [18] | Ribeiro N, Costapinheiro P, Henrique R, et al. Comprehensive Analysis of Secreted Protein, Acidic and Rich in Cysteine in Prostate Carcinogenesis:Development of a 3D Nanostructured Bone-Like Model[J]. J Biomed Nanotechnol, 2016, 12(8): 1–12. |
| [19] | 尹杰, 陈国卫, 刘斯, 等. SPARC对胃癌细胞系HGC27体内侵袭能力及MMP-2表达的影响[J]. 中国医药导刊, 2010, 12(8): 1387–8. [ Yin J, Chen GW, Liu S, et al. The Role of SPARC in the Invasion of Gastric Cancer in Vivo and Its Relationship with Metalloproteinase[J]. Zhongguo Yi Yao Dao Kan, 2010, 12(8): 1387–8. ] |
| [20] | Zhang JL, Chen GW, Liu YC, et al. Secreted protein acidic and rich in cysteine (SPARC) suppresses angiogenesis by down-regulating the expression of VEGF and MMP-7 in gastric cancer[J]. PLoS One, 2012, 7(9): e44618. DOI:10.1371/journal.pone.0044618 |
| [21] | Shin M, Mizokami A, Kim J, et al. Exogenous SPARC suppresses proliferation and migration of prostate cancer by interacting with integrin β1[J]. Prostate, 2013, 73(11): 1159–70. DOI:10.1002/pros.v73.11 |
| [22] | Chen G, Tian X, Liu Z, et al. Inhibition of endogenous SPARC enhances pancreatic cancer cell growth:modulation by FGFR1-Ⅲ isoform expression[J]. Br J Cancer, 2009, 102(1): 188–95. |
| [23] | Morrissey MA, Jayadev R, Miley GR, et al. SPARC Promotes Cell Invasion In Vivo by Decreasing Type IV Collagen Levels in the Basement Membrane[J]. PLoS Genet, 2016, 12(2): e1005905. DOI:10.1371/journal.pgen.1005905 |
| [24] | Mcclung HM, Thomas SL, Osenkowski P, et al. SPARC upregulates MT1-MMP expression, MMP-2 activation, and the secretion and cleavage of galectin-3 in U87MG glioma cells[J]. Neurosci Lett, 2007, 419(2): 172–7. DOI:10.1016/j.neulet.2007.04.037 |
| [25] | Barker TH, Baneyx G, Cardó-Vila M, et al. SPARC Regulates Extracellular Matrix Organization through Its Modulation of Integrin-linked Kinase Activity[J]. J Biol Chem, 2005, 280(43): 36483–93. DOI:10.1074/jbc.M504663200 |
| [26] | Piunti A, Pasini D. Epigenetic factors in cancer development:polycomb group proteins[J]. Future Oncol, 2011, 7(1): 57–75. DOI:10.2217/fon.10.157 |
| [27] | Okugawa Y, Grady WM, Goel A. Epigenetic Alterations in Colorectal Cancer:Emerging Biomarkers[J]. Gastroenterology, 2015, 149(5): 1204. DOI:10.1053/j.gastro.2015.07.011 |
| [28] | Portela A, Esteller M. Epigenetic modifications and human disease[J]. Nat Biotechnol, 2010, 28(10): 1057–68. DOI:10.1038/nbt.1685 |
| [29] | Gigek CO, Chen ES, Calcagno DQ, et al. Epigenetic mechanisms in gastric cancer[J]. Epigenomics, 2012, 4(3): 279–94. DOI:10.2217/epi.12.22 |
| [30] | Torres-Núñez E, Cal L, Suárez-Bregua P, et al. Matricellular Protein SPARC/Osteonectin Expression is Regulated by DNA Methylation in Its Core Promoter Region[J]. Dev Dyn, 2015, 244(5): 693–702. DOI:10.1002/dvdy.v244.5 |
| [31] | Heitzer E, Artl M, Filipits M, et al. Differential survival trends of stage Ⅱ colorectal cancer patients relate to promoter methylation status of PCDH10, SPARC, and UCHL1[J]. Mod Pathol, 2014, 27(6): 906–15. DOI:10.1038/modpathol.2013.204 |
 2017, Vol. 44
2017, Vol. 44