文章信息
- 肺腺癌组织中黑色素瘤相关抗原-As的表达及其临床意义
- Expressions of Melanoma Antigen-As in Lung Adenocarcinoma Tissues and Related Clinical Significance
- 肿瘤防治研究, 2017, 44(8): 530-534
- Cancer Research on Prevention and Treatment, 2017, 44(8): 530-534
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.16.1316
- 收稿日期: 2016-11-22
- 修回日期: 2017-04-28
2. 050011 石家庄,河北医科大学第四医院肿瘤研究所免疫室
2. Department of Immunology, Tumor Research Institute, The Fourth Hospital of Hebei Medical University, Shijiazhuang 050011, China
肺癌是目前世界上病死率最高的恶性肿瘤[1],根据我国最新统计数据显示,肺癌的新发病例和新增死亡病例均居于恶性肿瘤第一位[2]。近年来,通过结合放化疗、手术以及先进的影像诊断技术对肺癌患者进行诊治,并取得了显著进展,但肺癌患者的5年总生存率仍不足20%。因此,个体化药物、生物标志物等逐渐引起人们的重视。
癌/睾丸抗原(cancer/testis antigens, CTA)仅在睾丸的生殖细胞和胎盘的滋养层细胞中表达,而在其他正常人体组织中不表达,在多种肿瘤组织中不同程度的表达,被认为是肿瘤免疫治疗的理想靶点[3]。黑色素瘤相关抗原(Melanoma-associated antigens, MAGE)家族属于分化良好的CTA家族,包含至少55个成员,它们均存在特殊序列-MAGE同源结构域(MAGE homology domain, MHD)。基于其特殊的组织表达模式和基因结构,MAGE家族分为两个亚家族:MAGE-Ⅰ(MAGE-A、MAGE-B和MAGE-C)和MAGE-Ⅱ(MAGE-D)[4]。MAGE-A家族包括12个家族成员,并表达于黑色素瘤、乳腺癌、喉癌、膀胱癌、食管癌以及脑胶质瘤等多种肿瘤组织[5-11]。然而MAGE-A家族在LAC组织中的表达模式尚不清楚。
为了进一步探讨MAGE-A家族在LAC组织中的表达模式及其预后,我们对80例LAC组织及其相应癌旁组织应用MAGE-A(6C1)mAb抗体对MAGE-A1、-A2、-A3、-A4、-A6、-A10和-A12进行检测,并分析MAGE-A表达与临床病理特征以及预后的关系。
1 资料与方法 1.1 研究对象选取河北医科大学第四医院2005年9月—2006年3月住院的LAC患者,手术切除的肺癌组织及距离癌组织边缘5 cm以上的相应癌旁正常组织标本各80例,同时选取该院住院的5例前列腺癌患者术后的正常睾丸组织作为阳性对照。80例LAC患者均为首次发病,且术前未行放、化疗和内分泌治疗。所有组织标本均经病理组织学检查证实。80例肺癌患者中有76例获得完整随访资料,均采用电话回访方式。上述标本的获取均取得受试者或其家属的知情同意,通过医院伦理委员会批准。
80例肺癌标本中,男42例(52.5%),女38例(47.5%);< 60岁41例(51.25%),≥60岁39例(48.75%);按照美国肿瘤联合会(AJCC)2010第7版临床分期标准分为:Ⅰ~Ⅱ期46例(57.5%),Ⅲ~Ⅳ期34例(42.5%)。按照组织学分级分为:Ⅰ级10例(12.5%),Ⅱ级36例(45%),Ⅲ级34例(42.5%);有淋巴结转移的38例(47.5%),无淋巴结转移的42例(52.5%);肿瘤≤3 cm者38例(47.5%),> 3 cm者42例(52.5%)。
1.2 组织芯片制备组织芯片由生物芯片上海国家工程研究中心制备。所有组织蜡块常规病理切片后行HE染色,并在切片上根据典型病理部位作标记。利用组织芯片制作仪在受体蜡块打孔(直径1.5 mm),然后根据标记好的典型病理部位获取相应组织芯片放入受体蜡块阵列孔中,并记录组织编号。利用切片机(Leica公司,德国)以4 μm厚度进行连续切片以制备成组织芯片切片,每个点均再次经过HE染色以进行病理诊断。
1.3 主要试剂SP免疫组织化学染色试剂盒及浓缩型DAB试剂盒购自北京中杉金桥生物技术有限公司,鼠抗人MAGE-A(6C1)单克隆抗体(货号:sc-20034)购自英国Abcam公司,抗原修复液购自基因科技上海有限公司。
1.4 免疫组织化学法检测肺癌组织、癌旁组织及正常睾丸组织中MAGE-As蛋白的表达按SP免疫组织化学试剂盒说明书方法检测MAGE-As蛋白的表达情况。鼠抗人MAGE-As单克隆抗体以1:200稀释,生物素化山羊抗鼠二抗和辣根过氧物酶标记的链酶卵白素(三抗)为试剂盒中的原液,加DAB试剂显色后,用苏木精对比染色,中性树胶封片。以人正常睾丸组织作为阳性对照,以癌旁组织作为阴性对照。
免疫组织化学染色以细胞质内出现棕黄色颗粒为阳性,双盲法观察组织切片全部视野,采用半定量积分法判断结果:首先确定阳性定位,然后按照下述标准进行评分:(1)阳性细胞数≤5%为0分,5%~25%为1分,> 25%~50%为2分,> 50%~75%为3分,> 75%为4分;(2)染色阳性强度分为:无色为0分,淡黄色为1分,黄色为2分,棕黄色为3分。将(1)和(2)两者积分相乘,0分为阴性,> 0分为阳性。
1.5 统计学方法采用SPSS13.0统计软件,计数数据以百分率表示,采用卡方检验或连续校正的卡方检验统计MAGE-As的表达与肺腺癌的临床病理指标间的关系;Kaplan-Meier法对肺腺癌患者是否阳性表达MAGE-As蛋白进行生存分析;Cox回归模型针对阳性表达MAGE-As及相关的临床病理资料进行多因素分析,P < 0.05为差异有统计学意义。
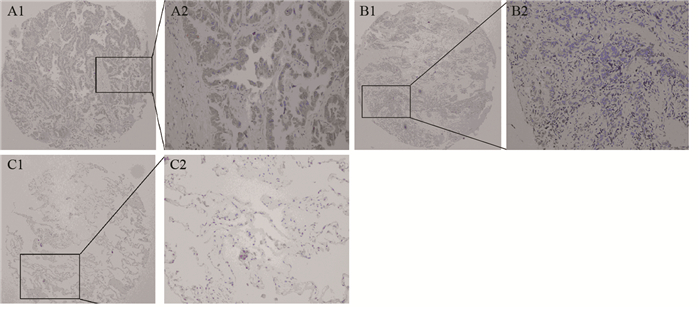
2 结果 2.1 MAGE-As蛋白在肺腺癌组织及相应癌旁组织中的表达免疫组织化学染色结果显示,MAGE-As蛋白在LAC组织中的阳性染色产物主要定位于细胞质,部分定位于细胞核,见图 1。80例癌旁组织未发现MAGE-As蛋白表达,LAC组织MAGE-As蛋白阳性表达率为46.25%(37/80),明显高于癌旁组织(P=0.000)。结果提示,MAGE-As是LAC的肿瘤相关抗原。
|
| A: positive MAGE-As expression in lung adenocarcinoma(LAC) tissues; B: negative MAGE-As expression in lung adenocarcinoma tissues; C: negative MAGE-As expression in human normal alveolar epithelial tissues 图 1 MAGE-As在肺腺癌组织、正常肺泡上皮组织中的表达(SP ×200) Figure 1 MAGE-As expression in human LAC and normal alveolar epithelial tissues (SP ×200) |
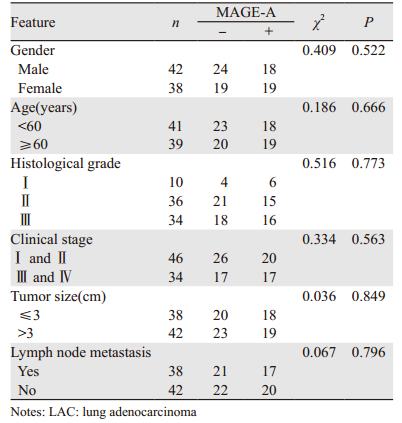
结果显示,MAGE-As蛋白表达与LAC患者的性别、年龄、临床分期、肿瘤大小、淋巴转移和组织学分级均无相关性,见表 1。
 |
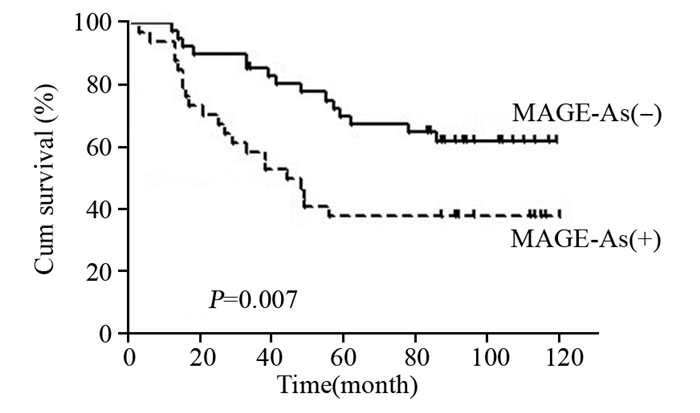
对MAGE-As蛋白表达阳性及阴性的LAC患者生存曲线进行Log rank检验,结果显示,MAGE-As蛋白表达阳性LAC患者的生存期显著低于MAGE-As蛋白表达阴性的患者(χ2=7.204, P=0.007),见图 2。
|
| Overall survival rate in the patients with positive MAGE-As expression (dashed line) was signicantly lower than that with negative MAGE-As expression (solid line) 图 2 肺腺癌患者的总体生存率与MAGE-As表达的关系 Figure 2 Correlation of overall survival with MAGE-As protein expression in LAC patients |
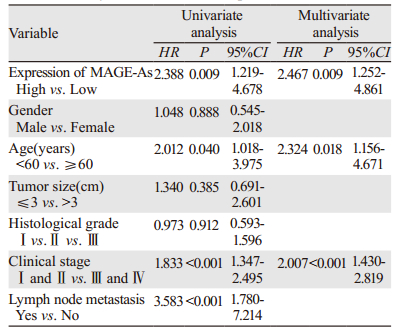
Cox回归模型单因素分析结果显示,仅有MAGE-As蛋白表达(P=0.009)、年龄(P=0.040)、临床分期(P < 0.001)和淋巴结转移(P < 0.001)有统计学意义,由于临床分期和淋巴结转移不是相互独立的两项指标,且临床分期包含淋巴结转移的相关信息,故仅有MAGE-As蛋白表达、年龄和临床分期进入回归模型进一步分析。多因素结果显示,MAGE-As蛋白表达(P=0.009)、年龄(P=0.018)和临床分期(P < 0.001)可作为LAC患者生存的独立预后因素,见表 2。
 |
基于肺癌表达肿瘤特异性抗原及其免疫原性,免疫疗法作为一种新兴的治疗方法应运而生[12]。免疫疗法是一种可以提高癌症患者生存并改善临床预后的理想方法。作为分化良好的CTA家族成员,MAGE-A(特别是MAGE-A3)免疫原已经应用于临床[13-15]。
常有文献报道NSCLC中有部分MAGE-A基因的表达[16-17]。通过多中心研究,MAGE-A3在Ⅰ和Ⅱ期的NSCLC患者中的表达率为39.2%[17]。而MAGE-A4在NSCLC中表达率为48%,在肺鳞状细胞癌的表达率为90%[18]。由于MAGE-A家族中存在高度保守序列MHD,很难制备抗体对其家族成员进行特异性检测,阻碍了研究组织中MAGE-A的表达情况。因此,大多数研究应用RT-PCR检测MAGE-A基因表达[17, 19-20]。最近有文献报道,MAGE-A9在不同组织学类型肺癌中均高表达[19-20]。然而,MAGE-A的12个家族成员在LAC组织中的表达情况仍不清楚。
为了评估MAGE-A家族成员是否可作为免疫治疗的特殊靶点,本研究对LAC组织中MAGE-A的表达模式进行分析。由于MAGE-A(6C1)单克隆抗体可以同时检测多个MAGE-A家族成员,包括MAGE-A1、-A2、-A3、-A4、-A6、-A10和-A12,本研究利用MAGE-A(6C1)单克隆抗体,采用免疫组织化学法检测MAGE-A家族的大多数成员,大大增加了LAC组织中MAGE-A家族的检出率,明显优于单个抗体。本研究结果显示MAGE-A蛋白在46.25%的肺癌组织中表达。然而,本研究并未发现MAGE-A表达与LAC患者的临床病理特征之间的关系。Kaplan-Meier曲线分析表明,MAGE-As蛋白表达阳性LAC患者的生存率显著低于MAGE-As蛋白表达阴性的患者。多因素分析进一步提示MAGE-As蛋白表达、年龄和临床分期可作为患者10年生存的独立危险因素。这些结果均与MAGE-A9在肺癌中的最新研究相一致[20-21]。
虽然MAGE-A蛋白的生物学功能仍未知,早期研究表明,去甲基化剂5-氮-脱氧胞苷刺激细胞后可诱导MAGE-A1的转录,猜测其他MAGE基因可能由类似机制调控[22]。DNA甲基化和组蛋白乙酰化可能导致了MAGE-A9基因的沉默[6]。越来越多的证据表明MAGE基因参与了肺癌的早期肿瘤形成以及调控细胞增殖和侵袭[23]。MAGE-A3蛋白的表达可能与表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor, EGFR-TKIs)靶向治疗NSCLC患者耐药相关,而且表达率越高,越易在较短的时间内获得耐药[24]。因此推测,MAGE-A表达有助于肿瘤细胞存活。以上基因的功能可能揭示了肺癌和肿瘤生长之间的关系,MAGE-A可作为抗肿瘤治疗的靶点。
本文利用组织芯片研究肺腺癌中蛋白的表达,组织芯片中的众多组织均采用统一的选材标准、相同的实验操作,因此较传统病理切片的实验误差小,提高了实验的准确性和可信性。本研究提示MAGE-A蛋白家族表达可能是LAC患者预后较差的指标以及可能作为肺癌免疫治疗的理想抗原。由于MAGE-A可能作为抗肿瘤治疗的靶点,因此可以考虑构建针对MAGE-A基因同源序列的复合抗原疫苗,为今后肿瘤的免疫治疗提供理论基础。免疫疫苗的构建以MAGE-A(6C1)抗体为前期实验基础,可能增加了疫苗的有效率,使更多的患者获益。
| [1] | Siegel RL, Miller KD, Jemal A. Cancer statistics, 2015[J]. CA Cancer J Ciln, 2015, 65(1): 5–29. DOI:10.3322/caac.21254 |
| [2] | Chen W, Zheng R, Baade PD, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115–32. DOI:10.3322/caac.21338 |
| [3] | Salmaninejad A, Zamani MR, Pourvahedi M, et al. Cancer/Testis antigens: expression, regulation, tumor invasion and use in immunotherapy of cancers[J]. Immuol Invest, 2016, 45(7): 619–40. DOI:10.1080/08820139.2016.1197241 |
| [4] | Van der Bruggen P, Traversari C, Chomez P, et al. A gene encoding an antigen recognized by cytolytic T lymphocytes on a human melanoma[J]. Science, 1991, 254(5038): 1643–7. DOI:10.1126/science.1840703 |
| [5] | Wang D, Wang J, Ding N, et al. MAGE-A1 promotes melanoma proliferation and migration through C-JUN activation[J]. Biochem Biophys Res Commun, 2016, 473(4): 959–65. DOI:10.1016/j.bbrc.2016.03.161 |
| [6] | Hou SY, Sang MX, Geng CZ, et al. Expressions of MAGE-A9 and MAGE-A11 in breast cancer and their expression mechanism[J]. Arch Med Res, 2014, 45(1): 44–51. DOI:10.1016/j.arcmed.2013.10.005 |
| [7] | Liu SH, Sang M, Xu Y, et al. Expression of MAGE-A1, -A9, -A11 in laryngeal squamous cell carcinoma and their prognostic significance: a retrospective clinical study[J]. Acta Otolaryngol, 2016, 136(5): 506–13. DOI:10.3109/00016489.2015.1126856 |
| [8] | Mengus C, Schultz-Thater E, Coulot J, et al. MAGE-A10 cancer/testis antigen is highly expressed in high-grade non-muscle-invasive bladder carcinomas[J]. Int J Cancer, 2013, 132(10): 2459–63. DOI:10.1002/ijc.27914 |
| [9] | 谷丽娜, 桑梅香, 刘飞, 等. 黑素瘤相关抗原-A9和-A11在食管鳞状细胞癌组织中的表达及其临床意义[J]. 中国肿瘤生物治疗杂志, 2015, 22(5): 630–6. [ Gu LN, Sang MX, Liu F, et al. expression and clinical significance of melanoma antigen-a9 and a11 in esophageal squamous cell caricinoma tissues[J]. Zhongguo Zhong Liu Sheng Wu Zhi Liao Za Zhi, 2015, 22(5): 630–6. DOI:10.3872/j.issn.1007-385X.2015.05.014 ] |
| [10] | Guo L, Sang M, Liu Q, et al. The expression and clinical significance of melanoma-associated antigen-A1, -A3 and -A11 in glioma[J]. Oncol Lett, 2013, 6(1): 55–62. |
| [11] | 刘维华, 桑梅香, 单保恩. 黑色素瘤相关抗原-A:食管癌免疫治疗新靶点[J]. 肿瘤防治研究, 2015, 42(6): 622–6. [ Liu WH, Sang MX, Shan BE. MAGE-A: New Target of Immunotherapy for Esophageal Cancer[J]. Zhong Liu Fang Zhi Yan Jiu, 2015, 42(6): 622–6. ] |
| [12] | Brahmer JR. Harnessing the immune system for the treatment of non-small-cell-lung cancer[J]. J Clin Oncol, 2013, 31(8): 1021–8. DOI:10.1200/JCO.2012.45.8703 |
| [13] | Pujol JL, Vansteenkiste JF, De Pas TM, et al. Safety and Immunogenicity of MAGE-A3 Cancer Immunotherapeutic with or without Adjuvant Chemotherapy in Patients with Resected Stage ⅠB to Ⅲ MAGE-A3-Positive Non-Small-Cell Lung Cancer[J]. J Thorac Oncol, 2015, 10(10): 1458–67. DOI:10.1097/JTO.0000000000000653 |
| [14] | Vansteenkiste J, Zielinski M, Linder A, et al. Adjuvant MAGE-A3 immunotherapy in resected non-small-cell lung cancer: phaseⅡ randomized study results[J]. J Clin Oncol, 2013, 31(1): 2396–403. |
| [15] | Karimi S, Mohammadi F, Porabdollah M, et al. Characterization of melanoma-associated antigen-a genes family differential expression in non-small-cell lung cancers[J]. Clin Lung Cancer, 2012, 13(3): 214–9. DOI:10.1016/j.cllc.2011.09.007 |
| [16] | Vansteenkiste JF, Cho BC, Vanakesa T, et al. Efficacy of the MAGE-A3 cancer immunotherapeutic as adjuvant therapy in patients with resected MAGE-A3-positive non-small-cell lung cancer (MAGRIT): a randomised, double-blind, placebo-controlled, phase 3 trial[J]. Lancet Oncol, 2016, 17(6): 822–35. DOI:10.1016/S1470-2045(16)00099-1 |
| [17] | Sienel W, Varwerk C, Linder A, et al. Melanoma associated antigen (MAGE)-A3 expression in Stages Ⅰ and Ⅱ non-small cell lung cancer: results of a multi-center study[J]. Eur J Cardiothorac Surg, 2004, 25(1): 131–4. DOI:10.1016/j.ejcts.2003.09.015 |
| [18] | Peikert T, Specks U, Farver C, et al. Melanoma antigen A4 is expressed in non-small cell lung cancers and promotes apoptosis[J]. Cancer Res, 2006, 66(9): 4693–700. DOI:10.1158/0008-5472.CAN-05-3327 |
| [19] | Karimi S, Mohammadi F, Porabdollah M, et al. Characterization of melanoma-associated antigen-a genes family differential expression in non-small-cell lung cancers[J]. Clin Lung Cancer, 2012, 13(3): 214–9. DOI:10.1016/j.cllc.2011.09.007 |
| [20] | Zhang S, Zhai X, Wang G, et al. High expression of MAGE-A9 in tumor and stromal cells of non-small cell lung cancer was correlated with patient poor survival[J]. Int J Clin Exp Pathol, 2015, 8(1): 541–50. |
| [21] | Zhai X, Xu L, Zhang S, et al. High expression levels of MAGE-A9 are correlated with unfavorable survival in lung adenocarcinoma[J]. Oncotarget, 2016, 7(4): 4871–81. DOI:10.18632/oncotarget.v7i4 |
| [22] | Adair SJ, Hogan KT. Treatment of ovarian cancer cell lines with 5-aza-2'-deoxycytidine upregulates the expression of cancer-testis antigens and class Ⅰ major histocompatibility complex-encoded molecules[J]. Cancer Immunol Immunother, 2009, 58(4): 589–601. DOI:10.1007/s00262-008-0582-6 |
| [23] | Liu XL, Sun N, Dong YN, et al. Anticancer effects of adenovirus-mediated calreticulin and melanoma-associated antigen 3 expression on non-small cell lung cancer cells[J]. Int Immunopharmacol, 2015, 25(2): 416–24. DOI:10.1016/j.intimp.2015.02.017 |
| [24] | Jin J, Liu BZ, Wu ZM. Evaluation of melanoma antigen gene A3 expression in drug resistance of epidermal growth factor receptor-tyrosine kinase inhibitors in advanced non-small cell lung cancer treatment[J]. J Cancer Res Ther, 2015, 11(8): 271–4. DOI:10.4103/0973-1482.170549 |
 2017, Vol. 44
2017, Vol. 44


