文章信息
- 肝细胞肝癌间质微环境与TLR3表达的相关性及其对预后的影响
- Correlation Between Stromal Microenvironment and TLR3 Expression, Prognosis Respectively in Hepatocellular Carcinoma
- 肿瘤防治研究, 2017, 44(4): 262-267
- Cancer Research on Prevention and Treatment, 2017, 44(4): 262-267
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.04.005
- 收稿日期: 2016-07-18
- 修回日期: 2016-09-12
2. 226001 南通,南通大学医学院病理解剖学系
2. Department of Pathological Anatomy, Medical School of Nantong University, Nantong 226001, China
据世界卫生组织统计,原发性肝细胞肝癌(hepatocellular carcinoma, HCC)在世界范围内发病率列第7位、死亡率列第4位[1],在中国分列第3、第2位[1]。HCC间质微环境是一个非常庞杂的体系,包括结缔组织、免疫细胞、细胞因子及血管微环境等,是HCC局部的间质内环境,贯穿于HCC发生发展的全过程。有研究表明[2],间质微环境在HCC的演进过程中起着至关重要的作用。Toll样受体3(Toll-like receptor 3, TLR3)为TLRs家族的重要成员。最近关于HCC的研究中对通过激活TLR3信号通路引起细胞凋亡和(或)使细胞毒性T细胞趋向HCC肿瘤床以发挥其杀伤作用[3-4]已达成共识。本研究通过免疫组织化学染色技术检测102例HCC间质中平滑肌肌动蛋白(α-SMA)表达的癌相关肌纤维母细胞、免疫活性细胞(CD3表达的T细胞、CD68表达的Kupffer细胞、CD56表达的自然杀伤NK细胞、CD21表达的树突状细胞DCs、CD117表达的肥大细胞)和CD34标记的血管内皮细胞,以及HCC细胞中TLR3表达,分析HCC中间质微环境与TLR3表达的相关性及其对预后的影响,探讨间质微环境在HCC演进过程中的重要作用。
1 资料与方法 1.1 患者资料由南通大学附属医院、南通市肿瘤医院和南通市第三人民医院共同提供的2003年1月1日至2004年12月31日118例手术切除的HCC石蜡标本。所有研究病例均具有完整的临床病理资料,术前均未行放化疗。出院后对118位患者每月采用信件、电话两种方式进行一次随访,随访率100%,其中收到完整回访信69例、完整电话随访93例、二者均成功者60例,总计随访成功102例,随访成功率86.4%(102/118),随访时间≥60月。结果显示102例HCC中,生存时间 < 5年65例,≥5年37例。男84例,女18例; < 50岁52例,≥50岁50例;乙型肝炎表面抗原(HBsAg)(-)71例、(+)31例。
1.2 组织芯片制作及免疫组织化学染色人体HCC组织芯片的制备利用已有专利技术[5]。免疫组织化学染色采用SP法,用已知的阳性切片作阳性对照,PBS代替一抗作阴性对照。结果判断:参考Hercept Test[6]的标准进行评分(阳性为相应部位显棕黄色颗粒,结构清晰及显色强于背景,不显色或与背景无差别显色者为阴性)。每例切片至少由两名有经验的病理医师随机镜检观察至少5个高倍镜(10×40)视野,计数每个视野中阳性细胞的百分率。根据Weidner[7]方法:任何一个呈CD34阳性的单个内皮细胞和(或)内皮细胞簇都可直接作为一个单位来计数,而凡是直径比8个红细胞平均直径大的管腔和(或)管腔具有较厚平滑肌的一定不可予以计算在内。于100倍镜下选取微血管最密集的3个视野计数微血管数目,即为微血管密度(microvessel density, MVD)值。
1.3 统计学方法采用SPSS19.0统计软件。卡方检验分析各指标,免疫组织化学检测百分率结果,运用Spearman等级相关分析有关指标间的互相关系。用Log rank检验行单因素分析具随访结果的病例且作出生存曲线(Kaplan-Meier)。P < 0.05为差异有统计学意义。
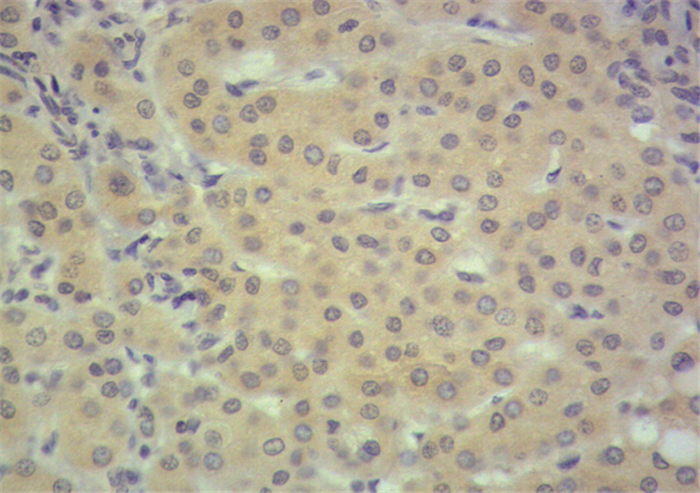
2 结果 2.1 HCC中TLR3的表达免疫组织化学结果显示TLR3主要表达于肿瘤细胞胞膜或胞质,见图 1。
|
| The positive expression of Toll-like receptor 3 (TLR3) located in the cytoplasm and was shown as brown particles 图 1 肝细胞肝癌中TLR3的阳性表达 (SP×400) Figure 1 Positive expression of TLR3 in hepatocellular carcinoma tissues (SP×400) |
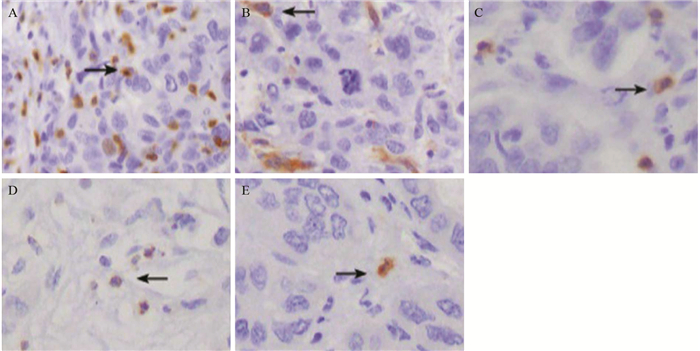
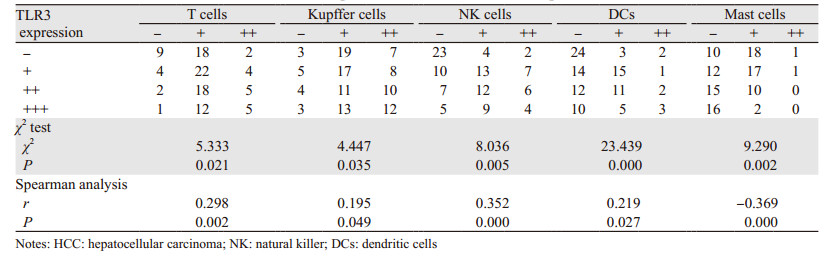
本组HCC间质中CD3、CD68、CD56、CD21和CD117表达见图 2。本组HCC中T细胞、Kupffer细胞、NK细胞和DCs与TLR3表达呈正相关;肥大细胞与TLR3表达呈负相关,见表 1。
|
| A: T cells with positive CD3 expression; B: Kupffer cells with positive CD68 expression; C: natural killer cells with positive CD56 expression; D: dendritic cells with positive CD21 expression; E: mast cells with positive CD117 expression; the positive expression all located in the cytoplasm 图 2 HCC中免疫活性细胞反应 (SP×400) Figure 2 Immunocompetent cell reaction in HCC tissues (SP×400) |
|
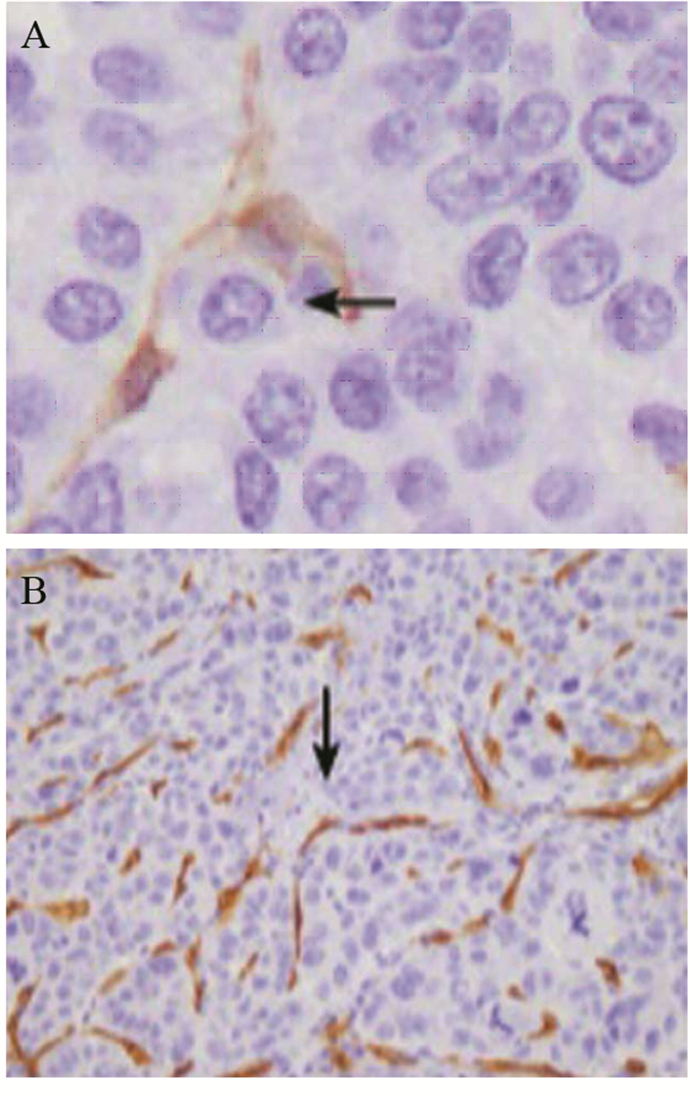
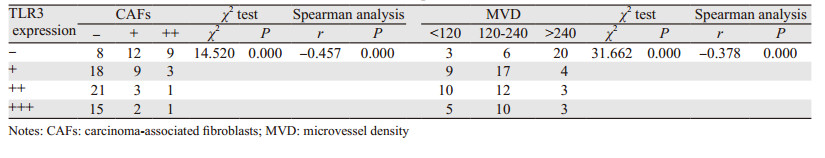
HCC间质中CAFs表达见图 3。α-SMA阳性的CAFs与TLR3表达呈负相关,见表 2。
|
| A: the positive expression of α-SMA located in the cytoplasm; B: the positive expression of CD34 located in the cytomembrane or cytoplasm 图 3 HCC中α-SMA阳性表达的癌相关肌纤维母细胞与CD34阳性表达的血管内皮细胞 (SP×400) Figure 3 Carcinoma-associated fibroblasts (CAFs) with positive α-SMA expression and vascular endothelial cells with positive CD34 expression in HCC (SP×400) |
|
CD34表达于HCC间质微血管内皮细胞膜或细胞质中,见图 3。HCC中MVD与TLR3表达差异有统计学意义(χ2=31.662, P < 0.01),并且呈显著负相关(r=-0.378, P < 0.01),见表 2。
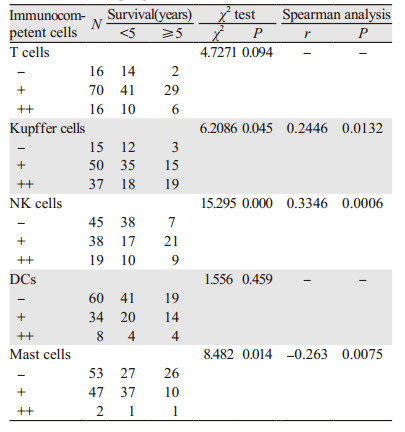
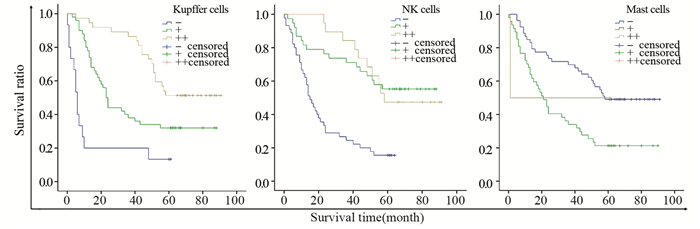
2.3 HCC间质微环境反应与预后的相关性 2.3.1 HCC间质免疫活性细胞反应与预后的相关性HCC中CD68阳性的Kupffer细胞反应和CD56阳性的NK细胞反应与预后呈正相关;CD117阳性的肥大细胞反应与预后呈负相关。Kaplan-Meier生存曲线结果显示CD68阳性的Kupffer细胞越多预后越好(P < 0.01);CD56阳性的NK细胞越多预后越好(P < 0.01);CD117阳性的肥大细胞越多预后越差(P < 0.01), 见表 3、图 4。
|
|
| 图 4 HCC伴Kupffer细胞、NK细胞和肥大细胞反应的生存率曲线 Figure 4 Kaplan-Meier survival curves of HCC patients with Kupffer cells, NK cells and Mast cells reaction |
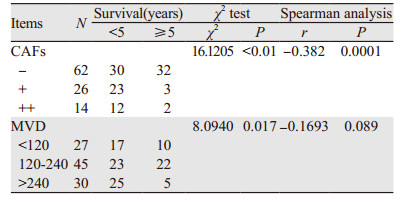
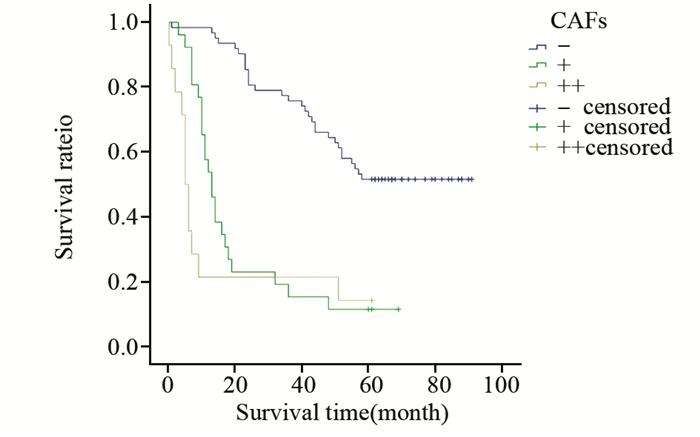
HCC中α-SMA阳性的CAFs与预后呈负相关,见表 4、图 5。
|
|
| 图 5 HCC中CAFs反应的生存率曲线 (P < 0.05) Figure 5 Kaplan-Meier survival curves of HCC patients with CAFs reaction (P < 0.05) |
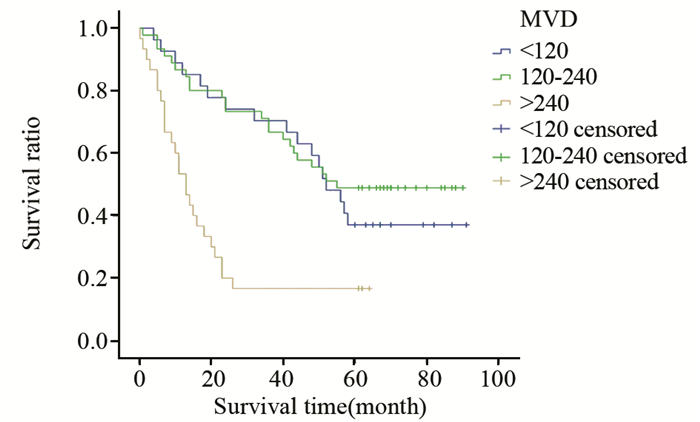
本组HCC生存≥5年者间质MVD较 < 5年者显著减少(χ2=8.0940, P < 0.05),且与预后呈负相关趋势,但差异无统计学意义(r=-0.1693, P > 0.05),见表 4、图 6。
|
| 图 6 HCC中MVD相关的生存率曲线 (P < 0.05) Figure 6 Kaplan-meier survival curves of HCC patients with MVD (P < 0.05) |
HCC微环境包括HCC细胞和间叶细胞及它们的表达产物、代谢物质等。HCC间质指的是上述除HCC细胞以外的所有成分。
HCC微环境中间质对HCC细胞的影响是一把双刃剑,对HCC的发展表现为或促进或抑制的作用,反之HCC细胞也可导致间质发生改变。对于HCC微环境的研究表明HCC间质是上皮细胞-间充质转化(epithelial mesenchymal transition, EMT)乃至HCC复发转移所必需[2]。HCC微环境的基质细胞主要有免疫细胞、CAFs和血管生成细胞3个部分组成。
已知TLRs对先天性免疫和获得性免疫能同时进行调节[8]。各种免疫细胞均能表达TLRs,甚至非免疫细胞也有TLRs的表达[9]。TLR3隶属于TLRs家族,哺乳动物细胞表面[10]及细胞内囊泡[3]均可见其表达。人类TLR3基因含有5个外显子,定位于4q35。
本研究检测到73例TLR3阳性表达于HCC细胞(总病例为102例),阳性率71.57%,比报道的略高[11],可能的原因一是本组病例Edmondson’s分级Ⅰ~Ⅱ级比例较高,二是本地区HCC常为慢性乙型肝炎后肝癌,乙肝病毒(hepatitis B virus, HBV)双链可使TLR3激活引起其表达增加等。
间质微环境中的免疫杀伤细胞负向调节着肿瘤的发生发展,其中最具代表性的为杀伤性T细胞,其次为NK细胞。在机体免疫系统对抗肿瘤的作用中,T细胞是排头兵,机体抗肿瘤反应的强度在一定程度上可从其数量和功能上反映出来。Faraji等研究显示肿瘤细胞表面表达的cadml能够抑制肿瘤细胞肺转移,并且对于肺转移的抑制作用依赖于CD8+T细胞的功能[12]。Bidwell等研究显示CD8+T细胞在乳腺癌转移特异性的免疫监视机制中发挥重要作用,肿瘤细胞中W7的表达能够抑制干扰素(interferon, IFN)介导的骨转移,去除CD8+T细胞和NK细胞能够使骨转移恢复,并缩短无转移生存时间[13]。巨噬细胞如浸润于肿瘤间质微环境中称为肿瘤相关巨噬细胞(tumor associated macrophages, TAM),Kupffer细胞即HCC中的TAM,对癌细胞起直接杀伤作用。TAM主要表现为促炎表型,还可以通过调节其他免疫细胞(由其分泌的细胞因子或细胞趋化因子介导)[14-16]来发挥其抗肿瘤活性。DCs是肿瘤间质微环境中的抗原提呈细胞(Antigen presenting cells, APCs),其功能是为T细胞、NK细胞和TAM提呈抗原,间接调节肿瘤局部的免疫反应[17]。
本研究观察到HCC间质微环境中T细胞、NK细胞、Kupffer细胞和DCs与TLR3表达呈正相关,并且肿瘤局部Kupffer细胞和NK细胞反应与患者预后呈正相关,而已知TLR3表达对HCC起免疫正调节作用,提示T细胞、NK细胞、Kupffer细胞和DCs能促进HCC局部抗肿瘤的免疫反应。本研究中T细胞反应与患者预后未呈相关性,可能系由间质中Kupffer细胞活性较强,消化了部分T细胞释放出的CD3所致;而DCs正是主要通过为T细胞提呈抗原发挥作用,所以本研究中DCs反应与患者预后亦未呈相关性。
肥大细胞可能通过以下几种途径促进肿瘤发展:(1)对正常信号通路的扰乱;(2)促进肿瘤性血管生成;(3)诱发免疫抑制状态;(4)分泌释放促肿瘤的生长因子[18]。本组HCC中肥大细胞反应与TLR3表达呈负相关,表明肥大细胞与TLR3对HCC的作用具有拮抗性,因此提示肥大细胞对HCC起免疫负调节作用,同时也印证了本研究中肥大细胞反应与患者预后呈负相关的结果。
正常组织中的成纤维细胞不活跃,而HCC间质微环境中的成纤维细胞(即类似CAFs,表达α-SMA)相对较活跃,分泌大量基质且能促进基质沉积形成HCC硬化背景[19],构成整个HCC微环境的中心骨架。本研究观察到HCC中α-SMA阳性的CAFs与TLR3表达呈负相关,证明TLR3能抑制HCC间质的纤维化,其可能的途径有:HCC间质微环境中免疫活性细胞的抗病毒免疫反应;使CAFs功能受抑以减少基质分泌和(或)减缓沉积速度。本组HCC中CAFs与预后呈负相关,证明CAFs能促进肿瘤细胞的生长与转移[20-21],同时也表明HCC间质微环境中的CAFs可以被HCC细胞TLR3表达的信号分子通过旁分泌抑制其表达α-SMA,减少HCC硬化背景、脉管浸润,提高HCC患者生存。
HCC不同于其他上皮性恶性肿瘤的是其间质富于血管,所以其主要转移途径并非淋巴道而是血道。研究显示门静脉内微瘤栓形成是HCC主要的转移形式[22],因此血管(尤其是门静脉)是HCC浸润、扩散和转移的高速通道。GUO等[23]研究表明21-核苷酸或更长的dsRNA通过激活HCC细胞中TLR3而非RNAi机制发挥抗血管生成作用。本研究发现HCC中MVD与TLR3表达呈负相关,而且与患者预后呈负相关,表明MVD与TLR3对HCC的作用相拮抗,同时两者之间又相互影响,相互制约。
提高对HCC微环境的认识,可以更好地了解HCC的发生机制,揭示HCC的发展规律,有利于开发全新有效的抗肿瘤治疗。不久的将来,多种以HCC微环境为靶点的治疗手段将不断出现,如重构HCC血管微环境的“饥饿疗法”、干扰HCC免疫微环境的“扶正祛邪疗法”等,这些措施将提高抗HCC的疗效,成为目前HCC治疗的有益补充。
| [1] | Ferlay J, Soerjomataram I, Dikshit R, et al. Cancer incidence and mortality worldwide: Sources, methods and major patterns in GLOBOCAN 2012[J]. Int J Cancer, 2015, 136(5): E359–86. DOI:10.1002/ijc.29210 |
| [2] | Leonardi GC, Candido S, Cervello M, et al. The tumor microenvironment in hepatocellular carcinoma (review)[J]. Int J Oncol, 2012, 40(6): 1733–47. |
| [3] | Li K, Chen Z, Kato N, et al. Distinct poly (I-C) and virus-activated signaling pathways leading to interferon-beta production in hepatocytes[J]. J Biol Chem, 2005, 280(17): 16739–47. DOI:10.1074/jbc.M414139200 |
| [4] | Salaun B, Coste I, Rissoan MC, et al. TLR3 can directly trigger apoptosis in human cancer cells[J]. J Immunol, 2006, 176(8): 4894–901. DOI:10.4049/jimmunol.176.8.4894 |
| [5] | 鄂群, 陈莉, 金国华. 石蜡组织芯片制备方法: 中国, CN101319971B[P]. 2010-12-01. [ E Q, Chen L, Jin GH. A method for preparing paraffin tissue chip: China, CN101319971B[P]. 2010-12-01. ] |
| [6] | 王秀玲, 益莉娜, 徐杭佩, 等. Hercept test试剂在乳腺癌中的表达及判断标准[J]. 临床与实验病理学杂志, 2004, 20(2): 251–2. [ Wang XL, Yi LN, Xu HP, et al. Expression and judgment standard of Hercept test regent in breast cancer[J]. Lin Chuang Yu Shi Yan Bing Li Xue Za Zhi, 2004, 20(2): 251–2. ] |
| [7] | Weidner N. Intratumor microvessel density as a prognostic factor in cancer[J]. Am J Pathol, 1995, 147(1): 9–19. |
| [8] | Lee SO, Brown RA, Razonable RR, et al. Association between a functional polymorphism in Toll-like receptor 3 and chronic hepatitis C in liver transplant recipients[J]. Transpl Infect Dis, 2013, 15(2): 111–9. DOI:10.1111/tid.2013.15.issue-2 |
| [9] | CHEN L, Xu YY, Zhou JM, et al. TLR3 dsRNA agonist inhibits growth and invasion of HepG2.2.15 HCC cells[J]. Oncol Rep, 2012, 28(1): 200–6. |
| [10] | Falco A, Miest JJ, Pionnier N, et al. β-Glucan-supplemented diets increase poly (I:C)-induced gene expression of Mx, possibly via Tlr3-mediated recognition mechanism in common carp (Cyprinus carpio)[J]. Fish Shellfish Immunol, 2014, 36(2): 494–502. DOI:10.1016/j.fsi.2013.12.005 |
| [11] | Yuan MM, Xu YY, Chen L, et al. TLR3 expression correlates with apoptosis, proliferation and angiogenesis in hepatocellular carcinoma and predicts prognosis[J]. BMC Cancer, 2015, 15(1): 245. DOI:10.1186/s12885-015-1262-5 |
| [12] | Faraji Farhoud, Pang Yanli, Walker Renard C, et al. Cadm1 Is a Metastasis Susceptibility Gene That Suppresses Metastasis by Modifying Tumor Interaction with the Cell-Mediated Immunity[J]. PLoS Genet, 2012, 8(9): e1002926. DOI:10.1371/journal.pgen.1002926 |
| [13] | Bidwell BN, Slaney CY, Withana NP, et al. Silencing of Irf7 pathways in breast cancer cells promotes bone metastasis through immune escape[J]. Nat Med, 2012, 18(8): 1224–31. DOI:10.1038/nm.2830 |
| [14] | Waidmann O, Koberle V, Bettinger D, et al. Diagnostic and prognostic significance of cell death and macrophage activation markers in patients with hepatocellular carcinoma[J]. J Hepatol, 2013, 59(4): 769–79. DOI:10.1016/j.jhep.2013.06.008 |
| [15] | Capece D, Fischietti M, Verzella D, et al. The inflammatory microenvironment in hepatocellular carcinoma: a pivotal role for tumor-associated macrophages[J]. Biomed Res Int, 2013, 2013: 187204. |
| [16] | Zhuang PY, Shen J, Zhu XD, et al. Direct transformation of lung microenvironment by interferon-alpha treatment counteracts growth of lung metastasis of hepatocellular carcinoma[J]. PLoS One, 2013, 8(3): e58913. DOI:10.1371/journal.pone.0058913 |
| [17] | Pulko V, Liu X, Krco CJ, et al. TLR3-stimulated dendritic cells up-regulate B7-H1 expression and influence the magnitude of CD8 T cell responses to tumorvaccination[J]. J Immunol, 2009, 183(6): 3634–41. DOI:10.4049/jimmunol.0900974 |
| [18] | Conti P, Castellani ML, Kempuraj D, et al. Role of mast cells in tumor growth[J]. Ann Clin Lab Sci, 2007, 37(4): 315–21. |
| [19] | Östman A. Cancer-associated fibroblasts: recent developments and emerging challenges[J]. Semin Cancer Biol, 2014, 25: 1–2. |
| [20] | Augsten M. Cancer-associated fibroblasts as another polarized cell type of the tumor microenvironment[J]. Front Oncol, 2014, 4: 62. |
| [21] | Chu TY, Yang JT, Huang TH, et al. Crosstalk with cancer-associated fibroblasts increases the growth and radiation survival of cervical cancer cells[J]. Radiat Res, 2014, 181(5): 540–7. DOI:10.1667/RR13583.1 |
| [22] | 程树群, 李楠, 吴孟超. 门静脉癌栓分型与治疗选择[J]. 中国普外基础与临床杂志, 2012, 19(3): 240–2. [ Cheng SQ, Li N, Wu MC. Treatment Choice on Hepatocellular Carcinoma with Different Types of Portal Vein Tumor Thrombus[J]. Zhongguo Pu Wai Ji Chu Yu Lin Chuang Za Zhi, 2012, 19(3): 240–2. ] |
| [23] | Guo ZY, Chen L, Zhu YY, et al. Double-stranded RNA-induced TLR3 activation inhibits angiogenesis and triggers apoptosis of human hepatocellular carcinoma cells[J]. Oncol Rep, 2012, 27(2): 396–402. |
 2017, Vol. 44
2017, Vol. 44
