文章信息
- 鼻咽癌调强放疗中腮腺平均吸收剂量预测模型研究
- Prediction Model of Parotid Mean Dose in Intensity Modulated Radiation Therapy on Nasopharyngeal Carcinoma
- 肿瘤防治研究, 2017, 44(4): 253-256
- Cancer Research on Prevention and Treatment, 2017, 44(4): 253-256
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.04.003
- 收稿日期: 2016-08-29
- 修回日期: 2016-12-01
大量文献报道显示调强放疗(intensity modulated radiationtherapy, IMRT)技术不仅提高了鼻咽癌患者的疗效,而且有效地改善了鼻咽癌患者治疗后的生活质量[1-7]。使靶区剂量尽量高,危及器官剂量尽量低,是放疗的最根本原则。但实际调强优化过程中,受优化方法、手段以及人为等因素影响,大多数放疗中心虽然危及器官控制在限定范围内,但由于缺少有效的预测与评估手段,危及器官的最终吸收剂量更多地依赖于各放疗单位医师的经验。危及器官与靶区之间有着较为复杂的关系,因此也会导致不同患者间危及器官受量有所不同,较早研究表明,危及器官受量和其与靶区之间的几何结构有相关性[8-10]。由于鼻咽癌患者腮腺与靶区位置毗邻,体积因人而异,分期的不同也会导致其吸收剂量的较大变化,本研究选取了鼻咽癌患者腮腺进行独立研究,以探索鼻咽癌调强放疗计划中腮腺体积与其Dmean和D50%之间的数学模型为例,寻求在不损失靶区处方剂量的同时,通过上述数学模型提前预测危及器官的吸收剂量。在不损失靶区剂量的前提下对其调强治疗计划进行前瞻性优化分析,寻找腮腺体积与Dmean和D50%之间的相关数学模型。为了比较不同患者间的腮腺平均剂量与D50%,靶区与腮腺相交区域剂量统一认定为靶区剂量。
1 资料与方法 1.1 患者资料随机选取西南医科大学附属医院肿瘤科50例鼻咽癌调强放疗患者,其中T2期21例、T3期19例、T4期10例,N0期9例、N1期12例、N2期13例、N3期10例、N4期6例。
1.2 靶区勾画医师根据2010年鼻咽癌调强放疗靶区及剂量设计指引专家共识[11]勾画肿瘤靶区(gross tumor volume,GTV):GTVnx、GTVrnp、GTVnd;临床靶区(clinical target volume,CTV):CTV1、CTV2;对上述对应各靶区扩3 mm作为计划靶区(planning target volume, PTV)。所有入组患者均由同一医师对靶区及危及器官的勾画。
1.3 处方剂量与计划评估要求(参见RTOG 0615与RTOG 0225规定)[12-13](1)处方剂量定义为95%的PTV所接收的最低吸收剂量;(2)PGTVnx,PGTVrnp单次剂量2.10~2.25 Gy,总剂量66~76 Gy;PGTVnd单次剂量2.00~2.25 Gy,总剂量66~70 Gy;PCTV1单次剂量1.80~2.05 Gy,总剂量60~62 Gy;PCTV2单次剂量1.80 Gy,总剂量56Gy。(3)计划评估要求:PTV接收≥110%处方剂量的体积 < 20%;PTV接受≥115%处方剂量的体积 < 5%;PTV接受 < 93%的处方剂量的体积 < 1%。
1.4 危及器官限定剂量主要危及器官限量也同样参见RTOG 0615与RTOG 0225规定;其中腮腺平均剂量 < 26 Gy,或对于腮腺与PCTV2相交体积过大的情况至少单侧D50% < 30 Gy或剂量尽量低。
1.5 治疗计划设计所有调强治疗计划均采用Pinnacle 8.0(Pinnacle3, version 8.0 m, Philips Medical Systems)治疗计划系统对50例鼻咽癌患者调强治疗计划进行前瞻性优化分析,采用6MV X线共面9野均分直接子野优化的设计方法。腮腺优化参数选取V23 < 30%~V30 < 30%与D50% < 20~30 Gy,权重在30~80之间进行反复修改,在使得每个患者靶区与腮腺相交区域剂量统一为靶区剂量前提下使得腮腺Dmean与D50%尽量低。
1.6 统计学方法从50例患者调强治疗计划中得出腮腺和PCTV2相交体积(Voverlap)与腮腺体积(Vparotid)的比值与腮腺平均剂量(Dmean)和处方剂量(Dprescription)比值的散点图,以及Voverlap/Vparotid与D50%/Dprescription的散点图,再通过Matlab软件对二者数据进行拟合,数据拟合过程中采用线性拟合、多项式拟合、Power拟合等方法。选取其中最优的拟合方法得出两者之间的相关公式。
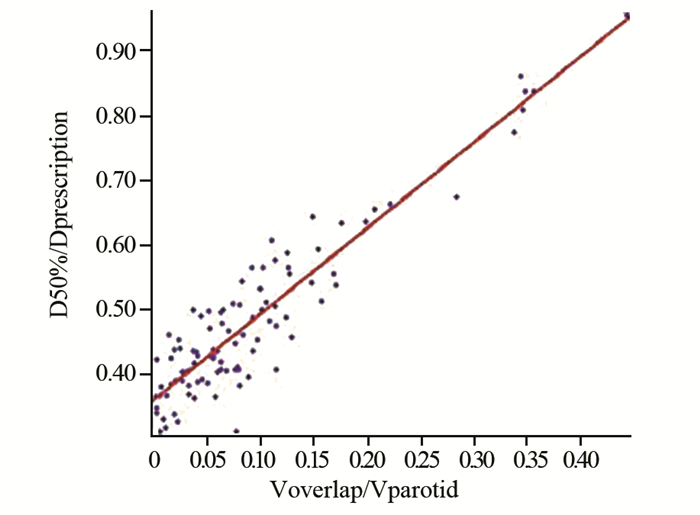
2 结果 2.1 散点图与相关性研究50例鼻咽癌患者腮腺体积散点图,见图 1;Vparotid与Dmean/Dprescription之间不存在相关性(相关系数r=-0.150),见图 2;Vparotid与D50%/Dprescription之间不存在相关性(r=-0.192),见图 3;Voverlap与Dmean/Dprescription之间存在显著正相关(置信度为0.01, r=0.758),Voverlap与D50%/Dprescription之间存在显著正相关(置信度为0.01, r=0.665);Voverlap/Vparotid与Dmean/Dprescription之间存在显著正相关(置信度为0.01, r=0.895),见图 4,Voverlap/Vparotid与D50%/Dprescription之间存在显著正相关(置信度为0.01, r=0.812),见图 5。所有相关性分析均采用Spearman相关法。
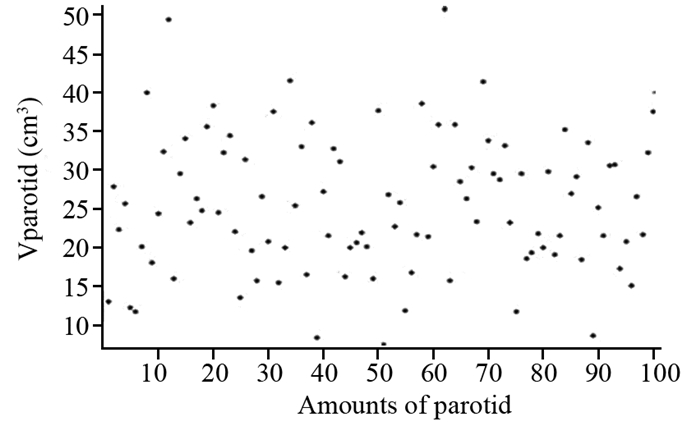
|
| 图 1 患者腮腺体积散点图 Figure 1 Parotid volume scatter plot of patients |
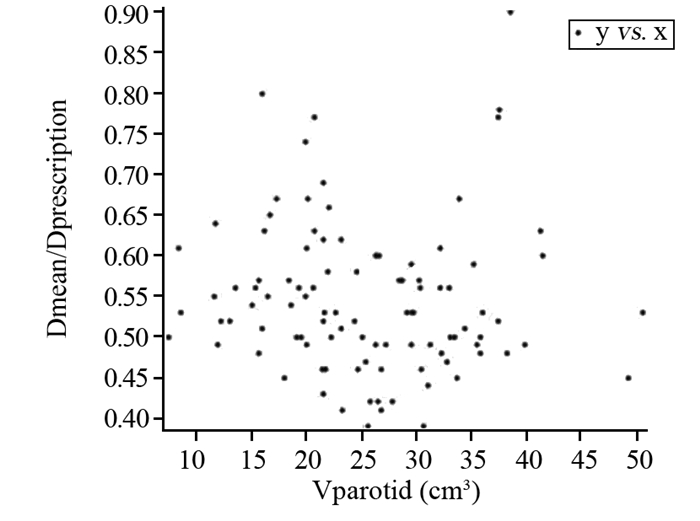
|
| 图 2 Vparotid与Dmean/Dprescription之间散点图 Figure 2 Scatter plot between Vparotid and Dmean/Dprescription |
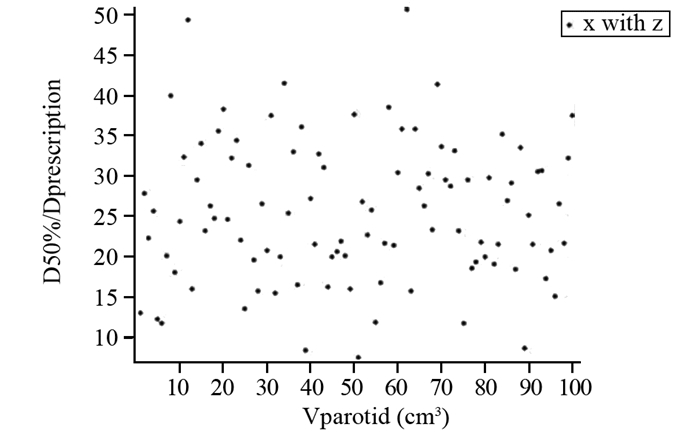
|
| 图 3 Vparotid与D50%/Dprescription之间散点图 Figure 3 Scatter plot between Vparotid and D50%Dprescription |
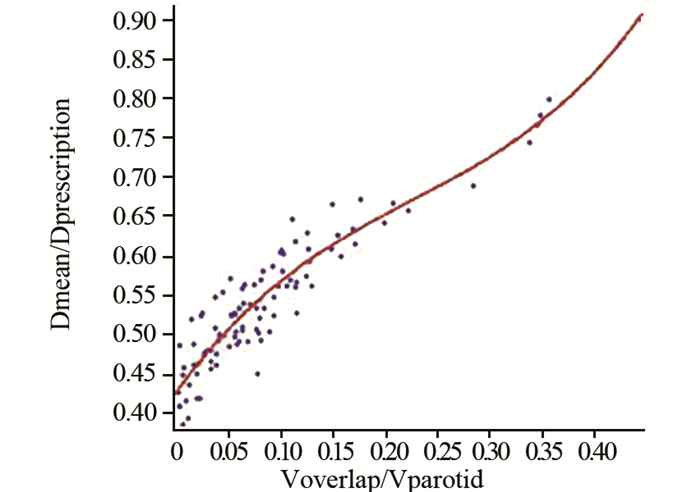
|
| 图 4 Voverlap/Vparotid与Dmean/Dprescription之间散点图 Figure 4 Scatter plot between Voverlap/Vparotid and Dmean/Dprescription |
|
| 图 5 Voverlap/Vparotid与D50%/Dprescription之间散点图 Figure 5 Scatter plot between Voverlap/Vparotid and D50%/Dprescription |
2.2.1 通过Matlab软件对图 4数据进行4次多项式拟合,得出如下公式:
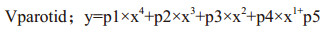 |
(1) |
其中,p1=1.468,p2=6.319,p3=-4.753,p4=1.809,p5=0.4286。
2.2.2 通过Matlab软件对图 5数据进行数据拟合,发现直接用线性拟合就可以很好地对其散点图进行拟合,说明两者之间正相关性非常显著,得出如下公式:
 |
(2) |
其中,p1=1.322,p2=0.3616。
3 讨论鼻咽癌调强放疗计划优化过程中,因患者的腮腺体积大小各异、分期的不同也会导致不同的Voverlap/Vparotid。杜克大学的Zhu等[14],以及华盛顿大学的Appenzoller等[15]通过器官-DVH关系预测模型,在制作IMRT计划前提前预测危及器官的DVH,以保证IMRT计划的质量,但上述方法较为复杂,需要提取治疗计划中危及器官每个采样点的剂量信息,且建模数据为回顾性分析,我国大多数放疗单位在现有设备基础上并不能将该模型应用到实际的IMRT优化计划中。
根据Yang和Moore等研究[16-17],运用预测模型可以明显提高计划效率,减少正常器官受量。而本研究发现鼻咽癌调强放疗计划中腮腺的体积与其Dmean和D50%之间并无相关关系,而Voverlap/Vparotid与Dmean和D50%之间有显著的正相关性,并给出了他们之间的相关数学模型,见公式(1)、(2)。在给定处方条件下通过Voverlap/Vparotid,在优化放疗调强计划前预测出Dmean与D50%,作为调强计划评估标准,从而减少放疗计划优化过程中主观因素造成的影响。公式(1)、(2)拟合方法简单,我国大多数放疗单位均可在现有治疗计划系统的基础上利用该方法建立适合自己科室治疗计划系统和设备的Voverlap/Vparotid与Dmean和D50%之间的相关数学模型。
上述研究并不只局限于鼻咽癌患者腮腺的Dmean和D50%的预测,对于其他部位接受调强放疗的患者,危及器官也可以通过上述本研究所采用的方法,得出其他危及器官体积与其吸收剂量之间的关系的拟合公式,在制作IMRT计划时提前预测每个危及器官吸收剂量。
调强计划在实际优化过程中仍有许多客观因素会影响其结果,例如为了更好地保护腮腺,是否需要降低其与靶区相交体积的剂量,需物理师与医生共同商量得出最终适合个体化的结论。从散点图上看,本研究仍需要加大样本数据量,采用多中心、更大样本数据,更准确的拟合出调强放疗时危及器官体积与其吸收剂量之间相关的数学模型,消除人为主观因素,使不同医院的患者能得到统一的标准,建立患者不同部位危及器官个体化的剂量限制统一质控模型,是未来的研究方向。
| [1] | Fang FM, Chien CY, Tsai WL, et al. Quality of life and survival outcome for patients with nasopharyngeal carcinoma receiving three-dimensional conformal radiotherapy vs. intensity-modulated radiotherapy-a longitudinal study[J]. Int J Radiat Oncol Biol Phys, 2008, 72(2): 356–64. DOI:10.1016/j.ijrobp.2007.12.054 |
| [2] | Lin SJ, Pan JJ, Lu H, et al. Nasopharyngeal carcinoma treated with reduced-volume intensity-modulated radiation therapy: report on the 3-year outcome of a prospective series[J]. Int J Radiat Oncol Biol Phys, 2009, 75(4): 1071–8. DOI:10.1016/j.ijrobp.2008.12.015 |
| [3] | Wong FC, Ng AW, Lee VH, et al. Whole-field simultaneous integrated-boost intensity-modulated radiotherapy for patients with nasopharyngeal carcinoma[J]. Int J Radiat Oncol Biol Phys, 2010, 76(1): 138–45. DOI:10.1016/j.ijrobp.2009.01.084 |
| [4] | Lee AW, Lau KY, Hung WM, et al. Potential improvement of tumor control probability by induction chemotherapy for advanced nasopharyngeal carcinoma[J]. Radiother Oncol, 2008, 87(2): 204–10. DOI:10.1016/j.radonc.2008.02.003 |
| [5] | Lai S, Li WF, Chen L, et al. How Does Intensity-modulated radiotherapy versus conventional two-dimensional radiotherapy influence the treatment results in nasopharyngeal carcinoma patients?[J]. Int J Radiation Oncol Biol Phys, 2011, 80(3): 661–8. DOI:10.1016/j.ijrobp.2010.03.024 |
| [6] | Kam MK, Teo PM, Chan RM, et al. Treatment of nasopharyngeal carcinoma with intensity-modulated radiotherapy: the Hong Kong experience[J]. Int J Radiat Oncol Biol Phys, 2004, 60(5): 1440–50. DOI:10.1016/j.ijrobp.2004.05.022 |
| [7] | Lin SJ, Lu JJ, Han L, et al. Sequential chemotherapy and intensity-modulated radiation therapy in the management of locoregionally advanced nasopharyngeal carcinoma: Experience of 370 consecutive cases[J]. BMC Cancer, 2010, 10: 39. DOI:10.1186/1471-2407-10-39 |
| [8] | Hunt MA, Jackson A, Narayana A, et al. Geometric factors influencing dosimetric sparing of the parotid glands using IMRT[J]. Int J Radiat Oncol Biol Phys, 2006, 66(1): 296–304. DOI:10.1016/j.ijrobp.2006.05.028 |
| [9] | Kevin LM, Brame RS, Daniel A, et al. Experience-base quality control of clinical intensity-modulated radiotherapy planning[J]. Int J Radiat Oncol Biol Phys, 2011, 81(2): 545–51. DOI:10.1016/j.ijrobp.2010.11.030 |
| [10] | Lian J, Yuan L, Ge Y, et al. Modeling the dosimetry of organ-at-risk in head and neck IMRT planning: an intertechnique and interinstitutional study[J]. Med Phys, 2013, 40(12): 121704. DOI:10.1118/1.4828788 |
| [11] | 中国鼻咽癌临床分期工作委员会. 2010鼻咽癌调强放疗靶区及剂量设计指引专家共识[J]. 中华放射肿瘤学杂志, 2010, 20(4): 267–9. [ Working committee for the clinical stage nasopharyngeal carcinoma (NPC) in China. 2010 expert consensus of nasopharyngeal carcinoma IMRT target and dosage design[J]. Zhonghua Fang She Zhong Liu Xue Za Zhi, 2010, 20(4): 267–9. ] |
| [12] | Radiation Therapy Oncology Group. A phase Ⅱ study of concurrent chemoradiotherapy using three-dimensional conformal radiotherapy (3D-CRT) or intensity-modulated radiation therapy (IMRT) +Bevacizumab (BV) for locally or regionally advanced nasopharyngeal cancer (RTOG 0615)[R/OL].[2011-03-05].https://www.mdanderson.org/patients-family/diagnosis-treatment/clinical-trials/clinical-trials-index/clinical-trials-detail.IDRTOG0615.html. |
| [13] | Radiation Therapy Oncology Group. A phase Ⅱ study of intensity modulated radiation therapy (IMRT) +/-chemotherapy for nasopharyngeal cancer (RTOG 0225) [R/OL]. [2011-03-05].https://www.mdanderson.org/patients-family/diagnosis-treatment/clinical-trials/clinical-trials-index/clinical-trials-detail.IDRTOG-0225. html. |
| [14] | Zhu XF, Ge YR, Li TR, et al. A planning quality evaluation tool for prostate adaptive IMRT based on machine learning[J]. Med Phys, 2011, 38(2): 719–26. DOI:10.1118/1.3539749 |
| [15] | Appenzoller LM, Michalski JM, Thorstad WL, et al. Predicting dose-volume histograms for organs-at-risk in IMRT planning[J]. Med Phys, 2012, 39(12): 7446–61. DOI:10.1118/1.4761864 |
| [16] | Yang Y, Ford EC, Wu B, et al. An overlap-volume-histogram based method for rectal dose prediction and automated treatment planning in the external beam prostate radiotherapy following hydrogel injection[J]. Med Phys, 2013, 40(1): 011709. |
| [17] | Moore KL, Brame RS, Low DA, et al. Experience-based quality control of clinical intensity-modulated radiotherapy planning[J]. Int J Radiat Oncol Biol Phys, 2011, 81(2): 545–51. DOI:10.1016/j.ijrobp.2010.11.030 |
 2017, Vol. 44
2017, Vol. 44


