文章信息
- miRNA-199a-5p对骨肉瘤细胞增殖及自噬的影响
- Effect of miRNA-199a-5p on Cell Proliferation and Autophagy in Osteosarcoma
- 肿瘤防治研究, 2017, 44(3): 197-201
- Cancer Research on Prevention and Treatment, 2017, 44(3): 197-201
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.03.009
- 收稿日期: 2016-06-16
- 修回日期: 2016-09-19
2. 473400 南阳,郑州大学附属南阳市中心医院肾病风湿免疫科;
3. 473400 南阳,郑州大学附属南阳市中心医院医务科
2. Department of Nephropathy Rheumatology, Nanyang Center Hospital Affiliated to Zhengzhou University, Nanyang 473400, China;
3. Medical Services Section, Nanyang Center Hospital Affiliated to Zhengzhou University, Nanyang 473400, China
骨肉瘤是一种常见的原发性骨肿瘤,好发于长骨干骺端,多表现为肉瘤细胞直接形成骨样组织[1-3]。目前并无特效的治疗手段,其治疗依然是手术为主,辅以术前后的放化疗,但复发率高,预后较差[4-6]。且80%的患者在临床确诊时就已经出现早期转移,因而手术并不能完全清除体内癌细胞,故而对骨肉瘤的遗传学及分子生物学的研究成为诊断和治疗骨肉瘤的新方向。
近年有研究发现miRNA-199a-5p在多种肿瘤中显示异常表达,如黑色素瘤、胶质细胞瘤及肝细胞瘤等[7-9]。miRNA-199a-5p是pre-miRNA-199a-1(位于19号染色体)和pre-miRNA-199a-2(位于1号染色体)裂解后得到的两种成熟miRNA之一。有报道显示其可抑制肝癌的侵袭转移[9],且在肺癌A549细胞中可通过激活Caspase发挥促凋亡作用[10];但是其与骨肉瘤的相关性目前并无明确的研究。本研究通过检测miRNA-199a-5p在人骨肉瘤组织及细胞中的表达情况,探讨其在骨肉瘤发生发展中所起的作用,并进一步探讨其对骨肉瘤细胞U2OS的增殖及自噬的影响和可能的作用机制。
1 材料与方法 1.1 材料人骨肉瘤细胞系U2OS及人正常成骨细胞hFOB1.19均购自中国科学院上海细胞库;胎牛血清(FBS),DMEM培养液及Opti-NEM培养液均购自美国Gibco公司;Lipofectamine2000及相关转染试剂购自美国Invitrogen公司;Cyclin D1、p27、pRb、Beclin1、LC3Ⅰ/Ⅱ及GAPDH单克隆抗体购自美国Santa Cruz公司;CCK-8细胞增殖分析试剂盒购自日本同仁化学研究所;细胞周期检测试剂盒购自南京凯基公司;miRNA-199a-5p mimics及SYBR Green I real-time PCR kit由上海吉玛制药技术有限公司提供;其余试剂均为国产市售分析纯。
1.2 样本收集收集郑州大学附属南阳市中心医院2010年10月—2015年10月间共32例普通经典型骨肉瘤患者的病理组织标本及相对应的癌旁正常组织。其中男12例,女20例,平均年龄31.4岁。在我院行手术治疗后将相应组织样本存放于-80℃液氮中,同时留存其详细病理报告。所有临床组织样本的获取均由患者知情同意并取得伦理学委员会批准,且入院之前未接受过放、化疗或手术治疗。
1.3 方法 1.3.1 细胞培养、转染和分组所有实验用细胞株均培养于含10%胎牛血清的常规DMEM培养液中,培养条件为37℃恒温、5%CO2。每2~3天换液,4~5天可传代。取对数生长期的细胞消化后接种至6孔板,待细胞生长至60%~80%融合,更换为1%胎牛血清的培养液同步化12 h,即可进行转染。分组设置如下:空白对照组(Control);阴性对照组(negative control mimics,NC);转染过表达组(miRNA-199a-5p mimics, 199a-5p-m)。转染方法如下:分别将miRNA-199a-5p mimics和Lipofectamine2000溶解于Opti-MEM培养液中室温孵育5 min,然后将两管溶液轻柔混合,室温静置反应20 min。最后将混合液添加至各组细胞中,并置于培养箱中培养6 h,而后更换为含10%胎牛血清的常规培养液继续培养48 h。提取细胞蛋白测定转染效率并进行后续实验分析。
1.3.2 CCK-8法测定细胞增殖取对数生长期细胞接种于96孔板中(1×104个/孔),各组细胞经相应处理后继续培养22 h,分别加入10 μl CCK-8试剂,置于培养箱中孵育2 h。酶标仪测定450 nm波长处各孔的吸光度值(OD)。每组设置三个复孔取平均值,同时设置空白对照。
1.3.3 流式细胞术检测细胞周期各组细胞经相应处理后用不含EDTA的胰酶消化并离心收集细胞,PBS漂洗细胞2次,1000 g/min离心并重悬细胞,加入70%无水乙醇于4℃下避光过夜固定细胞。1000 g/min离心并洗去乙醇,避光条件下加入碘化丙啶(PI)并于37℃孵育30min,然后采用流式细胞仪检测Ex=488 nm处的荧光强度。
1.3.4 Western blot测定蛋白表达水平各组细胞经相应处理后提取细胞蛋白,采用BCA试剂盒进行蛋白定量。然后调整各组蛋白总量至60 μg,加入4倍体积的上样缓冲液进行SDS-PAGE电泳。电泳后将蛋白转移至PVDF膜,用5%脱脂牛奶室温封闭90 min,按说明书要求加入一抗4℃孵育过夜,TBST洗涤3次,每次5 min;再加入相对应的二抗室温孵育120 min,TBST洗涤3次,每次10 min,暗室中显影、定影、冲洗胶片。所得结果采用Image J灰度分析进行蛋白半定量分析。
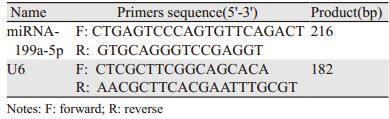
1.3.5 qRT-PCR检测蛋白相对表达量组织及细胞中总RNA的提取按照TRIzol一步法说明书进行。测定所提RNA样品在280 nm处的吸光度并定量。然后取2 μg总RNA以反转录酶催化合成cDNA,并采用SYBR Green实时荧光PCR的方法检测miRNA-199a-5p的表达。循环条件为95℃ 15 s,60℃ 30 s;72℃ 10 s,共45个循环;采用2-△△CT法分析基因的相对表达量。相应引物扩增的序列,见表 1。
所得数据均采用SPSS13.0统计学软件进行统计学分析。实验结果以均数±标准差(x±s)表示,计量资料两组之间的比较采用t检验,多组间比较采用方差分析,各组均数间的两两比较用Bonferroni校正的t检验,P < 0.05表示组间差异具有统计学意义。
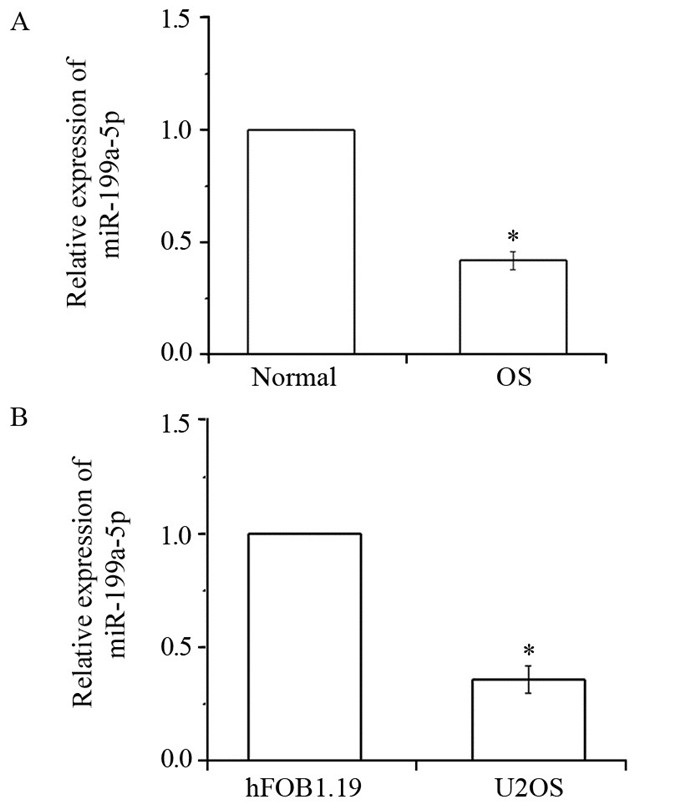
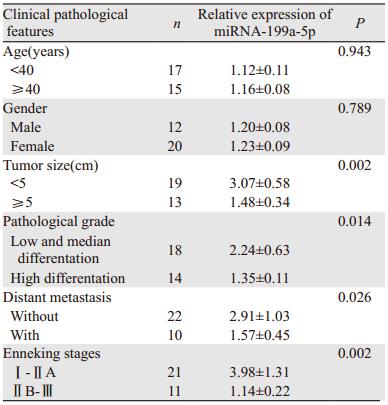
2 结果 2.1 miRNA-199a-5p在骨肉瘤组织及细胞中的表达RT-PCR结果显示:miRNA-199a-5p在骨肉瘤组织中的相对表达量是明显配对癌旁组织的(0.48±0.05)倍(P=0.009),见图 1A;在人骨肉瘤细胞系U2OS中miRNA-199a-5p的相对表达量是人正常成骨细胞系hFOB1.19的(0.36±0.06)倍(P=0.011),见图 1B。病理学资料统计分析显示:miRNA-199a-5p在骨肉瘤组织中的表达水平在年龄、性别因素组差异无明显统计学意义(P=0.943, P=0.789);而在肿块大小、远距转移、Enneking外科分期和病理分级因素组差异有统计学意义(P=0.002, P=0.026, P=0.002, P=0.014),见表 2。
|
| x±s, *: P < 0.05, compared with adjacent normal tissues group 图 1 骨肉瘤及配对正常组织 (A) 人骨肉瘤细胞系U2OS及人成骨细胞系hFOB1.19(B) 中miRNA-199a-5p的表达水平 Figure 1 The expression of miRNA-199a-5p in osteosarcoma and adjacent normal tissues (A), human osteosarcoma cell lines U2OS and osteoblast cell lines hFOB1.19(B) |
|
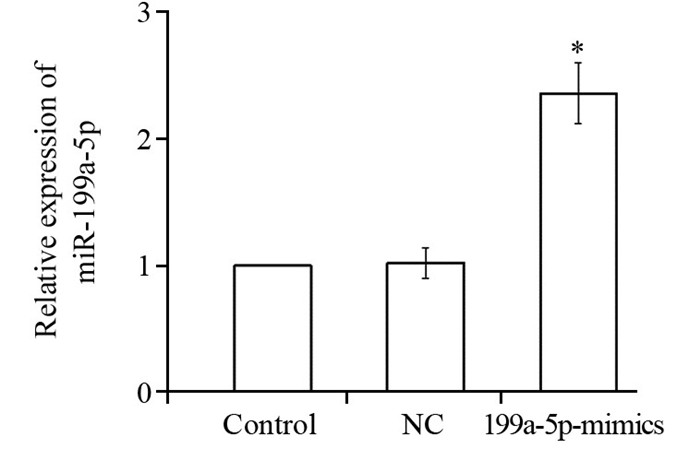
通过脂质体将miRNA-199a-5p mimics转染至U2OS细胞中,采用RT-PCR检测miRNA-199a-5p的表达水平。结果显示,转染miRNA-199a-5p mimics后,U2OS细胞中miRNA-199a-5p的mRNA表达水平增加至空白对照组的(2.36±0.24)倍(P=0.012),见图 2。
|
| NC: negative control group; x±s, n=6, *: P < 0.05, compared with control group 图 2 U2OS细胞转染miRNA-199a-5p mimics后miRNA-199a-5p的表达 Figure 2 The expression levels of miRNA-199a-5p in the U2OS cell after transfection of miRNA-199a-5p mimics |
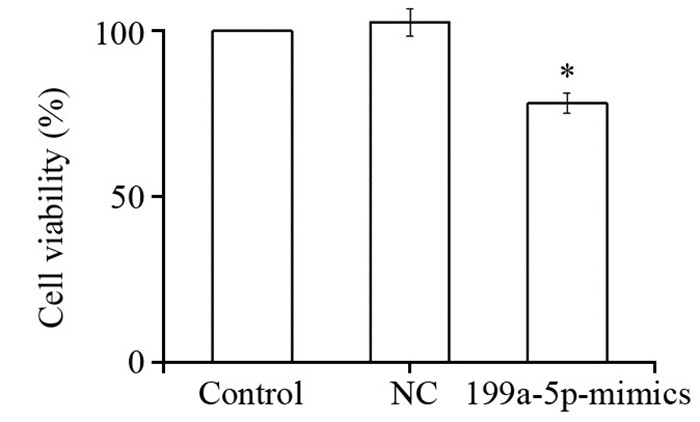
采用CCK-8法检测过表达miRNA-199a-5p对细胞活力的影响,结果显示,转染miRNA-199a-5p mimics后,U2OS的细胞活力显著降低(P=0.023),见图 3。
|
| x±s, n=6, *: P < 0.05, compared with control group 图 3 CCK-8检测过表达miRNA-199a-5p后U2OS细胞活力的变化 Figure 3 Cell viability of U2OS cells transfected with miRNA-199a-5p mimics determined by CCK-8 assay |
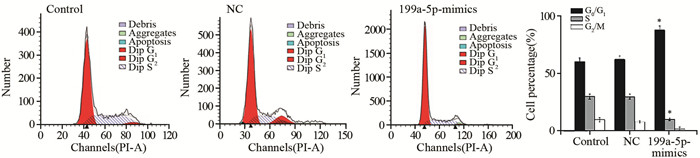
流式细胞术检测结果显示,过表达miRNA-199a-5p后,G0/G1期的细胞数占百分比增加至(87.82±3.69)%(P=0.016),S期细胞数所占百分比减少至(10.24±1.23)%(P=0.034),见图 4。说明过表达miRNA-199a-5p可抑制U2OS细胞周期由G0/G1期向S期转化。
|
| x±s, n=6, *: P < 0.05, compared with control group 图 4 流式细胞术检测过表达miRNA-199a-5p后U2OS细胞周期的变化 Figure 4 The cell cycle of U2OS cells transfected with miRNA-199a-5p mimics analyzed by flow cytometry |
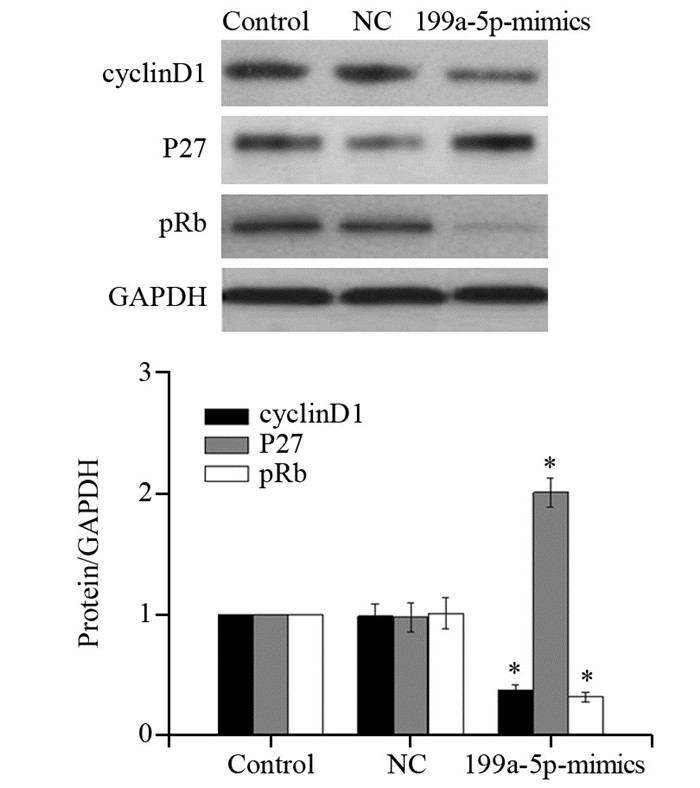
Western blot检测结果显示,转染miRNA-199a-5p mimics后细胞中cyclinD1、及pRb的表达显著降低(P=0.021, P=0.038),P27的表达则明显升高(P=0.003),见图 5。
|
| x±s, n=6, *: P < 0.05, compared with control group 图 5 过表达miRNA-199a-5p对U2OS细胞周期相关蛋白cyclinD1、P27及pRb表达的影响 Figure 5 Expression of cyclinD1, P27 and pRb in U2OS cells transfected with miRNA-199a-5p mimics |
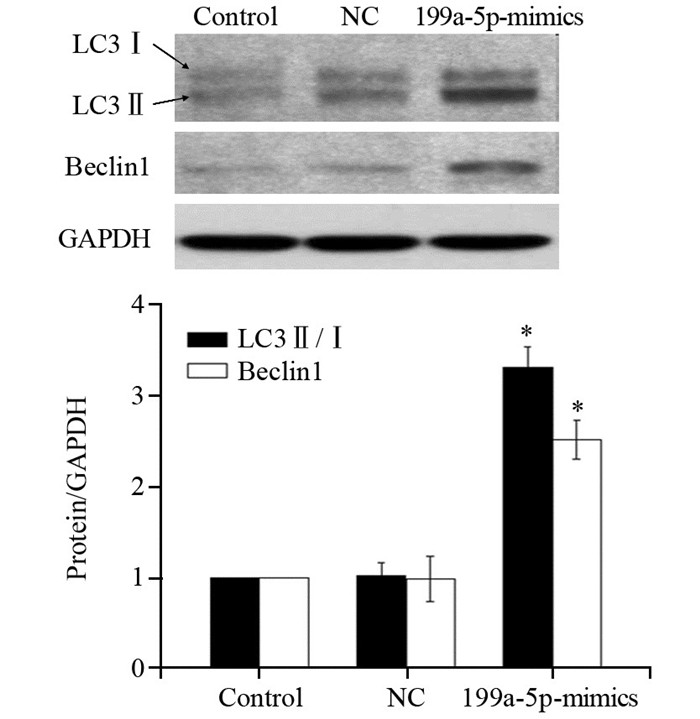
Western blot检测结果显示,转染miRNA-199a-5p mimics后细胞中Beclin1蛋白的表达显著增加(P=0.011),且LC3Ⅱ/Ⅰ的比值显著增加(P=0.002),见图 6。
|
| x±s, n=6, *: P < 0.05, compared with control group 图 6 过表达miRNA-199a-5p对U2OS细胞中LC3Ⅱ/Ⅰ和Beclin1表达的影响 Figure 6 Expression of LC3Ⅱ/Ⅰand Beclin1 in U2OS cells transfected with miRNA-199a-5p mimics |
微小RNA(microRNA, miRNA)是一种单链小分子RNA,约由19-25个核苷酸组成。研究发现[11-12],在人体中有着相当多的miRNA在骨肉瘤的发生发展中发挥着类似原癌基因或者抑癌基因的作用[13]。如miR-128在骨肉瘤组织中高表达且可促进骨肉瘤细胞U2OS及MG63的增殖[14],而miR-145则可以作为一种抑癌基因抑制骨肉瘤的发生发展[15-16]。本实验通过对骨肉瘤患者的组织样本及骨肉瘤细胞进行检测,发现在癌组织及骨肉瘤细胞系中同样显示出miRNA-199a-5p的低表达。进一步对所有纳入病例的病理学特征进行了分类和统计学分析,发现miRNA-199a-5p的表达与骨肉瘤的肿块大小、远距转移、Enneking外科分期和病理分级呈明显负相关关系。结果提示miRNA-199a-5p在骨肉瘤中低表达,且与骨肉瘤的的恶性生物学特性密切相关,可成为骨肉瘤临床治疗的一个潜在位点。
既往的大量研究显示miRNA-199a-5p在多种肿瘤中表现出抑癌基因的特性,抑制肿瘤的发生发展。Tsukigi等对54例肾细胞癌患者的临床样本分析显示59%的患者呈现miR-199a的低表达,并与患者的病理分级密切相关;且可通过靶向GSK-3β抑制细胞生长[17];在包括前列腺癌、结肠癌及膀胱癌等多种肿瘤中均可检测到miR-199a-5p的低表达,此外miR-30d、miR-181a和miR-199a-5p等可靶向GRP78抑制肿瘤细胞的增殖及增加其对化疗药物的敏感度[18]。本实验中我们通过外源性过表达人骨肉瘤细胞系U2OS中的miR-199a-5p,探讨其对骨肉瘤细胞增殖及自噬的影响。检测结果显示,转染miR-199a-5p mimics后,U2OS细胞的增殖速度减慢,同时周期进程也明显减慢,表明miR-199a-5p过表达可抑制骨肉瘤细胞的增殖。周期相关蛋白的表达分析则显示过表达miR-199a-5p可抑制U2OS细胞中周期素CyclinD1的表达,同时促进细胞周期依赖激酶抑制蛋白P27的表达,最终至pRb的磷酸化作用减弱,阻滞细胞通过G1/S调控点进入S期进行DNA复制。这一结果提示在骨肉瘤中,miR-199a-5p可能通过影响周期相关蛋白的表达,导致G1/S阻滞的出现而阻止细胞增殖,从而发挥抑癌作用。
自噬是凋亡之外的另一种细胞程序性死亡,且在肿瘤的发生发展中同时发挥着促癌及抑癌的作用[19-21]。前期有研究表明在乳腺癌细胞MDA-MB-231中,miR-199a-5p可通过上调DRAM1和BECN1激活细胞自噬,但是在乳腺癌细胞MCF-7中miR-199a-5p则可抑制电离辐射诱导的细胞自噬[22]。然而其在骨肉瘤细胞自噬中的作用并不明确。我们的检测结果发现,在U2OS细胞中过表达miR-199a-5p可明显观察到LC3Ⅱ/Ⅰ比值的升高,以及Beclin1蛋白表达的增加,表明细胞的自噬过程被激活。这一结果提示miR-199a-5p可激活骨肉瘤U2OS细胞的自噬过程,可能是其抑癌作用的另一个表现,但其具体的作用及涉及的相关机制还有待进一步探讨。
综上所述,miRNA作为一种新兴的基因治疗工具,在抗肿瘤的相关研究中具有广阔的前景,本研究的结果提示miR-199a-5p可作为骨肉瘤临床治疗的一个潜在位点。此外,由于研究条件的限制,miR-199a-5p在其他类型骨肉瘤细胞中的作用和相关的在体实验数据还需更进一步的研究。
| [1] | Anderson ME. Update on Survival in Osteosarcoma[J]. Orthop Clin North Am, 2016, 47(1): 283–92. DOI:10.1016/j.ocl.2015.08.022 |
| [2] | Yan GN, Lv YF, Guo QN. Advances in osteosarcoma stem cell research and opportunities for novel therapeutic targets[J]. Cancer Lett, 2016, 370(2): 268–74. DOI:10.1016/j.canlet.2015.11.003 |
| [3] | Sun L, Li Y, Zhang J, et al. Prognostic value of pathologic fracture in patients with high grade localized osteosarcoma: a systemic review and meta-analysis of cohort studies[J]. J Orthop Res, 2015, 33(1): 131–9. DOI:10.1002/jor.22734 |
| [4] | Isakoff MS, Bielack SS, Meltzer P, et al. Osteosarcoma: Current Treatment and a Collaborative Pathway to Success[J]. J Clin Oncol, 2015, 33(27): 3029–35. DOI:10.1200/JCO.2014.59.4895 |
| [5] | Fan Z, Patel S, Lewis VO, et al. Should High-grade Extraosseous Osteosarcoma be Treated with Multimodality Therapy Like Other Soft Tissue Sarcomas?[J]. Clin Orthop Relat Res, 2015, 473(11): 3604–11. DOI:10.1007/s11999-015-4463-y |
| [6] | Fauske L, Bondevik H, Bruland øS, et al. Negative and Positive Consequences of Cancer Treatment Experienced by Long-term Osteosarcoma Survivors: A Qualitative Study[J]. Anticancer Res, 2015, 35(11): 6081–90. |
| [7] | Yang X, Lei S, Long J, et al. MicroRNA-199a-5p inhibits tumor proliferation in melanoma by mediating HIF-1α[J]. Mol Med Rep, 2016, 13(6): 5241–7. |
| [8] | Gu S, Cheung HH, Lee TL, et al. Molecular mechanisms of regulation and action of microRNA-199a in testicular germ cell tumor and glioblastomas[J]. PLoS One, 2013, 8(12): e83980. DOI:10.1371/journal.pone.0083980 |
| [9] | Shen Q, Cicinnati VR, Zhang X, et al. Role of microRNA-199a-5p and discoidin domain receptor 1 in human hepatocellular carcinoma invasion[J]. Mol Cancer, 2010, 9: 227. DOI:10.1186/1476-4598-9-227 |
| [10] | Kim S, Lee UJ, Kim MN, et al. Micro RNA mi R-199a* regulates the MET proto-oncogene and the downstream extracellular signal-regulated kinase 2(ERK2)[J]. J Biol Chem, 2008, 283(26): 18158–66. DOI:10.1074/jbc.M800186200 |
| [11] | Chawla JP, Iyer N, Soodan KS, et al. Role of miRNA in cancer diagnosis, prognosis, therapy and regulation of its expression by Epstein-Barr virus and human papillomaviruses: With special reference to oral cancer[J]. Oral Oncol, 2015, 51(8): 731–7. DOI:10.1016/j.oraloncology.2015.05.008 |
| [12] | 周学, 杜宜兰, 金萍, 等. 癌症相关microRNAs与靶基因的生物信息学分析[J]. 遗传, 2015, 37(9): 855–64. [ Zhou X, Du YL, Jin P, et al. Bioinformatic analysis of cancer-related microRNAs and their target genes[J]. Yi Chuan, 2015, 37(9): 855–64. ] |
| [13] | Bilbao-Aldaiturriaga N, Gutierrez-Camino A, Martin-Guerrero I, et al. Polymorphisms in miRNA processing genes and their role in osteosarcoma risk[J]. Pediatr Blood Cancer, 2015, 62(5): 766–9. DOI:10.1002/pbc.v62.5 |
| [14] | Shen L, Chen XD, Zhang YH. MicroRNA-128 promotes proliferation in osteosarcoma cells by downregulating PTEN[J]. Tumour Biol, 2014, 35(3): 2069–74. DOI:10.1007/s13277-013-1274-1 |
| [15] | Tang M, Lin L, Cai H, et al. MicroRNA-145 downregulation associates with advanced tumor progression and poor prognosis in patients suffering osteosarcoma[J]. Onco Targets Ther, 2013, 6: 833–8. |
| [16] | Li E, Zhang J, Yuan T, et al. MiR-145 inhibits osteosarcoma cells proliferation and invasion by targeting ROCK1[J]. Tumour Biol, 2014, 35(8): 7645–50. DOI:10.1007/s13277-014-2031-9 |
| [17] | Tsukigi M, Bilim V, Yuuki K, et al. Re-expression of miR-199a suppresses renal cancer cell proliferation and survival by targeting GSK-3beta[J]. Cancer letters, 2012, 315(2): 189–97. DOI:10.1016/j.canlet.2011.10.008 |
| [18] | Su SF, Chang YW, Andreu-Vieyra C, et al. miR-30d, miR-181a and miR-199a-5p cooperatively suppress the endoplasmic reticulum chaperone and signaling regulator GRP78 in cancer[J]. Oncogene, 2013, 32(39): 4694–701. DOI:10.1038/onc.2012.483 |
| [19] | Li S, Wang L, Hu Y, et al. Autophagy regulators as potential cancer therapeutic agents: a review[J]. Curr Top Med Chem, 2015, 15(8): 720–44. DOI:10.2174/1568026615666150302105343 |
| [20] | Chen P, Cescon M, Bonaldo P. Autophagy-mediated regulation of macrophages and its applications for cancer[J]. Autophagy, 2014, 10(2): 192–200. DOI:10.4161/auto.26927 |
| [21] | Kenific CM, Debnath J. Cellular and metabolic functions for autophagy in cancer cells[J]. Trends Cell Biol, 2015, 25(1): 37–45. DOI:10.1016/j.tcb.2014.09.001 |
| [22] | Yi H, Liang B, Jia J, et al. Differential roles of miR-199a-5p in radiation-induced autophagy in breast cancer cells[J]. FEBS Lett, 2013, 587(5): 436–43. DOI:10.1016/j.febslet.2012.12.027 |
 2017, Vol. 44
2017, Vol. 44