文章信息
- 负载CD133+肝癌细胞RNA树突状细胞疫苗的免疫活性
- Immunological Competence of Dendritic Cell Vaccine Loaded with CD133+ Hepatocellular Carcinoma Cell RNA
- 肿瘤防治研究, 2017, 44(3): 184-188
- Cancer Research on Prevention and Treatment, 2017, 44(3): 184-188
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.03.006
- 收稿日期: 2016-06-16
- 修回日期: 2016-09-01
肝细胞肝癌(hepatocellular carcinoma, HCC)是我国高发的恶性肿瘤之一,约占全球HCC发生总数的70%,高居国内肿瘤死亡率第三位[1]。由于HCC具有对放化疗不敏感、术后易复发和转移的特点,因此探索更有效的治疗方法是一个亟待解决的问题。本研究利用流式细胞术从人HCC组织来源的肝癌细胞中分选出CD133+肝癌细胞,在体外经重组人白细胞介素-4(recombinant human interleukin-4, rhIL-4)、重组人粒细胞-巨噬细胞集落刺激因子(recombinant human granulocyte-macrophage colony-stimulating factor, rhGM-CSF)诱导培养人外周血单个核细胞(peripheral blood mononuclear cells, PBMC)得到树突状细胞(dendritic cells, DC),制备负载CD133+肝癌细胞RNA的DC疫苗,以期为在动物体内进行负载CD133+肝癌细胞RNA的DC疫苗实验奠定基础。
1 资料与方法 1.1 研究对象收集2015年3月1日至2015年12月10日广西医科大学附属肿瘤医院手术获得的新鲜肝癌组织样本,并采集肝癌患者外周血样本,以肝素(浓度20 u/ml)抗凝。患者在术前均未行放化疗,经病理诊断均为肝细胞性肝癌,且均签署了知情同意书。本研究遵循的程序获得广西医科大学附属肿瘤医院医学伦理委员会批准。
1.2 主要试剂RPMI 1640培养液、胎牛血清(fetal bovine serum, FBS)购自美国HyClone公司;胶原酶Ⅳ购自美国Sigma公司;淋巴细胞分离液购自北京索来宝公司;鼠抗人phycoerythrin(PE)-CD133/1(AC133)及其相对应的同型对照购自德国Miltenyi Biotec公司;鼠抗人FITC标记人类白细胞抗原(human leukocyte antigen, HLA)-DR、HLA-ABC、CD86、CD80、CD83及其相对应的同型对照购自美国BD公司。重组人白介素-2(recombinant human interleukin-2, rhIL-2)、rhIL-4、rhGM-CSF、重组人肿瘤坏死因子(recombinant human tumor necrosis factor-α,rhTNF-α)均购自美国R & D公司;白介素-12(interleukin-12, IL-12(P70) Platinum ELISA购自美国Affymetrix eBioscience公司。
1.3 HCC组织来源的肝癌细胞分离和原代培养收集新鲜肝癌组织样本,每例取10 g,洗净剪碎,经1 mg/ml的胶原酶Ⅳ消化30 min滤网过滤去渣,4℃下1 000 r/min离心5 min弃上清液;用完全培养液孵育10 min,细胞悬浮后经20%的Percoll在4℃下1 500 r/min离心5 min,收集细胞沉淀。将肝癌细胞用含有10%FBS、2 mmol/L谷氨酰胺、2 mmol/L三磷酸腺苷的RPMI 1640培养液培养48 h后,弃去未贴壁细胞,37℃、5%CO2饱和湿度的条件下以原代培养结合短暂传代培养的方法继续培养。
1.4 流式细胞术分选CD133+肝癌细胞和RNA提取将成功原代培养的肝癌细胞密度调整至1×106个/毫升,分别加入10 μl PE-CD133抗体或相对应的同型对照,充分混匀,4℃下避光孵育30 min后,利用流式细胞术分选出CD133+肝癌细胞,然后按照TRIzol试剂盒说明书进行RNA的提取,核酸定量仪测定OD260/280值(1.8~2.0)。
1.5 树突状细胞的体外培养应用葡聚糖-泛影葡胺密度梯度离心法分离出PBMC。将分离的PBMC用16 ml完全培养液重悬,分别加入到4个25 ml培养瓶,每个4 ml。置于在37℃、5%CO2饱和湿度的条件下培养2 h。收集非贴壁的PBMC,将其加入含10%胎牛血清及20 u/ml IL-2的完全培养液中继续培养。在所获贴壁的单个核细胞中,加入4 ml完全培养液、35 ng/ml rhIL-4、50 ng/ml rhGM-CSF,每2天半量换液,补加全量细胞因子,培养6天后,收集悬浮细胞(未成熟DC)继续培养。
1.6 负载CD133+肝癌细胞RNA树突状细胞疫苗制备收集培养第6天未成熟的DC,经PBS洗涤后,用无血清培养液重悬,制备成1×106个/毫升的细胞悬液,铺于6孔培养板中培养,每孔2 ml。每个培养孔分别加入20 μg/ml CD133+肝癌细胞RNA和肝癌细胞RNA,同时以没有负载RNA的DC作为阴性对照,置于37℃、5%CO2饱和湿度的条件下培养24 h。然后每孔分别加入40 ng/ml TNF-α刺激DC成熟,继续培养48 h后,可获得成熟的DC疫苗。负载CD133+肝癌细胞RNA、肝癌细胞RNA、和未负载RNA的成熟DC分别标记为CD133+肝癌细胞RNA-DC、肝癌细胞RNA-DC和成熟DC。
1.7 负载CD133+肝癌细胞RNA的DC抗原递呈相关分子的表达情况及分泌IL-12水平的检测收集CD133+肝癌细胞RNA-DC、肝癌细胞RNA-DC和成熟DC,制备成1×106个/毫升的细胞悬液,每管分别加入HLA-ABC、HLA-DR、CD86、CD80、CD83等荧光标记的抗体,根据抗体类型分别设置同型对照管。4℃下避光孵育30 min,PBS洗涤3次,流式细胞仪检测上述分子的表达。收集上述各类成熟DC培养液上清液,应用ELISA检测上述DC分泌IL-12的水平。
1.8 负载CD133+肝癌细胞RNA的DC刺激自体淋巴细胞增殖能力检测利用尼龙毛柱从非贴壁的PBMC中纯化T淋巴细胞。采用MTS法检测CD133+肝癌细胞RNA-DC、肝癌细胞RNA-DC和成熟DC刺激自体T淋巴细胞增殖能力。将三种不同DC分别和自体T淋巴细胞按照10:1的比例混合,每种不同的树突状细胞混合培养均设三个复孔,同时设无DC的自体T淋巴细胞对照孔,培养7天后,每孔加入20 μl MTS溶液,37℃、5%CO2培养箱孵育4 h,然后将96孔板200 g离心10 min,收集培养液的上清液,在酶标仪上读取490 nm的吸光度值。计算DC刺激自体T淋巴细胞增殖的能力。
1.9 统计学方法所有数据使用SPSS19.0软件处理,定量资料用(x±s)表示。多组间比较采用单因素方差分析,显著性检验水准为P < 0.05。
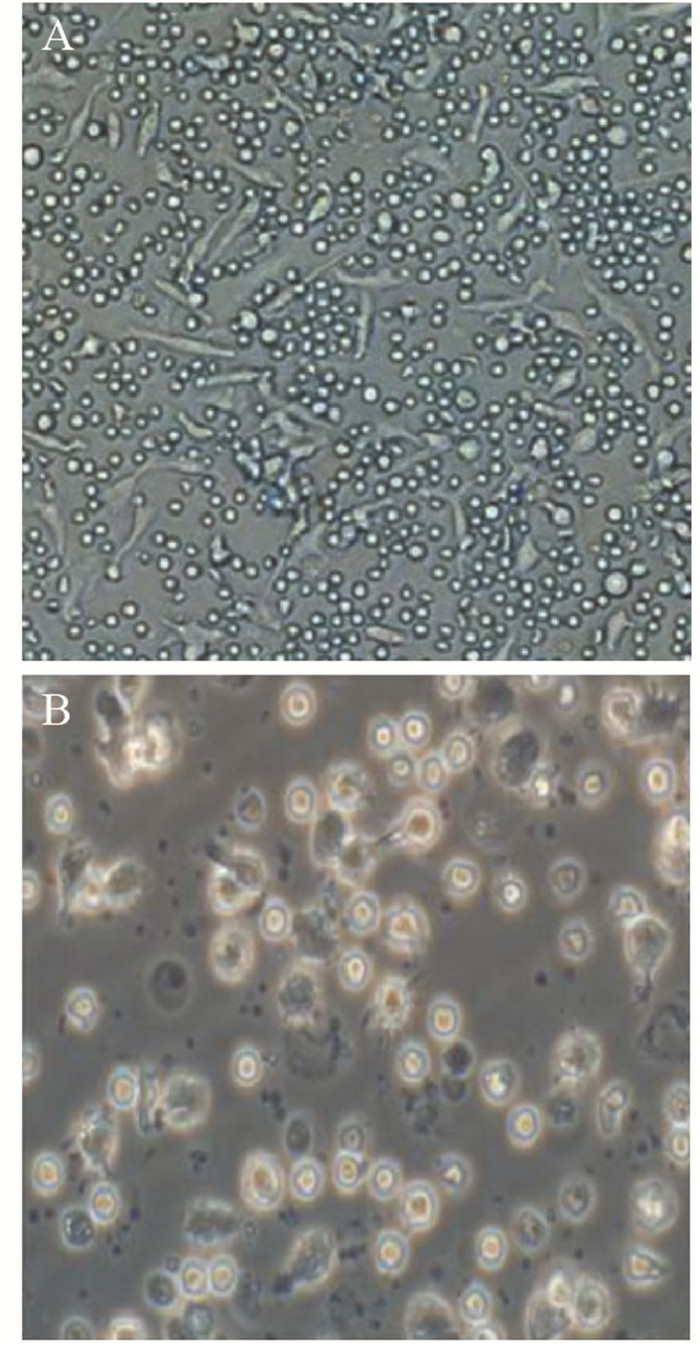
2 结果 2.1 DC的培养倒置显微镜观察树突状细胞形态,初期多呈散在分布的类圆形贴壁细胞,3~5天细胞体积增大,形态不规则,以条状多见,细胞表面有不规则突起。加入RNA和rhTNF-α促成熟48 h后,DC的形态发生改变,细胞悬浮生长,体积增大,可见细胞表面呈树枝样突起。CD133+肝癌细胞RNA-DC、肝癌细胞RNA-DC和成熟DC三者之间细胞形态未见明显差别,见图 1。
|
| A: cultured for 5d (×200); B: cultured for 7d (×400) 图 1 CD133+肝癌细胞RNA-DC形态图 Figure 1 Morphology of dendritic cell loaded with CD133+ hepatocellular carcinoma cell RNA (CD133+ HCC RNA-DC) |
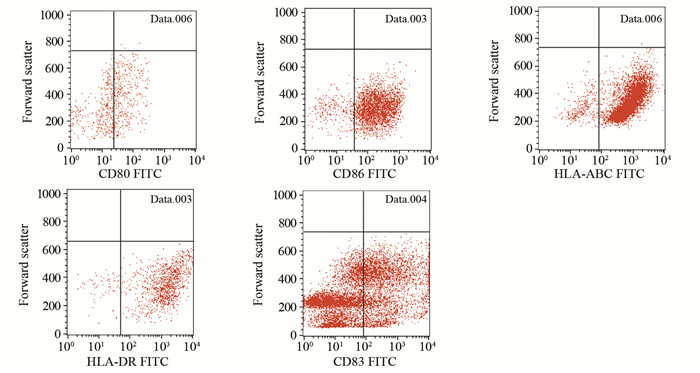
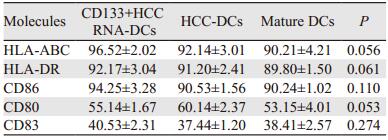
CD133+肝癌细胞RNA树突状细胞的抗原递呈相关分子表达水平符合成熟DC表型特征,HLA-ABC、HLA-DR、CD86、CD80、CD83表达水平与肝癌细胞RNA树突状细胞(肝癌细胞RNA-DC)和成熟DC比较,差异均无统计学意义(均P > 0.05)。CD133+肝癌细胞RNA-DC、肝癌细胞RNA-DC和成熟DC的上述分子具体表达水平见图 2、表 1。
|
| 图 2 负载CD133+肝癌细胞RNA的DC抗原递呈相关分子表达情况 Figure 2 Phenotypes expression of CD133+ HCC RNA-DC |
|
结果显示,CD133+肝癌细胞RNA-DC、肝癌细胞RNA-DC、成熟DC和未成熟DC分泌IL-12的量分别为(421.50±3.12)、(418.20±1.10)、(324.20±2.19)和(102.47±4.60)pg/ml,前两者之间差异无统计学意义(P=0.14)。CD133+肝癌细胞RNA-DC分泌IL-12的量分别高于成熟DC和未成熟DC(P=0.00, P=0.00)。肝癌细胞RNA-DC分泌IL-12的量分别高于成熟DC和未成熟DC(P=0.00, P=0.00)。
2.4 负载CD133+肝癌细胞RNA的DC刺激自体T淋巴细胞增殖能力检测结果显示,CD133+肝癌细胞RNA-DC、肝癌细胞RNA-DC、成熟DC和无DC的自体T淋巴细胞OD490值分别是(0.21±0.02)、(0.20±0.01)、(0.16±0.03)、(0.07±0.01)。前两者之间差异无统计学意义(P=0.107)。CD133+肝癌细胞RNA-DC的OD490值分别均高于成熟DC和无DC的自体T淋巴细胞(P=0.01, P=0.00)。肝癌细胞RNA-DC的OD490值分别高于成熟DC和无DC的自体T淋巴细胞(P=0.00, P=0.00)。
3 讨论生物治疗是继手术、放疗、化疗之后的第四种肿瘤治疗手段之一。树突状细胞(dendritic cells, DC)疫苗已在全球范围广泛开展抗肿瘤动物实验和临床试验,尤其在黑色素瘤[2]、肾癌[3]治疗方面取得了较大的研究进展。有研究提示,脑肿瘤干细胞总RNA作为DC的致敏物,较传统肿瘤抗原更能诱导出较强的抗肿瘤疗效[4]。研究证实,CD133可以作为肝癌干细胞的表面标志物[5]。本课题组前期研究提示,从HCC组织样本中分离获得的CD133+肝癌细胞只占HCC细胞的一小部分,并具有明显的肿瘤干细胞样特性[6]。
DC是目前已知的功能最强的专职抗原递呈细胞,能够识别、处理肿瘤抗原并把抗原信号传递给T淋巴细胞,从而诱导出高效而特异性的抗肿瘤免疫[7]。肿瘤患者存在全身性DC功能缺陷和肿瘤局部DC功能缺陷,DC的数量与癌旁组织以及良性的肿瘤相比仍然较少, 而且其功能状态大都异常, 主要表现为活化受到抑制、不能有效迁移进入次级淋巴器官以及异质性DC亚群的出现[8]。目前通过体外诱导功能正常的DC,以它作为疫苗可有效诱导抗肿瘤免疫反应。然而肝癌DC疫苗在临床研究中的治疗结果尚未令人满意[9-10],其原因主要是缺乏特异性肿瘤标志物,不能诱导特异性抗肝癌免疫反应。抗肝癌的DC疫苗选择的抗原有蛋白抗原、抗原肽、肿瘤细胞裂解物[11]等,本研究采用黏附培养法,根据DC前体单个核细胞半贴壁的特点,在培养早期去除淋巴细胞等悬浮细胞,而培养后期经rhTNF-α促成熟得到较高纯度的半悬浮状成长DC。谭德敏等[12]通过在培养液中加入rhIL-4、rhGM-CSF,诱导外周血单个核细胞培养得到成熟DC,而本研究采取rhIL-4、rhGM-CSF联合rhTNF-α培养方法得到的DC,其具有典型的DC形态特征,这与江龙委等[13]报道一致。
DC大量表达主要组织相容性复合物-Ⅱ类分子和其独特的形态学特征是鉴定成熟DC的标志物[14]。研究报道[15-16],成熟DC纯度表型在85%~95%,共刺激分子CD86表达量在80%~90%。本研究应用CD133+肝癌细胞RNA负载DC,经TNF-α活化后,符合成熟DC高表达HLA-ABC、HLA-DR、CD86、CD80、CD83表型特征,同时大量分泌IL-12。
IL-12具有激活T淋巴细胞增殖的能力,可诱导早期辅助性T细胞分化为Th1淋巴细胞,并启动细胞免疫应答。本研究中,CD133+肝癌干细胞RNA-DC与肝癌细胞RNA-DC在抗原递呈相关分子表达水平、分泌IL-12的水平和刺激T淋巴细胞增殖能力方面均没有明显差异,这可能说明两者在抗原递呈能力和分泌功能没有明显区别。但是它们分泌IL-12的能力和刺激T淋巴细胞增殖能力优于未负载RNA的成熟DC,这可能提示IL-12在DC疫苗激活T淋巴细胞增殖过程中发挥着重要作用。
总之,本研究采取rhIL-4、rhGM-CSF联合rhTNF-α培养方法得到的DC,符合成熟DC高表达抗原递呈相关分子的表型特征。实验结果提示以原代人CD133+肝癌细胞RNA作为抗原能够成功制备DC疫苗,并证明其在体外具有免疫活性。国内学者[17]利用CD133+Huh7肝癌细胞系RNA制备的DC疫苗能够诱导CD8+细胞毒性T淋巴细胞特异性反应。然而本研究负载原代人CD133+肝癌细胞RNA树突状细胞疫苗能否诱导更强的CD8+细胞毒性T淋巴细胞特异性反应,还需进一步研究。
| [1] | Chen W, Zheng R, Baade PD, et al. Cancer statistics in China, 2015[J]. Ca Cancer J Clin, 2016, 66(2): 115–32. DOI:10.3322/caac.21338 |
| [2] | Dillman RO, Mcclay EF, Barth NM, et al. Dendritic Versus Tumor Cell Presentation of Autologous Tumor Antigens for Active Specific Immunotherapy in Metastatic Melanoma: Impact on Long-term Survival by Extent of Disease at the Time of Treatment[J]. Cancer Biother Radiopharm, 2015, 30(5): 187–94. DOI:10.1089/cbr.2015.1843 |
| [3] | Anguille S, Smits EL, Lion E, et al. Clinical use of dendritic cells for cancer therapy[J]. Lancet Oncol, 2014, 15(7): e257–67. DOI:10.1016/S1470-2045(13)70585-0 |
| [4] | 肖宗宇, 陈晓娟, 杨艺, 等. 肿瘤干细胞样细胞RNA致敏树突状细胞治疗大鼠9L脑肿瘤[J]. 北京大学学报 (医学版), 2015, 47(4): 661–6. [ Xiao ZY, Chen XJ, Yang Y, et al. Experimental study of dendritic cells transfected with cancer stem like cells RNA against 9L brain tumors[J]. Beijing Da Xue Xue Bao (Yi Xue Ban), 2015, 47(4): 661–6. ] |
| [5] | Chan AW, Tong JH, Chan SL, et al. Expression of stemness markers (CD133 and EpCAM) in prognostication of hepatocellular carcinoma[J]. Histopathology, 2014, 64(7): 935–50. DOI:10.1111/his.2014.64.issue-7 |
| [6] | 林家耀, 张志明, 刘剑勇, 等. 肝细胞性肝癌组织CD133+细胞肿瘤干细胞特性的研究[J]. 中华肿瘤防治杂志, 2016, 23(4): 223–7. [ Lin JY, Zhang ZM, Liu JY, et al. Identification and characterization of cancer stem cells from CD133+ cells separated from hepatocellular carcinoma tissue[J]. Zhonghua Zhong Liu Fang Zhi Za Zhi, 2016, 23(4): 223–7. ] |
| [7] | Ma Y, Shurin GV, Peiyuan Z, et al. Dendritic Cells in the Cancer Microenvironment[J]. J Cancer, 2013, 4(1): 36–44. DOI:10.7150/jca.5046 |
| [8] | Zou W. Immunosuppressive networks in the tumour environment and their therapeutic relevance[J]. Nat Rev Cancer, 2005, 5(4): 263–74. DOI:10.1038/nrc1586 |
| [9] | Tada F, Abe M, Hirooka M, et al. PhaseⅠ/Ⅱ study of immunotherapy using tumor antigen-pulsed dendritic cells in patients with hepatocellular carcinoma[J]. Int J Oncol, 2012, 41(5): 1601–9. |
| [10] | Sun TY, Yan W, Yang CM, et al. Clinical research on dendritic cell vaccines to prevent postoperative recurrence and metastasis of liver cancer[J]. Genet Mol Res, 2015, 14(4): 16222–32. DOI:10.4238/2015.December.8.12 |
| [11] | 冯钟煦, 刘剑勇, 赵荫农, 等. H22细胞全细胞抗原负载的树突状细胞激活肿瘤浸润性淋巴细胞抗小鼠肝癌的实验[J]. 肿瘤防治研究, 2012, 39(10): 1179–82. [ Feng ZX, Liu JY, Zhao YN, et al. Anti-mouse Hepatoma Effect of Tumor-infiltrating Lymphocyte Stimulated by DCs Pulsed with H22 Full-cell Antigen[J]. Zhong Liu Fang Zhi Yan Jiu, 2012, 39(10): 1179–82. ] |
| [12] | 谭德敏, 向阳, 谭千林. 狼疮性肾炎患者外周血树突状细胞功能的研究[J]. 中国免疫学杂志, 2016, 32(4): 570–2. [ Tan DM, Xiang Y, Tan QL. Study on immune function of blood dendritic cells in patients with lupus nephritis[J]. Zhongguo Mian Yi Xue Za Zhi, 2016, 32(4): 570–2. ] |
| [13] | 江龙委, 蔡凯, 黄伟谦, 等. rhG-CSF与rhGM-CSF动员人外周血单核细胞后DC疫苗数量及功能变化的比较[J]. 肿瘤防治研究, 2015, 42(11): 1095–9. [ Jiang LW, Cai K, Huang WQ, et al. Comparison of rhG-CSF and rhGM-CSF Mobilization on Quantity and Function Change of Dendritic Cell-based Tumor Vaccine via Human Peripheral Blood Monocytes[J]. Zhong Liu Fang Zhi Yan Jiu, 2015, 42(11): 1095–9. ] |
| [14] | Kyte JA, Mu L, Aamdal S, et al. PhaseⅠ/Ⅱ trial of melanoma therapy with dendritic cells transfected with autologous tumor-mRNA[J]. Cancer gene ther, 2006, 13(10): 905–18. DOI:10.1038/sj.cgt.7700961 |
| [15] | Gao D, Li C, Xie X, et al. Autologous tumor lysate-pulsed dendritic cell immunotherapy with cytokine-induced killer cells improves survival in gastric and colorectal cancer patients[J]. PLoS One, 2014, 9(4): e93886. DOI:10.1371/journal.pone.0093886 |
| [16] | Xi HB, Wang GX, Fu B, et al. Survivin and PSMA Loaded Dendritic Cell Vaccine for the Treatment of Prostate Cancer[J]. Biol Pharm Bull, 2015, 38(6): 827–35. DOI:10.1248/bpb.b14-00518 |
| [17] | Sun JC, Pan K, Chen MS, et al. Dendritic cells-mediated CTLs targeting hepatocellular carcinoma stem cells[J]. Cancer Biol Ther, 2010, 10(4): 368–75. DOI:10.4161/cbt.10.4.12440 |
 2017, Vol. 44
2017, Vol. 44


