文章信息
- 利托那韦对卡波氏肉瘤相关疱疹病毒感染细胞LYN表达的影响
- Effects of Ritonavir on Expression of LYN in Kaposi's Sarcoma-associated Herpesvirus-infected Cells
- 肿瘤防治研究, 2017, 44(3): 168-171
- Cancer Research on Prevention and Treatment, 2017, 44(3): 168-171
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.03.003
- 收稿日期: 2016-06-07
- 修回日期: 2016-10-19
2. 830001 乌鲁木齐,新疆维吾尔自治区人民医院呼吸科;
3. 841000 库尔勒,巴音郭楞蒙古自治州人民医院皮肤性病科;
4. 310036 杭州,杭州师范大学医学院
2. Department of Pneumology, Xinjiang Uiger Municipal People' s Hospital, Urumuqi 830001, China;
3. Department of Dermatovenerology, Hospital of Bayingolin Mongol Autonomous Prefecture, Korla 841000, China;
4. Medical College of Hangzhou Normal University, Hangzhou 310036, China
在我国,由卡波氏肉瘤相关疱疹病毒(Kaposi’s sarcoma associated herpesvirus, KSHV)感染所引起的经典型卡波氏肉瘤(Kaposi’s sarcoma, KS),主要见于新疆的维吾尔族和哈萨克族人[1]。但是KSHV的致病机制目前仍不清楚。在前期研究中,我们运用Affymetrix表达谱芯片筛选了KS相关的差异表达基因[2],发现v-yes-1 Yamaguchi肉瘤病毒相关同源癌基因v-yes-1 Yamaguchi sarcoma viral related oncogene homolog(LYN)在KS组织中表达上调[3],且组织均为KSHV感染阳性[4]。LYN是非受体型酪氨酸蛋白激酶,在Ewing’s肉瘤、乳腺癌、前列腺癌和肺癌等多种肿瘤中异常表达[5-8]。
研究发现蛋白酶抑制剂利托那韦(ritonavir, RTV)可有效降低KSHV的致病性。RTV是否通过抑制LYN而抑制KSHV的致病性目前尚不清楚。本研究旨在探讨RTV对KSHV感染细胞HUVECs中LYN表达及活性的影响。
1 材料与方法 1.1 材料实验所用的新生儿脐带取自石河子大学医学院第一附属医院育龄健康产妇剖宫产后的新鲜胎儿脐带组织。实验方案经医学院伦理委员会批准,产妇及家属均签署知情同意书。
主要试剂:RPMI 1640培养液、ECM培养液、0.25%胰酶-EDTA、胎牛血清、青霉素、链霉素购自美国Gibco公司;CCK8试剂购自上海同仁公司;LYN购自加拿大BD公司,p-PI3K和p-AKT抗体购自美国Cell Signaling公司,β-actin购自北京中杉金桥公司;BCBL-1细胞系购自美国ATCC细胞库,RTV、RTV抑制剂PP2购自美国Sigma公司。
1.2 方法 1.2.1 细胞培养采用胶原酶灌注法原代培养HUVECs。将脐带用PBS浸泡,将磨平的50 ml注射器针头插入脐静脉。用PBS冲洗脐静脉,直至液体清亮。注入胶原酶,37℃水浴15 min。用培养液终止胶原酶反应,PBS冲洗脐静脉,并收集液体。800 r/min离心5 min后,将HUVECs接种于含5% FBS和1%ECGS的ECM培养液中培养,BCBL-1细胞用含5%FBS的RPMI 1640培养液培养,按常规37℃、5%CO2条件下培养,2~3天传代1次。所有实验操作均采用对数生长期细胞。
1.2.2 KSHV病毒感染HUVECsBCBL-1细胞为含有KSHV病毒的细胞,PMA刺激BCBL-1细胞72 h,用不含PMA的培养液培养24 h,收集细胞。在液氮和60℃水浴中反复冻融,使细胞膜破碎,离心,收集上清液(含KSHV)。用病毒:ECM培养液=1:5的病毒滤液感染HUVECs 48 h。
1.2.3 PCR扩增KS330233鉴定KSHV感染KSHV感染HUVECs48 h后,严格按照操作说明书提取细胞DNA,用PCR方法检测KSHV特异性序列KS330233。KS330233上游引物:3’-TCCGTGTTGTCTACGTCCAG-5’;下游引物:3’-AGCCGAAAGGA TTCCACCAT-5’。PCR反应条件:94℃ 5 min,94℃ 30 s,55℃ 30 s,72℃ 45 s,72℃ 5 min,4℃;35个循环。反应产物行2%琼脂糖凝胶电泳。
1.2.4 CCK8法测定RTV作用于HUVECs的最适浓度KSHV感染HUVECs48h后经0.25%胰酶消化,接种于96孔板中,每孔100 μl ECM培养液含3 000个细胞,培养8 h后,每孔加入终浓度分别为10、20、30、40、50 μmol/L的RTV。对照组加相应量的DMSO,另设空白组(只加培养液,无细胞),每组设3个复孔,加完RTV,继续培养48 h后每孔加入CCK8 10 μl,避光振荡摇匀,4 h后终止培养。在酶标仪上检测450 nm处的吸光度值(A450)。细胞生长抑制率(%)=(对照组A450值-实验组A450值)/(对照组A450值-空白组A450值)×100%。根据吸光度值计算细胞生长半数抑制浓度(half maximal inhibitory concentration, IC50),将IC50作为RTV作用于细胞的最适浓度。
1.2.5 RTV与LYN抑制剂PP2对KSHV感染的HUVECs细胞增殖能力的检测根据上述CCK8的IC50值选择RTV终浓度25 μmol/L处理KSHV感染的HUVECs。KSHV感染HUVECs 48 h后,换不含KSHV的培养液,实验组分别加入终浓度为25 μmol/L的RTV和10 μmol/L的PP2[9],对照组加同等量的DMSO,分别培养1、2、3、4、5 d后,采用CCK8法(操作同上)测定细胞增殖能力的变化。同时,培养72 h后,显微镜下观察细胞并分别提取各处理组总蛋白。
1.2.6 Western blot检测LYN、p-PI3K及p-AKT蛋白表达将实验组和对照组HUVECs分别用PBS洗涤3次,然后用预冷的含有蛋白酶抑制剂和磷酸酶抑制剂的细胞裂解液,按照说明书提取总蛋白,紫外分光光度计测定细胞蛋白浓度。测体积,加入相应量的4×上样缓冲液混匀煮沸8 min后上样行SDS-PAGE电泳。将凝胶中分离的蛋白电转至PVDF膜上,用含5%脱脂奶粉的TBST缓冲液室温封闭2 h,孵育一抗LYN(1:500)、p-PI3K(1:1 000)、p-AKT(1:1 000)和β-actin(1:10 000)4℃摇床过夜。洗膜,加入TBST稀释的相应种属的辣根过氧化物酶标记的二抗孵育2 h,发光、显影、定影。
1.3 统计学方法采用SPSS 17.0统计软件进行统计处理。CCK8检测细胞增殖采用直线回归与相关分析及配对样本t检验,P < 0.05为差异有统计学意义。
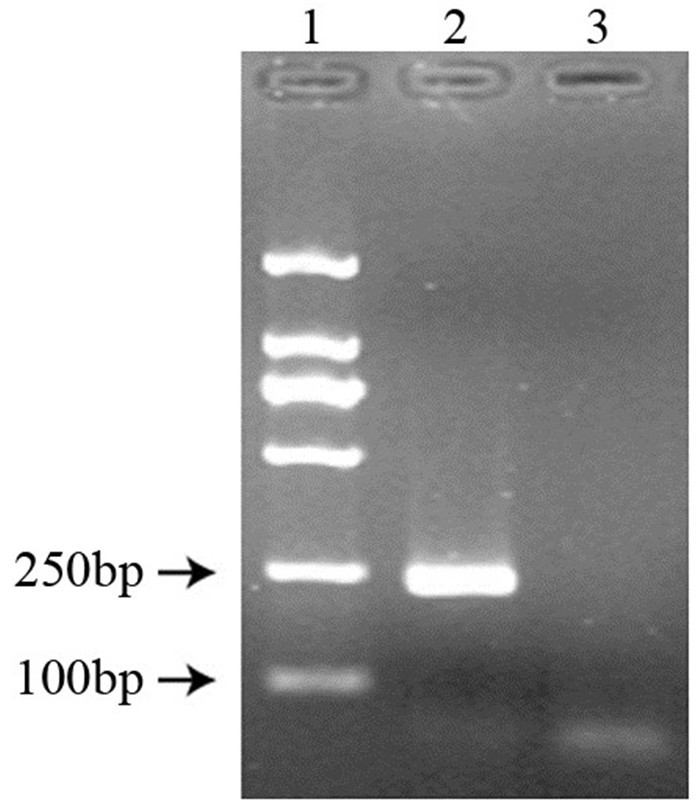
2 结果 2.1 PCR扩增KS330233鉴定KSHV成功感染HUVECsPCR检测结果所示KSHV感染HUVECs48 h后细胞内含有KSHV的特异性片段KS330233,证明感染成功,见图 1。
|
| 1: DNA marker; 2: KSHV infection; 3: Negative control 图 1 PCR扩增KS330233结果 Figure 1 Result of KS330233 amplified by PCR |
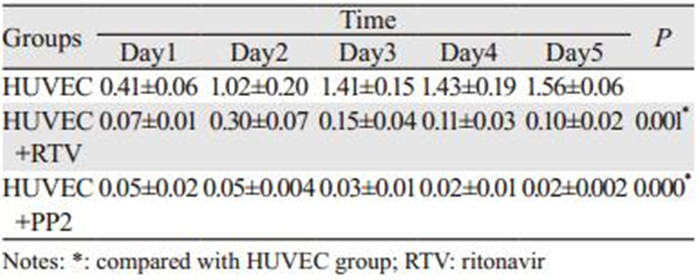
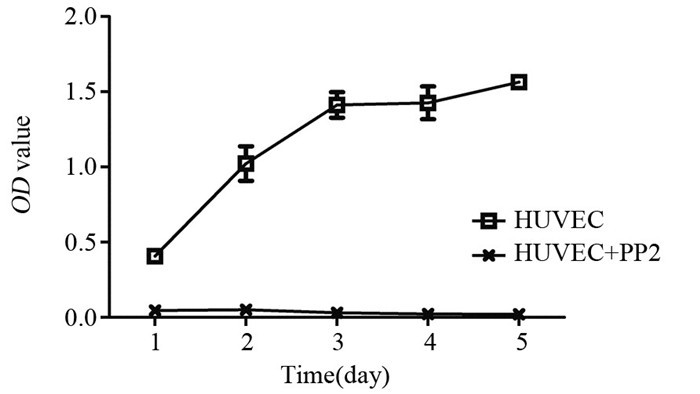
用不同浓度(10、20、30、40、50 μmol/L)RTV处理经KSHV感染后的HUVECs细胞,48 h后根据A450值计算IC50。以不同RTV的浓度与KSHV感染的HUVECs细胞增殖抑制率作直线回归与相关分析,结果显示RTV作用48 h,IC50为25.443 μmol/L,r=0.958, P < 0.05。以RTV终浓度25 μmol/L分别培养1~5 d,HUVEC+RTV与HUVEC组相比,细胞增殖抑制率差异有统计学意义(P=0.001)。随着时间延长,A450值逐渐降低,见表 1。表明RTV与KSHV感染的HUVECs细胞增殖的抑制率之间有显著的浓度、时间依赖关系。用10 μmol/L PP2处理KSHV感染的HUVECs,分别培养1~5 d,随着时间延长,实验组A450值均处于低水平,HUVEC+PP2与HUVEC组相比,差异有统计学意义(P=0.000),表明PP2可抑制KSHV感染细胞HUVECs增殖,见图 2。
|
|
| 图 2 PP2作用KSHV感染HUVECs细胞不同时间后对细胞增殖的影响 Figure 2 Effect of PP2 on proliferation of KSHV-infected HUVECs at different time |
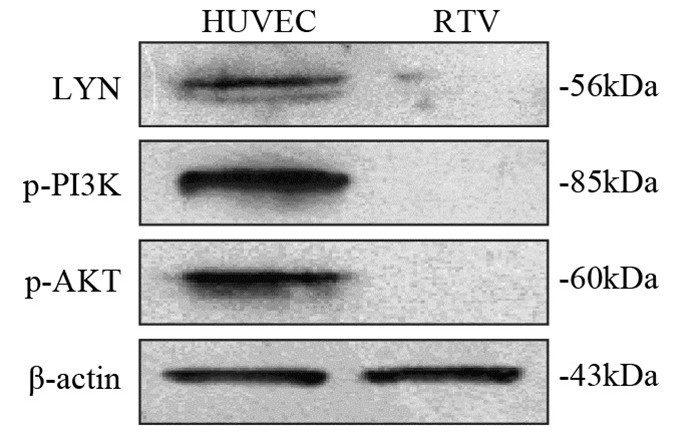
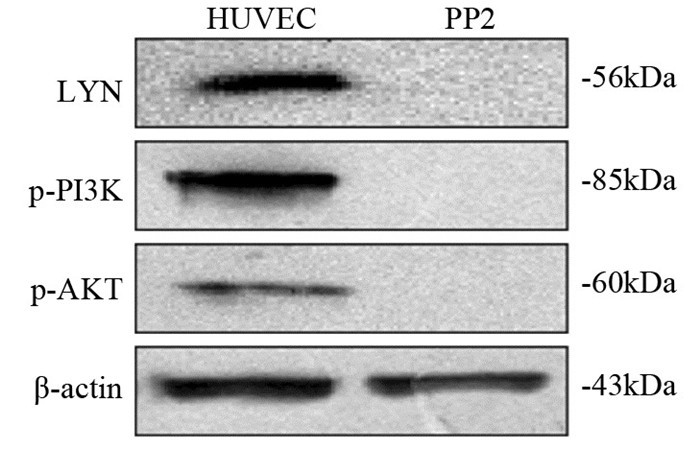
Western blot结果显示RTV组LYN蛋白表达明显受到抑制,并且p-PI3K和p-AKT表达也受到抑制,见图 3。PP2为LYN抑制剂,Western blot结果显示PP2组LYN明显受到抑制,表现为不表达。并且p-PI3K和p-AKT表达也受到抑制,见图 4。
|
| 图 3 RTV对KSHV感染HUVECs细胞中LYN、p-PI3K和p-AKT蛋白表达的影响 Figure 3 Effect of RTV on expression of LYN, p-PI3K and p-AKT in KSHV-infected HUVECs |
|
| 图 4 PP2对KSHV感染HUVECs细胞中LYN、p-PI3K和p-AKT蛋白表达的影响 Figure 4 Effect of PP2 on expression of LYN, p-PI3K and p-AKT in KSHV-infected HUVECs |
KSHV感染引起的KS是AIDS患者主要死亡原因之一,在KS治疗过程中,抗病毒治疗比较关键,因此开展抗KSHV相关药物研究具有重要临床意义。高效抗反转录病毒(highly-active antiretroviral, HAART)疗法在治疗AIDS的同时,降低了33%~95%的KS发病率,KS患者单纯用HAART治疗,好转率达到35%[10]。Cattamanchi等[11]监测了HIV和KSHV共感染患者咽拭子KSHV载量,发现HAART疗法与89%的患者KSHV流出减少有关。Sullivan等[12]检测了HIV患者用HAART疗法一年前后血清中KSHV的潜伏态和裂解态抗体以及病毒载量,认为HAART疗法可以加强机体抗KSHV的特异性免疫反应,从而抵抗KS的发生。HAART疗法的药物中包括蛋白酶抑制剂[13],其典型代表就是RTV。Barillari等[14]发现蛋白酶抑制剂可抑制肿瘤生长和肿瘤血管形成,可能是KS治疗的新方法。Lucia等[15]发现蛋白酶抑制剂药物效果与KS中ABCB1有关。Gantt等发现在体外蛋白酶抑制剂可以抑制KSHV复制[16]。蛋白酶抑制剂可能抑制KSHV感染的致病性,但其在KS中发挥作用的药物靶点和机制目前还不清楚。
我们在前期研究中发现KSHV感染的KS组织中,LYN表达增高。近期研究报道也提示LYN过表达与肿瘤的发生发展存在相关性。Sutton等发现在肺癌中LYN可激活PI3K/AKT信号通路[17]。本研究中用KSHV体外感染HUVECs来模拟KS的致病过程,发现KSHV感染后LYN表达增高。通过检测LYN抑制剂RTV和PP2对KSHV感染的HUVECs增殖的影响,发现它们均可抑制KSHV感染的HUVECs的增殖,提示LYN可能是RTV治疗KSHV感染疾病的药物作用靶点,其机制可能是通过抑制LYN表达及其下游的PI3K/AKT通路起作用。
本研究将RTV与KSHV感染联系起来,为临床寻找治疗KSHV感染相关疾病的药物靶点提供了新的思路。
| [1] | Zhang D, Pu X, Wu W, et al. Genotypic analysis on the ORF-K1 gene of human herpesvirus 8 from patients with Kaposi's sarcoma in Xinjiang, China[J]. J Genet Genomics, 2008, 35(11): 657–63. DOI:10.1016/S1673-8527(08)60087-9 |
| [2] | 李冬妹, 杨磊, 仙玲玲, 等. 用抑制性差减杂交构建新疆Kaposi肉瘤差异表达基因文库[J]. 中国生物工程杂志, 2005, 25(8): 65–9. [ Li DM, Yang L, Xian LL, et al. Construction of Differential Library of Xinjiang Kaposi's Sarcoma by Suppression Subtractive Hybridization[J]. Zhongguo Sheng Wu Gong Cheng Za Zhi, 2005, 25(8): 65–9. ] |
| [3] | 李冬妹, 张慧, 罗先道, 等. Kaposi肉瘤组织中lyn基因的表达分析[J]. 中国皮肤科杂志, 2010, 43(4): 256–8. [ Li DM, Zhang H, Luo XD, et al. Expression of lyn gene in Kaposi's sarcoma[J]. Zhongguo Pi Fu Ke Za Zhi, 2010, 43(4): 256–8. ] |
| [4] | Tan X, Li D, Wang X, et al. Claudin-2 downregulation by KSHV infection is involved in the regulation of endothelial barrier function[J]. J Cutan Pathol, 2014, 41(8): 630–9. DOI:10.1111/cup.2014.41.issue-8 |
| [5] | Thomas SM, Brugge JS. Cellular functions regulated by Src family kinases[J]. Annu Rev Cell Dev Biol, 1997, 13: 513–609. DOI:10.1146/annurev.cellbio.13.1.513 |
| [6] | Tabaries S, Annis MG, Hsu BE, et al. Lyn modulates Claudin-2 expression and is a therapeutic target for breast cancer liver metastasis[J]. Oncotarget, 2015, 6(11): 9476–87. DOI:10.18632/oncotarget |
| [7] | Wang X, Wen J, Li R, et al. Gene expression profiling analysis of castration-resistant prostate cancer[J]. Med Sci Monit, 2015, 21: 205–12. DOI:10.12659/MSM.891193 |
| [8] | Huang TH, Huo L, Wang YN, et al. Epidermal growth factor receptor potentiates MCM7-mediated DNA replication through tyrosine phosphorylation of Lyn kinase in human cancers[J]. Cancer Cell, 2013, 23(6): 796–810. DOI:10.1016/j.ccr.2013.04.027 |
| [9] | Jensen HA, Bunaciu RP, Varner JD, et al. GW5074 and PP2 kinase inhibitors implicate nontraditional c-Raf and Lyn function as drivers of retinoic acid-induced maturation[J]. Cell Signal, 2015, 27(8): 1666–75. DOI:10.1016/j.cellsig.2015.03.014 |
| [10] | Semeere AS, Busakhala N, Martin JN. Impact of antiretroviral therapy on the incidence of Kaposi's sarcoma in resource-rich and resource-limited settings[J]. Curr Opin Oncol, 2012, 24(5): 522–30. DOI:10.1097/CCO.0b013e328355e14b |
| [11] | Cattamanchi A, Saracino M, Selke S, et al. Treatment with valacyclovir, famciclovir, or antiretrovirals reduces human herpesvirus-8 replication in HIV-1 seropositive men[J]. J Med Virol, 2011, 83(10): 1696–703. DOI:10.1002/jmv.v83.10 |
| [12] | Sullivan SG, Hirsch HH, Franceschi S, et al. Kaposi sarcoma herpes virus antibody response and viremia following highly active antiretroviral therapy in the Swiss HIV Cohort study[J]. AIDS, 2010, 24(14): 2245–52. DOI:10.1097/QAD.0b013e32833b7830 |
| [13] | Kyeyune R, Saathoff E, Ezeamama AE, et al. Prevalence and correlates of cytopenias in HIV-infected adults initiating highly active antiretroviral therapy in Uganda[J]. BMC Infect Dis, 2014, 14: 496. DOI:10.1186/1471-2334-14-496 |
| [14] | Barillari G, Sgadari C, Toschi E, et al. HIV protease inhibitors as new treatment options for Kaposi's sarcoma[J]. Drug Resist Updat, 2003, 6(4): 173–81. DOI:10.1016/S1368-7646(03)00060-8 |
| [15] | Lucia MB, Anu R, Handley M, et al. Exposure to HIV-protease inhibitors selects for increased expression of P-glycoprotein (ABCB1) in Kaposi's sarcoma cells[J]. Br J Cancer, 2011, 105(4): 513–22. DOI:10.1038/bjc.2011.275 |
| [16] | Gantt S, Carlsson J, Ikoma M, et al. The HIV protease inhibitor nelfinavir inhibits Kaposi's sarcoma-associated herpesvirus replication in vitro[J]. Antimicrob Agents Chemother, 2011, 55(6): 2696–703. DOI:10.1128/AAC.01295-10 |
| [17] | Sutton P, Borgia JA, Bonomi P, et al. Lyn, a Src family kinase, regulates activation of epidermal growth factor receptors in lung adenocarcinoma cells[J]. Mol Cancer, 2013, 12: 76. DOI:10.1186/1476-4598-12-76 |
 2017, Vol. 44
2017, Vol. 44


