文章信息
- 前列腺腺癌组织中HPV16/18蛋白的表达及意义
- Expression and Significance of HPV16/18 Protein in Prostate Cancer Tissues
- 肿瘤防治研究, 2017, 44(2): 129-132
- Cancer Research on Prevention and Treatment, 2017, 44(2): 129-132
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.02.010
- 收稿日期: 2016-06-20
- 修回日期: 2016-12-25
2. 545005 柳州,广西医科大学第四附属医院泌尿外科
2. Department of Urology, The Fourth Affiliated Hospital of Guangxi Medical University, Liuzhou 545005, China
前列腺癌是泌尿生殖系统常见的恶性肿瘤之一,其发生发展与年龄因素、家族遗传性因素及种族因素等多种因素有关[1],但其发病具体机制尚不明确。既往文献报道人乳头瘤病毒(human papillomaviruses,HPV)尤其是高危型16/18与阴茎癌、肾癌、肺癌等多种肿瘤的发生发展相关[2]。关于HPV与前列腺癌的关系,国外早有报道,但国内相关文献报道罕见。本研究应用免疫组织化学Max Vision二步法对86例前列腺腺癌(prostate cancer)和80例良性前列腺增生(benign prostatic hyperplasia,BPH)标本进行HPV16/18检测,旨在探讨两组中的表达差异及与病理参数的关系。
1 资料与方法 1.1 资料病例组86例标本均取自2011—2015年间在广西医科大学第四附属医院泌尿外科行前列腺穿刺或手术切除的标本,并同时经我院病理科两位高年资病理医师诊断均为前列腺腺癌,术前未接受手术去势、药物去势或放化疗治疗。患者年龄50~88岁,平均年龄为(70.5±6.9)岁,参照《2014版中国泌尿外科疾病诊断指南》,按以下方法分组:(1)Gleason评分:根据评分分成两组(高-中分化组:≤7分、低分化组:>7分);(2)PSA值:分为4组(<4、4~10、>10~20、>20 ng/ml);(3)脉管侵犯:分成有脉管侵犯和无脉管侵犯2组;(4)淋巴结转移:分成有淋巴结转移和无淋巴结转移两组;(5)远处转移:分成有远处器官转移和无远处器官转移两组;(6)临床分期:分为T1+T2组和T3+T4组。对照组80例标本取自同时期在我院就诊的经穿刺或手术切除的前列腺增生标本,年龄55~85岁,平均年龄为 (71.7±7.3)岁。两组年龄比较差异无统计学意义。
1.2 方法所有实验标本经10%中性福尔马林固定、脱水、石蜡包埋,作5 μm连续切片,采取Max Vision两步法,无需修复。操作严格按照试剂说明书进行,实验同时设有阳性对照和空白对照。阳性对照采用HPV16/18感染的宫颈癌标本,空白对照采用PBS代替一抗,余实验步骤及条件均一致。一抗和二抗均购买于福州迈新公司。
1.3 结果判读前列腺增生和前列腺癌组织中HPV16/18着色定位于细胞胞核,染色呈现棕黄色颗粒即判读为阳性。着色部位出现在其他部位,或者在细胞核部位不着色即判读为阴性。
1.4 统计学方法所有检验均使用SPSS16.0软件进行分析,病例组与对照组之间的差异以及HPV16/18表达与前列腺腺癌组各临床病理参数之间的相关性比较采用卡方检验。P<0.05为差异有统计学意义。
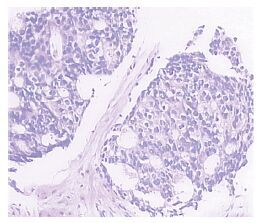
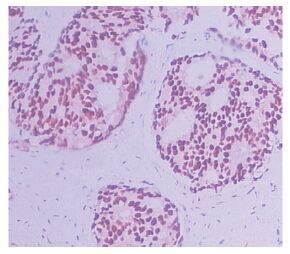
2 结果 2.1 HPV16/18在前列腺腺癌和前列腺增生组中的表达情况通过免疫组织化学检测,在前列腺腺癌细胞核中可见棕黄色颗粒着色,见图 1~2。通过数据统计,在86例前列腺腺癌组中HPV16/18阳性表达率为22.58%(22/86);在80例前列腺增生组中HPV16/18阳性表达率为11.25%(9/80),差异有统计学意义(χ2 =5.605,P=0.018)。
|
| 图 1 前列腺腺癌的病理形态 (IHC×100) Figure 1 Pathological morphology of prostatic adenocarcinoma (IHC×100) |
|
| 图 2 HPV16/18在前列腺腺癌中的表达 (IHC×100) Figure 2 Expression of HPV16/18 in prostate cancer tissues (IHC×100) |
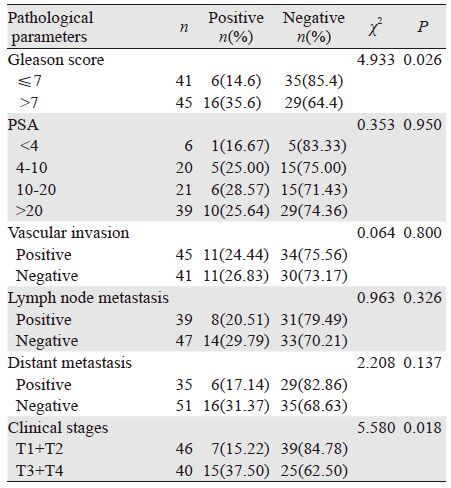
为了探讨HPV16/18的表达与前列腺腺癌组各临床病理参数之间的关系,本研究对比了前列腺腺癌中Gleason评分、PSA水平、有无脉管侵犯、有无淋巴结转移、有无远处转移、临床分期的HPV16/18表达情况,结果显示:HPV16/18的表达与Gleason评分和临床分期有一定的关系。在Gleason评分高-中分化组、低分化组,其阳性表达率分别为14.6%和35.6%,随评分越高,阳性率越高,差异有统计学意义(χ2=4.933,P=0.026)。在T1+T2和T3+T4分期组中的阳性表达率分别为15.22%及37.5%,差异有统计学意义(χ2=5.58,P=0.018),而与患者PSA水平、有无脉管侵犯、有无淋巴结转移和有无远处转移关系不大,差异无统计学意义(均P>0.05),见表 1。
 |
目前前列腺癌的发病率越来越高,但是早期前列腺癌的症状和体征同良性前列腺增生症无法区分。临床上常通过检测血清PSA来进行筛查,但具有一定的漏诊率。肿瘤的发生本身就是一个多因素、多步骤的过程,多种方法联合检测、评估可以提高肿瘤的检测率,从而达到早诊断、早治疗的目的。
人类乳头状瘤病毒属于多瘤病毒科,是一组形态和基因结构相似的特异性嗜人上皮细胞的小双链DNA病毒、无包膜、直径50~55 nm;其基因组大小约6.8~8.0 kb,由8个开放读码框架(open reading frame,ORF)和含有调节单位的非编码区(uncoding region,UCR)组成[3]。HPV具有严格的种属特异性,依据其引起病变的临床预后不同分为高危型和低危型,HPV16/18属于高危型,主要通过性生活接触传播。HPV通过皮肤黏膜的破损进入人体,感染具有增殖能力的皮肤或黏膜基底层细胞,并随着细胞的分化到达表层,进行大量的病毒复制并组装成熟、释放[4]。HPV病毒DNA则是以单拷贝或多拷贝的形式整合于细胞基因组中,并导致宿主基因组的改变,从而引起宿主染色体的不稳定性[5]。致癌机制主要是通过病毒转化蛋白E6、E7作用于细胞的癌基因和抑癌基因(包括 P53,Rb)而实现。
随着大家对HPV研究的越来越深入,HPV16/18与人类的某些恶性肿瘤的发生有密切关系,大量资料显示,HPV感染与宫颈癌、阴茎癌、睾丸肿瘤、膀胱癌、口咽部癌、肺癌等[6-11]多种肿瘤的发生有密切的关系。但HPV感染与前列腺腺癌的关系世界各地报道不一,且国内罕见报道。本研究发现,HPV16/18的表达在前列腺腺癌组明显高于前列腺增生组,差异有统计学意义(χ2=5.605,P=0.018)。Jalilvand等[12]发现,前列腺癌中HPV的表达率为10.4%,高于对照组,尤其是16/18型。Singh等[13]发现,前列腺癌组患者的HPV16/18的表达率高于前列腺增生组(P=0.0004),这就显示,HPV16/18与前列腺癌的发生有一定的相关性,本研究与部分学者研究成果相似。Aghakhani等[14]却持不同意见,他们的研究表示HPV16/18的表达在两组中无明显差异,HPV不参与前列腺癌的发生发展。反复思考其原因,其一可能与研究方法与标本量有关,各研究采用的方法不同,结果可能有所出入;标本量的大小也有可能对研究数据有影响。其二,不同地区研究标本的地域性、种族性、性生活方式等多种原因都有可能造成研究指标数值的波动。
在前列腺腺癌组内,通过比较各临床病理参数,发现HPV16/18的表达与Gleason评分和肿瘤的分期有关,Gleason评分越高,HPV16/18的表达率越高,差异有统计学意义(P=0.023)。肿瘤T3+T4组的表达率高于T1+T2组,差异有统计学意义(P=0.018)。但在PSA水平、有无脉管侵犯、有无淋巴结转移、有无远处转移方面差异无统计学意义(均P>0.05)。Gleason评分越高,肿瘤分化越差,侵袭能力越强,相应的肿瘤分期高的可能性越大,所以,本研究中Gleason评分和肿瘤的分期存在一致性,这与Singh等[13]的研究也是相似的,我们猜测,HPV16/18在前列腺癌的疾病进展中是否也发挥一定的作用,有待我们今后的进一步研究。
综上所述,HPV16/18在前列腺腺癌的表达明显高于前列腺增生组,且与肿瘤的Gleason评分和分期有关,说明HPV16/18参与前列腺腺腺癌的发生和发展,但具体机制目前尚无定论,有待我们进一步研究。从本研究中,我们可以得出一些提示,HPV16/18的检测是提高前列腺腺癌检测率的又一方法。
| [1] | Wang GM, Chen W. Progress and development trend of treatment for urological tumor[J]. Zhong Liu Fang Zhi Yan Jiu, 2014, 41 (2) : 97–9. [ 王国民, 陈伟. 泌尿系统肿瘤治疗的进展与展望[J]. 肿瘤防治研究, 2014, 41 (2) : 97–9. ] |
| [2] | Jalilvand S, Shoja Z, Hamkar R. Human papillomavirus burden in different cancers in Iran: a systematic assessment[J]. Asian Pac J Cancer Prev, 2014, 15 (17) : 7029–35. DOI:10.7314/APJCP.2014.15.17.7029 |
| [3] | Pizzol D, Putoto G, Chhaganial KD. Human papillomavirus (HPV) infection: a Mozambique overview[J]. Virusdisease, 2016, 27 (2) : 116–22. DOI:10.1007/s13337-016-0319-7 |
| [4] | Kajitani N, Satsuka A, Kawate A, et al. Productive lifecycle of human papillomaviruses that depends upon squamous epithelial differentiation[J]. Front Microbiol, 2012, 3 : 152–64. |
| [5] | Trottier H, Burchell AN. Epidemiology of Mucosal Human Papillomavirus Infection and Associated Diseases[J]. Public Health Genomics, 2009, 12 (5-6) : 291–307. DOI:10.1159/000214920 |
| [6] | Yang DX, Soulos PR, Davis B, et al. Impact of Widespread Cervical Cancer Screening: Number of Cancers Prevented and Changes in Race-specific Incidence[J]. Am J Clin Oncol, 2016, 22 (1) : 110–5. |
| [7] | Zhai JP, Li M, Wang QY, et al. Expression of CD82, hTERT protein and the relationship between HPV infection and penile cancer[J]. Zhonghua Nan Ke Xue Za Zhi, 2011, 17 (9) : 817–22. [ 翟建坡, 李鸣, 王其艳, 等. CD82、hTERT 蛋白的表达及HPV 感染与阴茎癌的关系研究[J]. 中华男科学杂志, 2011, 17 (9) : 817–22. ] |
| [8] | Feber A, Arya M, de Winter P, et al. Epigenetics markers of metastasis and HPV-induced tumorigenesis in penile cancer[J]. Clin Cancer Res, 2015, 21 (5) : 1196–206. DOI:10.1158/1078-0432.CCR-14-1656 |
| [9] | Kim SH, Joung JY, Chung J, et al. Detection of human papillomavirus infection and p16 immunohistochemistry expression in bladder cancer with squamous differentiation[J]. PLoS One, 2014, 9 (3) : e93525. DOI:10.1371/journal.pone.0093525 |
| [10] | Dvoryaninova OY, Chainzonov EL, Litvyakov NV. The clinical aspects of HPV-positive cancer of the oral cavity and oropharynx[J]. Vestn Otorinolaringol, 2016, 81 (1) : 72–7. DOI:10.17116/otorino201681172-77 |
| [11] | Colombara DV, Manhart LE, Carter JJ, et al. Prior human polyomavirus and papillomavirus infection and incident lung cancer: a nested case-control study[J]. Cancer Causes Control, 2015, 26 (12) : 1835–44. DOI:10.1007/s10552-015-0676-3 |
| [12] | Jalilvand S, Shoja Z, Hamkar R. Human papillomavirus burden in different cancers in Iran: a systematic assessment[J]. Asian Pac J Cancer Prev, 2014, 15 (17) : 7029–35. DOI:10.7314/APJCP.2014.15.17.7029 |
| [13] | Singh N, Hussain S, Kakkar N, et al. Implication of high risk Human papillomavirus HR-HPV infection in prostate cancer in Indian population-A pioneering case-control analysis[J]. Sci Rep, 2015, 5 : 7822. DOI:10.1038/srep07822 |
| [14] | Aghakhani A, Hamkar R, Parvin M, et al. The role of human papillomavirus infection in prostate carcinoma[J]. Scand J Infect Dis, 2011, 43 (1) : 64–9. DOI:10.3109/00365548.2010.502904 |
 2017, Vol. 44
2017, Vol. 44


