文章信息
- 外周血游离DNA含量和完整性的动态变化检测在胃癌诊治中的意义
- Significance of Content and Integrity Changes of Peripheral Blood Cell-free DNA in Diagnosis and Treatment in Gastric Cancer
- 肿瘤防治研究, 2017, 44(2): 118-123
- Cancer Research on Prevention and Treatment, 2017, 44(2): 118-123
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.02.008
- 收稿日期: 2016-05-23
- 修回日期: 2016-07-25
胃癌居消化系统的恶性肿瘤之首,近年来,“液体活检”十分火热,即仅通过患者的血液或其他体液来协助检测诊断病患。其中关于血浆或者血清中游离DNA在恶性肿瘤等疾病中的检测就是十分热门的一个研究领域。但是关于游离DNA的产生机制以及血清血浆的选择等仍然需要更进一步的研究。本实验采集胃癌患者的血浆和血清,提取其中的游离DNA,检测其含量和完整性的动态变化,探讨其在胃癌中的临床意义及两者之间的相关性。
1 资料与方法 1.1 一般资料收集苏州大学附属第一医院2015年1月至2016年3月就诊并入院的原发胃癌患者81例,其中男56例,女25例。年龄32~86岁,中位年龄65岁。按国际抗癌联盟/美国癌症联合委员会(UICC/AJCC)胃癌TNM分期标准(2010)分期,其中0期2例、Ⅰ期15例、Ⅱ期17例、Ⅲ期30例、Ⅳ期17例。诊断均经组织病理学证实,均无其他并发症,且所有患者均排除乙型肝炎、HIV等病毒感染性疾病,无系统性红斑狼疮、类风湿性关节炎等免疫性疾病,且无急性感染或创伤。同期选取18例胃良性肿瘤患者(包括8例胃平滑肌瘤,10例胃间质瘤)以及19例胃癌前病变(良性病变)的患者(5例胃溃疡,6例慢性萎缩性胃炎以及8例胃多发息肉),选取同期门诊健康体检者43例作为正常对照,其中男28例,女15例,年龄35~76岁,中位年龄62岁。
1.2 血浆和血清样本的采集与保存血清:于胃癌患者初诊未治疗前,取3 ml外周血于促凝管中,静置30 min,1600 r/min离心10 min,取上清液,置于-80℃冰箱中保存备用,其他组标本采取同样的采集方法。血浆:取3 ml外周血于EDTA抗凝管中,1 600 r/min离心10 min,取上清液,再16 000 r/min离心10 min,取上清液置于-80℃冰箱中保存备用。
1.3 血清DNA的提取按照QIACube DNA提取仪及微量血液基因组提取试剂盒说明书(QIAamp DNA Blood Mini Kit,Qiagen)提取血清游离DNA,提取分装后置 -80℃保存。
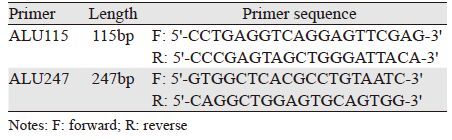
1.4 标准品的制备以及引物的设计和合成提取人基因组DNA作为标准品,由紫外分光光度计测量其原始浓度,倍比稀释至4×10-2、4×10-1、4、4×101、4×102 ng/ml 作为标准品。本试验根据人管家基因ALU重复序列设计的两对引物(ALU115和ALU247[1])的上下游序列以及片段长度见表 1。
于Light Cycler 480Ⅱ上扩增提取的DNA,质粒标准品,阴性对照(ddH2O),PCR总体系为SYBR Green Real Master Mix 9 μl,200 nmol/L上、下游引物各1 μl,双蒸水7 μl,模板2 μl。反应条件:94℃预变性1 min;94℃ 30 s,62℃ 20 s,72℃ 30 s,共45次循环。根据标准品的浓度梯度PCR仪自动分析绘制标准曲线,并根据标准曲线对内参基因进行定量分析以及绘制熔解曲线,血清游离DNA的完整性以247 bp的ALU247含量与115 bp的ALU115含量的比值定义。所有样本均设 2个复孔。
1.6 统计学方法所有数据的分析均采用SPSS19.0软件,数据经验证不符合正态分布,以中位数和四分位数间距表示,两组计量数据组间比较采用非参数检验Mann-Whitney U检验,多组计量数据组间比较采用非参数检验Kruskal-Wallis检验。不服从双变量正态分布的资料相关性采用Spearman相关性检验。以P<0.05为差异有统计学意义。
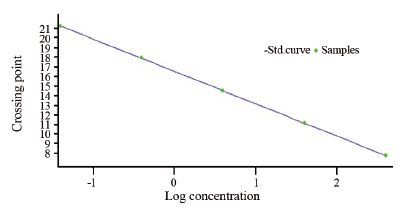
2 结果 2.1 标准曲线的建立成功构建浓度梯度的人基因组DNA质粒标准品的扩增曲线,见图 1。回归方程:Y=-3.368logX+16.50,R2=0.991,扩增效率E=0.981。ALU115和ALU247目的基因的熔解曲线也无杂峰。电泳图见图 2。
|
| Notes: F: forward; R: reverse 图 1 内参基因β-actin扩增的标准曲线 Figure 1 The standard curve of reference gene beta-actin amplification |

|
| 1-5: electrophoresis bands of 247bp ALU gene; 6-10: electrophoresis bands of 115bp ALU gene 图 2 ALU115和ALU247两片段电泳图 Figure 2 Electrophoresis of the two segments (ALU115 and ALU247) |
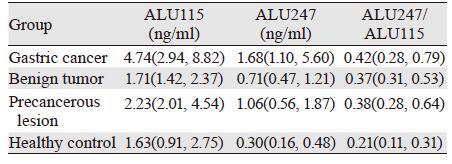
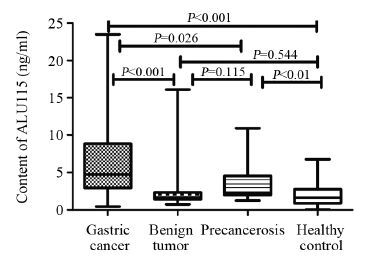
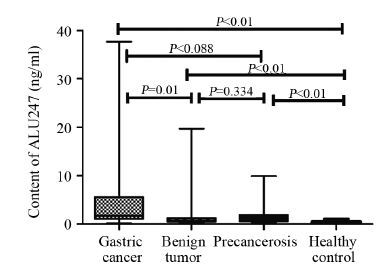
各组ALU115和ALU247的含量见表 2。经分析,两片段基因在四组之间的差异均有统计学意义(H值分别为50.912、79.106,均P<0.001)。ALU115片段在胃癌组中的值显著高于胃良性肿瘤、胃癌前病变以及健康对照组(U值分别为50.562、26.395、58.511,P值分别为0.000、0.026、0.000),但胃良性肿瘤组、癌前病变组、健康对照组之间比较差异无统计学意义(U值分别为-24.167、7.950,P值分别为0.115、0.544),见图 3。ALU247片段在胃癌组的值同样显著高于胃良性肿瘤组和健康对照组(U值分别为35.086、77.772,均P<0.01),同时健康对照组、胃良性肿瘤、胃癌前病变组之间比较,差异也有统计学意义(U值分别为42.686、57.502,均P<0.01)。但胃癌前病变组和胃癌组以及胃良性肿瘤组之间比较,差异无统计学意义(U值分别为20.271、-14.816,P值分别为0.088、0.334),见图 4。
 |
|
| 图 3 ALU115在各组之间的比较 Figure 3 Comparison between ALU115 in each group |
|
| 图 4 ALU247在各组之间的比较 Figure 4 Comparison between ALU247 in each group |
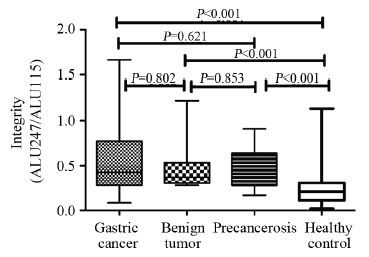
各组间血浆游离DNA完整性的差异均有统计学意义(H=37.173,P<0.001),健康对照组的值均显著低于胃癌组、胃良性肿瘤组以及胃癌前病变组(U值分别为51.830、48.787、45.953,均P<0.001),胃癌和胃良性肿瘤以及胃癌前病变组之间比较,差异无统计学意义(U值分别为3.043、5.877,P值分别为0.802,0.621),胃良性肿瘤和胃癌前病变之间比较,差异也无统计学意义(U=2.833,P=0.853),见表 2。各组之间定量和完整性的比较,见图 3~5。
|
| 图 5 完整性在各组之间的比较 Figure 5 Comparison the integrity between each group |
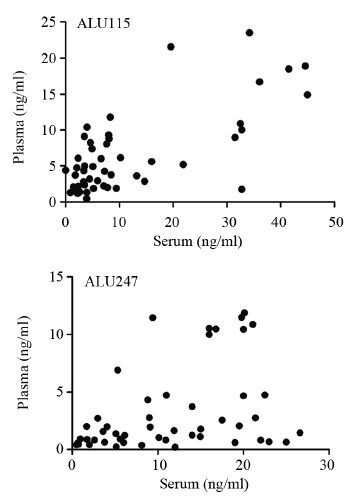
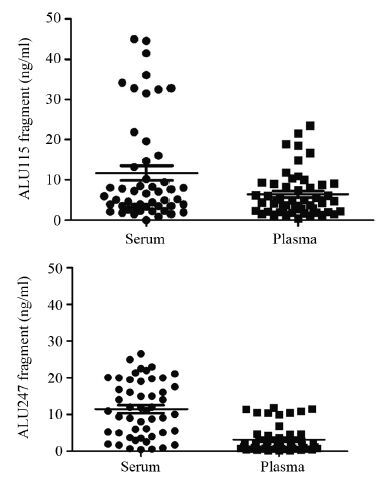
本实验同时选取了50例胃癌患者血清游离DNA的ALU115和ALU247的含量,探索其与血浆游离DNA含量的相关性。得出ALU115的相关系数r=0.592,两者之间显著相关(P<0.001),ALU247的相关系数r=0.400,P=0.02。两者血清和血浆比较的散点图见图 6。其中,两者血清中的含量均显著高于血浆,且范围和离散趋势更大,见图 7。
|
| 图 6 ALU115片段、ALU247片段血清和血浆相关性比较散点图 Figure 6 ALU115 fragment,ALU247 fragment serum and plasma correlation comparison scatter plot |
|
| 图 7 ALU115片段、ALU247片段血清和血浆游离DNA含量散点图 Figure 7 Scatter plots of ALU115 fragment,ALU247 fragment serum and plasma cf-DNA content |
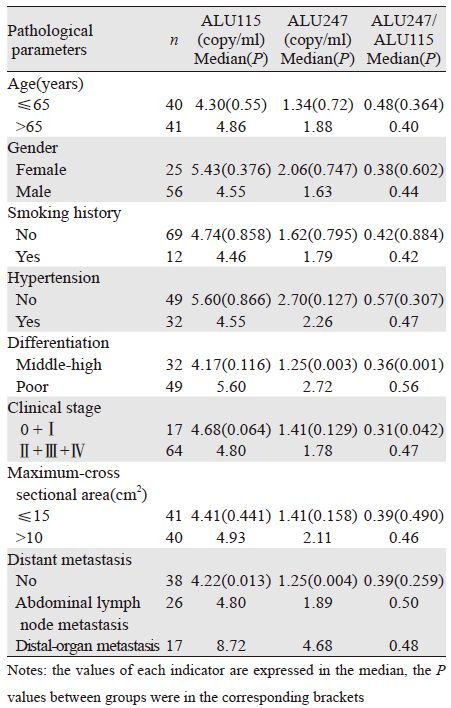
将胃癌患者按年龄、性别、有无吸烟史、有无高血压、分化程度、临床分期、肿块大小、是否合并转移等进行分组分析,结果表明,ALU115在肿瘤有无转移(腹腔淋巴结转移和远端脏器转移)上差异有统计学意义(H=8.612,P=0.013);ALU247在胃癌的分化程度上差异有统计学意义(U=3.009,P=0.003);在有无转移上差异也有统计学意义(H=11.265,P=0.004);完整性(ALU247/ALU115)在胃癌分化程度(U=3.236,P=0.001)和分期上差异有统计学意义(U=4.119,P=0.042),见表 3。
 |
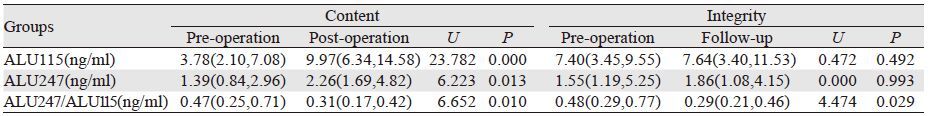
抽取36例胃癌患者术后3天内以及26例胃癌患者术后2月的血浆样本,测量其游离DNA的含量和完整性。术后ALU115和ALU247的含量均较术前高(U值分别为23.782、6.223;P值分别为0.000、0.013),而完整性则较术前低(U=6.652,P=0.010)。随访前后的ALU115和ALU247含量则差异无统计学意义,完整性随访后较随访前显著降低(U=4.474,P=0.029),见表 4。
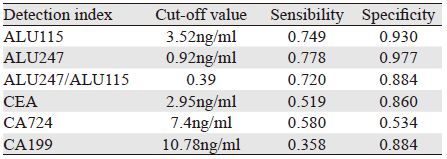 |
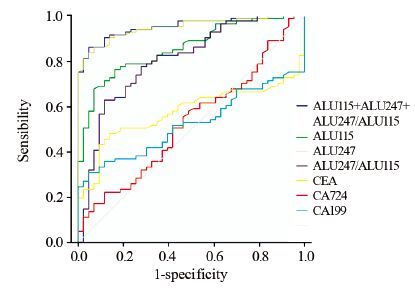
同时测量81例胃癌患者血清中CEA、CA724、CA199的含量,与游离DNA的含量作比较,得出AUCROC曲线下面积CEA、CA724、CA199、ALU115、ALU247、ALU247/ALU115分别为0.675、0.636、0.623、0.921、0.985、0.888;当采用ALU115+ALU247+完整性三个指标联合诊断时,其ROC曲线下面积达到0.986。当ALU247取0.92 ng/ml时,其敏感度为0.778,特异性为0.977,见图 8。各指标对应敏感度和特异性,见表 5。
|
| 图 8 各指标诊断的ROC曲线 Figure 8 ROC curves of various indexes |
研究表明,癌症患者血浆中游离DNA的含量是健康者的三到五倍,并且这些游离DNA含有与肿瘤相关的分子特性与改变[2]。在对血浆中游离DNA的定量方面,不同的研究者采用了不同的内参基因,包括β-actin[3]、GAPDH[4]等管家基因,他们具有稳定存在和表达的特征,但不同基因的拷贝量差异也决定了不同试验结果也不尽相同。近年来,更多研究倾向于采用非编码DNA,如ALU串联重复序列[5],ALU重复序列是人类基因组中最丰富的序列,每个基因组中有140万以上个拷贝,同时较编码基因甲基化更少,受影响也相对较小。Park等[5]在胃癌游离DNA的定量中即选用了81 bp的ALU内参基因,结果发现其在胃癌组和健康对照组有显著差异。
目前研究成果主要认为生物释放进入循环系统的核酸来源之一是生物体细胞坏死或凋亡[6]。正常细胞凋亡产生的游离DNA片段较小,只有100 bp左右,而细胞坏死产生的DNA片段相对较大,因此在机体发生恶性肿瘤等疾病状态下,由正常细胞亦或者是肿瘤细胞坏死产生的长片段的游离DNA含量相对较高。Jahr等[7]研究结果也发现在癌症的诊断中,长片段比短片段的敏感度和特异性更高;同样,针对结直肠癌的多片段研究[8]也证明了这一点。这为完整性的研究提供了理论依据。Umetani等[1]最早选用ALU115和ALU247两个基因片段作完整性的研究(ALU115的115 bp的短片段即包含在ALU247的247 bp的长片段内,两者有很好的相关性)。其结果表明,ALU247/ALU115不仅乳腺癌组显著高于健康组,在乳腺癌组内的比较中,淋巴结转移越多,分期越晚,乳腺癌内参基因完整性(ALU247/ALU115)相应也越高,原因可能是恶性肿瘤细胞经淋巴或血运播散,恶性程度越高,从死亡的肿瘤细胞释放到外周血中的长片段基因含量也越高。因此乳腺癌内参基因完整性和恶性肿瘤的侵袭和演进也有一定的相关性。本试验即采用了ALU基因的两个长短片段比值作胃癌完整性分析。
本试验结果表明,血浆游离DNA定量ALU247和ALU115长短片段在原发胃癌中的值显著高于其余三组,同时长片段在癌前病变组和健康组之间比较,差异也有统计学意义。这与Kim[9]、Park[5]等研究相符。原因可能是相比正常细胞凋亡产生的DNA片段、肿瘤细胞释放或者机体肿瘤负荷状态下细胞坏死释放的DNA片段更大更多(>200 bp)。同时健康组的完整性明显低于其他三组,这有可能成为癌症早期诊断的有效指标。
Lee等[10]对所选肺癌患者进行随访,发现较高的游离DNA含量往往跟肺癌患者的不良预后相关。本试验术后患者血浆游离DNA的含量显著升高,与Kim等[9]结果不符,其结果表明胃癌患者术后游离DNA的含量低于术前。原因可能是术后的应激状态或术后感染导致游离DNA暂时性的升高。同时随访时发现完整性较术前显著降低,表示机体体内可能处于恢复状态,体内的状态趋于稳定。因此血浆游离DNA的含量和完整性可以作为患者术后以及随访指标。
已有研究表明,游离DNA含量与乳腺癌淋巴结转移[11]、食管癌的肿瘤大小和远处转移[12]相关。本试验血浆游离DNA含量在有转移的胃癌(腹腔淋巴结转移和远端脏器转移)患者中均显著升高,表明游离DNA含量可以作为监测胃癌体内转移的指标。同时中晚期胃癌患者完整性值也显著高于早期胃癌患者,提示血浆游离DNA可以评估肿瘤的侵袭与演进,可以作为评价体内肿瘤负荷状态的指标。
目前究竟选择外周血样本的血清还是血浆用于胃癌的诊断和预后评估仍然有很多的讨论。Umetani等[13]认为,因为血浆中DNA以及凝血因子和相关蛋白均带负电荷等原因,血浆比血清的提取过程中更易丢失DNA;DNA血液分离的过程中会存在分配不均,因此作为肿瘤标志物检测,血浆比血清更适合。也有观点支持这一结论:因血清里加了促凝剂致白细胞更容易破碎,因此血清中存在白细胞中的DNA对游离DNA的污染(高分子量(>200 bp)。Park等[5]研究也认为,血浆中的游离DNA浓度范围相比血清大,且血清游离DNA含量在癌症组和正常组之间也有明显差异,因此血清的选择未必不如血浆。本试验结果表明,两片段在血浆和血清中均有明显的相关性,但是短片段的相关性明显大于长片段(相关系数r分别为0.592、0.400),其原因可能是长片段中存在着白细胞污染(>200 bp)。同时从二者的散点图可以看出,血清中的离散趋势相比血浆更大,因此血浆比血清更合适。
本试验同时存在着不足之处。首先,游离DNA的定量方面,目前没有研究对相同方法在不同实验室的结果的再现性进行评估,各个实验室之间也没有统一的实验方法,因此往往和其他实验室的研究结果存在差异。其次,为了使实验结果更可靠,后期需要加大样本量。同时为监测游离DNA对预后的作用,应该对患者进行长期的随访研究。
| [1] | Umetani N, Giuliano AE, Hiramatsu SH, et al. Prediction of breast tumor progression by integrity of free circulating DNA in serum[J]. J Clin Oncol, 2006, 24 (26) : 4270–6. DOI:10.1200/JCO.2006.05.9493 |
| [2] | CHUN FKH, Mueller I, Lange I, et al. Circulating tumour-associated plasma DNA represents an independent and informative predictor of prostate cancer[J]. BJU Int, 2006, 98 (3) : 544–8. DOI:10.1111/bju.2006.98.issue-3 |
| [3] | Tomita H, Ichikawa D, Ikoma D, et al. Quantification of circulating plasma DNA fragments as tumor markers in patients with esophageal cancer[J]. Anticancer Res, 2007, 27 (4C) : 2737–41. |
| [4] | Gang F, Guorong L, An Z, et al. Prediction of clear cell renal cell carcinoma by integrity of cell-free DNA in serum[J]. Urology, 2010, 75 (2) : 262–5. DOI:10.1016/j.urology.2009.06.048 |
| [5] | Park JL, Kim HJ, Choi BY, et al. Quantitative analysis of cell-free DNA in the plasma of gastric cancer patients[J]. Oncology Lett, 2012, 3 (4) : 921–6. |
| [6] | Choi JJ, Reich CF 3rd, Pisetsky DS. The role of macrophages in the in vitro generation of extracellular DNA from apoptotic and necrotic cells[J]. Immunology, 2005, 115 (1) : 55–62. DOI:10.1111/imm.2005.115.issue-1 |
| [7] | Jahr S, Hentze H, Englisch S, et al. DNA fragments in the blood plasma of cancer patients: quantitations and evidence for their origin from apoptotic and necrotic cells[J]. Cancer Res, 2001, 61 (4) : 1659–65. |
| [8] | Mouliere F, El Messaoudi S, Pang D, et al. Multi-marker analysis of circulating cell-free DNA toward personalized medicine for colorectal cancer[J]. Mol Oncol, 2014, 8 (5) : 927–41. DOI:10.1016/j.molonc.2014.02.005 |
| [9] | Kim K, Shin DG, Park MK, et al. Circulating cell-free DNA as a promising biomarker in patients with gastric cancer: diagnostic validity and significant reduction of cfDNA after surgical resection[J]. Ann Surg Treat Res, 2014, 86 (3) : 136–42. DOI:10.4174/astr.2014.86.3.136 |
| [10] | Lee YJ, Yoon KA, Han JY, et al. Circulating cell-free DNA in plasma of never smokers with advanced lung adenocarcinoma receiving gefitinib or standard chemotherapy as first-line therapy[J]. Clin Cancer Res, 2011, 17 (15) : 5179–87. DOI:10.1158/1078-0432.CCR-11-0400 |
| [11] | Agostini M, Enzo MV, Bedin C, et al. Circulating cell-free DNA: a promising marker of regional lymphonode metastasis in breast cancer patients[J]. Cancer Biomark, 2012, 11 (2-3) : 89–98. DOI:10.3233/CBM-2012-0263 |
| [12] | Tomochika S, Iizuka N, Watanabe Y, et al. Increased serum cell-free DNA levels in relation to inflammation are predictive of distant metastasis of esophageal squamous cell carcinoma[J]. Expe Thera Med, 2010, 1 (1) : 89–92. |
| [13] | Umetani N, Hiramatsu S, Hoon DSB. Higher Amount of Free Circulating DNA in Serum than in Plasma Is Not Mainly Caused by Contaminated Extraneous DNA during Separation[J]. Annals of the New York Academy of Sciences, 2006, 1075 (1075) : 299–307. |
 2017, Vol. 44
2017, Vol. 44