文章信息
- 低氧对前列腺癌PC3细胞上皮间质转化的影响
- Effect of Hypoxia on Epithelia-mesenchymal Transition of Prostate Cancer PC3 Cell
- 肿瘤防治研究, 2017, 44(2): 108-111
- Cancer Research on Prevention and Treatment, 2017, 44(2): 108-111
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.02.006
- 收稿日期: 2016-02-20
- 修回日期: 2016-06-15
2. 430060 武汉,武汉大学人民医院泌尿外科;
3. 430079 武汉,湖北省肿瘤医院泌尿外科
2. Department of Urology, Renming Hospital of Wuhan University, Wuhan 430060, China;
3. Department of Urology, Hubei Cancer Hospital, Wuhan 430079, China
前列腺癌为老年男性常见疾病,其发病率不断增高,居全球男性癌症发病率的第3位,癌症致死率第6位。我国前列腺癌发病率虽然远低于西方国家,但是近20年来随着人口老龄化及生活条件的改善,发病率逐渐增加。2009年,前列腺癌在我国男性恶性肿瘤发病率排名中排第6位[1]。
缺氧在实体肿瘤中的发生率约50%~60%[2],通常跟肿瘤进展、治疗抵抗和预后不良相关。在前列腺癌中,缺氧跟肿瘤进展相关,并且可能跟预后不良关系密切[3-4]。缺氧在恶性肿瘤侵袭与转移中发挥着重要作用,其中一个重要机制可能就是对肿瘤细胞上皮间质转化(epithelia- mesenchymal transition,EMT)的调节作用。EMT在胚胎早期发育、成体器官纤维化和肿瘤的发展中起着重要作用。本文拟探讨低氧对前列腺癌PC3细胞株上皮间质转化的影响,以此为肿瘤治疗提供一个思路。
1 材料与方法 1.1 材料前列腺癌PC3细胞株购自中国医学科学院基础医学研究所。HIF-1α兔抗人抗体、E-cadherin小鼠抗人抗体、N-cadherin兔抗人抗体和Vimentin兔抗人抗体均购自美国CST公司,羊抗鼠IgG二抗和羊抗兔IgG二抗均购自武汉博士德公司,ECL试剂盒购自美国Millipore公司。
1.2 方法 1.2.1 细胞培养常规培养条件是含10%胎牛血清(FBS)、100 u/ml青霉素和100 μg/ml链霉素的RPMI1640培养液,置于37℃、饱和湿度、5%CO2培养箱中培养。每日观察细胞生长情况,1~2天换液,待细胞长满至培养瓶80%左右传代,取生长状态良好的对数生长期细胞进行实验。分为常氧组和低氧组,分别置于常氧和低氧条件下培养24 h。低氧条件为使用低氧培养箱,调节气体浓度分别为O2 2%、N2 93%、CO2 5%,37℃培养,按设定的时间处理细胞。
1.2.2 细胞增殖MTT实验取96孔细胞培养板,每孔接种细胞约1×103个,分别在常氧和低氧条件下培养细胞24 h。每孔加MTT溶液(5 g/L)15 μl,37℃孵育4 h后每孔再加150 μl DMSO,振荡10 min,用酶联免疫检测仪读取每孔OD570nm值。
1.2.3 Matrigel侵袭实验将包被有Matrigel基质胶的Transwell小室放入24孔培养板中,上层加入200 μl无血清培养液单细胞悬液(含1×106个细胞),下室加入600 μl含10%胎牛血清培养液,常氧条件或低氧条件下培养24 h。用湿润的棉签擦去小室上层残留的基质胶和未穿过滤膜的细胞,4%多聚甲醛固定20 min,PBS漂洗3次,0.1%结晶紫染色10 min,PBS漂洗3次。取下聚碳酸酯微孔膜置于载玻片上,倒置显微镜下观察,任选5个视野(×200)计数,拍照。
1.2.4 Western blot检测分析提取细胞总蛋白,BCA法蛋白定量后分装、-70℃保存。取上述蛋白提取上清液(含蛋白约40 μg)进行聚丙烯酰胺凝胶电泳(SDS-PAGE,10%分离胶),将电泳分离后的蛋白质电转移至硝酸纤维素膜上,经封闭、洗脱后分别加入HIF-1α兔抗人抗体(1: 800),E-cadherin小鼠抗人抗体(1: 1 000)、N-cadherin兔抗人抗体(1: 1 000)和Vimentin兔抗人抗体(1: 1 000),4℃孵育过夜,洗膜后以相应的二抗室温孵育1 h,并以小鼠抗人β-actin单克隆抗体(1: 2 000)同上操作,作为上样对照。抗原—抗体复合物用ECL法显示,暗室X光胶片曝光。
1.2.5 免疫荧光检测细胞爬片后,先用4%多聚甲醛固定20 min,PBST反复漂洗3次,每次3 min;含0.5%胎牛白蛋白的PBST封闭2 h,PBST反复漂洗3次,每次3 min;加入HIF-1α兔抗人抗体约50 μl(1:50),4℃孵育过夜,PBST反复漂洗3次,每次3 min;用FITC标记的荧光二抗(1:100)室温孵育1 h,PBST反复漂洗3次,每次3 min;DAPI染核5 min,PBST反复漂洗3次,每次3 min;封片,荧光显微镜观察拍照。
1.2.6 siRNA干扰技术抑制HIF-1α的表达siRNA委托上海吉凯基因化学技术有限公司设计合成。干扰HIF-1α正义链的siRNA序列为:5’-GCC GCU CAA UUU AUG AAU ATT-3’。采用Lipfectime2000转染试剂,在常氧条件下,按照说明书将siRNA转染对数生长期PC3细胞株,设为干扰组。
1.3 统计学方法计量资料以均数±标准差表示,采用SPSS17.0统计软件进行分析,组间比较采用独立样本t检验,P<0.05为差异有统计学意义。
2 结果 2.1 低氧对前列腺癌PC3细胞株的增殖和侵袭力的影响MTT实验结果表明,低氧处理24 h后PC3细胞的增殖力显著增加,低氧条件下PC3细胞的增殖力是常氧条件下的1.51倍(低氧组 vs. 常氧组: 3.14±0.25 vs. 1.96±0.03,P=0.0032);Matrigel侵袭实验结果显示,低氧明显增加PC3细胞的侵袭力,低氧条件下侵袭过膜的细胞数显著多于常氧条件下的细胞数(低氧组 vs. 常氧组: 27.67±1.20 vs. 15.67±1.20,P=0.0021)。
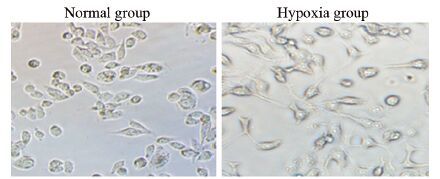
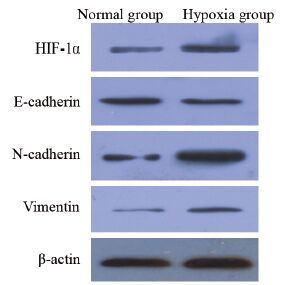
2.2 低氧增加低氧诱导因子的表达并促进前列腺癌PC3细胞株的上皮间质转化低氧促进前列腺癌PC3细胞发生显著的形态改变,使PC3细胞由短梭形的典型上皮样形态转化为纺锤状的成纤维样形态,见图 1。Western blot分析结果显示,跟常氧条件比较,低氧显著提高HIF-1α的表达(低氧组 vs. 常氧组: 3.17±0.20 vs. 0.99±0.02,P=0.0004),并显著增加间质细胞相关蛋白N-cadherin(低氧组 vs. 常氧组: 5.03±0.15 vs. 1.02±0.06,P<0.0001)和Vimentin的表达水平(低氧组 vs. 常氧组: 2.70±0.10 vs. 1.01±0.04,P=0.0001),显著降低上皮细胞相关蛋白E-cadherin的表达水平(低氧组 vs. 常氧组: 0.31±0.01 vs. 1.02±0.04,P <0.0001),见图 2。
|
| 图 1 低氧使PC3细胞发生显著的形态改变 Figure 1 Hypoxia induced significantly morphological change of PC3 cells |
|
| 图 2 Western blot检测常氧和低氧组细胞中各蛋白表达水平 Figure 2 Expressions of HIF-1α,E-cadherin,N-cadherin and Vimentin tested by Western blot in normal and hypoxia groups |
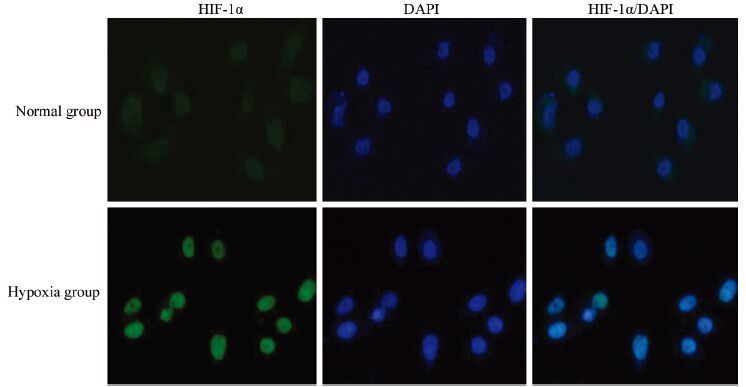
免疫荧光结果显示,在正常情况下,HIF-1α主要定位于PC3细胞质,缺氧24 h后,HIF-1α表达量增加,而且明显向细胞核内转位,见图 3。
|
| 图 3 免疫荧光检测HIF-1α的位置变化 Figure 3 Change of location of HIF-1α was detected by immunofluorescence |
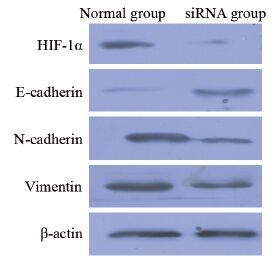
siRNA抑制HIF-1α的表达(常氧组vs.干扰组: 1.00±0.03 vs. 0.04±0.001,P<0.0001),E-cadherin的表达(常氧组vs. 干扰组: 1.00±0.05 vs. 6.67±0.18,P<0.0001)增加,N-cadherin(常氧组 vs. 干扰组: 1.00±0.06 vs. 0.19±0.01,P=0.0002)和Vimentin(常氧组vs. 干扰组: 1.02±0.05 vs. 0.30±0.01,P=0.0002)的表达减少,从而抑制上皮间质转化过程,见图 4。
|
| 图 4 Western blot检测常氧和干扰组细胞中各蛋白表达水平 Figure 4 Expressions of HIF-1α,E-cadherin,N-cadherin and Vimentin tested by Western blot in normal and siRNA groups |
随着前列腺特异性抗原(PSA)在前列腺癌普查中的应用,在欧美一些发达国家,绝大多数前列腺癌患者在发病早期即被确诊。但是,我国尚未开展血清PSA的前列腺癌普查,并且早期前列腺癌症状不明显,大部分患者被诊断为前列腺癌时已是晚期并发远处转移,患者死亡率高[5]。因此,阐明前列腺癌进展和转移的具体机制对于治疗前列腺癌意义重大。
EMT是一种快速、通常是可逆的细胞表型的变化,是具有细胞间紧密连接和黏附能力的上皮细胞转变成独立、有活动能力的间质细胞的过程。前列腺癌的转移是一个复杂的连续过程,包括肿瘤细胞与基底膜之间黏附能力下降、细胞外基质降解、进入和穿出血管或淋巴管、在远处形成转移瘤等环节。其中,肿瘤细胞与基底组织的黏附和局部浸润是肿瘤转移的关键环节。在肿瘤细胞中,EMT是其获得浸润转移能力的一个重要途径。因此,EMT被认为是前列腺癌发生转移的一个关键步骤[6]。在EMT启动后,E-钙黏附蛋白(E-cadherin)的表达下降,N-钙黏附蛋白(N-cadherin)、波形蛋白(Vimentin)等蛋白表达上调,其中E-cadherin表达的下降是EMT发生的关键指标[7-8]。一系列转录因子,如Twist、Snail、Slug、ZEB,可以直接或间接调节E-cadherin基因的转录。
在实体肿瘤中,低氧被广泛认为是治疗抵抗和不良预后的一个重要因素[9-10]。低氧诱导因子-1α(Hypoxia-inducible factor-1α,HIF-1α)是缺氧条件下调节肿瘤细胞缺氧反应的主要转录因子,在前列腺癌中有高表达。在有氧环境中,HIF-1α被泛素蛋白酶体快速降解,半衰期不足5 min;在低氧条件下,HIF-1α的降解被显著抑制,其构象发生改变,并通过第二信使—ROS与激酶系统发生联系,激活MAPK(或)PI3K,促使HIF-1α的磷酸化,HIF-1α稳定性增加,从而使HIF-1α与HIF-1β结合形成二聚体。此二聚体转位到核内,通过与启动子低氧反应元件(hypoia response elemet,HRE)中的结合位点结合,启动相应基因表达。缺氧能够诱导多种影响EMT过程的转录调节因子的表达,包括Twist、Snail、Slug、ZEB等,而这些转录因子大多已经被证明直接或间接受HIF-1α的调控[11]。本研究结果显示,低氧诱导前列腺癌细胞HIF-1α的表达,并促进EMT的发生;而利用siRNA抑制HIF-1α的表达可以逆转EMT的发生;因此,我们推测低氧可能通过增加HIF-1α的表达,促进HIF-1α向细胞核内转位,调节多种转录因子的表达,增加前列腺癌细胞的增殖和侵袭能力,并促进EMT的发生。
肿瘤微环境已经成为肿瘤的标志特征之一,是肿瘤生长的“土壤”。它具有组织缺氧、pH值降低、营养缺乏和肿瘤血管生成等特点。多种生长因子,如肝细胞生长因子HGF、转化生长因子TGF-β等,能够诱导肿瘤细胞发生EMT。其中,TGF-β常被用来在体外诱导肿瘤细胞发生EMT,但是,这并不能真正地模拟肿瘤生长的微环境。Milosevic等[12]进行了大规模的临床研究发现,前列腺癌组织局部缺氧跟接受根治性放射治疗后肿瘤局部复发和生化复发密切相关。本研究在体外细胞模型模拟体内缺氧环境对EMT的影响,更加贴近肿瘤微环境,结果显示缺氧不仅能够诱导EMT发生,并且增强前列腺癌细胞的增殖和侵袭能力。这将为研究前列腺癌转移的发病机制提供新的理论基础,使针对低氧的抗肿瘤成为前列腺癌治疗的新靶点。
| [1] | Han SJ, Zhang SW, Chen WQ, et al. Analysis of the status and trends of prostate cancer incidence in China[J]. Lin Chuang Zhong Liu Xue Za Zhi, 2013, 18 (4) : 330–4. [ 韩苏军, 张思维, 陈万青, 等. 中国前列腺癌发病现状和流行趋势分析[J]. 临床肿瘤学杂志, 2013, 18 (4) : 330–4. ] |
| [2] | Chan N, Milosevic M, Bristow RG. Tumor hypoxia, DNA repair and prostate cancer proregression: new targets and new therapies[J]. Future Oncol, 2007, 3 (3) : 329–41. DOI:10.2217/14796694.3.3.329 |
| [3] | Abrantes AM, Serra E, Goncalves C, et al. Tumour hypoxia and technetium tracers: in vivo studies[J]. Curr Radiopharm, 2012, 5 (2) : 99–105. DOI:10.2174/1874471011205020099 |
| [4] | Stewart GD, Ross JA, McLaren DB, et al. The relevance of a hypoxic tumour microenvironment in prostate cancer[J]. BJU Int, 2009, 105 (1) : 8–13. |
| [5] | Freedland SJ. Screening, risk assessment, and the approach to therapy in patients with prostate cancer[J]. Cancer, 2011, 117 (6) : 1123–35. DOI:10.1002/cncr.25477 |
| [6] | Emadi Baygi M, Soheili ZS, Schmitz I, et al. Snail regulates cell survival and inhibits cellular senescence in human metastatic prostate cancer cell lines[J]. Cell Biol Toxicol, 2010, 26 (6) : 553–67. DOI:10.1007/s10565-010-9163-5 |
| [7] | Friedl P, Alexander S. Cancer invasion and the microenvironment: plasticity and reciprocity[J]. Cell, 2011, 147 (5) : 992–1009. DOI:10.1016/j.cell.2011.11.016 |
| [8] | Yip WK, Seow HF. Activation of phosphatidylinositol 3-kinase/Akt signaling by EGF downregulates membranous E-cadherin and β-catenin and enhances invasion in nasopharyngeal carcinoma cells[J]. Cancer Lett, 2012, 318 (2) : 162–72. DOI:10.1016/j.canlet.2011.12.018 |
| [9] | Bristow RG, Hill RP. Hypoxia and metabolism. Hypoxia, DNA repair and genetic instability[J]. Nat Rev Cancer, 2008, 8(3):180-92. |
| [10] | Chan DA, Giaccia AJ. Hypoxia, gene expression, and metastasis[J]. Cancer Metastasis Rev, 2007, 26 (2) : 333–9. DOI:10.1007/s10555-007-9063-1 |
| [11] | Yang MH, Wu MZ, Chiou SH, et al. Direct regulation of TWIST by HIF-1alpha promotes metastasis[J]. Nat Cell Biol, 2008, 10 (3) : 295–305. DOI:10.1038/ncb1691 |
| [12] | Milosevic M, Warde P, Ménard C, et al. Tumor hypoxia predicts biochemical failure following radiotherapy for clinically localized prostate cancer[J]. Clinical Cancer Res, 2012, 18 (7) : 2108–14. DOI:10.1158/1078-0432.CCR-11-2711 |
 2017, Vol. 44
2017, Vol. 44
