文章信息
- 维生素C联合三氧化二砷对膀胱癌T-24细胞株的作用
- Combined Application of Vitamin C and Arsenic Trioxide in Inhibiting Bladder Cancer Cell Lines T-24 in vitro
- 肿瘤防治研究, 2017, 44(2): 103-107
- Cancer Research on Prevention and Treatment, 2017, 44(2): 103-107
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.02.005
- 收稿日期: 2016-06-20
- 修回日期: 2016-09-19
2. 541000 桂林,桂林医学院附属医院泌尿外科;
3. 541000 桂林,桂林医学院生物技术学院;
4. 044000 运城,运城市中心医院泌尿外科
2. Department of Urology, Affiliated Hospital of Guilin Medical College, Guilin 541000, China;
3. College of Biotechnology, Guilin Medical College, Guilin 541000, China;
4. Department of Urology, Yuncheng Central Hospital, Yuncheng 044000, China
膀胱癌是最常见的男性泌尿系统肿瘤,其发病率居于首位,近几年有逐渐上升的趋势[1]。临床常用的如卡介苗、丝裂霉素、表柔比星等抗有丝分裂药物[2],是常见的膀胱灌注药物,但它们不同程度上存在不良反应及较高的肿瘤复发率,因此,寻找安全且有效的膀胱癌药物是肿瘤治疗领域的瓶颈。三氧化二砷(As2O3)是中药砒霜的主要有效成分[3],具有杀伤白血病细胞、促进白血病细胞凋亡和诱导细胞分化三重作用[4]。国外研究显示,维生素C不仅对化疗药物所致的细胞损伤有保护作用,也对As2O3抗癌作用具有协同性[5-6]。本实验旨在探讨维生素C联合三氧化二砷对膀胱癌T-24细胞增殖、凋亡作用及其机制,为临床用药提供参考。
1 材料与方法 1.1 材料人T-24膀胱癌细胞株(中国科学院上海生科院细胞资源中心)、DMEM培养液和胎牛血清(美国Gibcol公司)、注射用As2O3(北京双鹭药业)、维生素C(广州南国药业有限公司)、CCK-8试剂盒(美国Sigma公司)、RT-PCR反应体系购自TaKaRa公司[宝生物工程(大连)有限公司]、caspase-3 mRNA和survivin mRNA引物(上海生工生物工程技术服务有限公司)、细胞裂解液和蛋白定量试剂盒(美国PIERCE公司)。
1.2 实验分组分为6组,其中As2O3组分为3组,分别加入0.4 μg/ml、4 μg/ml(临床常用量)、40 μg/ml的As2O3;维生素C组加入400 μg/ml(临床常用量)的维生素C;联合组加入400 μg/ml维生素C+0.4 μg/ml As2O3,对照组不做特殊处理。
1.3 细胞培养将T-24细胞置于含有10%胎牛血清的DMEM培养液中,内含100 u/ml青霉素、100 μg/ml链霉素,于37℃、5%CO2的培养箱中培养,用胰蛋白酶消化传代,取对数生长期细胞进行后续实验。
1.4 T-24细胞增殖曲线测定取对数生长期T-24细胞,接种到96孔板中,置于CO2的培养箱中24 h后,分别加入维生素C(400 μg/ml)组,不同浓度As2O3(0.4、4、40 μg/ml)组,联合(400 μg/ml维生素C+0.4 μg/ml As2O3)组,对照组不做特殊处理,每组设3个复孔。连续培养7天后每孔加入10 μl CCK-8液,继续培养2 h后吸出上清液,测定450 nm处吸光度(OD)值,用MTS法绘制细胞生长曲线。
1.5 细胞周期及凋亡率的测定取对数生长期细胞接种于10 cm培养皿中,在37℃、5%CO2的培养箱中培养24 h贴壁后,加入相应药物作用,对照组不加药物,培养24 h后收集贴壁细胞制成单细胞悬液,70%冷乙醇固定,PBS洗涤,RNase A 37℃孵育30 min。离心后弃上清液,加入PI染液,冰浴30 min,染色后筛网过滤,上流式细胞仪检测,Multicycle DNA分析软件测定。
1.6 survivin mRNA、caspase-3 mRNA测定取对数生长期T-24细胞,按对照组、维生素C(400 μg/ml)组、As2O3(0.4 μg/ml)组、As2O3(4 μg/ml)组、As2O3(40、μg/ml)组、联合(400 μg/ml维生素C+0.4 μg/ml As2O3)组,分别培养48 h后收集细胞,TRIzol试剂盒提取总RNA,反转录制备cDNA进行PCR实验。caspase-3 mRNA上游引物:5'-TGACCGAGGCTACATFCAGATGACACC-3',下游引物:5'-CAAGAGAGTTGGGCTGACCAGAAACAC-3',扩增产物365 bp;suvivin mRNA上游引物:5'-CCCTTTCTCAAGGACCACCGCATC-3',下游引物:5'-GCCAAGTCTGGCTCGTTCTCAGTG-3',扩增产物133 bp;β-actin上游引物:5'R 11;AGTGTGACGTGGACATCCGCA-3',下游引物:5'-ATCCACATCTGCTGGAAGGTGGAC-3',扩增产物243 bp。基因扩增后均取扩增产物用琼脂糖凝胶电泳检测,应用凝胶成像系统对电泳条带进行扫描分析,计算相对表达水平。
1.7 Western blot法检测suvivin、caspase-3蛋白水平按照PIERCE公司说明书步骤,细胞裂解液提取细胞蛋白,蛋白定量试剂盒定量,随后将蛋白样品用10% SDS-PAGE凝胶电泳,当蛋白进入分离胶后湿转法进行转膜。5%脱脂奶粉封闭1 h后加入一抗,4℃孵育过夜,之后加入二抗孵育1 h,ECL荧光显色后暗室X片曝光。
1.8 统计学方法应用SPSS19.0统计软件处理,所用实验均重复3次,实验数据用(x±s)表示,采用单因素方差分析,P<0.05为差异有统计学意义。
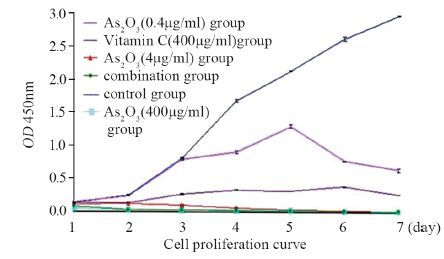
2 结果 2.1 各组药物作用后对T-24细胞增殖活性的影响联合组、维生素C(400 μg/ml)组、As2O3(4 μg/ml)组及As2O3(40 μg/ml)组均对T-24细胞增殖有显著抑制作用,且随着时间的延长而增加,呈时间依赖性。联合组对肿瘤细胞的抑制能力强于维生素C(400 μg/ml)组、As2O3(4 μg/ml)组及As2O3(40 μg/ml)组,见图 1。
|
| 图 1 T-24细胞在各组中的增殖情况 Figure 1 The proliferation of T-24 cell in different groups |
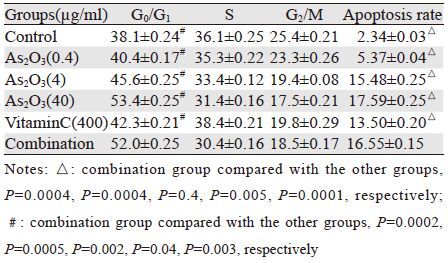
T-24细胞经过各组药物作用24 h后,联合组细胞凋亡率明显高于其他各组。联合组将细胞阻滞在G0/G1期,与其他各组比较,差异有统计学意义,见表 1。
 |
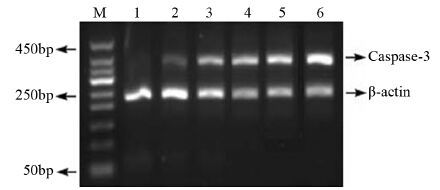
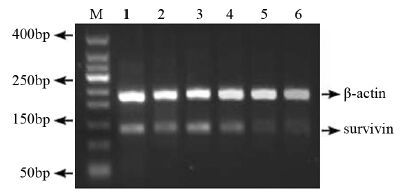
As2O3能上调caspase-3 mRNA的表达,下调survivin mRNA的表达,作用随着剂量的增加而加强,但联合组则能明显下调survivin mRNA的表达,促进caspase-3 mRNA的表达,效果优于对照组、As2O3(0.4 μg/ml)组、As2O3(4 μg/ml)组,见图 2~3。
|
| M: marker; 1: control group; 2: vitamin C(400μg/ml) group; 3: As2O3(0.4μg/ml) group; 4: As2O3(4μg/ml) group; 5: As2O3(40μg/ml) group; 6: combination group(400μg/ml vitamin C+0.4μg/ml AS2O3) 图 2 48 h后不同药物组中caspase-3因子的表达 Figure 2 Expression of the caspase-3 gene in different groups after 48h of culture |
|
| M: marker; 1: control group; 2: vitamin C(400μg/ml) group; 3: As2O3(0.4μg/ml) group; 4: As2O3(4μg/ml) group; 5: As2O3(40μg/ml) group; 6: combination group(400μg/ml vitamin C+0.4μg/ml As2O3) 图 3 48 h后不同药物组中survivin因子的表达 Figure 3 Expression of the survivin gene in different groups after 48 h of culture |
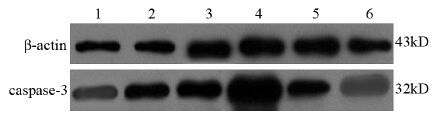
As2O3能上调caspase-3蛋白的表达,上调survivin蛋白的表达,作用随着剂量的增加而加强,但联合组则能明显下调survivin蛋白的表达,促进caspase-3蛋白的表达,效果优于对照组、As2O3(0.4 μg/ml)组及As2O3(4 μg/ml)组,但与As2O3(40 μg/ml)组相比无明显变化,见图 4~5。
|
| 1: As2O3(40μg/ml) group; 2: As2O3(4μg/ml) group; 3: As2O3(0.4μg/ml)group; 4: control group; 5: vitamin C(400μg/ml) group; 6: combination group(400μg/ml vitamin C+0.4μg/ml AS2O3) 图 4 48 h后不同药物组中β-actin、caspase-3蛋白的表达 Figure 4 Expression of the β-actin and caspase-3 protein in different groups after 48 h of culture |

|
| 1: control group; 2: vitamin C(400μg/ml) group; 3: As2O3(0.4μg/ml) group; 4: As2O3(4μg/ml) group; 5: As2O3(40μg/ml) group; 6: combination group(400μg/ml vitamin C+0.4μg/ml As2O3) 图 5 48 h后不同药物组中survivn蛋白的表达 Figure 5 Expression of the survivin proteins in different groups after 48 h of culture |
As2O3治疗急性早幼粒细胞白血病取得极好效果后,随之有研究表明其在其他抗肿瘤治疗方面具有突出的效果[7],已成为肿瘤治疗研究的热点之一。但是,As2O3不良反应较多,致死量及治疗量相接近,因此探讨AS2O3抗肿瘤机制对于其广泛应用于临床具有重要意义[8-9]。本研究发现As2O3对T-24细胞生长有抑制作用,呈剂量和时间依赖性,其机制可能与促使肿瘤细胞凋亡有关。目前,探讨肿瘤细胞凋亡的药物成为研究的热点与趋势,caspase是半胱氨酸蛋白酶家族成员之一,在细胞凋亡的过程中起关键作用[10]。细胞凋亡通路主要有线粒体通路、死亡受体通路、内质网通路,最后这三种通路汇聚到同一条通路,激活caspase-3并诱导细胞凋亡,因此,检测caspase-3的表达有助于早期提供细胞凋亡的证据[11]。survivin是目前最重要的凋亡抑制蛋白家族成员之一,它可直接或间接与caspase-3,caspase-7结合并抑制它们的活性,从而抑制细胞的凋亡。有研究显示caspase-3和survivin可能是As2O3作用的靶点。曾锦荣等[12]研究表明,As2O3能抑制肺癌细胞survivin的表达,抑制其增殖,还能上调caspase-3的表达,与剂量呈正相关。Haga等[13]研究发现caspase的激活只在对As2O3敏感的细胞系出现。
As2O3抑制肿瘤细胞生长的重要机制之一是阻滞细胞周期,它可调控一些关键蛋白,使细胞生长阻滞在G0/G1期,Li等[14]研究表明,伏立诺他和三氧化二砷单独应用可以抑制人急性早幼粒白血病细胞(NB4)的增殖并诱导细胞凋亡,联合应用可以提高效果,其机制可能与三氧化二砷增加组蛋白乙酰化作用,下调AKT蛋白激酶信号通路有关,但需要进一步研究。Beauchamp等[15]研究发现,三氧化二砷抗肿瘤机制可能为其联合半胱氨酸299抑制AMPK激酶的活性,从而增加哺乳动物雷帕霉素靶蛋白(mammalian,target of rapamycin,mTOR)的活性。而mTOR是PI3K/AKT/mTOR信号通路中最重要的下游效应蛋白之一,通过AMPK信号途径调节细胞生长和增殖[16]。梁晓燕等[17]发现,在人宫颈癌HeLa细胞恢复LKB1(一种丝/苏氨酸蛋白激酶)表达后细胞增殖减慢,极性恢复,其可能的机制是增强内源性的AMPK信号通路的活性,进而抑制细胞周期G1/S转换。本研究发现,As2O3(4 μg/ml)组和As2O3(40 μg/ml)组使T-24细胞阻滞在G0/G1期,凋亡率明显高于As2O3(0.4 μg/ml)组、对照组,从而抑制细胞增殖,是否通过PI3K/AKT/mTOR信号通路有待有进一步研究。同时,可抑制survivin mRNA、蛋白的表达,上调caspase-3 mRNA、蛋白的表达,与剂量呈正相关。但As2O3剂量过高可能对正常细胞产生毒性作用,从而限制了其临床应用。以As2O3为基础联合化疗为临床提供了新的思路。从细胞增殖曲线上看,As2O3(0.4 μg/ml)组对肿瘤增殖抑制作用弱于维生素C(400 μg/ml)组,这可能与维生素C在体内代谢情况,血药浓度及到达肿瘤组织的有效药物量有关;维生素C及As2O3在抗肿瘤方面存在争议,有研究表明单用维生素C临床剂量对肺腺癌裸鼠移植瘤没有明显的抑制作用。故本研究还需要进一步考虑深层次的机制。
维生素C可以清除体内有害氧自由基从而保护机体正常细胞,还可以进一步减少肿瘤细胞内本就缺乏的过氧化物酶,增加过氧化氢的产生,从而对肿瘤细胞产生杀伤作用[18]。正常组织细胞中过氧化物酶含量是肿瘤细胞的10~100倍,这有可能是维生素C杀伤肿瘤细胞的同时不损害正常细胞的重要原因。Fritz等[19]研究发现,低浓度维生素C可减少三氧化二砷化疗的不良反应。维生素C可使HeLa细胞阻滞在G0/G1期,抑制DNA合成而抑制细胞增殖。但有体外实验表明,低剂量对正常细胞有保护作用,而大剂量对细胞有杀伤作用,因此近年来维生素C被建议作用肿瘤药物的辅助治疗。
本实验提示,维生素C(400 μg/ml)组对T-24细胞有抑制效果,对survivin、caspase-3亦产生影响,但联合组抑制survivin mRNA、蛋白的表达,上调caspase-3 mRNA、蛋白的表达优于其他各组,抑制肿瘤增殖的效果明显,综上所述,维生素C与As2O3联用能更有效的促进膀胱癌T-24细胞的凋亡,其机制可能与上调caspase-3、下调survivin表达有关。本研究亦存在如下不足:具体抗肿瘤机制仍需探索,还需进行其他肿瘤的相关研究,为临床应用提供新方法奠定基础。
| [1] | Zhang M, Wu FP, Shi JC, et al. Combined application of replication adenovirus AD-Mk and mitomycin in bladder cancer cell[J]. Zhonghua Shi Yan Wai Ke Za Zhi, 2012, 29 (8) : 1633. [ 张明, 吴风鹏, 石金苓, 等. 条件复制腺病毒Ad-MK联合丝裂霉素对膀胱癌细胞的作用[J]. 中华实验外科杂志, 2012, 29 (8) : 1633. ] |
| [2] | Zhang Y, Jiang WB, Wang P. Clinical effect of bladder preserving resection and paclitaxel interventional treatment of invasive bladder cancer[J]. Zhonghua Sheng Hau Yao Wu Za Zhi, 2012, 33 (5) : 650–1. [ 张勇, 江文凛, 王平. 保留膀胱切除术联合紫杉醇介入治疗局部浸润性膀胱癌临床疗效[J]. 中国生化药物杂志, 2012, 33 (5) : 650–1. ] |
| [3] | Li HY, Cao LM, Wang J. Inhibition on proliferation, migration and invasion in human hepatocellular carcinoma SMMC-7721 cells by arsenic trioxide[J]. Zhongguo Lao Nian Xue Za Zhi, 2013, 33 (11) : 2572–4. [ 李海燕, 曹励民, 王娟. 三氧化二砷对人肝癌细胞SMMC-7721增殖、迁移及侵袭能力的影响[J]. 中国老年学杂志, 2013, 33 (11) : 2572–4. ] |
| [4] | Zhang XK, Luo JM, Sun J. Effects of 5-Aza-2′deoxycytidine.Combined with Arsenic Trioxide on SHP-1, JAK3, TYK2 Expression in U937 Cells[J]. Zhong Liu Fang Zhi Yan Jiu, 2014, 41 (7) : 728–33. [ 张小坤, 罗建民, 孙杰. 三氧化二砷联合5-杂氮-2′-脱氧胞苷对U937细胞SHP-1、JAK3、TYK2基因表达的影响[J]. 肿瘤防治研究, 2014, 41 (7) : 728–33. ] |
| [5] | Blasiak J, Kowalik J. Protective action of vitamin C against DNA damage induced by selenium-cisplatin conjugate[J]. Acta biochim Pol, 2001, 48 (1) : 233–40. |
| [6] | Grad JM, Bahlis NJ, Reis I, et al. Ascorbic acid enhances arsenic trioxide-induced cytotoxicity in multiple myeloma cells[J]. Blood, 2001, 98 (3) : 805–13. DOI:10.1182/blood.V98.3.805 |
| [7] | Chen G, He Y, Wu X, et al. In vitro and in vivo studies of pirarubicin-loaded SWNT for the treatment of bladder cancer[J].Braz J Med Biol Res, 2012, 45(8): 77l-6. |
| [8] | Zhang X, Jia S, Yang S, et al. Arsenic trioxide induces G2/M arrest in hepatocelhlar carcinoma cells by increasing the tumor suppressor PT'EN expression[J]. J Cell Biochem, 2012, 113 (11) : 3528–35. DOI:10.1002/jcb.24230 |
| [9] | Yuan T, Jiang GZ, Li HY. Influences of arsenic trioxide on lung cancer cell line NCI-H520[J]. Zhonghua Shi Yan Wai Ke Za Zhi, 2014, 31 (6) : 1292–3. [ 袁坦, 姜国忠, 李宏云. 三氧化二砷对肺癌细胞NCI-H520的影响[J]. 中华实验外科杂志, 2014, 31 (6) : 1292–3. ] |
| [10] | Bürzle M, Suzuki Y, Ackermann D, et al. The sodium dependent ascorbic acid transporter family SLC23[J]. Mol Aspects Med, 2013, 34 (2-3) : 436–54. DOI:10.1016/j.mam.2012.12.002 |
| [11] | Yu R, Schellhorn HE. Recent applications of engineered animal antioxidant deficiency models in human nutrition and chronic disease[J]. J Nutr, 2013, 143 (1) : 1–11. DOI:10.3945/jn.112.168690 |
| [12] | Zeng JR, Jiang BJ, Wang JY. Arsenic Trioxide(AS2O3) combined with vitamin C(Vit C) affect the activity of effect of arsenic trioxide(AS2O3) combined with vitamin C on caspase-3 and surviving in the subcutaneously transplanted tumor of drug resistant human lung carcinoma in nude mice[J]. Zhongguo Lao Nian Xue Za Zhi, 2011, 31 (24) : 4827–31. [ 曾锦荣, 蒋碧佳, 王绩英. 三氧化二砷联合维生素C对耐药性肺腺癌裸鼠移植瘤caspase-3、survivin活性的影响[J]. 中国老年学杂志, 2011, 31 (24) : 4827–31. ] |
| [13] | Haga N, Fujita N, Tsuruo T. Involvement of mitochondrial aggregation in arsenic trioxide(AS2O3)-induced apoptosis in human glioblastoma cells[J]. Cancer Sci, 2005, 96 (11) : 825–33. DOI:10.1111/cas.2005.96.issue-11 |
| [14] | Li X, Guan X, Li F, et al. Chemosensitivity enhancement toward arsenic trioxide by inhibition of histone deacetylase in NB4 cell line[J]. J Int Med Res, 2016, 44 (4) : 882–92. DOI:10.1177/0300060516646238 |
| [15] | Beauchamp EM, Kosciuczuk EM, Serrano R, et al. Direct Binding of Arsenic Trioxide to AMPK and Generation of Inhibitory Effects on Acute Myeloid Leukemia Precursors[J]. Mol Cancer Ther, 2015, 14 (1) : 202–12. DOI:10.1158/1535-7163.MCT-14-0665-T |
| [16] | Yang JP, Li SL, Zhao ZH, et al. Effects of mTOR siRNA and Rapamycin on mTOR and 4EBP1 Expressions in Human HeLa Cells[J]. Zhong Liu Fang Zhi Yan Jiu, 2014, 41 (1) : 40–5. [ 杨建萍, 李晟磊, 赵志华, 等. 雷帕霉素及mTOR siRNA对宫颈癌HeLa细胞mTOR和4EBP1表达的影响[J]. 肿瘤防治研究, 2014, 41 (1) : 40–5. ] |
| [17] | Liang XY, Wang PL, Tao XH. Inhibition of Hela cell proliferation by LKB1 through AMPK signaling pathway[J]. Chongqing Yi Ke Da Xue Xue Bao, 2013, 38 (1) : 45–7. [ 梁小燕, 王丕龙, 陶小红. LKB1通过AMPK信号通路抑制Hela细胞增殖的机制研究[J]. 重庆医科大学学报, 2013, 38 (1) : 45–7. ] |
| [18] | Gao F, Yi J, Shi GY, et al. Ascorbic acid enhances the apoptosis of U937 cells induced by arsenic trioxide in combination with DMNQ and its mechanism[J]. Zhonghua Xue Ye Xue Za Zhi, 2002, 23 (1) : 9–11. [ 高飞, 易静, 史桂英, 等. 维生素C增强氧化砷联用二甲萘醌诱导的U937细胞凋亡及其机制[J]. 中华血液学杂志, 2002, 23 (1) : 9–11. ] |
| [19] | Fritz H, Flower G, Weeks L, et al. Intravenous Vitamin C and Cancer: A Systematic Review[J]. Integr Cancer Ther, 2014, 13 (4) : 280–300. DOI:10.1177/1534735414534463 |
 2017, Vol. 44
2017, Vol. 44


