文章信息
- 5-氮杂胞苷增加鼻咽癌细胞株C666-1放射敏感度的实验
- 5-azacytidine Increases Radiation Sensitivity of Nasopharyngeal Carcinoma Cell Line C666-1
- 肿瘤防治研究, 2017, 44(2): 94-97
- Cancer Research on Prevention and Treatment, 2017, 44(2): 94-97
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.02.003
- 收稿日期: 2016-10-02
- 修回日期: 2016-12-06
放射治疗是鼻咽癌的主要治疗手段。然而肿瘤细胞的放射抗拒是治疗失败的重要原因之一。如何提高肿瘤细胞放射敏感度,提高控制率,降低正常组织毒性反应是重要的研究课题。5-氮杂胞苷(5-azacytidine,5-Aza)是胞嘧啶类似物,它不仅可以干扰RNA代谢、DNA和蛋白质合成,还可抑制DNA甲基转移酶减少细胞分裂时DNA甲基化水平[1]。研究表明,低药物浓度5-氮杂胞苷主要表现为去甲基化作用,高药物浓度表现出更大的细胞毒性(干扰DNA合成,并导致DNA损伤)[2]。最近研究发现,5-氮杂胞苷与放射敏感度有密切关系[3-4]。本研究以5-氮杂胞苷作用鼻咽癌细胞株C666-1,研究其对鼻咽癌细胞放射敏感度的影响并探讨其可能的作用机制。
1 材料与方法 1.1 实验材料 1.1.1 鼻咽癌细胞株C666-1由中山大学附属肿瘤医院实验室赠予。 1.1.2 主要试剂PRMI 1640培养液和胎牛血清购自美国Gibco公司;噻唑蓝(MTT)购自美国Sigma公司;流式细胞检测试剂购自南京凯基生物公司;一抗cleaved Caspase-3、cleaved PARP、γ-H2AX、β-actin及二抗购自美国Cell Signaling Technology公司。
1.2 实验分组及方法 1.2.1 细胞培养细胞在标准状态下(5% CO2、37℃)培养于含10%小牛血清、1%双抗的PRMI 1640培养液中,使用0.25%胰酶室温下消化,取二、三代对数期的细胞进行实验。
1.2.2 细胞处理及照射方法将实验细胞分成四组 (1)对照组:不做任何处理;(2)5-氮杂胞苷处理组:予不同浓度5-氮杂胞苷处理细胞 (0、500、1000、3000、5000 nmol/L);(3)单纯放疗组(RT):仅予放疗;(4)放疗+5-氮杂胞苷处理组:予5-氮杂胞苷处理细胞24 h后行放疗。用磷酸缓冲盐液(PBS)溶解5-氮杂胞苷。对照组用等量的PBS处理。标准状态下培养12 h至细胞贴壁后,室温下采用6 MV X射线进行照射。
1.2.3 MTT法测定增殖反应取对数生长期的C666-1细胞,制成细胞悬液,平铺于96孔细胞培养板中,细胞密度为2×103个每孔,细胞贴壁后加入如上不同浓度的5-氮杂胞苷(0、500、1000、3000、5000 nmol/L),每个浓度设3个平行孔,继续培养24、48、72 h,每孔加入20 μl 5 mg/ml MTT溶液,继续培养4 h后加入150 μl DMSO,振荡10 min,测定490 nm处吸光度值,计算细胞增殖抑制率(%)= (1-实验组平均吸光度值/对照组平均吸光度值)×100%。
1.2.4 克隆形成实验单细胞悬液C666-1接种6孔板,分为单纯放疗组与放疗+5-氮杂胞苷处理组,细胞分别给予0、2、4、6、8 Gy不同剂量照射,细胞照射后在标准状态下培养10~14天,克隆形成后同时收获。采用甲醇固定细胞集落15 min,吉姆萨染色30 min,自然晾干后进行克隆计数。细胞数≥50个的集落被作为存活克隆予以计数。克隆形成率(PE)=集落数/细胞接种数×100%,存活分数(SF)=计数所得克隆数/接种细胞数×PE。SF2为照射2 Gy时的细胞存活率,是反映细胞放射敏感度最重要的参数之一。放射增敏能力用增敏比(sensitivity enhancement ratio,SER)表示,SER=不用增敏剂时达到某一效应的放射剂量/使用增敏剂时达到同样效应的放射剂量。
1.2.5 流式细胞仪检测细胞周期细胞以3×105个细胞每瓶的密度接种于25 cm2培养皿中,贴壁后分为放疗组(4 Gy)和放疗(4 Gy)+5-氮杂胞苷组,继续培养24 h后收集细胞,按细胞周期检测试剂盒说明处理,用流式细胞仪测试。
1.2.6 Western blot分析收集不同处理组的C666-1细胞,加入400 μl预冷的细胞裂解液,提取蛋白。BCA法测定蛋白浓度,取等量蛋白置沸水中变性5 min,行SDS-PAGE垂直电泳,电转至PVDF膜,用脱脂奶粉室温封闭1 h,PBST洗膜,加入一抗,4℃缓慢摇动孵育过夜,PBST洗膜后加相应二抗,室温孵育1 h,PBST洗膜,加化学发光底物显色后暗室曝光洗片。
1.3 统计学方法所有数据用SPSS13.0软件进行统计分析,多组数据间比较采用单因素方差分析,组间两两比较采用t检验,以P<0.05为差异有统计学意义。
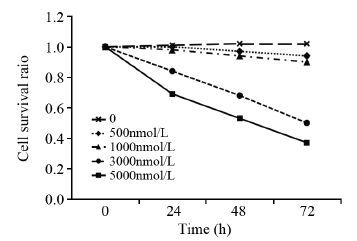
2 结果 2.1 5-氮杂胞苷对C666-1细胞增殖的影响MTT实验表明5-氮杂胞苷作用72 h后,细胞增殖抑制率随药物浓度(0、500、1000、3000、5000 nmol/L)的增加而增加,见图 1。当5-氮杂胞苷≤1000 nmol/L时,对细胞增殖基本没有影响(P=0.427)。为了排除5-氮杂胞苷本身对细胞增殖抑制的影响,本研究选择了1000 nmol/L作为工作浓度进行放疗增敏的研究。
|
| 图 1 不同浓度5-氮杂胞苷对C666-1细胞增殖的影响 Figure 1 Effect of 5-azacytidine at different concentrations on C666-1 cells growth |
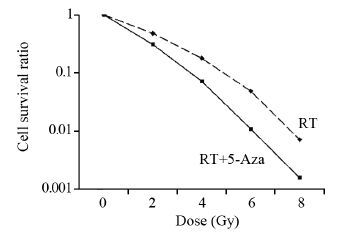
用不同剂量照射C666-1细胞,培养14天后计数集落及集落形成率,计算细胞存活分数并绘制细胞存活曲线,见图 2 。鼻咽癌细胞株C666-1接受电离辐射时SF2为48%,5-氮杂胞苷联合电离辐射时SF2为31%(P=0.002),放射增敏比为 1.37。
|
| 图 2 不同剂量放疗C666-1细胞存活曲线 Figure 2 Survival curves of C666-1 cells treated with different doses of radiotherapy(RT) |
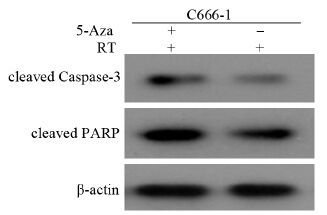
5-氮杂胞苷联合放疗处理C666-1细胞48 h后,凋亡相关蛋白cleaved Caspase-3和cleaved PARP表达较单纯放疗增多(P=0.001),见图 3。5-氮杂胞苷明显增强了电离辐射诱导细胞株C666-1的凋亡。
|
| 图 3 不同处理对C666-1细胞cleaved Caspase-3和cleaved PARP蛋白表达的影响 Figure 3 Effect of different treatments on protein expressions of cleaved Caspase-3 and cleaved PARP in C666-1 cells |
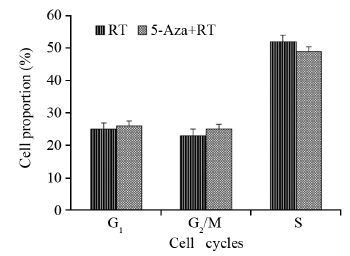
流式细胞检测发现5-氮杂胞苷联合放疗处理C666-1细胞24 h后,对比单纯放疗,细胞周期各期细胞所占比例差异无统计学意义(P=0.989)。其中C666-1细胞G2/M期细胞数25%(单纯放疗)vs. 27% (放疗+5-氮杂胞苷联)(P=0.734),见图 4。表明5-氮杂胞苷不是通过改变细胞周期来实现增加放射敏感度。
|
| 图 4 不同处理对C666-1细胞周期的影响 Figure 4 Effect of different treatments on C666-1 cells cycles |
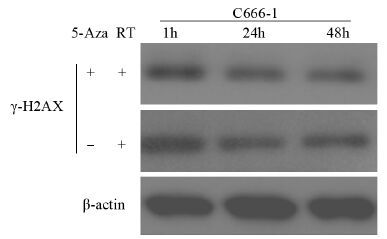
γ-H2AX是DNA损伤的重要蛋白标志物[5]。C666-1细胞在放疗后1 h γ-H2AX表达明显增加,随着时间推移,表达逐渐下降;在放疗后1、24、48 h检查5-氮杂胞苷联合放疗组与单纯放疗组C666-1细胞中γ-H2AX蛋白的表达,结果显示两组之间差异无统计学意义(P=0.862),见图 5,说明5-氮杂胞苷不是通过抑制DNA损伤修复增加放射敏感度。
|
| 图 5 不同处理对C666-1细胞γ-H2AX蛋白表达的影响 Figure 5 Effect of different treatments on protein expression of γ-H2AX in C666-1 cells |
鼻咽癌细胞放射抗拒是局部放疗失败的重要原因。如何改善鼻咽癌细胞的放射敏感度,实现个体化治疗是提高疗效的关键。5-氮杂胞苷作为胞嘧啶类似物,不仅具有直接抗肿瘤作用,还有去甲基化作用,是研究最广泛且已用于临床治疗的去甲基化药物[6]。除此之外,5-氮杂胞苷还可诱导肿瘤细胞多种生物学功能的改变,增加化疗敏感度。徐姝等发现5-氮杂胞苷通过上调miR-200c及EGFR表达,可增强非小细胞肺癌细胞对吉非替尼的敏感度[7]。Füller等在急性白血病和非小细胞肺癌的研究中发现,5-氮杂胞苷通过改变DNA甲基化状态,与多种化疗药物产生协同效应,增加药物的疗效[8]。綦晓艳等[9]研究发现,5-氮杂胞苷联合肿瘤坏死因子相关凋亡诱导配体(TRAIL)能诱导A549细胞凋亡的作用,逆转细胞对TRAIL的耐药性。因此,探索5-氮杂胞苷在恶性肿瘤治疗中的新作用机制,有可能为恶性肿瘤治疗手段提供新的思路和方法。
本实验结果显示,5-氮杂胞苷对鼻咽癌细胞C666-1的生长有明显抑制作用,在低浓度的5-氮杂胞苷进行放射增敏的研究中,发现5-氮杂胞苷处理C666-1细胞后SF2值减小,SER值>1,5-氮杂胞苷提高了C666-1细胞的放射敏感度。在其他肿瘤的研究中也有类似发现,Patties等研究发现去甲基化药物联合放疗可以显著抑制成人髓母细胞克隆形成[3];Qiu等在胃癌细胞中发现,去甲基化药物通过改变细胞周期分布及增加细胞凋亡率提高了放射敏感度[4];Hofstetter等去甲基化药物处理结肠癌细胞后,发现全基因组低甲基化后可以提高肿瘤细胞的放疗敏感度[10]。结合本研究结果与国外的研究发现,5-氮杂胞苷在多种肿瘤中具有一定放射增敏效应,对提高肿瘤放疗效果具有潜在的临床运用价值。
增加放射敏感度的机制一般与细胞周期的再分布、DNA损伤修复、诱导凋亡有密切关系[11-13]。在进一步的机制研究中发现在5-氮杂胞苷联合放疗的干预下,与单纯放疗相比C666-1细胞周期无明显变化,γ-H2AX的表达随着时间的推移亦无明显不同,值得关注的是,凋亡相关蛋白cleaved Caspase-3和cleaved PARP表达较单纯放疗增多。初步说明5-氮杂胞苷不是通过改变细胞周期的分布或者抑制DNA损伤修复来提高放疗敏感度,而是增加放疗后细胞凋亡率,提高了C666-1细胞放射敏感度。然而5-氮杂胞苷是通过改变了细胞的甲基化状态还是通过其他途径诱导了凋亡的发生,还需要深入的机制研究。
世界上40%的鼻咽癌发生于中国,又以广东、广西省等华南地区最为高发。在现行诊疗模式下,5年局部复发转移率仍有21%[14]。因此,提高鼻咽癌的治愈率,改善患者的生活质量,具有重大的社会需求和战略意义。本研究结果发现低浓度的5-氮杂胞苷具有增加电离辐射诱导的细胞凋亡,提高鼻咽癌细胞放射敏感度的作用,为进一步提高临床疗效提供新的途径。
| [1] | Licht JD. DNA Methylation Inhibitors in Cancer Therapy: The Immunity Dimension[J]. Cell, 2015, 162 (5) : 938–9. DOI:10.1016/j.cell.2015.08.005 |
| [2] | Ren J, Chu Y, Ma H, et al. Epigenetic interventions increase the radiation sensitivity of cancer cells[J]. Curr Pharm Des, 2014, 20 (11) : 1857–65. DOI:10.2174/13816128113199990529 |
| [3] | Patties I, Jahns J, Hildebrandt G, et al. Additive effects of 5-aza-2’-deoxycytidine and irradiation on clonogenic survival of human medulloblastoma cell lines[J]. Strahlenther Onkol, 2009, 185 (5) : 331–8. DOI:10.1007/s00066-009-1956-1 |
| [4] | Qiu H, Yashiro M, Shinto O, et al. DNA methyltransferase inhibitor 5-aza-CdR enhances the radiosensitivity of gastric cancer cells[J]. Cancer Sci, 2009, 100 (1) : 181–8. DOI:10.1111/cas.2009.100.issue-1 |
| [5] | Siddiqui MS, Fran?ois M, Fenech MF, et al. Persistent γH2AX: A promising molecular marker of DNA damage and aging[J]. Mutat Res Rev Mutat Res, 2015, 766 : 1–19. DOI:10.1016/j.mrrev.2015.07.001 |
| [6] | Cheishvili D, Boureau L, Szyf M. DNA demethylation and invasive cancer: implications for therapeutics[J]. Br J Pharmacol, 2015, 172 (11) : 2705–15. DOI:10.1111/bph.12885 |
| [7] | Xu S, Wu JZ, Cao HX, et al. 5-Aza-CdR enhances sensitivity of human non-small cell lung cancer cells togefitinib and its mechanisms[J]. Zhongguo Zhong Liu Sheng Wu Zhi Liao Za Zhi, 2013, 20 (1) : 26–9. [ 徐姝, 吴建中, 曹海霞, 等. 5-氮杂胞苷增强人非小细胞肺癌细胞对吉非替尼的敏感性及其机制[J]. 中国肿瘤生物治疗杂志, 2013, 20 (1) : 26–9. ] |
| [8] | Füller M, Klein M, Schmidt E, et al. 5-azacytidine enhances efficacy of multiple chemotherapy drugs in AML and lung cancer with modulation of CpG methylation[J]. Int J Oncol, 2015, 46 (3) : 1192–204. |
| [9] | Qi XY, Wang WW, Shi B, et al. Synergistic induction effect of 5-azacytidine and cisplatin combined with TRAIL on apoptosis of lung cancer A549 cells and its mechanism[J]. Zhong Liu, 2015, 35 (8) : 858–65. [ 綦晓艳, 王文武, 石斌, 等. 5-氮杂胞苷和顺铂联合TRAIL诱导肺癌A549细胞凋亡及其机制探讨[J]. 肿瘤, 2015, 35 (8) : 858–65. ] |
| [10] | Hofstetter B, Niemierko A, Forrer C, et al. Impact of genomic methylation on radiation sensitivity of colorectal carcinoma[J]. Int J Radiat Oncol Biol Phys, 2010, 76 (5) : 1512–9. DOI:10.1016/j.ijrobp.2009.10.037 |
| [11] | Huang L, Wang RZ. The cell cycle and tumor radiosensitivity[J]. Xinjiang Yi Ke Da Xue Xue Bao, 2008, 31 (11) : 1510–2. [ 黄莉, 王若峥. 细胞周期素与肿瘤放射敏感性[J]. 新疆医科大学学报, 2008, 31 (11) : 1510–2. ] |
| [12] | Zhong J, Xiong DQ, Luo H, et al. A primary investigation on relationship between radiosensitivity and radiation-induced apoptosis in three tumor cell lines[J]. Shi Yong Ai Zheng Za Zhi, 2007, 22 (6) : 560–4. [ 钟军, 熊戴群, 罗辉, 等. 肿瘤细胞放射敏感性与放射诱导凋亡关系的研究[J]. 实用癌症杂志, 2007, 22 (6) : 560–4. ] |
| [13] | Chen LP, Zhu XN. The regulation and significance of H2AX phosphorylation during DNA damage repair[J]. Ai Bian·Ji Bian·Tu Bian, 2011, 23 (2) : 148–51. [ 陈丽萍, 朱小年. DNA损伤修复过程中H2AX磷酸化的调控及其意义[J]. 癌变·畸变·突变, 2011, 23 (2) : 148–51. ] |
| [14] | Lee AW, Ngan RK, Tung SY, et al. Preliminary results of trial NPC-0501 evaluating the therapeutic gain by changing from concurrent-adjuvant to induction-concurrent chemoradiotherapy, changing from fluorouracil to capecitabine, and changing from conventional to accelerated radiotherapy fractionation in patients with locoregionally advanced nasopharyngeal carcinoma[J]. Cancer, 2015, 121 (8) : 1328–38. DOI:10.1002/cncr.v121.8 |
 2017, Vol. 44
2017, Vol. 44


