文章信息
- 高转移肺癌细胞株的建立及其肿瘤干细胞生物学特性
- Establishment of Human Lung Adenocarcinoma Cell Line A549 with High Metastasis and Biological Characteristics of Its Cancer Stem Cells
- 肿瘤防治研究, 2017, 44(2): 83-87
- Cancer Research on Prevention and Treatment, 2017, 44(2): 83-87
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.02.001
- 收稿日期: 2016-06-24
- 修回日期: 2016-11-18
肺癌已成为我国恶性肿瘤的首位死亡疾病,在确诊时,70%~80%的患者已失去手术切除机会。对于已无手术机会的患者,放化疗仍是重要的治疗手段[1]。但很多患者却因肿瘤的化疗耐药而易导致肿瘤的复发和残留,从而严重影响治疗效果。因此避免肺癌的复发与转移并提供新的治疗策略是当今亟需解决的问题。肺癌组织中一部分具备自我更新和增殖分化能力、致瘤性较强、并具有特异性标志物的细胞群,它们在肺癌的发生、发展、侵袭、转移、复发以及和耐药性获得起至关重要的作用[2]。近年来多种肺癌干细胞标志物相继被发现和报道,人们对肺癌干细胞的生物学功能有了更深入的认识。这些标志物的发现为靶向肺癌干细胞的治疗提供了新的思路[3]。本实验以肺癌细胞系A549细胞模型作为研究基础,建立高转移肺癌细胞株A549-V13,并初步证实CD133为肿瘤干细胞标志物,同时研究其体内外生物学功能,为靶向肺癌干细胞的治疗提供具有前景的依据。
1 材料与方法 1.1 材料人肺癌细胞系A549由中国医学科学院肿瘤研究所细胞及分子生物学实验室保存。常规细胞培养液、表皮生长因子(EGF)、碱性成纤维细胞生长因子(bFGF)、B27购自美国Gibco公司,胎牛血清(FBS)购自美国Hyclone公司,PKH26 Red Fluorescent Cell Linker Kit和DAPI购自美国Sigma公司,FITC-CD90、PE-CD133购自美国eBioscience公司。孔径为8 μm的Transwell小室购自美国Millipore公司。
1.2 细胞株人肺癌细胞系A549用含10%FBS的Mycoo’s 5A培养液培养。无血清球体细胞培养采用含有EGF(20 ng/ml)、bFGF(20 ng/ml)、B27(1:50)的DMEM-F12无血清培养液培养,在37℃、5%CO2培养箱中培养7 d,用于A549和A549-V13的spheroid(细胞球)细胞流式细胞荧光检测。
1.3 成瘤及转移性胰酶消化细胞制成单细胞悬液,按1×106/0.2 ml剂量接种10只裸鼠右腋窝皮下,观察成瘤潜伏期及皮下瘤生长方式,观察90 d。待皮下瘤长至直径约1 cm时,取裸鼠肺转移灶。无菌环境下,将肺转移灶放入无血清的培养液中,眼科剪剪碎,过100目筛网,用吸管将细胞悬液转移至离心管中洗涤,800 r/min离心5 min。弃洗液,用6 ml细胞生长液重悬细胞,加至T25培养瓶中体外培养。细胞长满后,扩大培养。待细胞数量足量后再次接种下一批裸鼠,按以上方法接种。如此反复接种12次,依次命名为A549-V3、A549-V5、A549-V7、A549-V9、A549-V11、A549-V13。
1.4 高转移肺癌细胞的形态学观察接种消化亲本A549细胞和高转移A549细胞系制成单细胞悬液,按5×103/ml接种于24孔板,在高倍显微镜(×100)下观察从亲本A549、A549-V3、A549-V5、A549-V7、A549-V9、A549-V11到A549-V13的形态学变化。
1.5 spheroid培养及A549-V13细胞PKH26染色将A549-V13消化为单个细胞后,按PKH26染料试剂盒说明书进行标记,1×104/ml的浓度置于含EGF(20 ng/ml)、bFGF(20 ng/ml)、B27(1:50)的DMEM-F12培养液中,于37℃、5%CO2培养箱中培养7 d,用于球体细胞免疫荧光。
1.6 流式细胞术分选A549、A549-V13中CD133+和CD90+细胞无菌环境中消化细胞为单细胞悬液,PBS洗两次,加入流式细胞标记CD133和CD90抗体,细胞孵育密度为1×107/ml,室温孵育1 h,PBS洗3次,室温孵育60 min,再用PBS洗涤3次,最后用含1%BSA的PBS重悬,流式细胞荧光分选仪检测阳性细胞比例或分选。
1.7 无血清悬浮培养检测A549和A549-V13细胞中CD133+自我更新能力分选A549和A549-V13的单细胞悬液以500个每孔接种于低黏附24孔板,进行0.8%甲基纤维素固体无血清悬浮培养,7~10 d后显微镜下计成球数。
1.8 Transwell侵袭实验检测A549和A549-V13中CD133+细胞侵袭能力分选A549和A549-V13细胞中CD133+、CD133-和亲本细胞,37℃孵育2 h,以4×104个每孔接种于预先包被好Matrigel胶的Transwell上室中,在37℃、5%CO2培养箱中培养24 h后,取下底膜,DAPI染色,封片,在荧光显微镜下观察穿膜细胞并计数。
1.9 CCK-8法检测A549和A549-V13细胞中CD133+细胞耐药性将流式细胞仪分选得到的CD133+细胞、亲本细胞、CD133-细胞以2 000个每孔接种于96孔板,每组细胞均用含0、0.15、0.3、0.6、0.9 μmol/L的5种不同浓度顺铂的培养液、37℃、5%CO2培养箱中培养,3 d换液,7 d后按照CCK-8试剂盒说明书加入CCK-8试剂,测定OD450值,用IC50软件计算各组IC50值。
1.10 BALB/c裸鼠致瘤实验检测A549和A549-V13细胞中CD133+致瘤性动物在实验前一天称重,按体质量分组使各种体质量的裸鼠在各组中平均分布,每组6只,A549和A549-V13流式分选细胞亚群(亲本、CD133+、CD133-细胞),各亚群按照2×102、2×103、2×104细胞数量分组,计数重悬于0.2 ml PBS中,一共18组。分选计数后接种于每只裸鼠右侧腋下,以各自的亲本组作为对照每周观察动物成瘤情况,3~4月后采用引颈法处死动物。
1.11 统计学方法用SPSS13.0统计学软件,计量数据以(x±s)表示,两组间均数比较采用t检验,P<0.05为差异有统计学意义。
2 结果 2.1 建立具有高转移潜力的细胞株A549-V13将裸鼠肺部转移灶接种至皮下成瘤后,通过机械分离法,获取转移性细胞株,从A549、A549-V3、A549-V5、A549-V7、A549-V9、A549-V11到A549-V13细胞生长稳定。初步建立肺癌细胞系A549的第十三代稳定的高转移细胞株,命名为A549-V13。
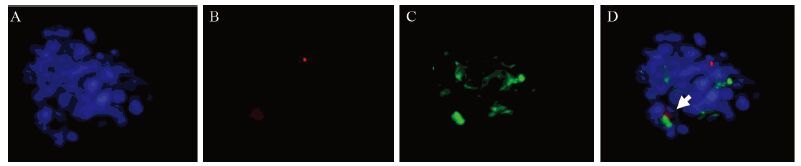
2.2 PKH26染色证明A549-V13中存在肿瘤干细胞将培养7 d中A549-V13的spheroid球体细胞固定后经细胞免疫荧光检测发现,肿瘤干细胞标志物CD133可识别标识PKH26荧光的肺癌干细胞,见图 1。
|
| A: DAPI; B: PKH26; C: CD133; D: Merge 图 1 免疫细胞荧光检测spheroid细胞中PKH26与CD133共染情况 (×400) Figure 1 Co-staining of PKH26 and CD133 in spheroid cells detected by immunofluorescence (×400) |
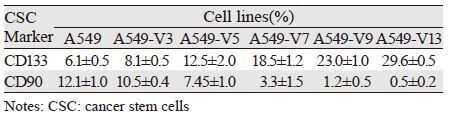
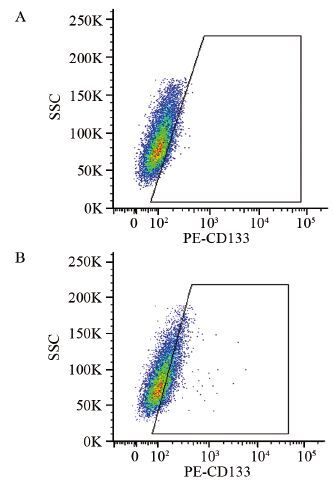
CD133[4]和CD90[5]是公认的肺癌干细胞标志物,在肺癌细胞系和组织中均得到证实。采用流式细胞术检测标志物CD133和CD90在A549亲本细胞及相关高侵袭细胞亚系中的表达情况,流式细胞结果显示,CD133在A549及其高侵袭细胞株A549-V13的表达比例逐渐升高,其中A549-V13中CD133+相比A549中CD133+提高4.85倍(29.6±0.5 vs. 6.1±0.5)%,而A549-V13中CD90+相比A549中CD90+降低了24.2倍(0.5±0.2 vs. 12.1±1.0)%,CD90+在A549-V13几乎不表达,见表 1、图 2。
 |
|
| 图 2 流式细胞荧光检测CD133在A549(A)和A549-V13细胞(B)中的表达 Figure 2 Expression of CD133 in A549(A) and A549-V13 cells(B) detected by flow cytometry |
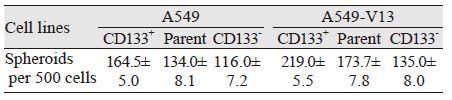
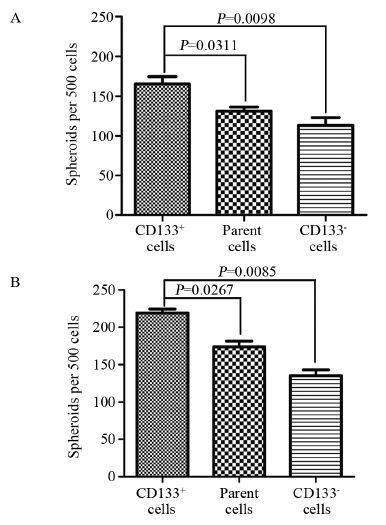
采用流式分选技术从A549和A549-V13细胞中分离出的CD133+细胞、CD133-细胞和亲本细胞进行0.8%甲基纤维素的无血清spheroid培养,7 d后观察两组细胞的成球情况。结果显示,A549-V13中CD133+细胞在无血清培养条件下成球数量显著高于亲本细胞和CD133-细胞(P<0.01),A549-V13的CD133+细胞的成球数较A549中的CD133+细胞高约1.34倍(219.0±5.5 vs. 164.5±5.0),且成球率为(43.8±1.1)% vs.(32.8±1.0)%。实验结果表明肿瘤干细胞标志物CD133在A549-V13细胞较亲本细胞具有更强的自我更新能力,干性特征更加增强,见表 2、图 3。
 |
|
| 图 3 A549(A)和A549-V13(B)的CD133+细胞、CD133-细胞和亲本细胞的自我更新能力分析 Figure 3 Self-renewal assay of CD133+,CD133- and parent cells in A549(A) and A549-V13 cells(B) |
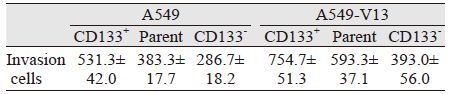
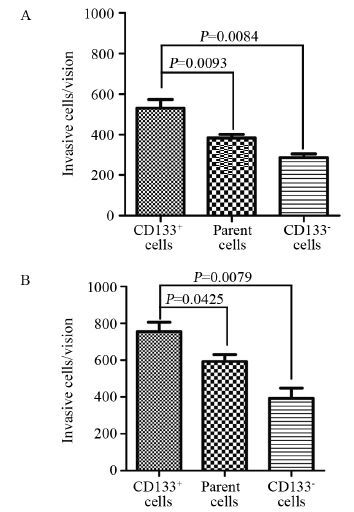
采用流式细胞分选技术从A549和A549-V13细胞中分离出CD133+细胞、CD133-细胞和亲本细胞,比较各组的侵袭能力。结果显示,A549-V13中CD133+细胞侵袭能力显著高于亲本细胞和CD133-细胞,A549-V13的CD133+细胞侵袭能力较A549中的CD133+细胞高约1.42倍(754.7±51.3 vs. 531.3±42.0),见表 3、图 4。表明肿瘤干细胞标志物CD133在A549-V13中具有更强的侵袭能力。
 |
|
| 图 4 A549(A)和A549-V13(B)的CD133+细胞、CD133-细胞和亲本细胞的侵袭能力分析 Figure 4 Invasion ability of CD133+,CD133- and parent cells in A549(A) and A549-V13 cells(B) |
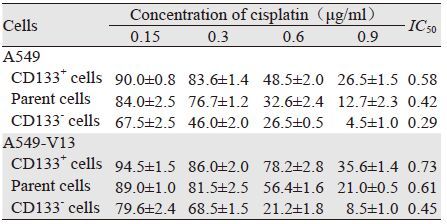
采用CCK-8法检测不同顺铂浓度下流式细胞术分选A549和A549-V13细胞中CD133+细胞、亲本细胞和CD133-细胞存活率,结果显示,A549-V13中CD133+细胞的耐药性较强,亲本细胞次之,CD133-细胞的耐药性较弱。表明A549-V13中CD133+细胞比A549中CD133+耐药性更强,其IC50提高1.26倍(0.73 vs. 0.58),证明A549-V13中CD133+细胞具有肿瘤干细胞抵抗化疗药物的特性,见表 4。
 |
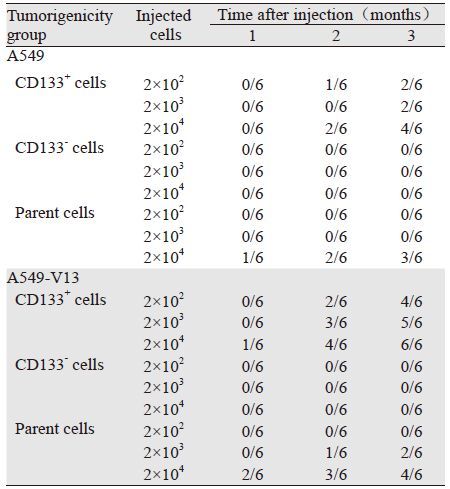
流式细胞术分选A549和A549-V13中CD133+细胞接种至4周龄左右的裸鼠体内,A549-V13中CD133-细胞在观察过程中始终没有出瘤,2月时,2×102个CD133+细胞有2/6致瘤,观察期达3月时,2×102个CD133+细胞即有4/6致瘤,而相同时间内,A549中CD133+细胞组则需2×104个细胞才能有相同的致瘤性,见表 5。说明A549-V13中CD133+细胞的致瘤性较A549中CD133+细胞强100倍,见表 5。该实验结果提示,A549-V13中CD133+细胞因富含有肿瘤干细胞而表现出强致瘤性,亲本细胞中因含较低比例的肿瘤干细胞表现出较弱的致瘤性,而CD133-组则因缺乏肿瘤干细胞而没有表现出致瘤性,即CD133+细胞的强致瘤性符合肿瘤干细胞判定的“金标准”。因此,我们认为A549-V13中CD133+细胞为肿瘤干细胞。
 |
肺腺癌是恶性肿瘤中最常见的一种。尽管有外科手术和局部的一些治疗方法,但肺癌对于传统化疗药的高抵抗性,以及肺癌的转移、复发,使得大部分肺癌患者预后不良,其中肺癌干细胞的存在被认为与肺癌的抗药性、转移及复发有着密切的关系。
目前,人们使用不同的方法已经从肺癌、肝癌、胃癌等不同组织中分离出具有不同标志物的干细胞亚群。但研究发现,不同肿瘤中的干细胞可能具有相同的标志物,而同一肿瘤中可能有多种不同的标志物,根据这些标志物在肿瘤中可以组成不同的干细胞亚群,而不同的干细胞亚群在不同肿瘤之间,甚至在同种肿瘤之间所表现出的干细胞特征并不相同[6];如CD133+表型可作为肝癌、胰腺癌、结肠癌、肺癌等肿瘤的干细胞亚群,但同时在肝癌干细胞中同样还有CD90+亚群[7],乳腺癌中还有CD44+CD24-/low亚群[8]、胰腺癌中还有CD133+CD44+CD24+亚群[9]、肺癌中还有ALDH1亚群[10]等。研究表明,不同亚群的肿瘤干细胞在体外实验中显示出不同的特性,这在一定程度上反映了不同肿瘤生物学行为的差异,同样也反映了同种肿瘤在不同个体间生物学行为的差异,有趣的是肺癌干细胞标志物CD90在高转移A549-V13几乎不表达,提示在肺癌细胞系中各肿瘤干细胞标志物亚群随着高转移细胞系的建立,其干细胞亚群的表达比例是动态变化,代表高转移肺癌的干细胞标志物CD133占主导地位。
本研究从肿瘤干细胞生物学特性出发,鉴定高转移肺癌细胞株A549-V13中的CD133+的干性特性,并进一步探讨肿瘤干细胞标志物CD133与肺癌转移和复发的相关性。结果显示,A549-V13中CD133识别的细胞经spheroid培养后可显著富集,同时CD133可与标识干细胞染料PKH26共染。为进一步证明CD133可特异性识别高转移肺癌干细胞,采用流式细胞术分选出A549-V13中CD133+细胞进行体内外功能实验,通过与A549中CD133+细胞相比,结果显示A549-V13中肿瘤干细胞标志物CD133比例显著高于A549。体内外功能显示,A549-V13中CD133+细胞具有更强的自我更新能力,侵袭能力提高1.42倍,耐药能力也显著增强,A549-V13中CD133+细胞在裸鼠皮下接种2×102个细胞3月即可致瘤(4/6),而A549中CD133+细胞接种2×102个细胞3月才能致瘤(2/6)。以上结果表明,通过连续不断筛选后建立的高转移细胞系A549-V13中,CD133的表达富集且体内外功能不断加强。综合这些实验结果,我们推测,肺癌的复发、转移和耐药与肿瘤干细胞CD133有紧密联系。本研究发现的代表肺癌转移干细胞CD133为靶向肺癌干细胞的治疗提供了新的治疗靶点,能在改善肺癌患者的预后中发挥重要作用,为我们在肺癌靶向治疗方面提供新的思路。
| [1] | Crunkhorn S. Cancer: Combination therapy for lung cancer[J]. Nat Rev Drug Discov, 2016, 15 (8) : 532. |
| [2] | Hardavella G, George R, Sethi T. Lung cancer stem cells-characteristics, phenotype[J]. Transl Lung Cancer Res, 2016, 5 (3) : 272–9. DOI:10.21037/tlcr |
| [3] | Yang J, Chen J, Wei J, et al. Immune checkpoint blockade as a potential therapeutic target in non-small cell lung cancer[J]. Expert Opin Biol Ther, 2016, 16 (10) : 1209–23. DOI:10.1080/14712598.2016.1214265 |
| [4] | Tawinwung S, Ninsontia C, Chanvorachote P. Angiotensin Ⅱ Increases Cancer Stem Cell-like Phenotype in Lung Cancer Cells[J]. Anticancer Res, 2015, 35 (9) : 4789–97. |
| [5] | Chen WJ, Ho CC, Chang YL, et al. Cancer-associated fibroblasts regulate the plasticity of lung cancer stemness via paracrine signalling[J]. Nat Commun, 2014, 5 : 3472. |
| [6] | Clevers H. The cancer stem cell: premises, promises and challenges[J]. Nat Med, 2011, 17 (3) : 313–9. |
| [7] | Yan X, Luo H, Zhou X, et al. Identification of CD90 as a marker for lung cancer stem cells in A549 and H446 cell lines[J]. Oncol Rep, 2013, 30 (6) : 2733–40. |
| [8] | Karakas D, Cevatemre B, Aztopal N, et al. Addition of niclosamide to palladium(Ⅱ) saccharinate complex of terpyridine results in enhanced cytotoxic activity inducing apoptosis on cancer stem cells of breast cancer[J]. Bioorg Med Chem, 2015, 23 (17) : 5580–6. DOI:10.1016/j.bmc.2015.07.026 |
| [9] | Vives M, Ginesta MM, Gracova K, et al. Metronomic chemotherapy following the maximum tolerated dose is an effective anti-tumour therapy affecting angiogenesis, tumour dissemination and cancer stem cells[J]. Int J Cancer, 2013, 133 (10) : 2464–72. DOI:10.1002/ijc.28259 |
| [10] | You Q, Guo H, Xu D. Distinct prognostic values and potential drug targets of ALDH1 isoenzymes in non-small-cell lung cancer[J]. Drug Des Devel Ther, 2015, 9 : 5087–97. |
 2017, Vol. 44
2017, Vol. 44
