文章信息
- CD147及其配体CypA在小鼠肝癌细胞Hepa1-6逃避T细胞免疫监视中的作用
- Role of CD147 and Its Ligand CypA in Hepatoma Carcinoma Hepa1-6 Cells Escaping from Immune Surveillance of T cells
- 肿瘤防治研究, 2017, 44(1): 17-22
- Cancer Research on Prevention and Treatment, 2017, 44(1): 17-22
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.01.004
- 收稿日期: 2016-04-25
- 修回日期: 2016-06-06
2. 116044 大连,大连医科大学基础医学院
2. College of Basic Medical Science, Dalian Medical University, Dalian 116044, China
据世界卫生组织调查,肝癌居男性恶性肿瘤发病率第五位,女性恶性肿瘤发病率第七位[1]。CD147是一种属于免疫球蛋白超家族的跨膜糖蛋白,可参与多种生理和病理生理过程[2],最典型的是作为细胞外基质金属蛋白酶诱导物(EMMPRIN)在组织重构、精子发生、神经形成及肿瘤转移中发挥作用。人类CD147分子具有269个氨基酸,细胞外区包含两个免疫球蛋白样结构域、三个糖基化位点并被高度糖基化[3]。研究表明,CD147在心血管疾病、阿尔茨海默病、免疫炎性反应、恶性肿瘤等疾病中呈高表达状态[4-6]。CD147可与亲环蛋白(cyclophilin, Cyp)结合促进免疫细胞趋化。亲环蛋白也称亲环素,发现于1984年,因其能与免疫抑制剂环孢菌素A(cyclosporinA, CsA)结合而得名。Cyp遍布于原核及真核生物中,而且含量丰富,在测定的人类所有正常和肿瘤组织中,均发现其存在[7]。CypA是亲环蛋白家族中含量最丰富的,是环孢菌素在细胞内的主要受体[8]。确定CD147作为细胞外Cyp信号受体[9]是对这一令人关注的分子生物学特性的新发现,近年来,CD147作为细胞外CypA和CypB的信号受体介导免疫细胞的趋化活性已得到证实[7]。
本研究旨在通过观察CypA对不同CD147表达水平的小鼠肝癌细胞的影响,以及对T细胞趋化作用的变化,探讨CypA和CD147分子的相互作用对肿瘤细胞和T细胞生物学行为的影响,对已有的肿瘤细胞逃避T细胞免疫监视的理论作以补充。
1 材料与方法 1.1 动物C57Bl/6j小鼠20只,雌性,6~8周,体质量(18±2)g,购于大连医科大学动物实验中心。
1.2 主要试剂DMEM培养液和RPMI 1640培养液均购自美国Gibco公司;FBS购自天津灏洋生物制品科技有限公司;DMSO购自美国Sigma公司;RIPA细胞裂解液和PMSF均购自碧云天生物有限公司;RNAiso Plus、反转录试剂盒和PCR试剂盒均购自宝生物工程有限公司;BCA蛋白含量检测试剂盒和CCK8试剂盒购自均凯基生物科技发展有限公司;NC膜购自美国Millipore公司;CD147shRNA购自上海吉玛公司;G418购自美国Calbiochem公司;重组小鼠CypA(50296-M08E)购自北京义翘神州生物技术有限公司;Anti-CD147(sc-25531)购自美国SANTA CRUS公司;Anti-GAPDH(AP0063)购自中国Bioworld生物科技有限公司;山羊抗兔IgG/HRP(ZDR-5306)购自北京中杉金桥生物技术有限公司;Anti-Mouse CD3e-PE(Catalog Number:12-0031;Clone:145-2C11)、Anti-Mouse CD19-FITC(Catalog Number:11-0193;Clone:eBio1D3)均购自美国eBioscience公司;ECL发光试剂盒购自美国Advansta公司。
1.3 主要实验器材低温超速离心机购自德国Eppendorf公司;CO2细胞培养箱购自美国Thermo Scientific公司;荧光显微镜购自日本Nikon公司;5 μm 24孔Transwell小室细胞培养板购自美国Corning公司;细胞培养皿及细胞培养板购自美国Corning公司;微量加样器购自德国Eppendorf公司;PCR仪购自美国Thermo Scientific公司;DYCZ-240型垂直板电泳槽、DYY-12型电泳仪和转膜仪均购自北京市六一仪器厂;凝胶成像分析系统购自美国Bio-Rad公司;酶标仪购自美国Thermo Electron Corporation公司;FACSealibur流式细胞仪购自美国BD公司;石蜡切片机JUNGRM2025购自德国Leica公司。
1.4 实验方法 1.4.1 细胞培养将小鼠肝癌细胞Hepa1-6接种于含10%胎牛血清(FBS),青霉素100 u/ml,链霉素100 μg/ml的DMEM培养液中,置于37℃、5% CO2的培养箱中,2天换液一次,取对数生长期细胞进行实验,用锥虫蓝拒染法检测活细胞数大于95%。
1.4.2 细胞转染及RNA干扰RNA干扰前24 h将Hepa1-6细胞培养于10%FBS的DMEM培养液中,使细胞达到60%~80%的汇合,将稀释好的含有绿色荧光蛋白(GFP)和G418抗性筛选标记的真核表达质粒载体pGPU6/GFP/Neo-CD147shRNA与Lipofectamine2000轻柔混匀,室温放置20 min,形成shRNA/Lip复合物,再将shRNA/Lip复合物加入到含有细胞和DMEM培养液的6孔板中,混合均匀。37℃、5%CO2培养箱中温育,6 h后更换培养液,24 h后更换含双抗的培养液,48 h后荧光显微镜下观察细胞转染效率。对转染后的细胞进行接种,接种当天,使用不添加G418的培养液;24 h后观察,待细胞完全贴壁后,对细胞进行换液处理,使用添加G418的完全培养液,G418终浓度为800 ng/μl;常规换液处理,维持G418浓度400 ng/μl;接种后第三周,培养皿内有单克隆形成;选取状态较好的克隆,将克隆移至96孔板进行培养,然后对克隆逐步进行放大培养,依次为96、24和6孔板,6、10 cm细胞培养皿,冻存细胞。
1.4.3 RNA提取和反转录PCR按产品说明书TRIzol法提取未转染组细胞(Hepa1-6)、转染含无义序列-shRNA的pGPU6/GFP/Neo载体组细胞(NC)及转染pGPU6/GFP/Neo-CD147shRNA后,经G418筛选得到的单细胞克隆(shRNA-C)的总RNA,并置于-80℃保存。反转录体系20 μl,包含RNA样品1 μg,按照TaKaRa反转录试剂盒说明书进行操作;反应条件为:25℃ 10 min,42℃ 60 min,99℃ 5 min,cDNA置于-20℃保存。PCR反应体系25 μl,反应条件:94℃预变性5 min;94℃变性30 s,59℃退火40 s,72℃延伸50 s,循环25次;72℃延伸10 min,4℃保存2 h。取5 μl PCR扩增产物经1%琼脂糖凝胶电泳,紫外灯下凝胶成像。CD147和GAPDH的上下游引物见表 1。
用RIPA裂解细胞,14 000 g离心15 min取上清液,蛋白浓度由BCA法检测得出。煮沸蛋白样品8 min以使其变性,以每孔30 μg的蛋白含量上样,经浓缩胶为6%、分离胶为10%的SDS-聚丙烯酰胺凝胶(SDS-PAGE)电泳分离。通过转膜仪将凝胶上的蛋白样品移至硝酸纤维素膜上,5%脱脂奶粉(用TBST配制)在室温环境中封闭2 h。分别与1:500兔抗小鼠CD147、GAPDH多克隆抗体4℃孵育过夜。用TBST洗膜3次,每次15 min。然后均匀滴加HRP标记的山羊抗兔IgG(1:3 000稀释)抗体,室温孵育1 h,再用TBST洗膜3次,每次15 min。滴加ECL发光液,于Bio-Rad凝胶成像分析系统检测结果。
1.4.5 CCK8法检测细胞增殖情况取96孔板,每孔加入100 μl含2 000个细胞的DMEM全培养液,37℃、5%CO2细胞培养箱中培养24 h。按实验分组加入CypA,使其终浓度分别为0、1、10、100、200和500 ng/ml,培养24 h。每孔加入10 μl CCK-8溶液。用只加相同量细胞培养液和CCK-8溶液的孔作为空白对照,在细胞培养箱内继续孵育1 h。酶标仪450 nm测定吸光度值。
1.4.6 流式细胞仪分选小鼠T细胞实验断颈处死C57Bl/6j小鼠,75%乙醇浸泡消毒后取脾脏和淋巴结,用玻璃注射器芯在细胞筛上研磨,制备单细胞悬液。用15 ml离心管收集悬液,1 500 r/min室温离心5 min,弃上清液。根据细胞数,加入5~10 ml FACS液,混悬,锥虫蓝计数,1 500 r/min室温离心5 min,弃上清液,加入1 ml FACS液,混悬。加入Anti-Mouse CD3e-PE/Anti-Mouse CD19-FITC,4℃避光孵育30 min。再加入9 ml FACS液,颠倒混悬2~3次,1 500 r/min室温离心5 min,弃上清液。根据细胞数,加入1~2 ml FACS液,混悬,置冰上,避光,用BD FACSAriaTMⅡ流式细胞仪分选T细胞。
1.4.7 趋化实验实验各组用含1%BSA的RPMI 1640培养液100 μl重悬小鼠T细胞,以每孔5×104个细胞接种入于Transwell上室,下室中加入500 μl含1%BSA的RPMI 1640培养液,每种细胞均分为实验组和对照组,实验组下室趋化液含200 ng/ml CypA,对照组则不含CypA,5%CO2、37℃培养箱中孵育1 h,Giemsa染色,镜检,每组设3复孔,每孔显微镜下取4个随机视野计数。趋化活性以趋化指数(chemotaxis index, CI)表示,即每个实验组与对照组迁移到下室细胞数的比值。
1.4.8 C57Bl/6j小鼠皮下成瘤实验将约107Hepa1-6细胞或Hepa1-6-CD147shRNA细胞用0.25%胰酶消化3 min后,用0.9%氯化钠溶液吹打收集,1 200 r/min离心5 min,洗涤,重复二次,用1 ml注射器接种至C57Bl/6j小鼠腹股沟皮下,使其生长20天,每5天用游标卡尺测量肿瘤大小,并按公式V=1/2×(L×W2)计算肿瘤体积。
1.5 统计学方法采用SPSS Statistics17.0统计软件,用单因素方差分析(ANOVA)比较各组间的统计学差异,两组间比较用LSD法分析,P < 0.05为差异有统计学意义。
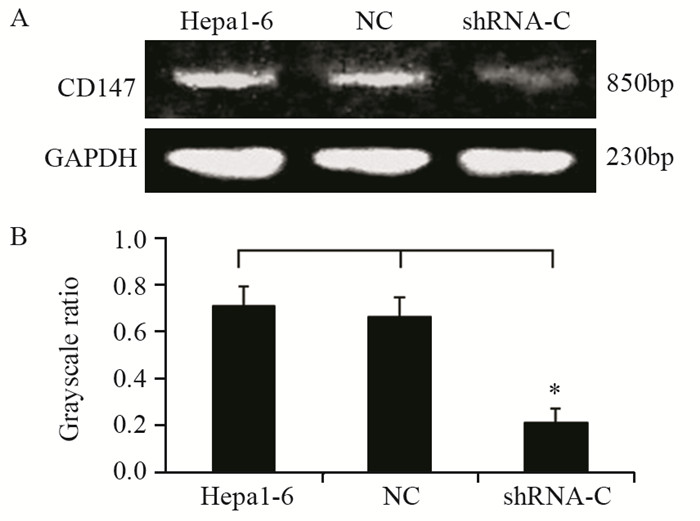
2 结果 2.1 小鼠肝癌细胞中CD147 mRNA的表达水平各组细胞的电泳条带图像经Gel-Pro Analyzer软件分析后计算灰度比值CD147/GAPDH。RT-PCR结果显示:转染pGPU6/GFP/Neo-CD147shRNA后,经G418筛选得到的单细胞克隆(shRNA-C)的CD147 mRNA水平显著低于其他组细胞,差异有统计学意义(P=0.000),Hepa1-6细胞与NC细胞的CD147 mRNA水平差异无统计学意义(P=0.281),见图 1。每组实验重复三次。
|
| A: the expression of CD147 in the cells of each group detected by RT-PCR; B: the grayscale ratio of CD147 and GAPDH in the cells of each group; Hepa1-6: Hepa1-6 cells without transfection of CD147shRNA; NC: Hepa1-6 cells transfected with pGPU6/GFP/Neo vector containing nonsense sequence shRNA; shRNA-C: After the transfection of pGPU6/GFP/Neo-CD147shRNA, the single cell clone was obtained by G418 screening; *: P < 0.01, compared with Hepa1-6 (ANOVA) cells 图 1 RT-PCR检测各组细胞中CD147 mRNA的表达情况 Figure 1 Expression of CD147 mRNA in Hepa1-6, NC and shRNA-C cells detected by RT-PCR |
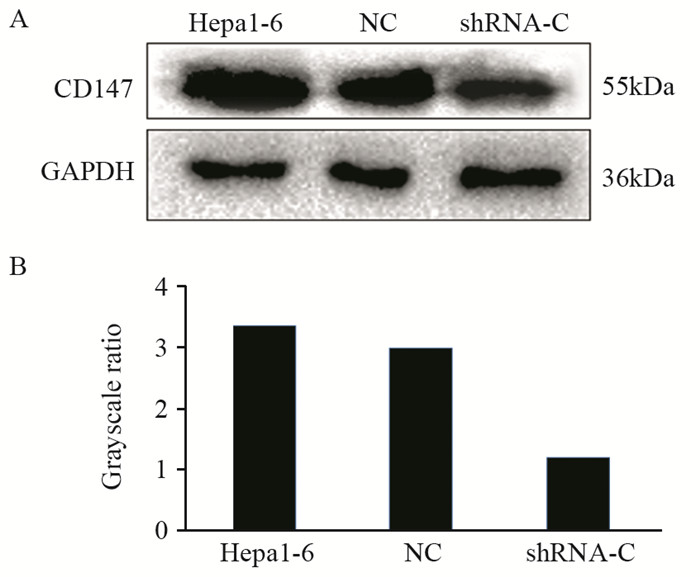
Western blot结果显示,转染pGPU6/GFP/Neo-CD147shRNA后,经G418筛选得到的单细胞克隆(shRNA-C)的CD147蛋白表达水平明显低于其他各组,见图 2。
|
| A: the expression of CD147 in the cells of each group detected by Western blot; B: tthe grayscale ratio of CD147 and GAPDH in the cells of each group 图 2 Western blot检测各组细胞中CD147蛋白的表达情况 Figure 2 Expression of CD147 protein in Hepa1-6, NC and shRNA-C cells detected by Western blot |
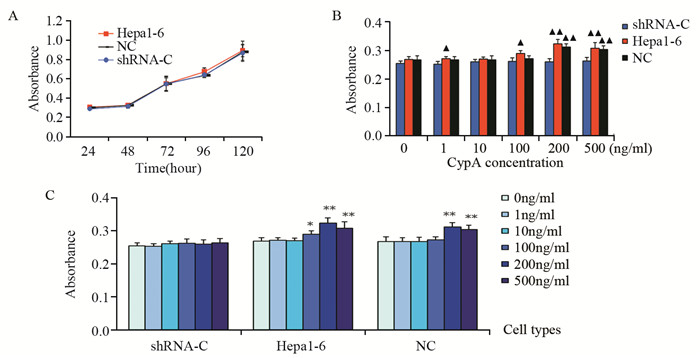
各组细胞铺板后经120 h,相互比较各时间点吸光度值,差异均无统计学意义(P > 0.05),见图 3A;各组细胞加入不同浓度的CypA后,450 nm吸光度值的比较,其中当CypA浓度达到200 ng/ml和500 ng/ml时,Hepa1-6和NC组与shRNA-C组细胞比较差异有统计学意义(P < 0.01),见图 3B;不同浓度的CypA作用于细胞24 h后,对Hepa1-6组和NC组细胞有显著的促增殖作用,而对shRNA-C组细胞的促增殖作用不明显(P > 0.05),见图 3C。
|
| A: the proliferation of Hepa1-6, NC and shRNA-C cells without CypA; B: the proliferation of the cells in each group after CypA administration, Hepa1-6, NC group were compared with shRNA-C group; C: the proliferation of the cells in each group after CypA administration, compared with 0ng/ml; ▲: P < 0.05, compared with shRNA-C group; ▲▲: P < 0.01, compared with shRNA-C group; *: P < 0.05, compared with 0ng/ml; **: P < 0.01, compared with 0ng/ml 图 3 CCK8法检测各组细胞增殖情况 Figure 3 Cells proliferation in each group detected by Cell Counting Kit-8 |
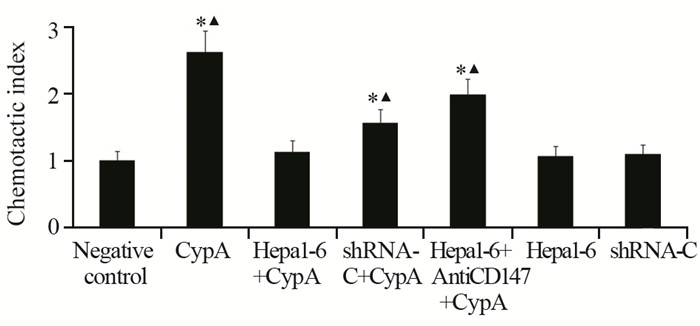
当Transwell下室中只加入200 ng/ml CypA(CypA)后,CI为2.62,与对照组(negative control)比较差异有统计学意义(P=0.000);当CypA与Hepa1-6细胞共同位于下室(Hepa1-6+CypA)时,CI为1.13,CypA对小鼠T细胞的趋化作用显著性降低(P=0.000);当CypA与shRNA-C组细胞共同位于下室(shRNA-C+CypA)或CypA与Hepa1-6细胞共同位于下室并加入CD147抗体(Hepa1-6+AntiCD147+CypA)时,CI分别为1.57和1.99,与“Hepa1-6+CypA”组比较差异有统计学意义(均P=0.000),见图 4。
|
| *: P < 0.01, compared with Hepa1-6+CypA; ▲: P < 0.01, compared with negative control 图 4 Transwell小室法检测细胞趋化作用 Figure 4 T cells chemotaxis induced by CypA detected by Transwell chamber |
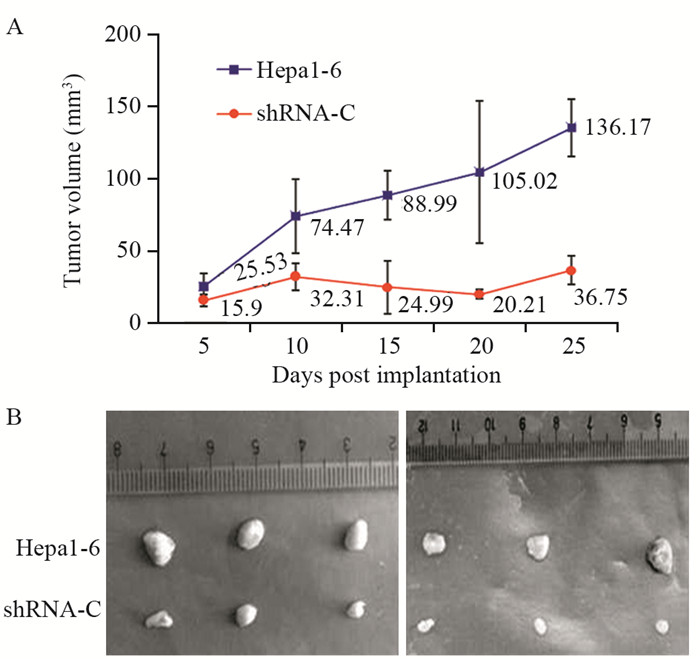
接种Hepa1-6细胞和shRNA-C细胞10天后,两组肿瘤体积比较差异有统计学意义(P=0.014),见图 5A;接种细胞20天后解剖小鼠取出肿瘤,可见Hepa1-6细胞的成瘤体积明显大于shRNA-C细胞的成瘤体积,见图 5B。
|
| A: tumor size was measured on day 5, 10, 15, 20 and 25 after the injection and tumor volume was calculated as V=1/2×(L×W2); B: tumors were excised for gross comparision on day 20 after the injection 图 5 C57Bl/6j小鼠皮下成瘤实验 Figure 5 Subcutaneous tumor formation in c57bl/6j mice |
大量研究证实,CD147在正常组织细胞中弱表达或不表达,而在心血管疾病、阿尔茨海默病、免疫炎性反应,尤其是恶性肿瘤中呈高表达状态。现已检测出CD147在肝癌、肺癌、乳腺癌、头颈鳞癌、前列腺癌、黑色素瘤、胶质瘤、淋巴瘤等多种恶性肿瘤细胞中高表达,具有刺激基质细胞产生基质金属蛋白酶,导致细胞外基底膜降解、基质渗透以及促进肿瘤细胞侵袭和转移的作用[4-6]。CD147除在肿瘤细胞中高表达外,也普遍存在于免疫细胞的表面,在活化的T细胞、B细胞、树突状细胞、单核细胞和巨噬细胞中也呈高表达状态[10],其对免疫细胞的成熟、活化和趋化至关重要。研究表明,CD147在肝癌细胞中明显上调,与肝癌的侵袭、转移、细胞增殖和代谢、抗凋亡及抵抗氧化应激机制密切相关[11-15]。Cyp的130多个成员[16]中,与CD147相互作用关系研究较多的是CypA和CypB,而这些研究大多是针对免疫炎性反应方面的[3]。CypA主要分布于胞质,是一种高度保守的蛋白,具有肽酰脯氨酰顺反异构酶(PPIase)活性,参与蛋白折叠、组装、胞内运输及信号转导等,具有分子伴侣的作用。血管平滑肌细胞在受到氧化应激后可分泌CypA,促进内皮细胞增殖[17]。对Cyp的研究虽大部分集中在细胞内,但越来越多的研究结果表明,Cyp在胞外也具有重要的功能。如CypA和CypB这两种Cyp家族中最丰富的成员,能够启动靶细胞的信号事件[3]。除CypA和CypB外,还没有证据证明Cyp家族中的其他成员能够被分泌到细胞外[3],胞外存在这些蛋白质的原因是由于细胞死亡释放。CypB在人乳和血浆中均可被检测到,CypA则主要由于细胞受到炎性刺激和氧化应激时被分泌到细胞外。在动脉粥样硬化中,内皮细胞、单核细胞、血管平滑肌细胞及血小板可在过量的活性氧作用下分泌CypA至细胞外[18]。CypA也与T细胞等炎性细胞的功能相关,分泌型CypA能介导中性粒细胞、单核细胞及嗜酸粒细胞等炎性细胞的趋化[19]。研究表明,CypA与CDl47能以配体-受体的形式结合参与中性粒细胞、嗜酸粒细胞及T细胞的趋化[20-21]。
本研究首先检测细胞外CypA对不同CD147表达水平的小鼠肝癌细胞Hepa1-6增殖情况的影响,结果显示下调Hepa1-6细胞的CDl47水平后,显著降低了CypA对肿瘤细胞的促增殖作用,再次证明了CypA可通过与肿瘤细胞的CD147作用促进其增殖[22]。为了探讨CypA在不同CD147水平的肿瘤细胞的干预下,其趋化T细胞的能力是否会有变化,本研究利用Transwell小室法检测其趋化活性,结果显示,在加入Hepa1-6细胞后,CypA趋化T细胞的能力与加入Hepa1-6-CD147shRNA细胞相比,有显著降低,说明肿瘤细胞有可能利用其CD147抑制CypA趋化T细胞,进而逃避T细胞的免疫监视作用。本研究的体内实验显示Hepa1-6细胞在C57Bl/6j小鼠皮下的成瘤体积显著大于Hepa1-6-CD147shRNA细胞在C57Bl/6j小鼠皮下的成瘤体积,表明了在体内环境中CD147表达水平较高的肿瘤细胞的生存状况优于CD147表达水平较低的肿瘤细胞。这些实验结果可以证明在肿瘤细胞逃避T细胞的免疫监视过程中,CDl47参与了CypA对细胞生物学特性的影响,这即对已有的肿瘤细胞逃避T细胞免疫监视的理论作以补充,也为将其作为新的肿瘤治疗靶分子提供了更充实的理论依据。
| [1] | El-Serag HB. Hepatocellular carcinoma[J]. N Engl J Med, 2011, 365 (12) : 1118–27. DOI:10.1056/NEJMra1001683 |
| [2] | Landskron J, Taskén K. CD147 in regulatory T cells[J]. Cell Immunol, 2013, 282 (1) : 17–20. DOI:10.1016/j.cellimm.2013.04.008 |
| [3] | Yurchenko V, Constant S, Eisenmesser E, et al. Cyclophilin-CD147 interactions: a new target for anti-inflammatory therapeutics[J]. Clin Exp Immunol, 2010, 160 (3) : 305–17. DOI:10.1111/cei.2010.160.issue-3 |
| [4] | Iacono KT, Brown AL, Greene MI, et al. CD147 immunoglobulin superfamily receptor function and role in pathology[J]. Exp Mol Pathol, 2007, 83 (3) : 283–95. DOI:10.1016/j.yexmp.2007.08.014 |
| [5] | Kanekura T, Chen X. CD147/basigin promotes progression of malignant melanoma and other cancers[J]. J Dermatol Sci, 2010, 57 (3) : 149–54. DOI:10.1016/j.jdermsci.2009.12.008 |
| [6] | Kim K, Kim H, Jeong K, et al. Release of overexpressed CypB activates ERK signaling through CD147 binding for hepatoma cell resistance to oxidative stress[J]. Apoptosis, 2012, 17 (8) : 784–96. DOI:10.1007/s10495-012-0730-5 |
| [7] | Yurchenko V, Constant S, Bukrinsky M. Dealing with the family: CD 147 interactions with cyclophilins[J]. Immunology, 2006, 117 (3) : 301–9. DOI:10.1111/imm.2006.117.issue-3 |
| [8] | Liu X, Zhao Z, Liu W. Insights into the roles of cyclophilin A during influenza virus infection[J]. Viruses, 2013, 5 (1) : 182–91. DOI:10.3390/v5010182 |
| [9] | Yurchenko V, Zybarth G, O'Connor M, et al. Active site residues of cyclophilin A are crucial for its signaling activity via CD147[J]. J Biol Chem, 2002, 277 (25) : 22959–65. DOI:10.1074/jbc.M201593200 |
| [10] | Malesevic M, Gutknecht D, Prell E, et al. Anti-inflammatory Effects of Extracellular Cyclosporins Are Exclusively Mediated by CD147[J]. J Med Chem, 2013, 56 (18) : 7302–11. DOI:10.1021/jm4007577 |
| [11] | Ru NY, Wu J, Chen ZN, et al. HAb18G/CD147 is involved in TGF-β-induced epithelial-mesenchymal transition and hepatocellular carcinoma invasion[J]. Cell Biol Int, 2015, 39 (1) : 44–51. DOI:10.1002/cbin.v39.1 |
| [12] | Liang Q, Han Q, Huang W, et al. HAb18G/CD147 regulates vinculin-mediated focal adhesion and cytoskeleton organization in cultured human hepatocellular carcinoma cells[J]. PLoS One, 2014, 9 (7) : e102496. DOI:10.1371/journal.pone.0102496 |
| [13] | Huang Q, Li J, Xing J, et al. CD147 promotes reprogramming of glucose metabolism and cell proliferation in HCC cells by inhibiting the p53-dependent signaling pathway[J]. J Hepatol, 2014, 61 (4) : 859–66. DOI:10.1016/j.jhep.2014.04.035 |
| [14] | Tang J, Guo YS, Zhang Y, et al. CD147 induces UPR to inhibit apoptosis and chemosensitivity by increasing the transcription of Bip in hepatocellular carcinoma[J]. Cell Death Differ, 2012, 19 (11) : 1779–90. DOI:10.1038/cdd.2012.60 |
| [15] | Kim K, Kim H, Jeong K, et al. Release of overexpressed CypB activates ERK signaling through CD147 binding for hepatoma cell resistance to oxidative stress[J]. Apoptosis, 2012, 17 (8) : 784–96. DOI:10.1007/s10495-012-0730-5 |
| [16] | Romano PG, Horton P, Gray JE. The Arabidopsis cyclophilin gene family[J]. Plant Physiol, 2004, 134 (4) : 1268–82. DOI:10.1104/pp.103.022160 |
| [17] | Yang H, Li M, Chai H, et al. Effects of cyclophilin A on cell proliferation and gene expressions in human vascular smooth muscle cells and endothelial cells[J]. J Surg Res, 2005, 123 (2) : 312–9. DOI:10.1016/j.jss.2004.08.026 |
| [18] | Tian-Tian Z, Jun-Feng Z, Heng G. Functions of cyclophilin A in atherosclerosis[J]. Exp Clin Cardiol, 2013, 18 (2) : e118–24. |
| [19] | Bukrinsky MI. Cyclophilins: unexpected messengers in intercellular communications[J]. Trends Immunol, 2002, 23 (7) : 323–5. DOI:10.1016/S1471-4906(02)02237-8 |
| [20] | Sherry B, Yarlett N, Strupp A, et al. Identification of cyclophilin as a proinflammatory secretory product of lipopolysaccharide-activated macrophages[J]. Proc Natl Acad Sci U S A, 1992, 89 (8) : 3511–5. DOI:10.1073/pnas.89.8.3511 |
| [21] | Damsker JM, Bukrinsky MI, Constant SL. Preferential chemotaxis of activated human CD4+ T cells by extracellular cyclophilin A[J]. J Leukoc Biol, 2007, 82 (3) : 613–8. DOI:10.1189/jlb.0506317 |
| [22] | Obchoei S, Weakley SM, Wongkham S, et al. Cyclophilin A enhances cell proliferation and tumor growth of liver fluke-associated cholangiocarcinoma[J]. Mol Cancer, 2011, 10 : 102. DOI:10.1186/1476-4598-10-102 |
 2017, Vol. 44
2017, Vol. 44



