文章信息
- GSTP1基因对人肝癌细胞系HepG2增殖和侵袭能力的影响
- Effects of GSTP1 on Proliferation and Invasion of Human HepG2 Cells
- 肿瘤防治研究, 2016, 43(12): 1039-1042
- Cancer Research on Prevention and Treatment, 2016, 43(12): 1039-1042
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2016.12.006
- 收稿日期: 2016-03-29
- 修回日期: 2016-06-23
2. 050000 石家庄,河北医科大学第二医院体检中心;
3. 050057 石家庄,河北省人民医院消化内科;
4. 063000 唐山,唐山市工人医院肝胆外科
2. Physical Examination Center, The Second Affiliated Hospital of Hebei Medical University, Shijiazhuang 050000, China;
3. Department of Gastroenterology, Hebei General Hospital, Shijiazhuang 050057, China;
4. Department of Hepatobiliary Surgery, Tangshan Gongren Hospital, Tangshan 063000, China
谷胱甘肽S-转移酶(glutathione S-transferases, GSTs)是具有多种亚家族、多基因和多种生理功能的一组超基因家族,因在致癌物解毒和抗癌药物代谢中所起的重要作用而得到不断深入的研究。近年来大量研究结果表明,许多肿瘤的发病危险度与GST多态性明显相关[1-6]。GSTs的分子基因多态性可引起酶分子结构、功能和水平的改变,从而影响细胞的解毒能力,因此被认为与肿瘤易感性有关[7],近年来研究认为GSTs多态性可能与恶性白血病[1-2]、肺癌[3]、乳腺癌[4-5]和前列腺癌[6]等恶性肿瘤的发生相关。目前研究发现肝癌的发生和预后同时受到环境因素[8]、治疗手段和肿瘤遗传易感性的影响,而个体对肝癌的遗传易感性与机体对致癌物质的解毒能力密切相关。本实验采取腺病毒载体转染的手段,获得过表达/沉默GSTP1基因的HepG2细胞,通过CCK-8法和Transwell小室法检测转染腺病毒后HepG2细胞的细胞活力和侵袭能力的变化,以及采用Western blot检测相关蛋白表达的变化。
1 材料与方法 1.1 材料人肝癌细胞系HepG2(中南大学湘雅医院细胞中心,中国);过表达/沉默GSTP1(Ad-GSTP1/ Ad-shGSTP1)腺病毒及病毒载体(上海和元生物有限公司,中国);RPMI 1640培养液,胰蛋白酶,CCK-8试剂(Sigma公司,美国);DMEM培养液(Gibco公司,美国);Transwell小室(Corning公司,美国);Trizol和引物(Invitrogen公司,美国)抗Akt(sc-8312) 、mTOR (sc-8319) 、p-Akt (sc-135651)、p-mTOR抗体 (sc-101738) 和HRP标记抗兔二抗(sc-2030)(Santa Cruz公司,美国)。
1.2 方法 1.2.1 细胞培养和分组将人肝癌细胞系HepG2置于含10%胎牛血清的RPMI 1640培养液中,在5%CO2、37℃恒温培养箱中进行贴壁培养,待细胞增殖至培养瓶的80%~90%时,用胰蛋白酶进行消化,传代。实验分为:空白对照组(Control);载体组(Vehicle):转染空载病毒;高表达组(Ad-GSTP1):转染GSTP1腺病毒;低表达组(Ad-shGSTP1):转染Ad-shGSTP1腺病毒。
1.2.2 腺病毒载体转染在进行腺病毒转染前18 h,将HepG2细胞以1×105个/孔铺到96孔板中,在转染时培养至约2×105个/孔。更换含6 μg/ml聚凝胺的2 ml新鲜培养液,加入适量病毒悬液,于37℃孵育24 h,用新鲜培养液更换含病毒的培养液,继续培养。
1.2.3 实时荧光定量PCR(qPCR)法检测转染细胞中GSTP1的mRNA表达收集各组细胞,按照TRIzol说明书裂解细胞,使用氯仿提取总RNA,用紫外分光光度法测定RNA样品的A260值,并进行定量。建立反转录反应,GSTP1的mRNA上游引物:5’-TATTTCCCAGTTCGAGGCCG-3’,下游引物:5’-TCCTGCTGGTCCTTCCCATA-3’;内参GAPDH的mRNA上游引物:5’- CTCTGCTCCTCCTGTTCGAC-3’,下游引物:5’- GCGCCCAATACGACCAAATC-3’。扩增条件为:94℃ 5 min、92℃ 30 s、62℃ 30 s、74℃ 1 min,32个循环。反应结束后,标准曲线和扩增曲线PCR仪器自动生成,所得结果直接在荧光定量操作系统中进行比较分析,目标基因的相对定量用2-ΔΔCT计算。
1.2.4 CCK-8法检测各组细胞的细胞活力收集经相应处理后的各组细胞,以2×103微升/孔铺到96孔板中,每孔加入RPMI 1640培养液100 μl,继续培养,分别在6、12和24 h后加入10 μl LCCK-8溶液,置于37℃、5%CO2恒温培养箱中培养4 h。于波长450 nm处检测各孔吸光度值(A),每组设6复孔。另设单孔只加入培养液不加入HepG2细胞作为空白对照,计算各组细胞的细胞活力。
1.2.5 Transwell侵袭实验收集经相应处理后各组细胞,离心后弃上清液,调整细胞为2×108个/毫升,向已用Matrigel包被的小室底部膜上室面的小室中加入200 μl细胞悬液,并在下室中加入500 μl含有10%胎牛血清的DMEM培养液;将Transwell小室置于37℃、5%CO2的培养箱中培养20~24 h,弃去上室培养液,用5%戊二醛固定15 min,4℃;PBS洗涤,0.1%结晶紫染色5 min,蒸馏水漂洗,用棉球轻轻擦去小室上表面细胞,置于光学显微镜下观察,5倍目镜,40倍物镜,选取3个视野,计数染色细胞。
1.2.6 Western blot检测相关蛋白表达离心收集经相应处理的各组细胞,提取总蛋白并测定蛋白浓度,每道加入50 μg蛋白进行SDS-PAGE电泳,电转至PVDF膜上,用含5%脱脂奶粉的PBS缓冲液封闭1 h,加入相应一抗,4℃,过夜,再加入相应二抗,室温,1 h,化学发光法显色,ChemiDocMP全能型成像分析系统保存图像。
1.3 统计学方法所有数据采用SPSS15.0统计软件进行统计分析。实验数据采用均数±标准差(x±s)表示,组间采用单因素方差分析(One-way ANOVA),各组均数间两两比较采用bonferroni校正的t检验,以P<0.05为差异具有统计学意义。
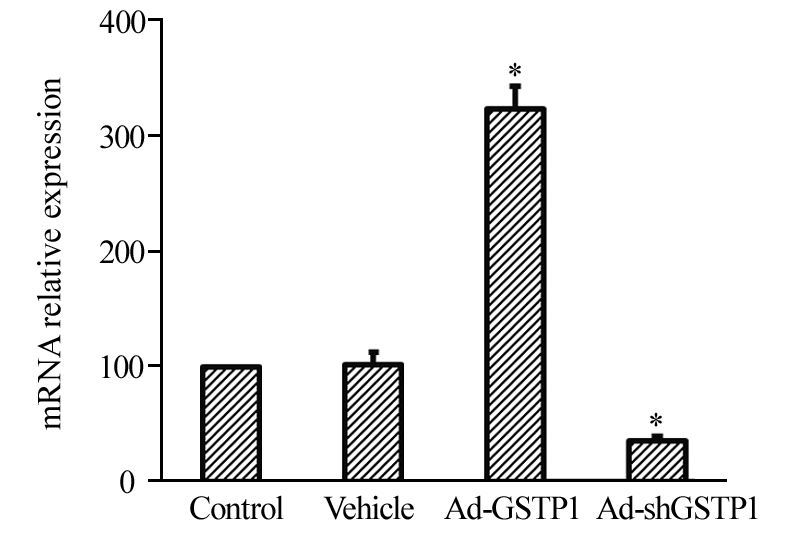
2 结果 2.1 qPCR法检测GSTP1的mRNA表达水平采用病毒转染后,与Control组相比,Ad-GSTP1组中GSTP1呈高表达(P=0.01),Ad-shGSTP1组中GSTP1 mRNA呈低表达(P=0.01),提示病毒转染成功,见图 1。
|
|
*: P<0.05, compared with Control group Ad-GSTP1 HepG2 cells were infected with Ad-GSTP1; Ad-shGSTP1 HepG2 cells were infected with Ad-shGSTP1 图 1 病毒转染后HepG2细胞中GSTP1的相对mRNA表达水平 (n=3) Figure 1 mRNA expression of GSTP1 in HepG2 cells after transfection with virus (n=3) |
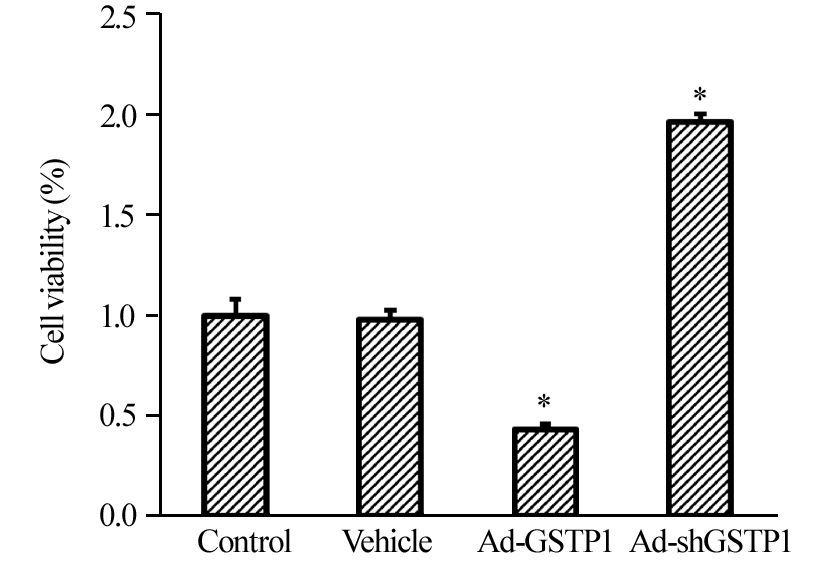
过表达/沉默GSTP1后,与Control相比,过表达GSTP1后,HepG2细胞的细胞活力显著降低(P=0.01),而沉默GSTP1后,HepG2细胞的细胞活力显著升高(P=0.02),见图 2。
|
| *: P<0.05, compared with Control group 图 2 各组HepG2细胞的细胞活力变化 (n=3) Figure 2 Cell viability of HepG2 cells in each group (n=3) |
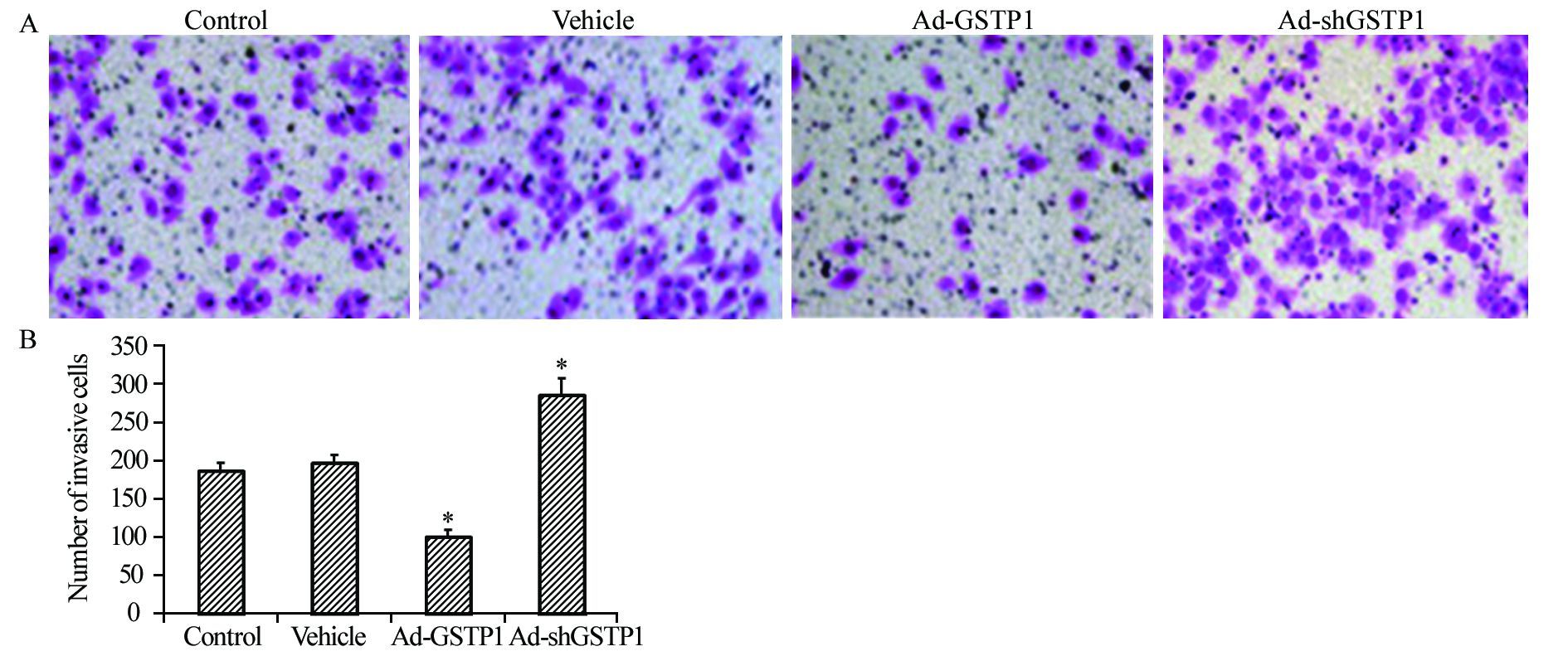
过表达/沉默GSTP1后,过表达GSTP1可显著降低HepG2细胞的侵袭能力(P=0.03),而沉默GSTP1则显著增加其侵袭能力(P=0.02),见图 3。
|
| A: dyeing figure of Transwell invasion assay (×200) ; B: the number of invasive cells; *: P<0.05, compared with Control group (n=3) 图 3 各组HepG2细胞侵袭能力的变化 Figure 3 Invasion ability of HepG2 cells in each group |
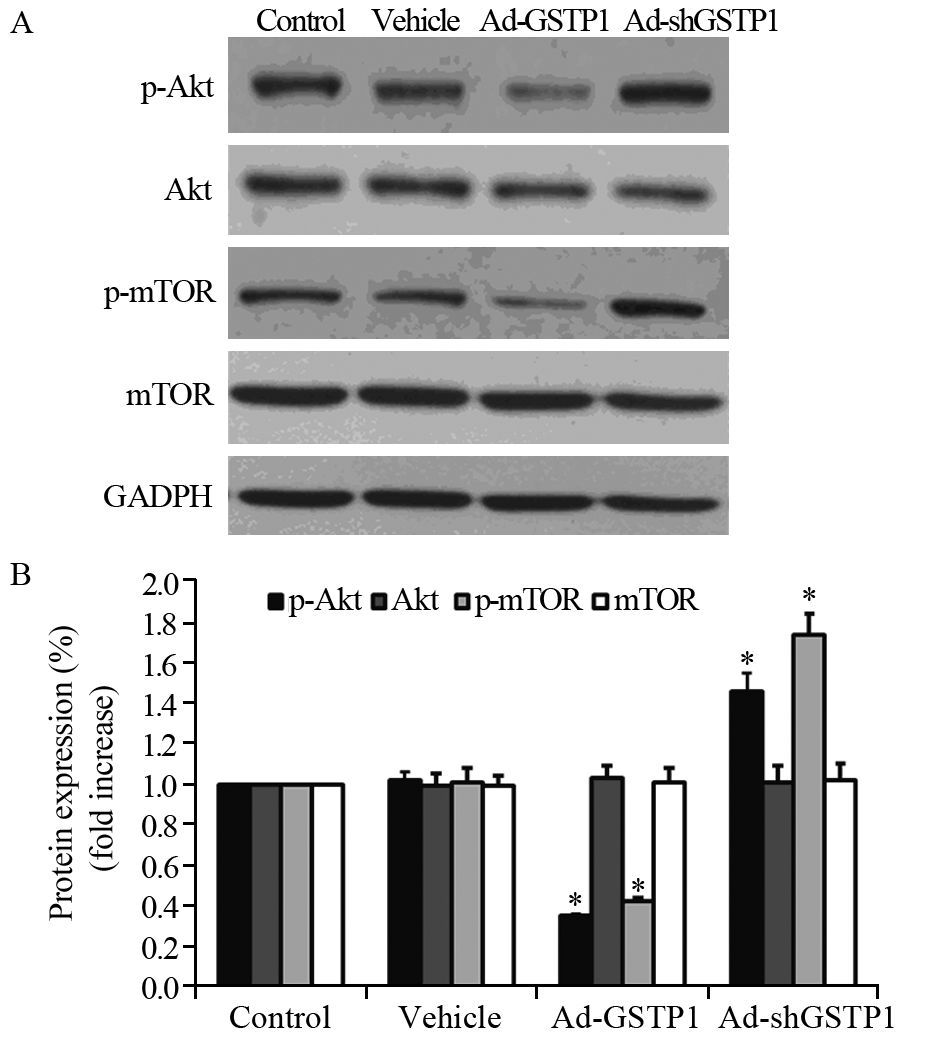
与Control相比,过表达GSTP1后,HepG2细胞中Akt和mTOR的蛋白表达没有显著变化,p-Akt(P=0.03)和p-mTOR(P=0.01)的蛋白表达显著降低;p-Akt和p-mTOR的蛋白表达结果则显著增加,见图 4。
|
| A: Western blot assay of Akt, mTOR, p-Akt and p-Mtor expression; B:Graph of Western blot band; *: P<0.05, compared with Control group 图 4 各组HepG2细胞的Akt、mTOR、p-Akt、p-mTOR的蛋白表达水平 (n=3) Figure 4 Protein expression of Akt, mTOR, p-Akt and p-mTOR in HepG2 cells of each group (n=3) |
在哺乳动物,GSTs至少有5种亚型13个同工酶,一种结合于内质网膜上,称为微粒体GST, 另外4种亚型存在于胞质中,根据物理化学性质和基因结构差异分别命名为GSTα(GSTA)、GSTθ (GSTT)、GSTμ(GSTM)和GSTπ(GSTP)[9]。微粒体GST基因定位于第12号染色体,胞质GSTα、θ、μ和π则分别定位于6号、22号、1号和11号染色体[9]。外源性物质进入体内的代谢通常分为两步进行,先由Ⅰ相代谢酶细胞色素P450(CYP)催化羟基化、还原、氧化等反应,使外源物激活为活性或毒性更强的物质,再由Ⅱ相代谢酶GST或N-乙酰基转移酶(NAT)催化结合反应,使结合产物灭活,并增加代谢产物水溶性以利排泄。一方面,GST可以将谷胱甘肽(GSH)以阴离子(GS-)形式结合于亲电性的内源化合物(如白三烯类)和外源性物质 (如致癌物、抗肿瘤药物等);另一方面,GST本身具有配基结合蛋白性质,可以结合非底物性的疏水配基如亚铁血红素、胆红素、甾醇类等以及亲脂性的抗癌药物,以增加这些化合物的化学稳态,或进行灭活反应,从而发挥解毒功能[10]。研究表明,肝癌患者的GSTP1基因中1a/1a、1a/1b和1b/1b亚型的发生率也与正常人群中的发生率存在显著性差异,携带GSTP1Ⅴal/Ⅴal基因的人发生肝癌的风险是对照组人群的1.93倍[11]。同时,GSTP1Ⅱe/Ⅴal或携带GSTP1Ⅴal/Ⅴal基因的肿瘤患者预后比携带GSTP1Ⅱe/Ⅱe基因型的患者预后好,相对危险度HR为0.34[11]。同样,GSTs基因多态性同样有可能影响肿瘤的治疗尤其是化疗效果,对肿瘤患者生存率造成影响。
PI3K-Akt/mTOR信号通路广泛存在于细胞中,通过磷酸化调控许多与细胞增殖、分化、代谢和凋亡有关的蛋白,进而抑制细胞的凋亡并促进肿瘤的生长。Akt是PI3k主要的下游信息转导途径,PI3k被激活后可导致Akt的磷酸化,使其获得最大活性。mTOR是PI3K/Akt通路的下游效应物,Akt活化后继而会导致mTOR的磷酸化[12-13]。肿瘤细胞中Akt通道激活后,导致mTOR的过度激活,可促使细胞周期大大加快[14]。本实验结果显示过表达GSTP1后,HepG2细胞中p-Akt和p-mTOR的蛋白表达显著降低,而沉默GSTP1则p-Akt和p-mTOR的蛋白表达显著增加,提示GSTP1基因可能通过Akt/mTOR信号通路调控HepG2细胞的增殖能力。
在分子水平上,通过构建过表达/沉默GSTP1基因的人肝癌HepG2细胞,结果发现,当过表达GSTP1基因时,HepG2细胞的增殖与侵袭能力显著降低,而当沉默GSTP1基因后,HepG2细胞的增殖与侵袭能力则显著增加,提示GSTP1基因可能与肝癌的发生发展有关系,其作用机制可能与PI3K/Akt/mTOR信号通路有关。
| [1] | Guven M, Unal S, Erhan D, et al. Role of glutathione S-transferase M1, T1 and P1 gene polymorphisms in childhood acute lymphoblastic leukemia susceptibility in a Turkish population[J]. Meta Gene, 2015, 5 : 115–9. DOI:10.1016/j.mgene.2015.06.002 |
| [2] | Kassogue Y, Dehbi H, Quachouh M, et al. Association of glutathione S-transferase (GSTM1 and GSTT1) genes with chronic myeloid leukemia[J]. Springerplus, 2015, 4 : 210. DOI:10.1186/s40064-015-0966-y |
| [3] | Wang Y, Ren BU, Zhang L, et al. Correlation between metabolic enzyme GSTP1 polymorphisms and susceptibility to lung cancer[J]. Exp Ther Med, 2015, 10 (4) : 1521–7. |
| [4] | Sun N, Sun X, Chen B, et al. MRP2 and GSTP1 polymorphisms and chemotherapy response in advanced non-small cell lung cancer[J]. Cancer Chemother Pharmacol, 2010, 65 (3) : 437–46. DOI:10.1007/s00280-009-1046-1 |
| [5] | Zhong SL, Jiang SG, Tang JH, et al. Association of GSTs gene polymorphism with reponse to chemotherapy in breast cancer[J]. Lin Chuang Jian Yan Za Zhi, 2010, 28 (6) : 438–4. [ 钟山亮, 蒋胜高, 唐金海, 等. 谷胱甘肽S转移酶基因多态性与乳腺癌化疗疗效的关系[J]. 临床检验杂志, 2010, 28 (6) : 438–4. ] |
| [6] | Kwom DD, Lee JW, Han DY, et al. Relationship between the glutathione-S-transferase P1, M1, and T1 genotypes and prostate cancer risk in korean subjects[J]. Korean J Urol, 2011, 52 (4) : 247–52. DOI:10.4111/kju.2011.52.4.247 |
| [7] | Zhao YJ. The research of the relationship between the polymorphisms of GSTM1, GSTT1 and GSTP1 with cliniopathology features, chemotherapy response and toxicities in breast cancer[D]. Ningxia Yi Ke Da Xue, 2014. [ 赵艳姣. GSTM1、GSTT1和GSTP1基因多态性与乳腺癌临床病理特征、化疗疗效及毒性的研究[D]. 宁夏医科大学, 2014. ] |
| [8] | Su CH. The association study between HBV infection, environmental factors, polymorphisms and the risk of heptatocellular carcinoma in Xiamen[D]. Fujian Yi Ke Da Xue, 2015. [ 苏成豪. 厦门地区HBV感染、环境因素及基因多态性与原发性肝癌的关联研究[D]. 福建医科大学, 2015. ] |
| [9] | Orlewski J, Orlewska E. Effects of genetic polymorphisms of glutathione S-transferase genes (GSTM1, GSTT1, GSTP1) on the risk of diabetic nephropathy: a meta-analysis[J]. Pol Arch Med Wewn, 2015, 125 (9) : 649–58. |
| [10] | Shaban NZ, Salem HH, Elsadany MA, et al. Distribution of Glutathione S-Transferase Omega Gene Polymorphism with Different Stages of HBV Infection Including Hepatocellular Carcinoma in the Egyptian Population[J]. Asian Pac J Cancer Prev, 2016, 17 (4) : 2145–50. DOI:10.7314/APJCP.2016.17.4.2145 |
| [11] | Li CG, Zhao ZM, Hu MG, et al. Predictive role of glutathione-S transferase gene polymorphisms in risk and prognosis of hepatocellular carcinoma Asian[J]. Asian Pac J Cancer Prev, 2012, 13 (7) : 3247–52. DOI:10.7314/APJCP.2012.13.7.3247 |
| [12] | |
| [13] | Zhai CG, Ji XP, Wang HF, et al. Roles of selective inhibition of PI3K/Akt/mTOR signaling pathway on rabbit primary macrophage autophagy and possible pechnism[J]. Zhongguo Dong Mai Ying Hua Za Zhi, 2014, 22 (1) : 7–12. [ 翟纯刚, 季晓平, 王和峰, 等. 抑制PI3K/Akt/mTOR信号通路对兔原代巨噬细胞自体吞噬的影响及机制[J]. 中国动脉硬化杂志, 2014, 22 (1) : 7–12. ] |
| [14] | Li J, Huang S, Zhang J, et al. Mesenchymal stem cells ameliorate inflammatory cytokine-induced impairment of AT-II cells through a keratinocyte growth factor-dependent PI3K/Akt/mTOR signaling pathway[J]. Mol Med Rep, 2016, 13 (5) : 3755–62. |
 2016, Vol. 43
2016, Vol. 43
