文章信息
- 布洛芬通过PI3K/Akt/mTOR信号通路调控肝癌QGY-7703细胞迁移和侵袭的机制
- Mechanism of Ibuprofen Regulating Migration and Invasion of Liver Cancer QGY-7703 Cells Through PI3K/Akt/mTOR Signaling Pathway
- 肿瘤防治研究, 2016, 43(12): 1035-1038
- Cancer Research on Prevention and Treatment, 2016, 43(12): 1035-1038
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2016.12.005
- 收稿日期: 2016-02-26
- 修回日期: 2016-06-24
布洛芬是临床上最常用于癌痛镇痛的一种非选择性抑制COX的非甾体类抗炎药(non-steroids anti-inflammatory drugs, NSAIDs)。布洛芬在癌痛镇痛的应用过程中对癌细胞生物行为的影响,已成为近年来研究的热点,然而其对肝癌细胞迁移、侵袭能力的影响如何及其作用机制鲜有报道。因此,本课题旨在研究布洛芬对肝癌QGY-7703细胞生物行为的影响,并探讨布洛芬调控肝癌细胞生物行为的可能机制。
1 材料与方法 1.1 试剂和仪器GY-7703细胞由广西壮族自治区肿瘤防治研究所实验室提供;99%纯度的布洛芬购自大连美仑生物技术有限公司,实验中用DMSO溶解(DMSO终体积分数小于1‰),-20℃避光冷藏备用;RPMI 1640培养液、胎牛血清、胰蛋白酶、DMSO购自美国Gibco公司;Transwell细胞培养板购自美国康宁公司;TRIzol购自美国Invitrogen公司;PCR引物、反转录试剂盒和Real-time PCR试剂盒购自大连宝生物工程有限公司;Matrigel凝胶购自美国BD公司;鼠抗人PTEN单克隆抗体、鼠抗人Akt单克隆抗体、鼠抗人p-Akt单克隆抗体、鼠抗人mTOR单克隆抗体、鼠抗人p-mTOR单克隆抗体、鼠抗人MMP-9单克隆抗体、鼠抗人β-actin单克隆抗体和山羊抗鼠辣根过氧化物酶标记二抗购自美国Santa Cruz公司。CKX41型倒置显微镜、Western blot图像分析软件、Prism7300实时定量PCR和VICTOR3 酶标仪由广西医科大学肿瘤防治研究所实验室提供。PCR引物序列见表 1。
人肝癌细胞株QGY-7703培养于10%胎牛血清、100 u/ml青霉素及100 μg/ml链霉素的RPMI 1640培养液中,置37℃、5%CO2、95%湿度细胞培养箱,细胞贴壁80%时以0.25%胰酶消化传代,2~3天传一代。取对数生长期的细胞,采用随机数字表法,将QGY-7703细胞分为对照组C组和实验组B组,药代动力学研究显示人口服布洛芬达最大推荐量时,血浆药物浓度峰值可达到1 000 μmol/L[1],据此选择不同的临床相关浓度,将实验组又随机分为三个亚组:B1组(布洛芬浓度为250 μmol/L),B2组(布洛芬浓度为500 μmol/L)、B3组(布洛芬浓度为1 000 μmol/L);对照组(C组)加入等容量的RPMI 1640培养液。
1.3 Transwell实验检测细胞迁移能力取对数生长期的QGY-7703细胞按照1×106个接种于25 cm2培养瓶,贴壁后在相应组加入不同浓度布洛芬或培养液。分别培养至24、48、72 h后,以0.25%的胰酶消化细胞,用无血清RPMI 1640培养液重悬细胞,分别将各组细胞悬液的密度调整至5×105个每毫升。在下室加10%胎牛血清的RPMI 1640培养液600 μl,上室加入100 μl细胞悬液。在细胞培养箱孵育24 h后,棉签擦去上室上面的细胞,迁移至滤膜下表面的细胞用结晶紫染色后,随机选择5个高倍(×200)显微视野并统计滤膜下表面的细胞数目,以平均数来表示各组QGY-7703细胞的迁移能力,每组实验重复6次。
1.4 Transwell实验检测细胞侵袭能力实验步骤大体同细胞迁移实验,差异在于聚碳酸多孔滤膜表面铺上Matrigel,其余步骤和方法相同,随机选择5个高倍(×200)显微视野并统计滤膜下表面的细胞数目,以平均数来表示各组QGY-7703细胞的侵袭能力。
1.5 Real-time PCR检测细胞PI3K、PTEN和MMP-9基因的表达收集经不同浓度布洛芬处理48 h后的各组QGY-7703细胞,TRIzol法提取RNA,按照反转录试剂盒说明反转录为cDNA。4倍浓度梯度稀释模板cDNA并制作标准曲线,确定基因的扩增效率,确定cDNA上样浓度,反转录产物作为下一步PCR模版。PCR引物序列,见表 1。PCR反应条件:预变性95℃ 30 s,变性95℃ 5 s,60℃ 30 s 退火及延伸,循环40次。按照Real-time PCR试剂盒说明书进行操作。每组做6个复孔,每次实验重复6次,采用2-ΛΛCT法计算相对表达量。
1.6 Western blot法检测细胞PTEN、Akt、p-Akt、mTOR、p-mTOR和MMP-9蛋白的表达收集经不同浓度布洛芬处理48 h后的各组QGY-7703细胞,提取蛋白,用BCA蛋白质检测试剂盒测定并调节蛋白浓度,-70℃冰箱保存备用。各组取相应蛋白经SDS-PAGE分离后转到PVDF膜上。PVDF膜放入封闭缓冲液(含5%脱脂奶粉TBS),室温封闭1 h,分别加入PTEN、Akt、mTOR、p-Akt、p-mTOR和MMP-9一抗,4℃过夜,用辣根过氧化酶标记的二抗室温孵育2 h。化学发光法显色,凝胶成像分析仪进行图像分析,以β-actin作为内参照,用目的蛋白吸光度值/内参照吸光度值的比值进行统计比较,每组实验重复6次。
1.7 统计学方法采用SPSS13.0统计学软件进行分析,实验数据以均数±标准差(x±s)表示,组间比较采用单因素方差分析,两两比较采用SNK-q检验,P<0.05为差异有统计学意义。
2 结果 2.1 布洛芬对QGY-7703细胞迁移能力的影响与C组比较,B1、B2、B3三组细胞迁移至膜下的细胞数明显减少,差异有统计学意义(P<0.01),迁移至膜下的细胞数依照布洛芬作用浓度增加和时间的延长而依次下降,具有浓度和时间的依赖性,差异有统计学意义(P<0.01),见表 2。
 |
与C组比较,B1、B2、B3三组细胞侵袭至膜下的细胞数显著减少,差异有统计学意义(P<0.01);随着布洛芬作用时间的延长、浓度的增加侵袭至膜下细胞数依次降低,呈浓度和时间依赖性,差异有统计学意义(P<0.01),见表 2。
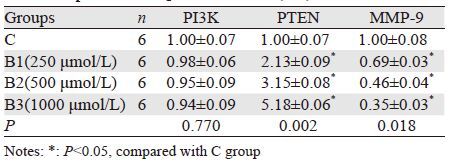
2.3 布洛芬对QGY-7703细胞PI3K、PTEN和MMP-9基因表达的影响与C组比较,B1、B2、B3组PI3K mRNA表达无明显变化,差异无统计学意义(P>0.05);PTEN mRNA表达明显升高,且随着布洛芬作用浓度的增加,PTEN mRNA表达依次升高,差异有统计学意义(P<0.05);MMP-9 mRNA表达显著下调,差异有统计学意义(P<0.05);随着布洛芬作用浓度的增加,B1、B2、B3组MMP-9 mRNA表达依次降低,具有浓度依赖性,差异有统计学意义(P<0.05),见表 3。
 |
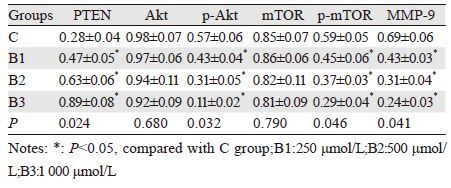
与C组比较,B1、B2、B3组Akt和mTOR的蛋白表达量无明显的变化,差异无统计学意义(P>0.05);PTEN蛋白表达显著升高而p-Akt、p-mTOR和MMP-9的蛋白表达明显下降,差异有统计学意义(P<0.05);随布洛芬作用浓度的增加,B1、B2、B3组PTEN蛋白表达依次升高,而p-Akt、p-mTOR和MMP-9的蛋白表达依此下降,具有浓度依赖性,差异有统计学意义(P<0.05),见表 4、图 1。
 |
|
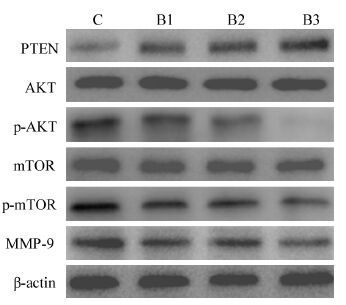
| 图 1 布洛芬对QGY-7703细胞PTEN、Akt、p-Akt、mTOR、p-mTOR和MMP-9蛋白表达的影响 Figure 1 Effects of ibprofen on PTEN, Akt, p-Akt, mTOR, p-mTOR and MMP-9 protein expression in QGY-7703 cells |
本研究结果发现,实验组细胞迁移和侵袭能力均明显降低,且依照布洛芬作用的浓度越大及作用时间越长,QGY-7703细胞的迁移和侵袭能力越降低。说明,布洛芬能够抑制肝癌QGY-7703细胞的迁移和侵袭能力,具有浓度及时间的依赖性。近年来国内外研究表明,布芬能抑制多种肿瘤细胞的侵袭和转移,其中包括卵巢癌、胶质瘤、肺癌和乳腺癌等[2-3],这与本研究的结果一致。
本研究检测PI3K/Akt/mTOR通路相关因子的表达,发现布洛芬能够上调肝癌QGY-7703细胞PTEN基因和蛋白表达,并下调MMP-9基因和蛋白的表达,且p-Akt和p-mTOR的蛋白表达也明显下调,且具有浓度依赖性。而PI3K的基因表达量以及总Akt和总mTOR的蛋白表达量均无明显的变化。说明PI3K/Akt/mTOR信号通路参与了布洛芬对肝癌QGY-7703细胞的抑制作用的调控。
PI3K/Akt/mTOR是蛋白质合成的主要信号调节途径,参与多种细胞增殖、迁移和侵袭等能力的调节[4-6],因此其在肿瘤的发生和发展中扮演着重要的角色。Menon等研究发现临床肝癌组织中,mTOR在核酸和蛋白质水平均异常高表达,而mTOR在中分化和低分化肝癌组织中尤其明显,进一步表明PI3K/Akt/mTOR信号通路异常激活可能是肝癌发生的重要机制[7]。布洛芬作用于肝癌QGY-7703细胞后,PI3K/Akt/mTOR信号通路中Akt的激活受到了抑制,进而通过TSC1/2复合物抑制下游因子mTOR的激活。另外,PTEN基因是一种肿瘤抑制基因,位于人类第10号染色体上,对PI3K/Akt/mTOR信号通路有负性调节作用。当PTEN基因发生突变或缺失时可激活PI3K/Akt/mTOR信号途径,利于肿瘤的发生和发展,这在前列腺癌、胶质瘤、子宫内膜癌和黑色素瘤中都具有较高的发生率[8-9]。有研究表明,肝细胞癌(HCC)中存在PTEN基因的缺失或失活,而且PTEN的异常表达可能在HCC的发生、进展和肝内转移等生物学行为中发挥作用[10-11]。另外,基质金属蛋白酶(如MMP-9)能降解细胞外基质中的多种蛋白成分,在肿瘤细胞侵袭和转移中起关键性作用,MMP-9也是PI3K/Akt/mTOR信号通路重要的下游靶点之一,该通路的活化可以诱导MMP-9的表达促进肿瘤细胞的迁移和侵袭[12-13]。
因此,本研究表明了布洛芬具有抑制肝癌细胞迁移和侵袭的能力,其机制可能是通过上调PTEN的表达、抑制PI3K/Akt/mTOR通路活性,进而抑制MMP-9的活性和表达。
| [1] | Lockwood GF, Albert KS, Gillespie WR, et al. Pharmacokinetics of ibuprofen in man. I. Free and total area/dose relationships[J].Clin Parmacol Ther, 1983, 34(1): 97-103. |
| [2] | Gunjal PM, Schneider G, Ismail AA, et al. Evidence for induction of a tumor metastasis-receptive microenvironment for ovarian cancer cells in bone marrow and other organs as an unwanted and underestimated side effect of chemotherapy/radiotherapy[J]. J Ovarian Res, 2015, 8 : 20. DOI:10.1186/s13048-015-0141-7 |
| [3] | Zhu LS, Wang H, Chen J, et al. Ibuprofen suppresses proliferation and metastasis of human non-small cell lung cancer cell line NCI-H460 and breast cancer cell line SKBR3[J]. Di Er Jun Yi Da Xue Xue Bao, 2014, 35 (12) : 1327–32. [ 祝丽双, 王浩, 陈佳, 等. 布洛芬抑制人NSCLC细胞株NCI-H460 和乳腺癌细胞株SKBR3增殖和转移的机制探讨[J]. 第二军医大学学报, 2014, 35 (12) : 1327–32. ] |
| [4] | Dobbin ZC, Landen CN. The importance of the PI3K/AKT/MTOR pathway in the progression of ovarian cancer[J]. Int J Mol Sci, 2013, 14 (4) : 8213–27. DOI:10.3390/ijms14048213 |
| [5] | Bai H, Li H, Li W, et al. The PI3K/AKT/mTOR pathway is a potential predictor of distinct invasive and migratory capacities in human ovarian cancer cell lines[J]. Oncotarget, 2015, 6 (28) : 25520–32. DOI:10.18632/oncotarget |
| [6] | Matsuoka T, Yashiro M. The Role of PI3K/Akt/mTOR Signaling in Gastric Carcinoma[J]. Cancers(Basel), 2014, 6 (3) : 1441–63. |
| [7] | Menon S, Yecies JL, Zhang HH, et al. Chronic activation of mTOR complex 1 is sufficient to cause hepatocellular carcinoma in mice[J]. Sci Signal, 2012, 5 (217) : ra24. |
| [8] | Milella M, Falcone I, Conciatori F, et al. PTEN: Multiple Functions in Human Malignant Tumors[J]. Front Oncol, 2015, 5 : 24. |
| [9] | Ocana A, Vera-Badillo F, Al-Mubarak M, et al. Activation of the PI3K/mTOR/AKT pathway and survival in solid tumors: systematic review and meta-analysis[J]. PLoS One, 2014, 9 (4) : e95219. DOI:10.1371/journal.pone.0095219 |
| [10] | Peyrou M, Bourgoin L, Foti M. PTEN in liver diseases and cancer[J]. World J Gastroenterol, 2010, 16 (37) : 4627–33. DOI:10.3748/wjg.v16.i37.4627 |
| [11] | Sendor AB, Hacker KE, Chen S, et al. Von Hippel-Lindau status influences phenotype of liver cancers arising from PTEN loss[J]. Gastrointest Cancer, 2015, 5 : 61–71. |
| [12] | Zhang FY, Hu Y, Que ZY, et al. Shikonin Inhibits the Migration and Invasion of Human Glioblastoma Cells by Targeting Phosphorylated beta-Catenin and Phosphorylated PI3K/Akt: A Potential Mechanism for the Anti-Glioma Efficacy of a Traditional Chinese Herbal Medicine[J]. Int J Mol Sci, 2015, 16 (10) : 23823–48. DOI:10.3390/ijms161023823 |
| [13] | Chang L, Zhao D, Liu HB, et al. Activation of sonic hedgehog signaling enhances cell migration and invasion by induction of matrix metalloproteinase-2 and -9 via the phosphoinositide-3 kinase/AKT signaling pathway in glioblastoma[J]. Mol Med Rep, 2015, 12 (5) : 6702–10. |
 2016, Vol. 43
2016, Vol. 43



