文章信息
- 靶向沉默RNF2基因对食管癌细胞放射敏感度的影响
- Effect of Gene Silencing of RNF2 on Radiosensitivity of Esophageal Carcinoma Cells
- 肿瘤防治研究, 2016, 43(10): 829-834
- Cancer Research on Prevention and Treatment, 2016, 43(10): 829-834
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2016.10.002
- 收稿日期: 2015-09-18
- 修回日期: 2016-03-10
2. 050011 石家庄,河北医科大学第四医院放 疗科;
3. 050011 石家庄,河北医科大学第四医院检验科
2. Department of Radiation Oncology, The Fourth Affiliated Hospital of Hebei Medical University, Shijiazhuang 050011, China;
3. Department of Laboratory, The Fourth Affiliated Hospital of Hebei Medical University, Shijiazhuang 050011, China
食管癌是一种常见的具有高发病率和死亡率的恶性肿瘤。据2014年世界癌症报告统计,食管癌发病率居恶性肿瘤第8位,死亡率居世界癌症的第6位[1]。放疗是治疗食管癌的重要方法之一,然而,放射线照射后引起的细胞损伤会产生细胞周期阻滞,为受损细胞的修复创造了条件,降低了放射线对肿瘤细胞的杀伤作用,是肿瘤细胞产生放射抵抗的重要原因[2]。RNF2基因作为多梳基因家族成员之一,在多种恶性肿瘤中高表达,如垂体腺瘤、胚胎性癌、胃癌、淋巴瘤、胰腺癌等[3-4],并发现其在DNA损伤修复、细胞周期调控、细胞凋亡等方面起着重要作用[5]。为了鉴定RNF2在调控放射损伤修复中的重要作用,本研究通过siRNA抑制RNF2的表达以观察其对食管癌ECA109细胞增殖和周期的影响,并检测了其对食管癌的放射增敏作用,为食管癌的临床治疗提供新的依据。
1 材料与方法 1.1 细胞系及主要试剂食管癌ECA109细胞为河北医科大学第四医院科研中心提供。小片段siRNA、脂质体转染试剂Lipofectamine RNAiMAX均为美国Invitrogen公司生产。兔抗人BMI-1单克隆抗体、单克隆抗体β-actin购自美国Abcam公司;碱性磷酸酶标记的IgG羊抗兔二抗为北京博奥森生物公司生产;BCIP/NBT底物显色试剂盒为美国Ameresco公司生产;TRIzol试剂购自美国Solarbio公司,氯仿、异丙醇、乙醇均购自北京化学试剂厂;反转录试剂盒购自美国Thermo公司。
1.2 细胞培养和照射细胞贴壁生长在玻璃培养瓶,加入含100 u/ml青霉素和100 μg/ml链霉素以及10%胎牛血清(FBS)的RPMI 1640培养液,置5%CO2饱和湿度的培养箱中培养,每2~3天传代一次。应用6-MVX线直线加速器照射ECA109食管癌细胞株,取机架角180°,源皮距100 cm,照射面积20 cm×20 cm,培养瓶下置0.5 cm组织补偿膜,室温下照射,照射剂量为6 Gy。
1.3 细胞转染当食管癌ECA109细胞贴壁生长达到80%~90%融合时,脂质体Lipofectamine RNAiMAX包裹小片段siRNA,转染ECA109细胞。细胞分为5组:control组、NC组、RNF2 siRNA1实验组、RNF2 siRNA2实验组、RNF2 siRNA3实验组。siRNA序列如下(只列出正义链):RNF2 siRNA1:5'-GGUAACGCCACUGUUGAUCACUUAU-3';RNF2 siRNA2:5'-CAGUGAGAAGCAGUAUACCAUUUAU-3';RNF2 siRNA3:5'-CACAGUGAAUUAAUGUGCCCAAUUU-3';NC组:5'-UUCUCCGAACGUGUCACGUTT-3'。转染24 h后收集细胞提取总RNA和蛋白,RT-PCR和Western blot法分别检测基因和蛋白表达,取干扰效果最佳序列的小片段siRNA进行后续实验。
1.4 RT-PCR检测由上海生工生物技术服务有限公司负责设计、合成引物,RNF2引物序列正义链为:5'-AGCACAATAATCAGCAAGCACTC-3',反义链为:5'-GCTCCACTACCATTTTCAATCTG-3',扩增大小112 bp。GAPDH基因引物序列:上游引物:5'-CGCTGAGTACGTCGT GGAGTC-3’,下游引物:5'-GCTGATGATCTTGAGGCTGTTGTC-3’,拟扩增的片段长度为172 bp。PCR反应条件为:94℃ 5 min;然后94℃ 30s,56℃ 30s,72℃ 45s进行30个循环;72℃ 5 min;2%琼脂糖凝胶电泳,采用Genesys软件观察、拍照。
1.5 Western blot检测相关蛋白表达根据蛋白提取试剂盒说明提取细胞总蛋白,用BCA法测定蛋白浓度,10%的SDS-PAGE分离,转膜、封闭,加入一抗RNF2(1:5 000稀释),4℃温度过夜,碱性磷酸酶标记IgG二抗(1:10 000)于37℃摇床温育1 h,TBST洗三次,每次5 min,然后Odyssey红外成象系统软件拍照,β-actin为内参。
1.6 MTT法检测转染对细胞增殖能力的影响取对数生长期的ECA109细胞,调整细胞浓度为5×104个每毫升。接种96孔培养板,100 μl每孔,37℃、5%CO2饱和湿度条件下过夜,次日转染沉默BMI-1的最佳干扰小片段RNA,并将转染空载体及未转染的ECA109作为阴性对照组(NC组)和空白对照组(control组),分别在照射后24、48和72 h收集细胞,MTT法检测各组细胞的增殖活性,每组设3个复孔。
1.7 细胞克隆形成实验检测细胞放射敏感度取对数生长期的各组细胞,消化后计数,稀释后得到不同浓度的细胞。根据不同细胞数目给予不同的照射剂量。细胞个数分别为200、400、600、1 000、5 000个,相应照射剂量分别为0、2、4、6、8 Gy,每组照射剂量设3个平行孔。照射后培养14天,甲醛固定,结晶紫染色,显微镜下计数≥50个细胞数的克隆数,计算克隆形成率。计算公式:接种效率(plating efficiency, PE)=对照组克隆数/细胞接种数×100%,存活分数(surviving fraction, SF)=实验组克隆数/(细胞接种数×PE)。实验重复3次。在Graph Pad Prism 5.0软件中,使用单击多靶模型计算放射生物学参数并拟合剂量存活曲线。
1.8 流式细胞术分析各组照射前、后食管癌细胞周期和凋亡的变化取上述各组细胞在照射后24 h收集,用PBS洗涤3遍,并重新悬浮于预冷的70%乙醇中,4℃固定2 h;离心弃固定液,用PBS悬浮细胞5 min后于300目筛网过滤;加入PI(propidium iodide)染液,室温反应10 min,4℃避光染色30 min,用流式细胞仪(Beckman)应用Single histogram statistic分析软件测定各实验组食管癌细胞周期的变化。
收集照射后24 h的ECA109食管癌细胞,用PBS洗涤3遍,弃上清液,加100 μl 1×缓冲液,再加入Annexin V 2.5 μl,4℃静置5 min;加入PI 10 μl,4℃静置5 min,然后加入1×缓冲液400 μl,轻晃混匀,上机检测各实验组食管癌细胞的凋亡分布。
1.9 统计学方法所有数据采用SPSS13.0统计学软件进行统计分析,实验结果以(x±s)表示,组间比较用重复测量设计资料方差分析,P < 0.05判定为差异有统计学意义。
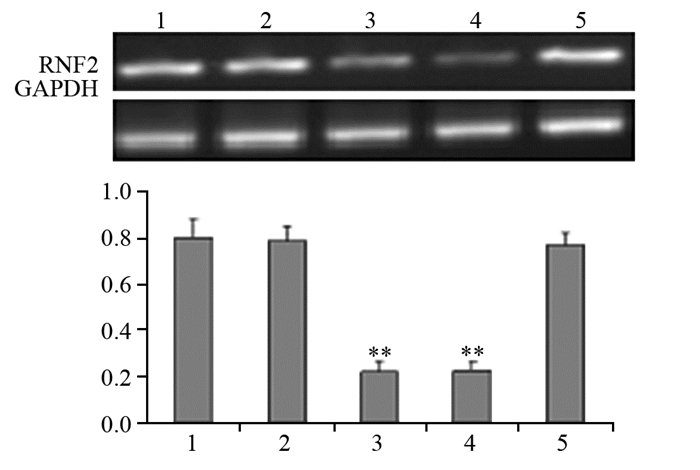
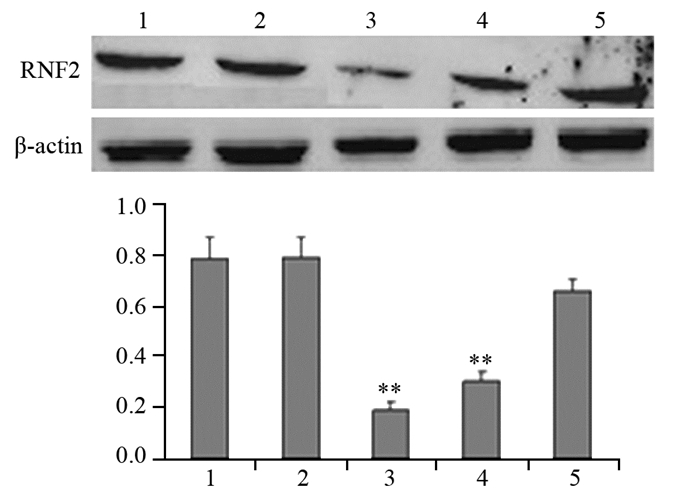
2 结果 2.1 食管癌细胞株ECA109转染前、后RNF2 mRNA和蛋白的表达分别提取瞬时转染的siRNA组(RNF2 siRNA1、RNF2 siRNA2、RNF2 siRNA3)和NC组、control组细胞总RNA和蛋白,对各组RNF2基因和蛋白进行检测。RT-PCR结果发现,3对靶向siRNA序列组的RNF2 mRNA相对表达量较control组均有不同程度的下降,尤以RNF2 siRNA1和siRNA2组下降最为明显(均P=0.000),NC组和control组之间RNF2 mRNA的相对表达量的差异无统计学意义(P=0.759),见图 1。同时,Western blot检测结果显示,与control组相比,siRNA1~3组的RNF2蛋白表达的干扰效率分别为75.48%(0.193±0.029 vs. 0.787±0.084)、61.37%(0.304±0.037 vs. 0.787±0.084)、16.26%(0.659±0.047 vs. 0.787±0.084),RNF2 siRNA1、siRNA2与control组、NC组相比,差异有统计学意义,且RNF2 siRNA1下降的更明显(均P=0.000);NC组与control组相比(0.792±0.075 vs. 0.787±0.084),差异未见统计学意义(P=0.790),见图 2。
|
| 1: control group; 2: NC group; 3: siRNA1 group; 4: siRNA2 group; 5: siRNA3 group; **: P < 0.01, compared with control group or NC group 图 1 RT-PCR检测转染后各组细胞中RNF2 mRNA的表达 Figure 1 mRNA expression of RNF2 after transient transfection detected by RT-PCR |
|
| 1: control group; 2: NC group; 3: siRNA1 group; 4: siRNA2 group; 5: siRNA3 group; **: P < 0.01, compared with control group or NC group 图 2 Western blot检测转染后各组细胞中RNF2蛋白的表达 Figure 2 Protein expression of RNF2 after transient transfection detected by Western blot |
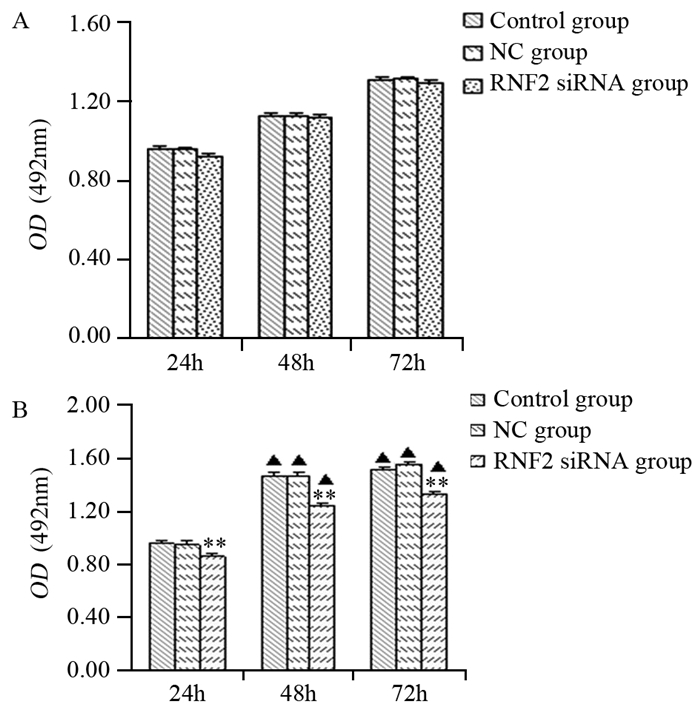
与NC组相比,RNF2 siRNA组中细胞的增殖水平在照射后24、48、72 h明显降低(均P=0.000),而control组与NC组细胞比较,差异无统计学意义(P=0.339, P=0.961, P=0.214),见图 3。此外,未照射时,NC组与RNF2 siRNA组相应的24、48、72 h比较,差异未见统计学意义(P=0.539, P=0.345, P=0.937),提示基因RNF2转染对食管癌细胞的增殖未见明显影响。并且control组、NC组、RNF2 siRNA组分别在照射后48 h(P=0.000, P=0.000, P=0.015)和72 h(P=0.000, P=0.000, P=0.018)增殖水平明显高于其相应照射前水平,而三组分别在照射后24 h增殖水平与照射前没有明显差异(P=0.925, P=0.695, P=0.124)。
|
| A: the proliferation activity of cells before irradiation; B: the proliferation activity of cells after irradiation; **: P < 0.01, compared with control group or NC group; ▲: P < 0.05, compared with the proliferation activity of cells before irradiation 图 3 照射前后食管癌细胞株ECA109在不同时间的增殖水平 Figure 3 Proliferation activity of ECA109 cells in different groups before and after irradiation detected by MTT assay |
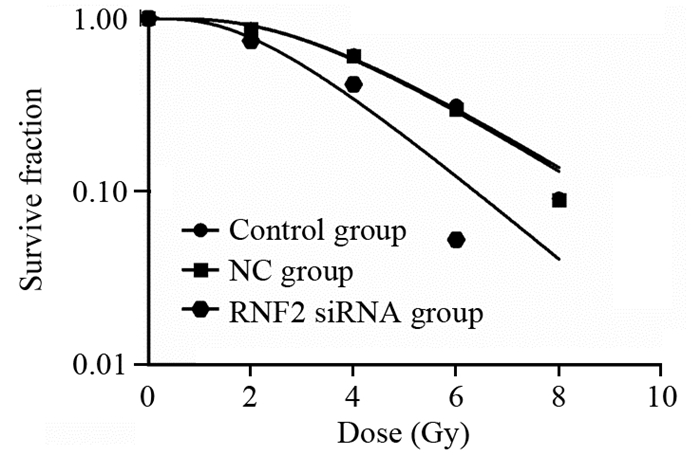
克隆形成实验结果显示control组、NC组、RNF2 siRNA组的D0值分别为2.45、2.43、1.70 Gy;Dq值分别为3.03、2.93、2.43 Gy;外推数N值分别为3.444、3.300、4.174;SF2值分别为0.8662、0.8512、0.7654。由此得出,control组和NC组放射敏感度未见明显差异,而RNF2 siRNA组的放射敏感度显著高于control组和NC组,见图 4。
|
| 图 4 克隆形成实验检测BMI-1对细胞增殖的影响 Figure 4 Effect of BMI-1 on cells proliferation measured by clone conformal assay after irradiation |
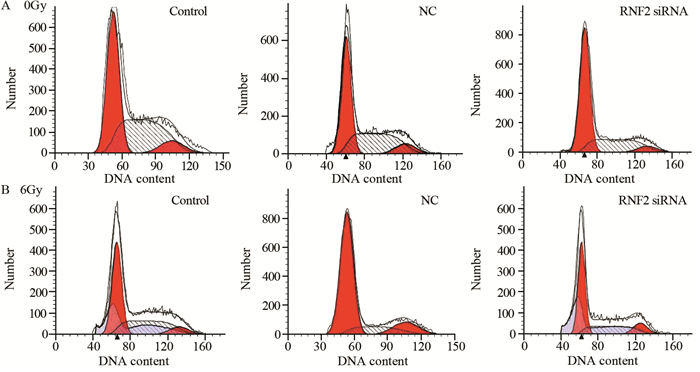
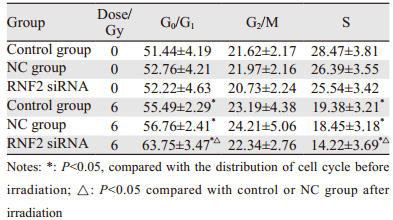
照射后24 h,control组、NC组、RNF2 siRNA组细胞中G0/G1期的比例均较未照射组升高,差异具有统计学意义(P=0.005, P=0.002, P=0.000),且RNF2 siRNA组比control组和NC组G0/G1期比例升高的更明显,差异有统计学意义(均P=0.000);而照射后RNF2 siRNA组S期比例明显低于control组和NC组(均P=0.000),且control组、NC组和RNF2 siRNA组S期比例均分别低于相应未照射组(均P=0.000);照射前后各组处于G2/M期的细胞比例未见显著性差异(P=0.309, P=0.845, P=0.945),见图 5、表 1。
|
| 图 5 流式细胞术检测照射前(A)、后(B) BMI-1对细胞周期的影响 Figure 5 Effect of BMI-1 on cell cycle detected by flow cytometry before (A) and after (B) irradiation |
|
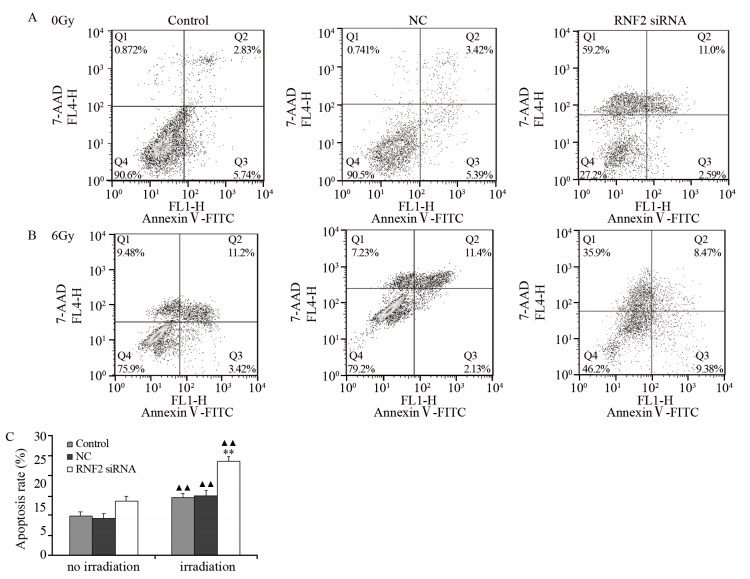
流式细胞术检测结果显示,6 Gy放射线照射后control组、NC组、RNF2 siRNA组ECA109细胞凋亡率均分别高于相应未照射组(P=0.001, P=0.001, P=0.000),而照射前,RNF2 siRNA组细胞凋亡率较control组和NC组高,但差异未见统计学意义(P=0.198, P=0.104);照射后,RNF2 siRNA组细胞凋亡率明显高于control组、NC组,且差异具有统计学意义(均P=0.000),见图 6。
|
| A: the distribution of cells apoptosis before irradiation; B: the distribution of cells apoptosis after irradiation; C: corresponding histogram of apoptosis rate; **: P < 0.01 compared with control or NC group; ▲▲: P < 0.01, compared with no irradiation 图 6 照射前、后食管癌ECA109细胞株凋亡分布 Figure 6 Distribution of cells apoptosis in ECA109 cells before and after irradiation |
RNF2蛋白是一个带有指环结构的泛素连接酶(E3),是一种转录抑制蛋白,属于多梳基因家族(polycomb group, PcG)成员,由336个氨基酸组成,在多种肿瘤中高表达,与基因转录、肿瘤生长、侵袭、迁移等方面关系密切[4, 6]。RNF2基因的突变和失活致使细胞基因不稳定、DNA双链断裂修复受损,出现对放射线的高度敏感,因此抑制肿瘤细胞内RNF2蛋白的表达可显著增加肿瘤细胞对放射治疗的敏感度,增加放射治疗的疗效[7]。此外,DNA损伤后,RNF2可被招募到损伤部位,从而为损伤修复创造条件[8-9]。本实验通过利用RNA干扰技术降低人食管癌细胞中RNF2的表达,联合X线照射,进一步研究RNF2基因与食管癌细胞放射敏感度的关系。
本研究针对RNF2基因的不同位点设计合成了3对siRNA序列,通过RT-PCR和Western blot检测食管癌细胞中RNF2在mRNA和蛋白水平的表达,结果发现3对干扰序列对RNF2的表达均有不同程度的抑制作用,尤其是siRNA1抑制作用更加明显,此外本研究中MTT结果显示照射前control组、NC组和干扰组细胞的增殖能力无明显差异,说明采用的转染方法安全可靠。然而,照射后干扰组细胞的增殖水平显著低于control组和NC组,表明RNF2基因干扰联合X线照射可有效抑制细胞的生长。本实验结果与Chen等[10]在胰腺癌中的研究相似,抑制基因RNF2的表达可显著降低胰腺癌细胞增殖和肿瘤体积的增长。
为了检测转染后对肿瘤细胞放射敏感度的影响,本研究采用了克隆形成实验来验证食管癌细胞的存活能力,结果发现干扰组细胞的Dq值明显小于control组和NC组的Dq值,Dq值表示细胞对亚致死损伤修复能力大小,Dq值越小,表明细胞的亚致死损伤修复能力越弱,放射线对细胞的杀伤力越大;SF2指肿瘤细胞经2 Gy照射后的细胞存活分数,是评价肿瘤细胞内在放射敏感度的重要指标,本研究中干扰组细胞的SF2明显低于control组和NC组,表明干扰RNF2的表达后显著增加了肿瘤细胞的放射敏感度。本实验结果与国外学者Zhou等[7]在神经胶质瘤中的研究一致,敲低RNF2基因的表达可明显提高神经胶质瘤细胞U87对X射线的放射敏感度。
细胞的放射敏感度与细胞周期和凋亡的关系密切,细胞周期阻滞在照射后DNA损伤修复中起重要作用,为照射后DNA损伤修复创造条件,有效地抑制了放射线对细胞的杀伤作用,从而为降低放射敏感度提供了可能[11-12]。有研究发现RNF2的高表达会引起S期增加,而敲低RNF2表达会诱导肺癌细胞G1期比例增加,S期降低[5],在脑胶质瘤细胞中也有类似报道[7]。本研究中结果与上述报道相似,X线照射后干扰组细胞G0/G1期比例显著高于control组和NC组,S期比例明显降低,提示干扰RNF2的表达在一定程度上诱导了周期阻滞在G0/G1期,抑制了细胞周期向S期过渡,阻止了细胞生长,促进了放射线对细胞的杀伤力,增加了细胞凋亡,从而提高了食管癌细胞的放射敏感度。有研究表明,X射线照射后,DNA双链发生断裂,泛素化连接酶RNF2首先诱导组蛋白H2AX发生泛素化,泛素化的H2AX易被活化的ATM激酶磷酸化形成γ-H2AX,从而促使下游基因MDC1和53BP1聚集到DNA双链断裂处,感应和放大损伤信号,进而影响细胞增殖水平和周期分布;下调RNF2基因表达后,H2AX磷酸化水平明显受抑,其接受损伤信号的能力下降,不能及时向下游传递损伤信号,细胞生长缓慢、周期阻滞功能受损,下游基因损伤修复能力下降,进而诱导细胞凋亡的发生,从而增强了放射敏感度[13-14]。并且本研究中抑制RNF2基因的表达后,细胞的凋亡显著增加,与Wen等[15]在结肠癌中的报道一致。此外,为进一步探讨RNF2基因对食管癌放射增敏的作用机制,我们在前期研究中发现,RNF2蛋白与γ-H2AX蛋白之间存在时间和剂量依赖性,且敲低RNF2基因后,γ-H2AX蛋白的表达显著降低,这表明RNF2基因可能通过调控γ-H2AX蛋白的表达,从而在食管癌放射损伤修复中发挥作用[16]。
综上所述,本研究结果证实,RNA干扰技术抑制RNF2基因表达后,联合X线照射可有效地抑制细胞增殖水平,且通过诱导G0/G1期阻滞增强了食管癌细胞对电离辐射的放射敏感度,为食管癌的放射治疗和基因治疗提供理论研究。RNF2基因沉默和放疗的联合应用将有助于改善食管癌患者的长期生存,对食管癌的临床应用具有重大意义。
| [1] | Montgomery EA. Oesophageal cancer//Stewart BW, Wild CP.World Cancer Report 2014[M]. Lyon: International Agency for Research on Cancer, 2014: 374-82. |
| [2] | Liu ZK, Zhu SC, Su JW, et al. Short hairpin RNA-mediated MDC1 gene silencing enhances the radiosensitivity of esophageal squamous cell carcinoma cell line ECA109[J]. Nan Fang Yi Ke Da Xue Xue Bao, 2010, 30 (8) : 1830–4. [ 刘志坤, 祝淑钗, 苏景伟, 等. 靶向沉默人基因MDC1表达对食管细胞放射增敏作用的实验研究[J]. 南方医科大学学报, 2010, 30 (8) : 1830–4. ] |
| [3] | Sánchez-Beato M, Sánchez E, González-Carreró J, et al. Variability in the expression of polycomb proteins in different normal and tumoral tissues. A pilot study using tissue microarrays[J]. Mod Pathol, 2006, 19 (5) : 684–94. DOI:10.1038/modpathol.3800577 |
| [4] | Martínez-Romero C, Rooman I, Skoudy A, et al. The epigenetic regulators Bmi1 and Ring1B are differentially regulated in pancreatitis andpancreatic ductal adenocarcinoma[J]. J Pathol, 2009, 219 (2) : 205–13. DOI:10.1002/path.v219:2 |
| [5] | Su WJ, Fang JS, Cheng F, et al. RNF2/Ring1b negatively regulates p53 expression in selective cancer cell types to promote tumor development[J]. Proc Natl Acad Sci U S A, 2013, 110 (5) : 1720–5. DOI:10.1073/pnas.1211604110 |
| [6] | Bosch A, Panoutsopoulou K, Corominas JM, et al. The Polycomb group protein RING1B is overexpressed in ductal breast carcinoma and is required to sustain FAK steady state levels in breast cancer epithelial cells[J]. Oncotarget, 2014, 5 (8) : 2065–76. DOI:10.18632/oncotarget |
| [7] | Zhou C, Yang F, Xi W, et al. Effect of RNF2 knockdown on apoptosis and radiosensitivity in glioma U87 cells[J]. Xi Bao Yu Fen Zi Mian Yi Xue Za Zhi, 2014, 30 (5) : 471–5. [ 周春辉, 杨帆, 席文锦, 等. 下调环指蛋白2的表达促进U87脑胶质瘤细胞凋亡并增强其放射敏感性[J]. 细胞与分子免疫学杂志, 2014, 30 (5) : 471–5. ] |
| [8] | Jackson SP, Durocher D. Regulation of DNA damage responses by ubiquitin and SUMO[J]. Mol Cell, 2013, 49 (5) : 795–807. DOI:10.1016/j.molcel.2013.01.017 |
| [9] | Panier S, Durocher D. Push back to respond better: regulatory inhibition of the DNA double-strand break response[J]. Nat Rev Mol Cell Biol, 2013, 14 (10) : 661–72. DOI:10.1038/nrm3659 |
| [10] | Chen S, Chen J, Zhan Q, et al. H2AK119Ub1 and H3K27Me3 in molecular staging for survival prediction of patients with pancreatic ductal adenocarcinoma[J]. Oncotarget, 2014, 5 (21) : 10421–33. DOI:10.18632/oncotarget |
| [11] | Xu XH, Liu XY, Su J. ShRNA targeting Bmi-1 sensitizes CD44+ nasopharyngeal cancer stem-like cells to radiotherapy[J]. Oncol Rep, 2014, 32 (2) : 764–70. |
| [12] | Dong Q, Sharma S, Liu H, et al. HDAC inhibitors reverse acquired radio resistance of KYSE-150R esophageal carcinoma cells by modulating Bmi-1 expression[J]. Toxicol Lett, 2014, 224 (1) : 121–9. DOI:10.1016/j.toxlet.2013.10.014 |
| [13] | Liu ZK, Zhu SC, Yang J, et al. Effect of RNAi against 53BP1 gene on radiosensitivity of human esophageal carcinoma cells[J]. Zhongguo Ai Zheng Za Zhi, 2012, 22 (3) : 189–95. [ 刘志坤, 祝淑钗, 杨洁, 等. RNA干扰53BP1基因表达对食管癌放射敏感性的影响[J]. 中国癌症杂志, 2012, 22 (3) : 189–95. ] |
| [14] | Pan MR, Peng G, Hung WC, et al. Monoubiquitination of H2AX Protein Regulates DNA Damage Response Signaling[J]. J Biol Chem, 2011, 286 (32) : 28599–607. DOI:10.1074/jbc.M111.256297 |
| [15] | Wen W, Peng C, Kim MO, et al. Knockdown of RNF2 induces apoptosis by regulating MDM2 and p53 stability[J]. Oncogene, 2014, 33 (4) : 421–8. DOI:10.1038/onc.2012.605 |
| [16] | Yang X, Ma M, Sang M, et al. Radiosensitization of esophageal carcinoma cells by knockdown of RNF2 expression[J]. Int J Oncol, 2016, 48 : 1985–96. |
 2016, Vol. 43
2016, Vol. 43


