文章信息
- 度洛西汀对多西他赛化疗所致大鼠神经病理性疼痛的影响
- Effect of Duloxetine on Docetaxel-induced Neuropathic Pain in Rats
- 肿瘤防治研究, 2016, 43(9): 758-761
- Cancer Research on Prevention and Treatment, 2016, 43(9): 758-761
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2016.09.006
- 收稿日期: 2016-03-20
- 修回日期: 2016-05-17
神经病理性疼痛是一种非常严重的临床问题,它广泛发生在糖尿病、带状疱疹感染以及肿瘤等众多患者身上[1]。其中,化疗药物产生的神经病理性疼痛,常常导致患者出现焦虑、抑郁、虚弱、睡眠障碍等情绪障碍[2];症状严重的病例,化疗所致神经毒性甚至导致化疗计划的推迟或终止而影响了患者的抗肿瘤治疗。度洛西汀是一种五羟色胺(5-hydroxytryptamine,5-HT)和去甲肾上腺素(norepinephrine,NE)再摄取抑制剂(serotonin noradrenalin reuptake inhibitor,SNRI),作为一种抗抑郁药物,被广泛用于多种慢性神经病理性疼痛(如糖尿病外周神经疼痛、纤维肌痛等)[3]。尽管度洛西汀对于慢性神经疼痛非常有效,但是其对化疗药物引起的神经病理性疼痛的研究还很有限。本研究主要探讨度洛西汀对化疗诱导的大鼠神经病理性疼痛的疗效,从而为找到治疗人类化疗诱导的神经病理性疼痛药物提供方向。
1 材料与方法 1.1 动物和分组实验采用成年雄性SD大鼠(体质量200 g左右,来源于华中科技大学同济医学院实验动物中心)。实验方案遵从美国国立卫生研究院关于实验动物的指南[4],经华中科技大学动物保护委员会批准。大鼠饲养温度为20℃~23℃,能自由地得到食物和水份,每天光照时间和黑暗时间均为12 h。24只大鼠被平均分配成4组(n=6)。Ⅰ组(正常对照组):正常的大鼠不给予任何药物;Ⅱ组(度洛西汀组):大鼠仅仅接受度洛西汀(10 mg/kg,口服),共8天,每天1次;Ⅲ组(多西他赛组):大鼠给予多西他赛(10 mg/kg)单药尾静脉注射;Ⅳ组(度洛西汀治疗组):给予多西他赛单药的大鼠随后每天给予度洛西汀(10 mg/kg,口服),共8天,每天1次。治疗前1天定义为D0。在第8天,所有的大鼠进行行为学检测后被处死,其中一部分进行L4~6脊髓背根神经节(dorsal root ganglia,DRG)P物质(substance P,SP)检测。
1.2 药物多西他赛(法国安万特制药公司)用0.9%氯化钠溶液进行稀释。对Ⅲ、Ⅳ组大鼠给予10 mg/kg的多西他赛,尾静脉注射。度洛西汀(美国礼来公司)用蒸馏水稀释给药量为10 mg/kg,给予Ⅱ组和Ⅳ组。
1.3 一般毒性每天监测给药后大鼠的一般情况,包括体质量、健康状态、活力,每两天给予1次记录。
1.4 痛域测定方法机械性痛阈测试:大鼠置入单独的铁丝笼中,给予10 min适应后,用4 g的von Frey丝对准大鼠后足的足底中心给予刺激,持续5 s。当大鼠的后足因为刺激而出现抬足反射时考虑为阳性,未出现抬足反射为阴性,阳性反应率记录为20次刺激中缩腿的百分比。4g von Frey丝主要用于测定机械性痛觉异常。
热痛阈测试:将大鼠放入单独的塑料笼中并给予30 min的适应时间后,一道光束由热辐射测痛仪(UgoBasile,意大利)射向大鼠的足底中心部位,大鼠因无法耐受热痛出现抬足动作,这时光束会自动切断并记录时间。光束的照射时间最长为20 s以防止皮肤损伤。左右足各5次,取平均值。
冷痛阈测试:将大鼠置入铁丝笼中适应30 min,用细注射器对准大鼠的足背中心给予1滴丙酮。对丙酮的阳性反应为大鼠在滴丙酮后出现迅速的抬足反射。其耐受时间记录为从大鼠抬足到大鼠再次放下后足休息。左右足各5次,取平均值。
1.5 RT-PCR法测定L4~6脊髓DRG的SP含量第8天,每组各取3只大鼠安乐死后进行检查。TRIzol? reagent(Invitrogen,美国)提取大鼠L4~6脊髓DRG总RNA,反转录为cDNA[5]。用ΔΔCT法来测定P物质mRNA含量。引物为:SP上游引物:5’-CAGAGGAAATCGGTGCCAAC-3’;下游引物:5’-CTGCTGAGGCTTGGGTCTTC-3’。β-actin上游引物:5'-CGTTGACATCCGTAAAGACCTC-3’;下游引物:5’-TAGGAGCCAGGGCAGTAATCT-3’ 。
1.6 统计学方法实验数据采用SPSS13.0统计软件处理,正态计量数据表达为均值±标准误(x±s)。各项指标的组间均值比较用单因素方差分析(one-way ANOVA)。P<0.05表示差异有统计学意义。
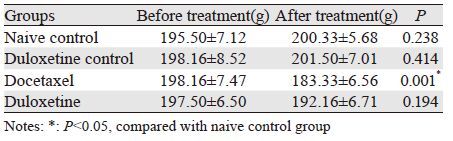
2 结果 2.1 一般毒性没有大鼠在实验中死亡。度洛西汀组和正常对照组的体质量没有差异,表明大鼠对度洛西汀具有较好的耐受。多西他赛组大鼠的活力和进食明显减少,体质量明显下降,见表 1。
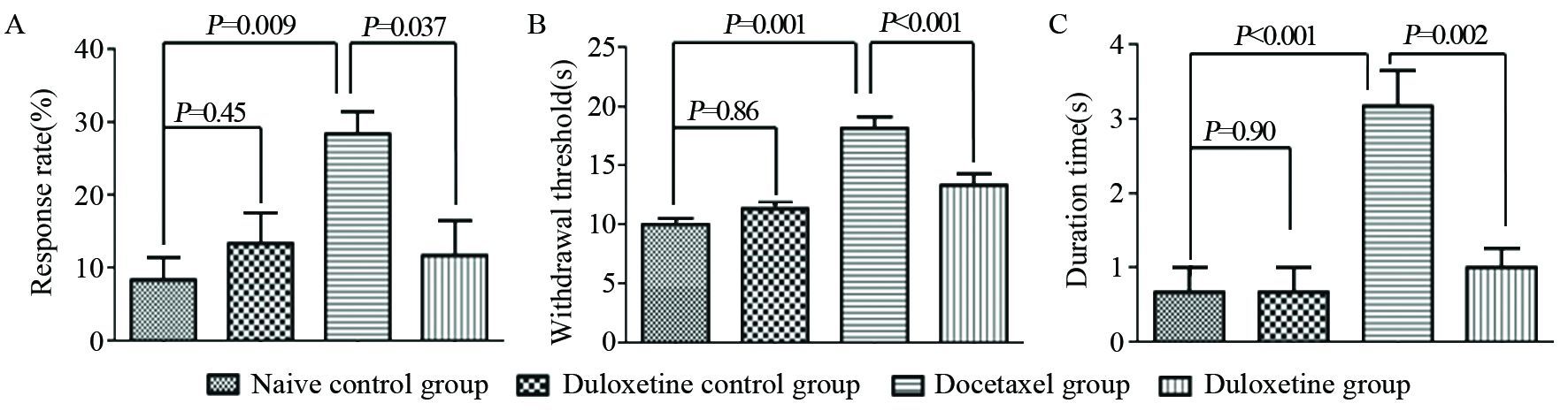
与正常对照组相比,多西他赛能显著降低正常对照组大鼠的机械痛阈[(28.33±3.07)% vs.(8.33±3.07)%,P=0.009],而度洛西汀[(13.33±4.21)% vs.(8.33±3.07)%,P=0.037]并不会引起机械性痛觉异常,然而度洛西汀治疗组能减轻多西他赛导致的机械性痛觉异常[(11.67±4.77)% vs.(28.33±3.07)%,P=0.037]。多西他赛能明显引起正常对照组大鼠的热痛觉过敏[(18.17±0.95) vs.(10.00±0.52),P<0.001]。给予度洛西汀能明显减轻多西他赛导致的热痛觉过敏[(13.33±0.95) vs.(18.17±0.95),P=0.001]。而在冷痛阈实验中,多西他赛能明显增加正常对照组大鼠丙酮实验的耐受时间[(3.17±0.48) vs.(0.67±0.33),P<0.001],给予度洛西汀能明显的减轻多西他赛所致的冷痛觉异常[(1.00±0.26) vs.(3.17±0.48),P=0.002],见图 1。多西他赛单药化疗能显著降低正常大鼠的机械痛阈,引起正常大鼠的热痛觉过敏,增加正常大鼠丙酮的耐受时间,是一个较好的多西他赛所致神经病理性疼痛动物模型。
|
| 中文注解 A: mechanical allodynia; B: heat hypoalgesia; C: cold allodynia 图 1 四组小鼠机械性痛觉、热痛觉、冷痛觉痛域测定结果 Figure 1 Mechanical allodynia,heat hypoalgesia and cold allodynia of four groups |
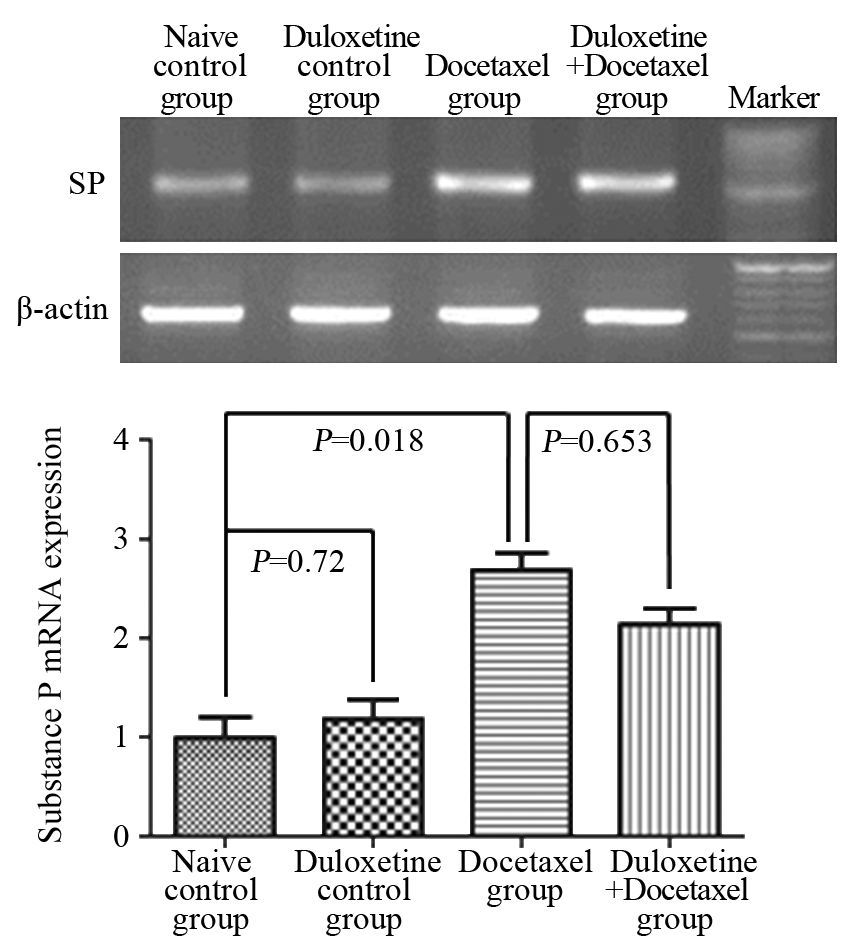
与正常对照组(1.00±0.30)相比,多西他赛(2.68±0.25)能明显增加L4-6脊髓DRG的SP释放(P=0.018)。而单独给予度洛西汀不能增加SP的释放,见图 2。与此同时,给予度洛西汀也不能减少多西他赛所致SP的释放(P=0.653)。
|
| 图 2 小鼠L4~6脊髓DRG的SP mRNA含量 Figure 2 mRNA expression of SP in L4~6 dorsal root gonglia (DRG) |
化疗药物导致的神经毒性是肿瘤治疗中的常见问题,可以发生在高达90%的化疗患者中。并且,随着肿瘤患者生存期的延长,神经毒性成为肿瘤医生面临的一个越来越棘手的问题。本研究建立了单次给予多西他赛的大鼠神经病理性模型,并且探讨了度洛西汀在多西他赛化疗模型中的作用。结果发现,单次给予大鼠多西他赛即可产生明显的神经病理性疼痛,表现为机械性痛觉异常,热痛觉过敏,冷痛觉异常,L4~6脊髓DRG的SP释放增加。这些特点和其他化疗药物导致的神经毒性相似,如泰素,奥沙利铂,长春新碱等[6]。同时,这些化疗药物神经毒性模型对冷热刺激的表现也和人类的化疗后神经症状相似,证实了该大鼠模型是一种有效研究化疗神经毒性的模型。
度洛西汀是一种常见的抗抑郁药物,已被美国FDA批准用于糖尿病周围神经病理性疼痛及慢性肌纤维疼痛。五羟色胺(5-HT)和去甲肾上腺素(NE)是两种重要的调节内源性疼痛的神经递质,抑制机制的失衡会导致中枢敏化,从而导致持续性疼痛。已有研究[7, 8]表明,度洛西汀主要通过非选择性抑制神经元对5-HT和NE的再摄取,从而提高中枢NE和5-HT的浓度,其抑制5-HT重吸收及NE重吸收的比例为9.4:1,这种非选择性吸收可能使其止痛效果好于文拉法辛(30:1)及米那普伦(1:1)。并且,5-HT和NE重吸收抑制剂可以增强抑制通路的功能,减少脊髓疼痛信号的上传,达到止痛的作用,其和多种神经递质受体以及离子通道关系不大[7, 8]。部分研究提示,在大鼠神经瘤的病理性疼痛模型中,度洛西汀能够明显减少大鼠机械性痛觉异常,与本研究结果类似[9]。而在化疗所致神经病理性疼痛方面,对度洛西汀的研究主要集中在临床应用上,早期的个例报道及小规模的开放性临床研究提示度洛西汀对化疗所致神经病理性疼痛可能有效[10, 11]。JAMA杂志上发布的一个大规模的Ⅲ期RCT研究则里程碑性地证实了度洛西汀在化疗所致神经病理性疼痛中的有效性,尤其是对奥沙利铂引起的神经毒性[12],其也成为美国临床肿瘤学会(ASCO)专家组唯一推荐用于治疗化疗所致神经毒性的药物[13]。对于度洛西汀的动物研究则相对较少,而我们的研究发现,度洛西汀能明显改善大鼠化疗所致神经病理性疼痛的行为学,如机械性疼痛、热痛觉和冷痛觉异常。
SP是一种含有10个氨基酸的神经肽类物质,广泛存在于中枢和外周神经系统,以脊髓含量最高,尤其是三叉神经节DRG等,在机体受到刺激时由感觉神经纤维释放,从而起着传导疼痛的作用,是小分子神经肽类物质的代表[14]。有研究发现,在炎性反应所致的神经病理性疼痛中,大鼠L4~6脊髓DRG中的SP明显增高。而镇痛药可以明显降低DRG内SP的含量,从而减轻疼痛[15]。基于上述发现,我们推测SP有可能参与了多西他赛化疗所致的神经病理性疼痛的痛觉传导过程,多西他赛能增加SP的释放。本实验结果表明,多西他赛的确增加了SP的释放,但是度洛西汀并没有通过调节SP来达到镇痛作用,其在化疗中的止痛作用可能为其他途径,需要我们做进一步的研究。
综上所述:在大鼠模型中,多西他赛能产生神经病理性疼痛,如机械性痛觉异常,热痛觉减退,冷痛觉异常,以及DRG中SP的释放。而度洛西汀能明显改善大鼠化疗所致神经病理性疼痛,可能是一种潜在有效的治疗多西他赛化疗诱导的神经病理性疼痛的药物,但具体机制仍需更深入的研究。
| [1] | Dworkin RH, O’Connor AB, Audette J, et al. Recommendations for the pharmacological management of neuropathic pain: an overview and literature update[J]. Mayo Clin Proc, 2010, 85 (Suppl3) : S3–14. |
| [2] | Anastassiou E, Iatrou CA, Vlaikidis N, et al. Impact of pregabalin treatment on pain, pain-related sleep interference and general well-being in patients with neuropathic pain: a non-interventional, multicentre, post-marketing study[J]. Clin Drug Investig, 2011, 31 (6) : 417–26. DOI:10.2165/11589370-000000000-00000 |
| [3] | Finnerup NB, Attal N, Haroutounian S, et al. Pharmacotherapy for neuropathic pain in adults: a systematic review and meta-analysis[J]. Lancet Neurol, 2015, 14 (2) : 162–73. DOI:10.1016/S1474-4422(14)70251-0 |
| [4] | Zimmermann M. Ethical guidelines for investigations of experimental pain in conscious animals[J]. Pain, 1983, 16 (2) : 109–10. DOI:10.1016/0304-3959(83)90201-4 |
| [5] | Zhang J, Chen L, Su T, et al. Electroacupuncture increases CB2 receptor expression on keratinocytes and infiltrating inflammatory cells in inflamed skin tissues of rats[J]. J Pain, 2010, 11 (12) : 1250–8. DOI:10.1016/j.jpain.2010.02.013 |
| [6] | Carlson K, Ocean AJ. Peripheral neuropathy with microtubule-targeting agents: occurrence and management approach[J]. Clin Breast Cancer, 2011, 11 (2) : 73–81. DOI:10.1016/j.clbc.2011.03.006 |
| [7] | Finnerup NB, Sindrup SH, Jensen TS. The evidence for pharmacological treatment of neuropathic pain[J]. Pain, 2010, 150 (3) : 573–81. DOI:10.1016/j.pain.2010.06.019 |
| [8] | Javed S, Petropoulos IN, Alam U, et al. Treatment of painful diabetic neuropathy[J]. TherAdv Chronic Dis, 2015, 6 (1) : 15–28. DOI:10.1177/2040622314552071 |
| [9] | Miyazaki R, Yamamoto T. The efficacy of morphine, pregabalin, gabapentin, and duloxetine on mechanical allodynia is different from that on neuroma pain in the rat neuropathic pain model[J]. Anesth Analg, 2012, 115 (1) : 182–8. DOI:10.1213/ANE.0b013e31824f94ca |
| [10] | Takenaka M, Lida H, Matsumoto S, et al. Successful treatment by adding duloxetine to pregabalin for peripheral neuropathy induced by paclitaxel[J]. Am J Hosp Palliat Care, 2013, 30 (7) : 734–6. DOI:10.1177/1049909112463416 |
| [11] | Yang YH, Lin JK, Chen WS, et al. Duloxetine improves oxaliplatin-induced neuropathy in patients with colorectal cancer: an open-label pilot study[J]. Support Care Cancer, 2012, 20 (7) : 1491–7. DOI:10.1007/s00520-011-1237-2 |
| [12] | Smith EM, Pang H, Cirrincione C, et al. Effect of duloxetine on pain, function, and quality of life among patients with chemotherapy-induced painful peripheral neuropathy: a randomized clinical trial[J]. JAMA, 2013, 309 (13) : 1359–67. DOI:10.1001/jama.2013.2813 |
| [13] | Hershman DL, Lacchetti C, Dworkin RH, et al. Prevention and anagement of chemotherapy-induced peripheral peuropathy in survivors of adult cancers: American Society of Clinical Oncology clinical practice guideline[J]. J Clin Oncol, 2014, 32 (18) : 1941–67. DOI:10.1200/JCO.2013.54.0914 |
| [14] | Kant V, Kumar D, Kumar D, et al. Topical application of substance P promotes wound healing in streptozotocin-induced diabetic rats[J]. Cytokine, 2015, 73 (1) : 144–55. DOI:10.1016/j.cyto.2014.12.015 |
| [15] | Ambalavanar R, Dessem D, Moutanni A, et al. Muscle inflammation induces a rapid increase in calcitonin gene-related peptide (CGRP) mRNA that temporally relates to CGRP immunoreactivity and nociceptive behavior[J]. Neuroscience, 2006, 143 (3) : 875–84. DOI:10.1016/j.neuroscience.2006.08.015 |
 2016, Vol. 43
2016, Vol. 43