文章信息
- CGB5对卵巢癌OVCAR-3细胞血管生成拟态形成的影响
- Effect of CGB5 on Human Epithelial Ovarian Cancer Cell Line OVCAR-3 in Vasculogenic Mimicry Formation
- 肿瘤防治研究, 2016, 43(9): 733-737
- Cancer Research on Prevention and Treatment, 2016, 43(9): 733-737
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2016.09.001
- 收稿日期: 2015-11-18
- 修回日期: 2016-04-16
2. 226001 南通,南通大学附属医院病理科;
3. 226001南通,南通大学医学院电镜室
2. Department of Pathology, Affiliated Hospital of Nantong University, Nantong 226001, China;
3. Department of Electron Microscopy, Medical College, Nantong University, Nantong 226001, China
肿瘤组织的生存、转移和复发[1]需要足够的血液供应,多年来以血管内皮细胞(endothelial cell,EC)为靶点的肿瘤抗血管治疗被认为是重要甚至是唯一途径[2-3]。但单纯以EC为靶点的抗血管治疗在部分高度恶性的肿瘤中并未能有效改善患者的5年生存率。血管生成拟态(vasculogenic mimicry,VM)是近年来被证实的无EC参与的另一种血管形成方式,VM无血管内皮内衬,肿瘤细胞可以随时脱落进入血管并随血流发生转移,拥有VM的恶性肿瘤,大多容易复发转移、预后差、生存率低。
人绒癌的合体滋养细胞可分泌人绒毛膜促性腺激素(human chorionic gonadotropin,HCG),滋养细胞侵犯子宫肌层后可发生血管重铸,肿瘤浸润宿主后形成的微循环管腔与卵巢癌细胞VM有着惊人的相似,于是我们推测HCG在卵巢癌细胞VM形成过程中发挥重要作用。本研究用过表达质粒上调及小干扰RNA(small interfering RNA,siRNA)下调卵巢癌OVCAR-3细胞中HCG的表达,并在裸鼠模型上观察HCG表达对OVCAR-3细胞VM形成的影响。
1 材料与方法 1.1 材料及试剂卵巢癌OVCAR-3细胞和绒癌BeWo细胞株均购自中国典型培养物保藏中心。SPF级4~6周龄BALB/c雌性裸鼠由中国科学院动物实验中心提供,动物实验在SPF级实验动物室进行。慢病毒载体和质粒购自美国Invitrogen公司。胎牛血清和RPMI 1640培养液购自美国Gibco公司。总RNA提取试剂RNAiso Plus、反转录试剂盒PrimeScript RT Reagent Kit购自日本TaKaRa公司。PCR引物由上海生工合成。ELISA试剂盒、免疫组织化学试剂盒、HE染色试剂盒购自武汉博士德生物工程有限公司。PAS染色试剂盒购自美国Sigma公司。大鼠抗小鼠CD34抗体购自美国Santa Cruz公司。JEOL-1230透射电子显微镜装置购自日本Tokyo公司。
1.2 方法 1.2.1 CGB5上调或下调细胞株构建采用慢病毒载体转染的方法[4],在卵巢癌OVCAR-3细胞中分别转染CGB5过表达载体、空载体、CGB5 siRNA及无关序列siRNA。另将未处理的OVCAR-3细胞作为空白细胞对照,高表达CGB5的绒癌BeWo细胞作为阳性对照。用实时定量PCR检测转染后CGB5的表达,各组分别为:空白细胞对照(blank control),CGB5过表达组(CGB5),空载体组(blank vector),CGB5干扰组(CGB5 siRNA),无关序列siRNA组(scramble siRNA),BeWo细胞组(BeWo)。
1.2.2 实时定量PCR用TRIzol提取细胞总RNA后,用SYBR Green One-Step qRT-PCR试剂盒进行定量PCR检测,反应程序为:50℃反转录反应3 min,95℃预变性5 min,95℃变性15 s,60℃退火并延伸,循环40次。CGB5上游引物:5’-CTACTGCCCCACCATGACC-3’,下游引物:5’-ATGGACTCGAAGCGCACATC-3’;内参GAPDH上游引物:5’-AAGGTGAAGGTCGGAGTC-3’,下游引物:5’-GAAGATGGTGATGGGATTTC-3’。
1.2.3 裸鼠皮下移植瘤模型的建立取36只裸鼠,随机分成6组,每组6只。分别将6株细胞(空白细胞、CGB5过表达细胞、空载体细胞、CGB5干扰细胞、无关序列siRNA细胞和BeWo细胞组),以200 μl(每只1×106细胞),注入裸鼠右侧腋窝皮下建立皮下移植瘤模型,待肿瘤生长到直径1~2 cm左右取下标本。
1.2.4 HE染色将裸鼠卵巢肿瘤组织做成石蜡切片,二甲苯脱去切片中的石蜡,再经由高浓度到低浓度乙醇,最后置入蒸馏水。将已置入蒸馏水后的切片放入苏木精水溶液中染色数分钟。盐酸及氨水中分色,各数秒钟。流水冲洗1 h后置入蒸馏水片刻。置入70%和90%乙醇中脱水各10 min。置入乙醇伊红染色液染色2~3 min。染色后的切片经纯乙醇脱水,再经二甲苯使切片透明,中性树胶封片。
1.2.5 CD34-PAS双染色首先进行CD34免疫组织化学染色:裸鼠卵巢肿瘤组织石蜡切片于37℃过夜后以二甲苯脱蜡15 min×3次。分别经无水乙醇×10 min,95%乙醇×10 min,80%乙醇×10 min,蒸馏水×10 min,脱二甲苯。3% H2O2室温孵育20 min,以阻断内源性过氧化物酶活性。PBS洗5 min×3次。切片置入抗原修复液中60℃水浴25 min,以修复抗原。PBS洗5 min×3次。擦干PBS,置玻片于湿盒内,以1.5%正常山羊血清封闭。滴加一抗,湿盒置4℃冰箱过夜。取出玻片,以PBS洗5 min×3次,擦干。滴加二抗,室温下放置l h。PBS洗5 min×3次。切片置入DAB中染色,镜下观察染色情况,DAB显色后,于显微镜下控制显色时间,待血管内皮细胞着色后,放入PBS中以终止反应。然后进行PAS染色:将切片置于0.5%过碘酸溶液中氧化8~15 min,以10 min为佳;流水冲洗3 min后,置于Sehiff液中,避光条件下反应15~30 min,一般以15 min为宜;蒸馏水洗1 min×3次,流水冲洗3~5 min;苏木精对比染色细胞核,盐酸-乙醇分化,氨水返蓝;常规梯度乙醇脱水、二甲苯透明,中性树胶封片。
1.2.6 透射电子显微镜观察取裸鼠卵巢肿瘤组织块小于1 mm3。固定:2.5%戊二醛4℃预固定2 h→PBS洗涤15 min×3次→l%饿酸4℃后固定2 h。清洗:PBS洗涤15 min×3次。脱水及置换(各15 min):50%乙醇→70%乙醇→90%乙醇→90%乙醇:90%丙酮(1:1)→90%丙酮,以上在4℃进行→100%丙酮,室温进行3次置换。浸透:样品在纯丙酮:包埋液(2:l)室温浸透3 h→纯丙酮:包埋液(1:2)室温过夜→纯包埋液37℃浸透2 h。固化:样品37℃过夜→45℃ 12 h→60℃ 24 h。LKB-I型超薄切片机切片50 nm。3%醋酸铀-枸椽酸铅双染色。JEOL-1230透射电子显微镜观察,拍片。
1.2.7 微血管数(microvesseldensity,MVD)计数方法 计数微血管时先在低倍显微镜(×100)下扫描整个视野,选择血管最密集的10个区域,即“热点”,然后转至高倍镜(×400)下计数10个视野的微血管数,取其平均值,即为该组织切片每高倍视野的微血管数。
1.3 统计学方法采用SPSS19.0统计软件对实验数据进行统计学分析。多组均数比较采用单因素方差分析,两组间比较采用独立样本t检验,P<0.0.05为差异有统计学意义。
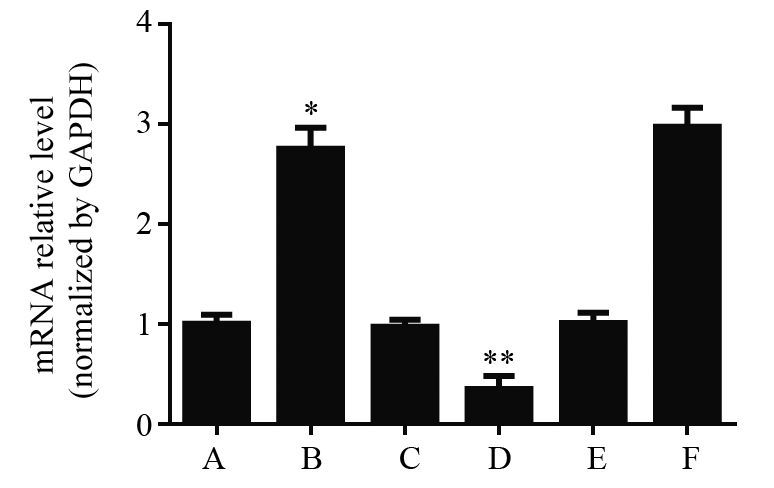
2 结果 2.1 实时定量PCR鉴定构建细胞株中CGB5的mRNA表达实时定量PCR检测结果显示,CGB5组的CGB5表达显著升高,CGB5 siRNA组的CGB5表达被抑制,阳性对照BeWo细胞中CGB5高表达,见图 1。
|
| *,**: all P=0.000,compared with Blank control group; A: Blank control group; B: CGB5 group; C: Blank vector group; D: CGB5 siRNA group; E: Scramble siRNA group; F: BeWo group 图 1 实时定量PCR鉴定构建细胞株中CGB5的表达 Figure 1 mRNA levels of CGB5 in constructed cells detected by real-time quantitive PCR |
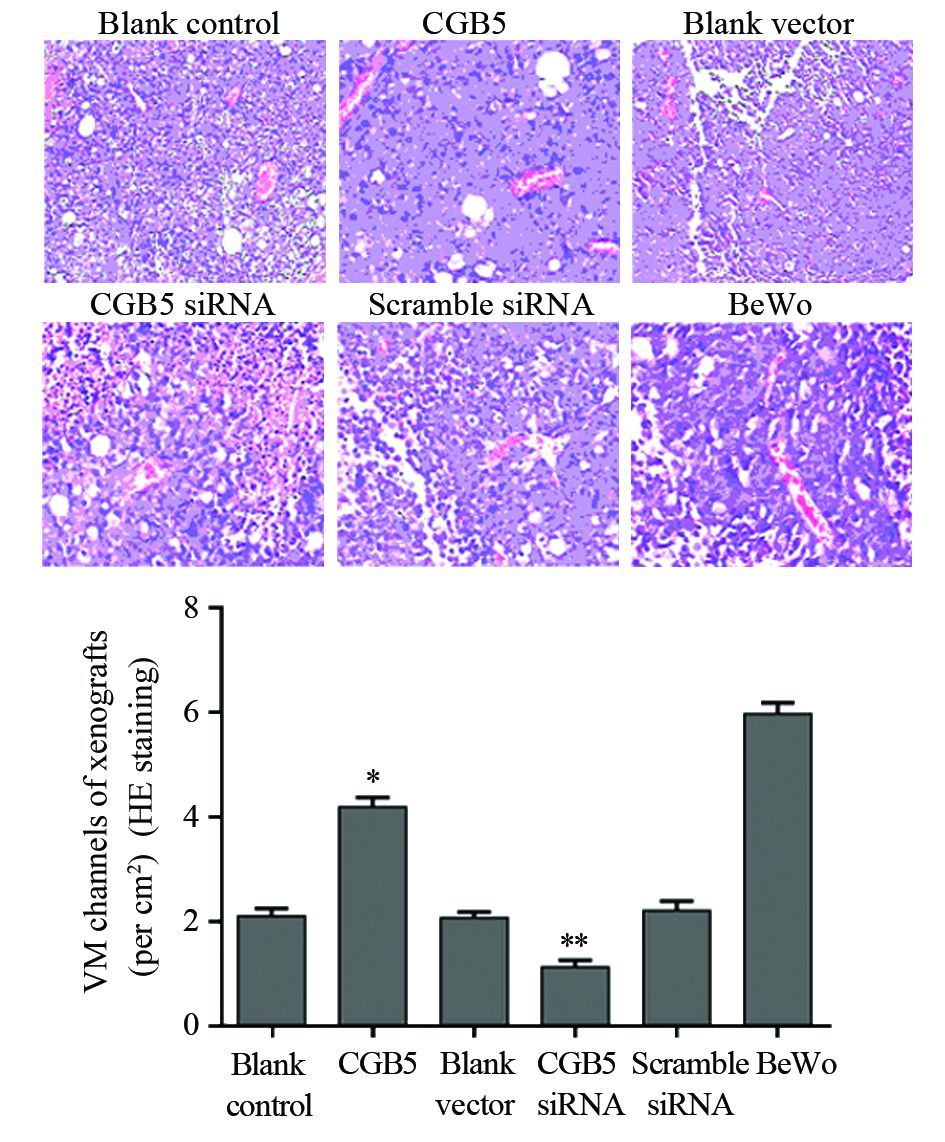
HE染色可见只有肿瘤细胞围成的管道样结构,中间有红细胞通过的即为VM。通过微血管计数可知:CGB5过表达组的血管生成拟态的数量较对照组显著增加,而CGB5干扰组的血管生成拟态的数量较对照组显著减少,见图 2。
|
| *,**: all P=0.000,compared with Blank control group 图 2 HE染色观察各组中血管生成拟态的形成 Figure 2 VM formations in different groups observed by HE staining |
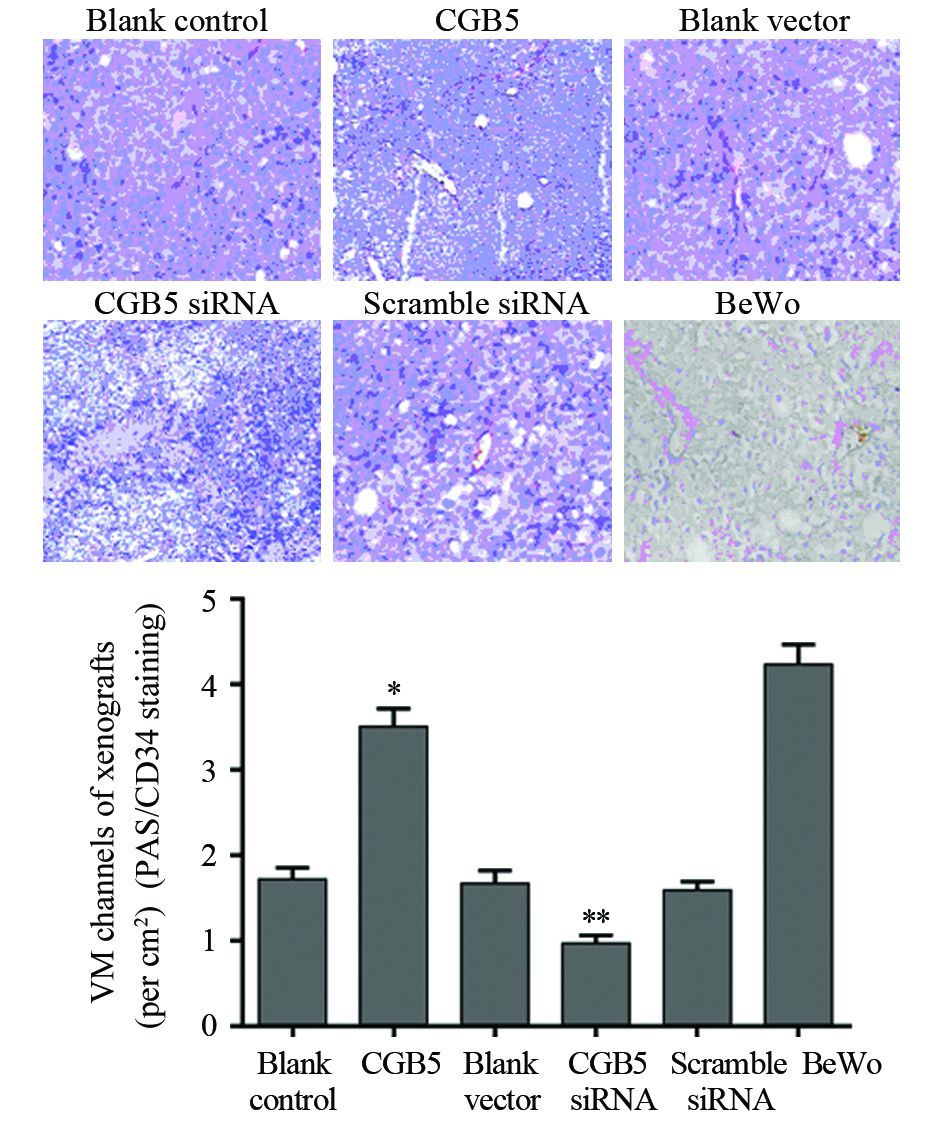
CD34-PAS双染色可见CD34染色阴性,PAS染色阳性的管道样结构,中间有大量红细胞通过的即为VM。通过微血管计数可知:CGB5过表达组的血管生成拟态的数量较对照组显著增加,而CGB5干扰组肿瘤组织大量坏死,其血管生成拟态的数量较对照组显著减少,见图 3。
|
| *: P=0.000,compared with Blank control group; **: P=0.0012,compared with Blank control group 图 3 CD34-PAS双染色观察各组中血管生成拟态的形成 Figure 3 VM formations in different groups observed by CD34-PAS double staining |
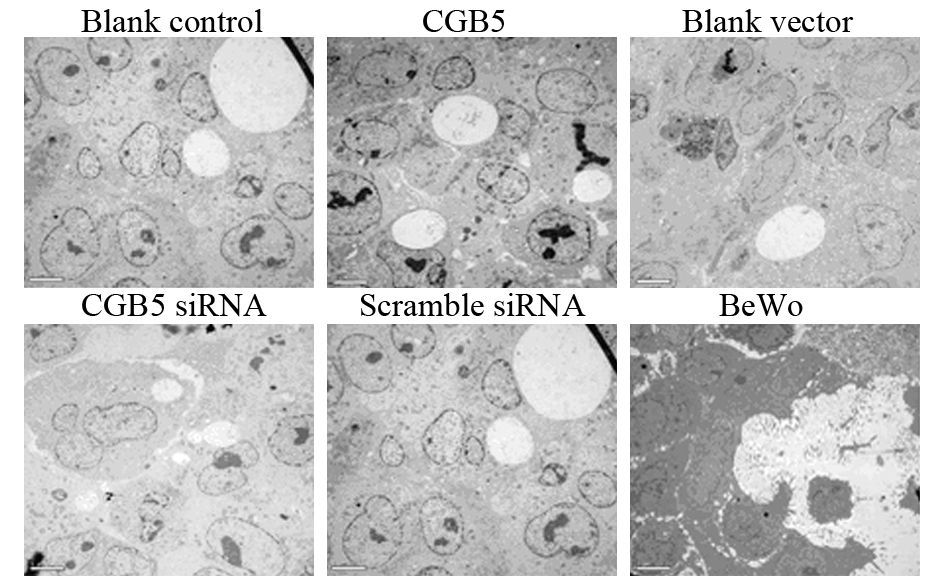
采用透射电子显微镜可以很明显地观察到各组中肿瘤细胞所围成的管道样结构,中间有红细胞通过。同样发现,CGB5过表达组的血管生成拟态的数量较对照组显著增加,见图 4。
|
| 图 4 透射电子显微镜下各组肿瘤中血管生成拟态的形成 Figure 4 VM formations in different groups examined by transmission electron microscopy |
卵巢癌是一种实体肿瘤,由肿瘤的实质和间质组成。肿瘤间质中存在着大量的微血管,直接影响着肿瘤细胞的生长、侵袭和转移,肿瘤的生长和转移都依赖于新生血管的生成[5]。传统意义上,肿瘤新生血管的生成主要包括:血管生成和血管发生。近年来,很多其他类型的血管形成也被一一证实,包括芽生式、套叠式、充塞式、内皮祖细胞的参与、马赛克式及血管生成拟态[6],其中没有内皮细胞参与的方式即血管生成拟态具体指具有高度侵袭性的肿瘤细胞能够模仿内皮细胞的表型形成基质丰富的血管网状结构,并有血浆和红细胞通过[7-9]。目前,继黑色素瘤后,VM又在乳腺癌、前列腺癌、肝癌、肾癌、胃癌、成胶质细胞瘤、结肠直肠癌、绒癌、卵巢癌及膀胱癌中被证实[7-19]。
研究发现,当实体恶性肿瘤刚形成时,没有自身的血管系统,主要通过周围组织的渗透作用来获取营养,这一时期称为肿瘤的无血管期。当肿瘤组织块长至直径约1~2 cm时,若仅靠单纯的周围组织渗透作用,已不能满足肿瘤细胞尤其肿块中央部位的细胞生长所需营养。而实际上,当肿块直径大于1 cm时,却很少出现明显的组织坏死。这一时期称为血管期,因为有大量的新生血管生成[20]。本研究成功构建了裸鼠皮下移植瘤模型,并取血管期的直径为1~2 cm的肿瘤组织作为研究标本。
HCG是由合体滋养细胞分泌的一种糖蛋白,研究发现,HCG除了作为一种与妊娠相关因子外,也是一种促血管因子[21]。例如,HCG可以通过促进内皮细胞的增生和血管内皮生长因子(vascular endothelial growth factor,VEGF)的表达来增加子宫动脉血流及促进卵巢新生血管发生[22-23];受孕期间,HCG也可诱导胎盘新生血管的发生等[24],所以我们也大胆猜测HCG可能与卵巢癌血管生成拟态也有着密切关系。HCG由α和β两个亚基组成的一个异源二聚体,其中α亚基与黄体生成素α亚基几乎完全相同,β-HCG又是一个由β1、β2、β3、β5、β7和β8这6个同源基因组成的亚基[25-27]。所以本研究选取了CGB5来研究HCG与卵巢癌之间的关系。
本研究利用成功建立的CGB5上调或下调及其相应对照的卵巢癌细胞OVCAR-3、高表达CGB5的BeWo绒癌细胞构建了裸鼠皮下移植瘤模型,取肿瘤组织同时用HE染色、CD34-PAS双染色及透射电子显微镜观察各组中血管生成拟态的形成,与对照组相比,结果均显示CGB5过表达组的VM数量显著增加,而CGB5干扰组的VM数量显著减少。
综上所述,如果HCG确实与卵巢癌血管生成拟态的形成有密切联系,那么随着对血管生成拟态的进一步深入研究,人们对卵巢癌的浸润、转移、复发等恶性生物学行为的认识和防治也将会进一步深入。这将为我们今后临床工作中卵巢癌的治疗提供一种新的思路。
| [1] | Qiao L, Liang N, Zhang J, et al. Advanced research on vasculogenic mimicry in cancer[J]. J Cell Mol Med, 2015, 19 (2) : 315–26. DOI:10.1111/jcmm.2015.19.issue-2 |
| [2] | Vartanian AA, Burova OS, Stepanova EV, et al. Melanoma vasculogenic mimicry is strongly related to reactive oxygen species level[J]. Melanoma Res, 2008, 17 (6) : 370–9. |
| [3] | Bridges EM, Harris AL. The angiogenic process as a therapeutic target in cancer[J]. Biochem Pharmacol, 2011, 81 (10) : 1183–91. DOI:10.1016/j.bcp.2011.02.016 |
| [4] | Gao SN, Zhang YQ, Su M, et al. Effect of CGB5 on human epithelial ovarian cancer cell line OVCAR-3 in the tumor formation rates and growth speed in vivo[J]. Nantong Da Xue Xue Bao(Yi Xue Ban), 2015, 1 : 13–6. [ 高赛楠, 张玉泉, 苏敏, 等. CGB5对卵巢癌细胞OVCAR-3成瘤率及成瘤速度影响的体内研究[J]. 南通大学学报(医学版), 2015, 1 : 13–6. ] |
| [5] | Abdollahi A, Folkman J. Evading tumor evasion: Current concepts and perspectives of anti-angiogenic cancer therapy[J]. Drug Resist Updat, 2010, 13 (1-2) : 16–28. DOI:10.1016/j.drup.2009.12.001 |
| [6] | Li X, Wu M, Pan L, et al. Tumor vascular-targeted co-delivery of anti-angiogenesis and chemotherapeutic agents by mesoporous silica nanoparticle-based drug delivery system for synergetic therapy of tumor[J]. Int J Nanomedicine, 2015, 11 : 93–105. |
| [7] | Zhang S, Man L, Gu Y, et al. Thalidomide influences growth and vasculogenic mimicry channel formation in melanoma[J]. J Exp Clin Cancer Res, 2008, 27 : 60. DOI:10.1186/1756-9966-27-60 |
| [8] | Sun W, Fan YZ, Zhang WZ, et al. A pilot histomorphology and hemodynamic of vasculogenic mimicry in gallbladder carcinomas in vivo and in vitro[J]. J Exp Clin Cancer Res, 2011, 30 : 46. DOI:10.1186/1756-9966-30-46 |
| [9] | Hess AR, Seftor EA, Seftor RE, et al. Phosphoinositide 3-kinase regulates membrane Type 1-matrix metalloproteinase (MMP) and MMP-2 activity during melanoma cell vasculogenic mimicry[J]. Cancer Res, 2003, 63 (16) : 4757–62. |
| [10] | Shirakawa K, Wakasugi H, Heike Y, et al. Vasculogenic mimicry and pseudo-comedo formation in breast cancer[J]. Int J Cancer, 2002, 99 (6) : 821–8. DOI:10.1002/(ISSN)1097-0215 |
| [11] | Guzman G, Cotler SJ, Lin AY, et al. A pilot study of vasculogenic mimicry immunohistochemical expression in hepatocellular carcinoma[J]. Arch Pathol Lab Med, 2007, 131 (12) : 1776–81. |
| [12] | Sharma N, Seftor RE, Seftor EA, et al. Prostatic tumor cell plasticity involves cooperative interactions of distinct phenotypic subpopulations: Role in vasculogenic mimicry[J]. Prostate, 2002, 50 (3) : 189–201. DOI:10.1002/(ISSN)1097-0045 |
| [13] | Vartanian AA, Stepanova EV, Gutorov SL, et al. Prognostic significance of periodic acid-Schiff-positive patterns in clear cell renal cell carcinoma[J]. Can J Urol, 2009, 16 (4) : 4726–32. |
| [14] | El Hallani S, Boisselier B, Peglion F, et al. A new alternative mechanism in glioblastoma vascularization: tubular vasculogenic mimicry[J]. Brain, 2010, 133 (Pt 4) : 973–982. |
| [15] | Li M, Gu Y, Zhang Z, et al. Vasculogenic mimicry: a new prognostic sign of gastric adenocarcinoma[J]. Pathol Oncol Res, 2010, 16 (2) : 259–66. DOI:10.1007/s12253-009-9220-7 |
| [16] | Baeten CI, Hillen F, Pauwels P, et al. Prognostic role of vasculogenic mimicry in colorectal cancer[J]. Dis Colon Rectum, 2009, 52 (12) : 2028–35. DOI:10.1007/DCR.0b013e3181beb4ff |
| [17] | Shih IeM. Trophoblastic vasculogenic mimicry in gestational choriocarcinoma[J]. Mod Pathol, 2011, 24 (5) : 646–52. DOI:10.1038/modpathol.2010.231 |
| [18] | Sood AK, Fletcher MS, Zahn CM, et al. The clinical significance of tumor cell-lined vasculature in ovarian carcinoma: implications for anti-vasculogenic therapy[J]. Cancer Biol Ther, 2002, 1 (6) : 661–4. DOI:10.4161/cbt.316 |
| [19] | Li Q, Yang JR, Li JF. Experiment of Vasculogenic Mimicry in Transitional Cell Carcinoma of Bladder[J]. Zhong Liu Fang Zhi Yan Jiu, 2011, 38 (6) : 651–3. [ 李清, 杨金瑞, 李解方. 膀胱移行细胞癌血管生成拟态的实验[J]. 肿瘤防治研究, 2011, 38 (6) : 651–3. ] |
| [20] | Tang HS, Feng YJ, Yao LQ. Angiogenesis, vasculogenesis, and vasculogenic mimicry in ovarian cancer[J]. Int J Gynecol Cancer, 2009, 19 (4) : 605–10. DOI:10.1111/IGC.0b013e3181a389e6 |
| [21] | Zygmunt M, Herr F, Keller-Schoenwetter S, et al. Characterization of human chorionic gonadotropin as a novel angiogenic factor[J]. J Clin Endocrinol Metab, 2002, 87 (11) : 5290–6. DOI:10.1210/jc.2002-020642 |
| [22] | Due?as-Garcia OF, Diaz-Sotomayor M, Rico-Olvera H. Utility of the pulsatility index of the uterine arteries and human chorionic gonadotropin in a series of cases of placenta accreta[J]. J Obstet Gynaecol Res, 2011, 37 (8) : 1112–6. DOI:10.1111/jog.2011.37.issue-8 |
| [23] | Berndt S, Perrier d'Hauterive S, Blacher S, et al. Angiogenic activity of human chorionic gonadotropin through LH receptor activation on endothelial and epithelial cells of the endometrium[J]. FASEB J, 2006, 20 (14) : 2630–2. DOI:10.1096/fj.06-5885fje |
| [24] | Michel RM, Aguilar JL, Arrieta O. Human chorionic gonadotropin as an angiogenic factor in breast cancer during pregnancy[J]. Med Hypotheses, 2007, 68 (5) : 1035–40. DOI:10.1016/j.mehy.2006.05.072 |
| [25] | Hamada AL, Nakabayashi K, Sato A, et al. Transfection of Antisense Chorionic Gonadotropin β Gene into Choriocarcinoma Cells Suppresses the Cell Proliferation and Induces Apoptosis[J]. J Clin Endocrinol Metab, 2005, 90 (8) : 4873–9. DOI:10.1210/jc.2004-2458 |
| [26] | Kubiczak M, Walkowiak GP, Nowak-Markwitz E, et al. Human chorionic gonadotropin beta subunit genes CGB1 and CGB2 are transcriptionally active in ovarian cancer[J]. Int J Mol Sci, 2013, 14 (6) : 12650–60. DOI:10.3390/ijms140612650 |
| [27] | G?odek A, Kubiczak MJ, Walkowiak GP, et al. Methylation status of human chorionic gonadotropin beta subunit promoter and TFAP2A expression as factors regulating CGB gene expression in placenta[J]. Fertil Steril, 2014, 102 (4) : 1175–82. DOI:10.1016/j.fertnstert.2014.06.016 |
 2016, Vol. 43
2016, Vol. 43


