文章信息
- NSCLC的疫苗治疗研究进展
- Progress in Vaccines Against Non-small Cell Lung Cancer
- 肿瘤防治研究, 2016, 43(8): 721-727
- Cancer Research on Prevention and Treatment, 2016, 43(8): 721-727
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2016.08.015
- 收稿日期: 2015-11-06
- 修回日期: 2016-02-25
据世界卫生组织报道,肺癌的发病率在癌症发病率中占第二位,死亡率遥居首位,其总的5年生存率约18%[1]。80%~85%肺癌患者是非小细胞肺癌(non-small cell lung cancer,NSCLC)[2]。大多数患者发现时已属于晚期,失去手术机会,而放疗、化疗不良反应大,大部分患者治疗效果不理想。近几年,由于分子靶向治疗的发展,肺癌患者有了莫大的受益,对治疗水平有了显著的提高,同时减轻了药物的不良反应[3-4]。
多数肿瘤的发生与基因改变相关,这就导致新抗原的产生,免疫系统即对“外来物”进行识别,并引导T细胞相关反应[5-7]。以前认为,肺癌属于非典型免疫原性肿瘤。随着肿瘤免疫学的发展,发现NSCLC亦是一种免疫原性肿瘤,可以表达肿瘤相关抗原[8]。肺癌免疫治疗主要分为被动免疫治疗、主动免疫治疗和支持性免疫治疗。主动免疫治疗主要分为抗原特异性免疫治疗和靶向免疫治疗,其中,特异性免疫治疗主要为疫苗,而靶向免疫治疗主要为检查点阻滞抑制剂(CTLA-4和PD1/PD-L1)等。被动免疫治疗最常见的形式是注射重组细胞因子、免疫效应细胞、DC细胞和单克隆抗体等。支持性免疫治疗指通过非特异性的增加机体本身的免疫系统,包括免疫调节剂等。
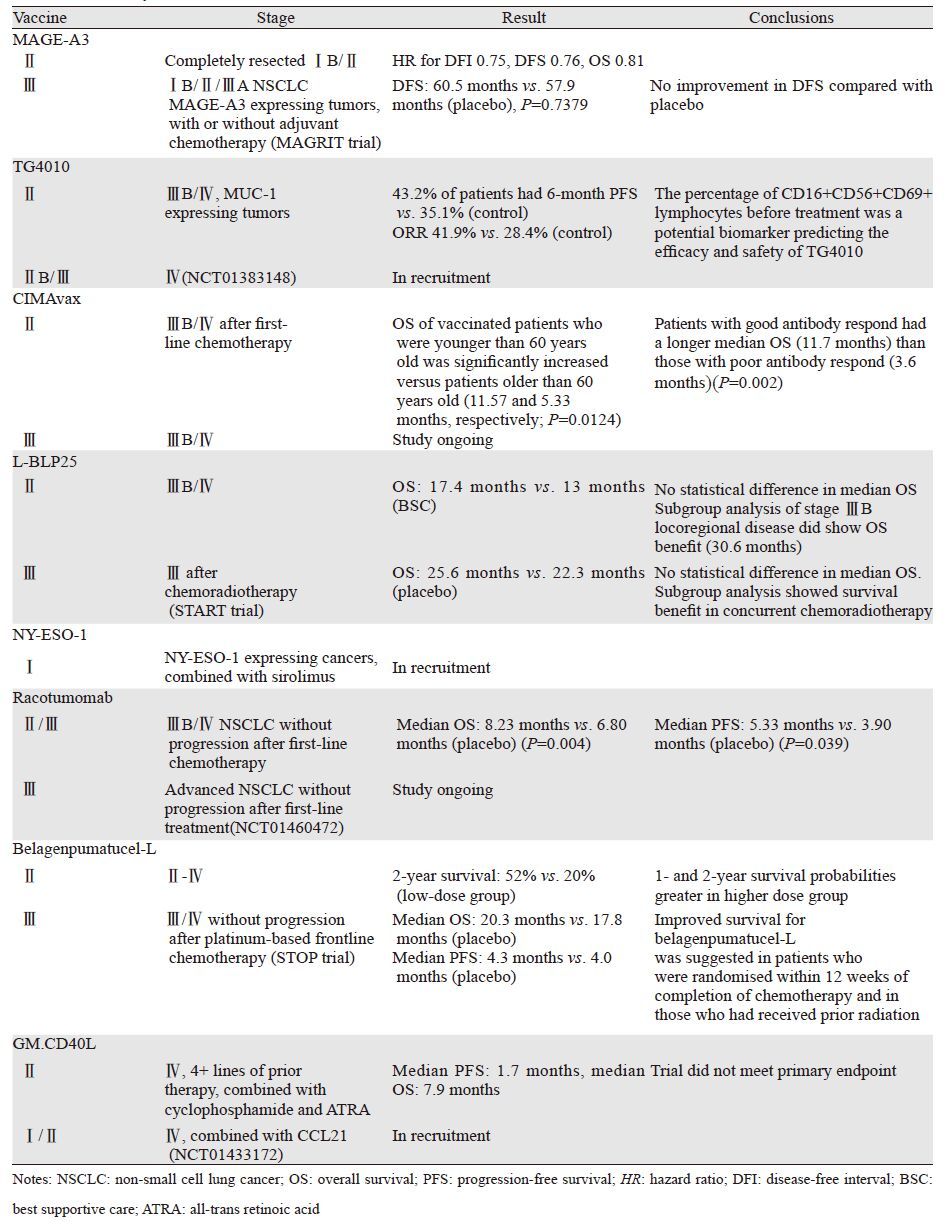
疫苗曾被用来预防和治疗肿瘤。例如,乙肝疫苗和重组HPV疫苗就是能预防可致癌的病毒感染所致的肿瘤发生。肺癌的疫苗治疗经验仍不足。因此,本文主要就非小细胞肺癌疫苗研究进展进行综述,以了解这一领域的最新进展。就疫苗的组成类型分为以下几种类别。非小细胞肺癌疫苗治疗总概要,见表 1。
蛋白疫苗包括MAGE-A3疫苗、TG4010疫苗、EGF疫苗CIMAvax。其中EGF疫苗CIMAvax是古巴研制的,并且在最近的临床试验中得到证明,它在晚期非小细胞肺癌患者治疗中的疗效十分确切。
1.1 MAGE-A3疫苗黑色素瘤相关抗原(MAGE-A3)几乎只在肿瘤组织中表达,除了睾丸和胎盘,不在其他正常组织中表达。据报道,该抗原在35%的早期非小细胞肺癌组织中表达,而在55%的晚期非小细胞肺癌患者中表达。该抗原的功能尚不明确,但是该抗原的高表达与预后不良密切相关[9]。另一项研究发现,在104例NSCLC中,未见同一标本中部分肿瘤细胞MAGE-3抗原表达阳性而另一部分表达阴性的情况,只见到全部肿瘤细胞MAGE-3抗原表达阳性或阴性,说明选用MAGE-3基因产物作为靶分子对抗原表达阳性的患者进行免疫治疗,有可能对该类NSCLC患者的全部肿瘤细胞均产生杀伤效应[10]。MAGE-A3疫苗是由重组融合蛋白(MAGE-A3和流感嗜血杆菌蛋白D)与提高免疫反应的蛋白佐剂(ASO2b和AS15)组合而成的蛋白疫苗。
一项随机对照的二期临床试验[11],入组对象是完整切除的ⅠB/Ⅱ期MAGE-A3阳性的NSCLC患者,共182例。被随机分配到疫苗组(n=122)和安慰剂组(n=60)。疫苗组的患者先接受5次诱导接种,每3周一次。后再行巩固接种治疗,每3月一次。以无疾病间期(disease-free interval,DFI)为主要试验终点。数据显示,DFI(HR=0.75)、DFS(HR=0.76)、OS(HR=0.81)均分别有所提高。组间结果比较差异无统计学意义。在该试验中没有发现疫苗有显著的不良反应。
在晚期黑色素瘤试验中,发现了能预测MAGE-A3免疫治疗活性的基因标记。基于此理论,从MAGE-A3免疫治疗中获益的早期NSCLC患者的Ⅱ期试验中,基因标记阳性的患者,疫苗组与安慰剂组相比,显示了可喜的DFI(P=0.06)。然而,基因标记阴性的患者中,DFI没有明显的不同(P=0.65)[12]。
基于该疫苗的潜在临床应用意义,研究者发起一项Ⅲ期临床试验(MAGRIT,NCT00480025)[13],把MAGE-A3疫苗作为完整切除的ⅠB~ⅢA期MAGE-A3阳性的NSCLC患者的辅助治疗。在标准的外科治疗伴或不伴辅助化疗后,患者将接受超过27月的疫苗治疗。DFS是主要试验终点。2 272例患者被随机分配入组。结果提示,试验组中位DFS是60.5月,安慰剂组是57.9月(P=0.7379)。而没有接受辅助化疗的患者中,试验组的中位DFS是58月,对照组是56.9月(P=0.7572)。严重不良事件在两组间无明显差异。该研究提示不管是在总受试人群还是没有接受化疗的人群,MAGE-A3疫苗对比安慰剂没有增加DFS。这个试验也没有证实上述基因标记对MAGE-A3的治疗获益有预测意义。
1.2 TG4010疫苗MUC1是在表皮细胞表面的过度糖基化的跨膜蛋白[14]。MUC1通常在肿瘤细胞中过表达,并发生异常糖基化,这通常导致细胞不可逆的凋亡、T细胞抑制以及不良预后。TG4010是该抗原重组的病毒疫苗,载体是修改后的Ankara病毒,经修改处理后不仅表达肿瘤相关性抗原MUC1抗原,也表达IL-2[15]。外源性注射IL-2是一个较强的免疫佐剂,它可以改变MUC1引起的免疫抑制[16]。
一项关于148例MUC1阳性的ⅢB期/Ⅳ期NSCLC患者的Ⅱ期随机对照试验(RCT)[17],接受6周期的一线GP方案化疗伴或不伴TG4010疫苗治疗。疫苗先每周注射,共6次,以后每3周一次,直至疾病进展。主要试验终点是PFS达6月。结果显示,试验组PFS达6月的占43.2%,而安慰剂组占35.1%(P=0.307)。中位OS也没有显著不同(疫苗组10.7月vs. 安慰剂组10.3月)。亚组分析显示,NK细胞活化水平是疫苗有效性的潜在预测因素。NK细胞活化水平高的患者,中位OS要明显低于那些正常的患者(11.3月vs. 18月,P=0.020)。NK细胞活化水平正常的患者,PFS达6月的占58%。疫苗有关的不良反应轻微,大多数为注射部位的反应、腹痛和发热。TIME是一项TG4010参与Ⅳ期NSCLC免疫治疗的ⅡB/Ⅲ期试验(NCT01383148),将重新评估TG4010疫苗加上一线化疗的疗效。该临床试验的主要试验终点是活化NK细胞在Ⅱ期试验中的预测价值以及Ⅲ期试验中的疗效,目前仍在招募志愿者中。
1.3 人重组EGFR(rHU-EGF-P64K/Montanide ISA 51;CIMAvax EGF)EGFR在细胞间和NSCLC的样本中都出现过表达,并且与肿瘤的过度增殖、分化程度低、淋巴结转移率高风险以及不良预后有关[18]。CIMAvax EGF,一种重组的人生长因子疫苗,由重组EGF融合转运蛋白P64K,以及Montanide ISA 51组成。
在一项Ⅱ期临床试验中[19],应用EGF疫苗后73%患者血液中检查到很好的抗EGF反应,58%患者可以有效阻断EGF/EGFR信号通路。一项Ⅱ期临床试验,收集了80例ⅢB期或Ⅳ期患者,接受一线化疗后,被随机分配到EGF疫苗组或BSC组[20]。患者在疫苗注射前3天接受环磷酰胺治疗,CIMAvax每周注射,4次后每月注射,直至病情进展。疫苗组中有51.3%的患者获得了良好的抗EGF反应。且治疗组有延长生存期的倾向(治疗组6.5月vs. 对照组5.3月,P=0.098)。亚组分析显示,年龄低于60岁的患者,明显获益(11.57月 vs. 5.33月,P=0.0124)。EGF抗体滴度大于1:4 000,或者4倍于治疗之前免疫效价的患者,中位OS为11.7月,其余的患者中位OS为3.6月(P=0.002)。为了对比CIMAvax EGF疫苗在晚期NSCLC患者中的疗效,一项Ⅲ期临床试验拟入组579例晚期NSCLC患者。该试验还会揭示高于60岁或低于60岁的亚组分析结果(NCT01444118)。
2 肽疫苗 2.1 L-BLP25疫苗L-BLP25疫苗是一种肽疫苗,由一段来自MUC1蛋白的BLP25脂肽(包含25个氨基酸)与一个免疫佐剂(单磷酰脂质A)以及可以促进APC摄取的脂质体转运系统连接而成[21]。
一项Ⅱ期RCT中,共入组171例ⅢB期或Ⅳ期NSCLC患者,一线治疗后疾病缓解或稳定[22]。随机分到L-BLP25疫苗组(n=88)或BSC组(n=83)。试验组经3天环磷酰胺300 mg/m2治疗后,再行8次每周L-BLP25疫苗治疗,以后每6周一次,直至病情进展。结果显示,试验组中位OS是17.4月,而BSC组是13月(P=0.112)。亚组分析,主要受益者是Ⅲ期行放化疗的患者。试验组与BSC组的中位OS分别是30.6月、13.3月(P=0.092)。疫苗主要不良反应为流感样症状和轻微的注射部位反应。另一项Ⅲ期国际间RCT试验(START)[23],对比了L-BLP25维持治疗(n=829)和安慰剂(n=410)在Ⅲ期NSCLC患者的疗效。入组患者经序贯或同步放化疗后疾病稳定或缓解。疫苗组先每周行疫苗治疗,持续8周后改为每6周给药,直至病情进展。主要终点OS在两组间没有明显差异(25.6月 vs. 22.3月,P=0.123)。亚组分析显示,疫苗组中行同步放化疗的患者OS显著提高:疫苗组30.8月、安慰剂组20.6月(P=0.016)。序贯放化疗的患者中疫苗组和安慰剂组的中位OS分别是19.4月、24.6月(P=0.38)。评估不可切除的Ⅲ期NSCLC亚洲患者中疫苗L-BLP25加上BSC对比安慰剂加上BSC疗效的Ⅲ期临床试验INSPIRE结果估计将于明年得出。另一项关于Ⅲ期不可切除的NSCLC患者行放化疗后,L-BLP-25疫苗联合贝伐单抗的Ⅱ期试验(NCT00828009),将于2016年结束。
2.2 NY-ESO-1(New York esophageal squamous cell carcinoma-1)抗原特异性肿瘤疫苗NY-ESO-1是一种肿瘤特异性抗原,在1/4~1/3的所有肺癌、黑色素瘤、卵巢癌、食管癌、膀胱癌和前列腺癌的患者有表达,且与肿瘤高级别相关。NY-ESO-1f(NY-ESO-191-110)肽疫苗,已结束的Ⅰ期临床试验[24],10例入组患者中2例肺癌患者及1例食管癌患者病情稳定,均对于疫苗耐受良好。疫苗治疗后,9例(9/10)患者体内诱发出NY-ESO-1抗体反应,9例(9/10)患者体内CD4+及CD8+T细胞增加。2013年,Eikawa等[25]报道,长肽段的NY-ESO-1肽疫苗能很好地引出对NY-ESO-1的体液免疫和细胞免疫,比短的效果要好,也优于完整的蛋白疫苗。能很好地引出HLA限制的CD8+T细胞的免疫反应。
2014年,Wada等[26]报道,该试验所用NY-ESO-1肿瘤疫苗,包括了4种合成的重叠长肽,其中包含了NY-ESO-1分子中高免疫性区域。该试验疫苗由各0.25 mg的三种30-mer长的NY-ESO-1肽段和1种32-mer长的NY-ESO-1肽段、0.2KE沙培林OK-432和1.25 ml Montanide ISA-51合成。试验结果提示该合成肿瘤疫苗能很好地被耐受,并能很好地引出NY-ESO-1特异性体液反应和CD4+、CD8+T细胞反应。疫苗加上西罗莫司在表达NY-ESO-1的实体肿瘤中疗效的Ⅰ期临床试验正在进行(NCT01522820),试验将于2016年结束。关于能识别NY-ESO-1的基因改造的T细胞,加上树突状细胞结合NY-ESO-1抗原的疫苗治疗的Ⅱ期试验,现正在招募晚期或复发的肺癌患者(NCT01697527)。试验将于2018年结束。
3 神经节苷脂疫苗神经节苷脂是鞘糖脂与一个或多个唾液酸连接而成,它通常都表达在肿瘤细胞表面,它还参与细胞间识别、细胞基质黏附和细胞分化。NeuGc-GM3是神经节苷脂正常Neu乙酰化形式的变异,因此可用作肿瘤细胞的特异性识别信号,这也让它成为了免疫治疗很好的靶点[27]。
Racotumomab(以前被称为IE10):Racotumomab是一种靶向肿瘤相关性神经节苷脂NeuGcGM3的抗个体基因型疫苗,能引起抗NeuGc-GM3的体液和细胞反应[28-29]。一项随机对照试验比较了Racotumomab与安慰剂治疗一线化疗后ⅢB/Ⅳ期NSCLC患者的疗效[30]。一线化疗后病情稳定的ⅢB/Ⅳ期NSCLC患者1:1随机分配到Racotumomab组(每2周接种一次,共5次,后每4周再次接种)或安慰剂组。即使疾病进展也继续治疗,直到出现不良反应或体力状态严重下降的情况才停止治疗。主要研究终点是OS。176例患者被随机分配到Racotumomab组(n=87)和安慰剂组(n=89)。Racotumomab组中位OS 8.23月,安慰剂组中位OS 6.80月(P=0.004)。Racotumomab组中位PFS 5.33月,安慰剂组中位PFS 3.90月(P=0.039)。Racotumomab最常见不良反应是注射部位疼痛、骨痛和乏力。这些患者获得了对NeuGcGM3神经节苷脂的IgM和IgG抗体反应。关于Racotumomab对比BSC在一线化疗后疾病稳定的晚期NSCLC患者中疗效的随机多中心的Ⅲ期试验正在进行。
4 全细胞疫苗 4.1 Belagenpumatucel-LBelagenpumatucel-L是同种异体全细胞肿瘤疫苗。疫苗制备自四株肺癌细胞株,包括2株肺腺癌、1株鳞癌、1株大细胞癌,用含TGF-β2的反义转基因质粒进行转染[31]。有文献报道,TGF-β2水平的升高与癌症患者免疫抑制有关,并且TGF-β2水平与NSCLC患者的预后呈反比例相关[32]。该疫苗设计会使反义质粒转染所诱导的TGF-β2基因沉默,以减少该细胞因子的产生,从而提高该疫苗的免疫原性。
在一项Ⅱ期剂量对照试验中,共入组75例Ⅱ~Ⅳ期NSCLC患者。接受1.25×107、2.5×107或者5×107细胞/次的疫苗注射,每月注射一次或者每两月注射一次,共16次[31]。结果显示,疫苗相关的生存率与给药剂量相关,高剂量组的患者2年生存率为52%,低剂量组的患者只有20%。关于Belagenpumatucel-L的Ⅲ期RCT(STOP)的结果已经得出[33]。试验入组对象是Ⅲ/Ⅳ期NSCLC患者,经一线化疗后没有出现疾病进展。共入组532名患者,被随机分配到Belagenpumatucel-L组(25×106 cell/0.4 ml,n=270)和安慰剂组(n=262)。试验组接受共18次的每月一次的疫苗注射,并在21、24月各注射一次。试验组的中位OS是20.3月,安慰剂组是17.8月(P=0.594)。中位PFS没有显著差异(P=0.947)。亚组分析发现,接受放化疗的患者,试验组和安慰剂组的中位OS分别是28.4月、16.0月(P=0.032)。接受放化疗并在治疗结束后12周内接受随机并治疗的患者中,中位OS试验组为28.4月,对照组是10.3月(P=0.013)。Belagenpumatucel-L主要的不良反应是局部注射反应、咳嗽、疲乏等反应。
4.2 DC疫苗DC是体内专职抗原递呈细胞和最佳的天然免疫佐剂。具有独特的刺激T细胞增殖的能力,是机体免疫应答的始动者。目前,已建立多种方法制备基于DC的肿瘤疫苗,如用肿瘤细胞裂解物或凋亡的肿瘤细胞等冲击致敏DC、肿瘤相关抗原肽段直接致敏DC、将肿瘤相关抗原基因通过电穿孔或质粒DNA或病毒性载体直接转染DC等[34]。其中,INGn-225是p53修饰的腺病毒转染的DC疫苗。Chiappori等[35]报道了INGn-225治疗SCLC患者的Ⅱ期临床试验结果,INGn-225能诱导强烈免疫应答,特别是能增强患者对后续化疗的敏感度,有78%对p53应答的患者可在后续化疗中受益。而一项DC疫苗的Ⅰ期临床研究[36],15例Ⅲ/Ⅳ期NSCLC患者在2周内接受3次3×106、6×106或12×106DC疫苗皮下注射。5例患者暴露肿瘤裂解液之后,产生更多的γ-干扰素。2例患者出现混合应答,肿瘤有缓解,提示有一定的临床获益。
4.3 GM-CSF系列疫苗GM-CSF是刺激巨噬细胞和DC细胞等抗原递呈细胞增殖、活化和趋化的细胞因子。GVAX是携带GM-CSF基因腺病毒载体转染的自体肿瘤细胞疫苗。2004年,Nemunaitis等[37]报道了GVAX治疗83例NSCLC患者的Ⅰ~Ⅱ期临床试验结果,其中3例晚期患者完全缓解的时间分别持续了6、18和22月以上。试验结果显示,接种后每24 h分泌的GM-CSF浓度高于40 ng/106cells接种后分泌GM-CSF≥40 ng/24 h/106cells的患者其中位生存期为17月,比接种后产生GM-CSF浓度低的患者获得更长的生存期(P=0.028)。2006年,Nemunaitis等[38]报道GVAX的改良版bystander GVAX是由自体来源的肿瘤细胞与同种异体的GM-CSF分泌细胞株的混合修改制作而成的。试验入组86例晚期患者,证明了bystander GVAX的灵活性。但是它的免疫应答效应及临床效应不比GVAX更有优势。新式GVAX疫苗制作上的灵活性,该疫苗的疗效值得更进一步的研究。
GM.CD40L旁观者细胞,它能募集树突状细胞和产生特异性抗肿瘤的T细胞反应,在体外试验中,当有两种混合的细胞系时,它能提高对自体肿瘤细胞的抗肿瘤效应[39]。一项关于GM.CD40L联合环磷酰胺和全反式维甲酸在NSCLC患者中的Ⅱ期试验[40],入组共24例患者。在接受至少3次疫苗注射后,10例(42%)患者疗效评价为SD。试验因没有达到主要观察终点而被终止。中位PFS为1.7 m,中位OS为7.9 m,1年存活率为33%。CCL21是强有力的趋化因子,在肺腺癌的小鼠模型中,它可以使肿瘤中CD4+和CD8+细胞增多,以及γ干扰素、GM-CSF和IL-12的增多[41]。同时伴有免疫抑制分子PGE-2和TGF-β水平下降。关于GM.CD40L联合CCL21的一项随机的Ⅰ/Ⅱ期试验正在开展(NCT01433172)。
5 展望及未来研究方向关于疫苗治疗在肺癌中的应用还有很长的路要走,还有很多问题亟待解决。例如,关于评价免疫反应疗效的标准问题、预测治疗效果及预后的基因标记以及生物标志物等。有研究发现[42],肺癌相关血清蛋白3(LASEP3)在198/361例NSCLC患者的肿瘤标本当中表达,并提示该标志物的高表达与不良预后有关。NSCLC患者的血清LASEP3水平高于健康志愿者,提示该标志物可能是潜在的诊断及预测预后的生物标志物,并可作为肺癌或其他实体肿瘤的治疗靶点。
未来肺癌免疫治疗的研究方向还包括以下方面:伴随远隔效应、疫苗的联合治疗、治疗顺序等。(1)伴随远隔效应是在放疗后会释放抗原以刺激效应细胞,诱导放射野外的区域肿瘤细胞死亡的免疫调节现象。这个现象,在新一代的检查点抑制剂的治疗中大量地被观察到[43-45]。这为进一步寻找疫苗疗法的关键合作伙伴奠定了基础。(2)近年来,有不少试验探索了疫苗的联合治疗。包括联合免疫检查点阻滞剂等方法。大量证据表明肿瘤微环境可能有免疫识别的介入,甚至有检查点抑制物的存在[46]。因此,关于GM.CD40L疫苗加上PD1抑制剂在晚期NSCLC患者一线治疗的试验正在计划当中。(3)本文中提及到的,在有效化疗的基础上,肺癌疫苗可能提高抗肿瘤效应。但关于疫苗治疗的介入时间,与其他治疗联合的顺序,仍是一个需要去解答的问题。
| [1] | Siegel RL, Miller KD, Jemal A. Cancer Statistics, 2015[J]. CA Cancer J Clin, 2015, 65 (1) : 5–29. DOI:10.3322/caac.21254 |
| [2] | Herbst RS, Heymach JV, Lippman SM. Lung cancer[J]. N Engl J Med, 2008, 359 (13) : 1367–80. DOI:10.1056/NEJMra0802714 |
| [3] | Kwak EL, Bang YJ, Camidge DR, et al. Anaplastic lymphoma kinase inhibition in non-small cell lung cancer[J]. N Engl J Med, 2010, 363 (18) : 1693–703. DOI:10.1056/NEJMoa1006448 |
| [4] | Maemondo M, Inoue A, Kobayashi K, et al. Gefitinib or chemotherapy for non-small-cell lung cancer with mutated EGFR[J]. N Engl J Med, 2010, 362 (25) : 2380–8. DOI:10.1056/NEJMoa0909530 |
| [5] | Pardoll D. Does the immune system see tumors as foreign or self?[J]. Annu Rev Immunol, 2003, 21 : 807–39. DOI:10.1146/annurev.immunol.21.120601.141135 |
| [6] | Ribas A, Butterfield LH, Glaspy JA, et al. Current developments in cancer vaccines and cellular immunotherapy[J]. J Clin Oncol, 2003, 21 (12) : 2415–32. DOI:10.1200/JCO.2003.06.041 |
| [7] | Zou W. Immunosuppressive networks in the tumour environment and their therapeutic relevance[J]. Nat Rev Cancer, 2005, 5 (4) : 263–74. DOI:10.1038/nrc1586 |
| [8] | Decoster L, Wauters I, Vansteenkiste JF. Vaccination therapy for non-small-cell lung cancer: review of agents in phase Ⅲdevelopment[J]. Ann Oncol, 2012, 23 (6) : 1387–93. DOI:10.1093/annonc/mdr564 |
| [9] | Gure AO, Chua R, Williamson B, et al. Cancer-testis genes are coordinately expressed and are markers of poor outcome in non-small-cell lung cancer[J]. Clin Cancer Res, 2005, 11 (22) : 8055–62. DOI:10.1158/1078-0432.CCR-05-1203 |
| [10] | Liu QL, Zhang CQ, Ma KT. Expression of MAGE-3 gene product in non-small cell lung cancer[J]. Zhonghua Zhong Liu Za Zhi, 2000, 22 (2) : 138–40. [ 刘庆伦, 张昌卿, 马凯涛. 非小细胞肺癌MAGE-3基因产物的表达[J]. 中华肿瘤杂志, 2000, 22 (2) : 138–40. ] |
| [11] | Vansteenkiste J, Zielinski M, Linder A, et al. Adjuvant MAGE-A3 immunotherapy in resected non-small-cell lung cancer: phase Ⅱ randomized study results[J]. J Clin Oncol, 2013, 31 (19) : 2396–403. DOI:10.1200/JCO.2012.43.7103 |
| [12] | Ulloa-Montoya F, Louahed J, Dizier B, et al. Predictive gene signaturein MAGEA3 antigen-specific cancer immunotherapy[J]. J Clin Oncol, 2013, 31 (19) : 2388–95. DOI:10.1200/JCO.2012.44.3762 |
| [13] | Vansteenkiste JF, C ho, B, Vanakesa, T, et al. MAGRIT, a double blind, randomized, placebo-controlled phase Ⅲ study to assess the efficacy of the recMAGE-A3+ AS15 cancer immunotherapeutic as adjuvant therapy in patients with resected MAGE-A3-positive non-small cell lung cancer (NSCLC)[J]. Ann Oncol, 2014, 25 (Suppl 4) : iv409–16. |
| [14] | Vlad AM, Kettel JC, Alajez NM, et al. MUC1 immunobiology: from discovery to clinical applications[J]. Adv Immunol, 2004, 82 : 249–93. DOI:10.1016/S0065-2776(04)82006-6 |
| [15] | Ramlau R, Quoix E, Rolski J, et al. A phase Ⅱ study of TG4010 (Mva-Muc1-Il2) in association with chemotherapy in patients with stage Ⅲ/Ⅳ non-small-cell lung cancer[J]. J Thorac Oncol, 2008, 3 (7) : 735–44. DOI:10.1097/JTO.0b013e31817c6b4f |
| [16] | Agrawal B, Krantz MJ, Reddish MA, et al. Cancer-associated MUC1 mucin inhibits human T-cell proliferation, which is reversible by IL-2[J]. Nat Med, 1998, 4 (1) : 43–9. DOI:10.1038/nm0198-043 |
| [17] | Quoix E, Ramlau R, Westeel V, et al. Therapeutic vaccination with TG4010 and first-line chemotherapy in advanced non-small-cell lung cancer: a controlled phase 2B trial[J]. Lancet Oncol, 2011, 12 (12) : 1125–33. DOI:10.1016/S1470-2045(11)70259-5 |
| [18] | Rodríguez PC, Rodríguez G, González G, et al. Clinical development and perspectives of CIMAvax EGF, Cuban vaccine for non-small-cell lung cancer therapy[J]. MEDICC Rev, 2010, 12 (1) : 17–23. |
| [19] | García B, Neninger E, de la Torre A, et al. Effective inhibition of the epidermal growth factor/epidermal growth factor receptor binding by antiepidermal growth factor antibodies is related to better survival in advanced non-small-cell lung cancer patients treated with the epidermal growth factor cancer vaccine[J]. Clin Cancer Res, 2008, 14 (3) : 840–6. DOI:10.1158/1078-0432.CCR-07-1050 |
| [20] | Neninger Vinageras E, de la Torre A, Osorio Rodríguez M, et al. Phase Ⅱ randomized controlled trial of an epidermal growth factor vaccine in advanced non-small-cell lung cancer[J]. J Clin Oncol, 2008, 26 (9) : 1452–8. DOI:10.1200/JCO.2007.11.5980 |
| [21] | Sangha R, Butts C. L-BLP25: a peptide vaccine strategy in non-small-cell lung cancer[J]. Clin Cancer Res, 2007, 13 (15Pt 2) : 4652s–4. |
| [22] | Butts C, Murray N, Maksymiuk A, et al. Randomized phase ⅡB trial of BLP25 liposome vaccine in stage ⅢB and Ⅳ non-small-cell lung cancer[J]. J Clin Oncol, 2005, 23 (27) : 6674–81. DOI:10.1200/JCO.2005.13.011 |
| [23] | Butts CA, Socinski MA, Mitchell P, et al. Tecemotide (L-BLP25) versus placebo after chemoradiotherapy for stage Ⅲ non-small-cell lung cancer (START): a randomised, double-blind, phase 3 trial[J]. Lancet Oncol, 2014, 15 (1) : 59–68. DOI:10.1016/S1470-2045(13)70510-2 |
| [24] | Kakimi K, Isobe M, Uenaka A, et al. A phase Ⅰ study of vaccination with NYESO-1f peptide mixed with Picibanil OK-432 and Montanide ISA-51 in patients with cancers expressing the NY-ESO-1 antigen[J]. Int J Cancer, 2011, 129 (12) : 2836–46. DOI:10.1002/ijc.25955 |
| [25] | Eikawa S, Kakimi K, Isobe M, et al. Induction of CD8 T-cell responses restricted to multiple HLA class Ⅰ alleles in a cancer patient by immunization with a 20-mer NY-ESO-1f (NY-ESO-1 91-110) peptide[J]. Int J Cancer, 2013, 132 (2) : 345–54. DOI:10.1002/ijc.27682 |
| [26] | Wada H, Isobe M, Kakimi K, et al. Vaccination with NY-ESO-1 overlapping peptides mixed with picibanil OK-432 and Montanide ISA-51 in patients with cancers expressing the NY-ESO-1 antigen[J]. J Immunother, 2014, 37 (2) : 84–92. DOI:10.1097/CJI.0000000000000017 |
| [27] | Malykh YN, Schauer R, Shaw L. N-Glycolylneuraminic acid in human tumours[J]. Biochimie, 2001, 83 (7) : 623–34. DOI:10.1016/S0300-9084(01)01303-7 |
| [28] | Vázquez AM1, Hernández AM, Macías A, et al. Racotumomab: an anti-idiotype vaccine related to N-glycolyl-containing gangliosides-preclinical and clinical data[J]. Front Oncol, 2012, 2 : 150. |
| [29] | Neninger E, Díaz RM, de la Torre A, et al. Active immunotherapy with IE10 anti-idiotype vaccine in patients with small cell lung cancer: report of a phase Ⅰ trial[J]. Cancer Biol Ther, 2007, 6 (2) : 145–50. DOI:10.4161/cbt.6.2.3574 |
| [30] | Alfonso S, Valdés-Zayas A, Santiesteban ER, et al. A randomized, multicenter, placebo-controlled clinical trial of racotumomab-alum vaccine as switch maintenance therapy in advanced non-small cell lung cancer patients[J]. Clin Cancer Res, 2014, 20 (14) : 3660–71. DOI:10.1158/1078-0432.CCR-13-1674 |
| [31] | Nemunaitis J, Dillman RO, Schwarzenberger PO, et al. Phase Ⅱstudy of belagenpumatucel-L, a transforming growth factor beta-2 antisense gene-modified allogeneic tumor cell vaccine in non-small-cell lung cancer[J]. J Clin Oncol, 2006, 24 (2) : 4721–30. |
| [32] | Nemunaitis J, Murray N. Immune-modulating vaccines in non-small-cell lung cancer[J]. J Thorac Oncol, 2006, 1 (7) : 756–61. |
| [33] | Giaccone G, Bazhenova LA, Nemunaitis J, et al. A phase Ⅲ study of belagenpumatucel-L, an allogeneic tumour cell vaccine, as maintenance therapy for non-small cell lung cancer[J]. Eur J Cancer, 2015, 51 (16) : 2321–9. DOI:10.1016/j.ejca.2015.07.035 |
| [34] | Tuyaerts S, Aerts JL, Corthals J, et al. Current approaches in dendritic cell generation and future implications for cancer immunotherapy[J]. Cancer Immunol Immunother, 2007, 56 (10) : 1513–37. DOI:10.1007/s00262-007-0334-z |
| [35] | Chiappori AA, Soliman H, Janssen WE, et al. INGN-225: a dendritic cell-based p53 vaccine (Ad.p53-DC) in small cell lung cancer: observed association between immune response and enhanced chemotherapy effect[J]. Expert Opin Biol Ther, 2010, 10 (6) : 983–91. DOI:10.1517/14712598.2010.484801 |
| [36] | Um SJ, Choi YJ, Shin HJ, et al. Phase Ⅰ study of autologous dendritic cell tumor vaccine in patients with non-small cell lung cancer[J]. Lung Cancer, 2010, 70 (2) : 188–94. DOI:10.1016/j.lungcan.2010.02.006 |
| [37] | Nemunaitis J, Sterman D, Jablons D, et al. Granulocyte-macrophage colony-stimulating factor gene-modified autologous tumor vaccines in non-small-cell lung cancer[J]. J Natl Cancer Inst, 2004, 96 (2) : 326–31. |
| [38] | Nemunaitis J, Jahan T, Ross H, et al. Phase 1/2 trial of autologous tumor mixed with an allogeneic GVAX vaccine in advanced-stage non-small-cell lung cancer[J]. Cancer Gene Therapy, 2006, 13 (6) : 555–62. DOI:10.1038/sj.cgt.7700922 |
| [39] | Dessureault S, Alsarraj M, McCarthy S, et al. A GMCSF/CD40L producing cell augments anti-tumor T cell responses[J]. J Surg Res, 2005, 125 (2) : 173–81. DOI:10.1016/j.jss.2004.11.036 |
| [40] | Creelan BC, Antonia S, Noyes D, et al. Phase Ⅱ trial of a GM-CSF-producing and CD40L-expressing bystander cell line combined with an allogeneic tumor cell-based vaccine for refractory lung adenocarcinoma[J]. J Immunother, 2013, 36 (8) : 442–50. DOI:10.1097/CJI.0b013e3182a80237 |
| [41] | Sharma S, Yang SC, Hillinger S, et al. CCL21-mediated anti-tumor responses require IFN gamma, MIG/CXCL9 and IP-10/CXCL10[J]. Mol Cancer, 2003, 2 : 22. DOI:10.1186/1476-4598-2-22 |
| [42] | Takano A, Nakamura Y, Daigo Y. Characterization of a lung cancer growth factor, LASEP3 as a serological and prognostic biomarker and therapeutic target[J]. Ann Oncol, 2013, 24 (suppl 9) : ix31–65. |
| [43] | Postow MA, Callahan MK, Barker CA, et al. Immunologic correlates of the abscopal effect in a patient with melanoma[J]. N Engl J Med, 2012, 366 (10) : 925–31. DOI:10.1056/NEJMoa1112824 |
| [44] | Hiniker SM, Chen DS, Reddy S, et al. A systemic complete response of metastatic melanoma to local radiation and immunotherapy[J]. Transl Oncol, 2012, 5 (6) : 404–7. DOI:10.1593/tlo.12280 |
| [45] | Golden EB, Demaria S, Schiff PB, et al. An abscopal response to radiation and ipilimumab in a patient with metastatic non-small cell lung cancer[J]. Cancer Immunol Res, 2013, 1 (6) : 365–72. DOI:10.1158/2326-6066.CIR-13-0115 |
| [46] | Harper J, Sainson RC. Regulation of the anti-tumor immune response by cancer-associated fibroblasts[J]. Semin Cancer Biol, 2014, 25 : 69–77. DOI:10.1016/j.semcancer.2013.12.005 |
 2016, Vol. 43
2016, Vol. 43