文章信息
- 外周血PTEN、RASSF1A甲基化及其mRNA表达与结节性甲状腺疾病的关系
- Relationship of Methylation Status and mRNA Expression of PTEN, RASSF1A in Peripheral Blood with Thyroid Nodule Disease
- 肿瘤防治研究, 2016, 43(7): 577-581
- Cancer Research on Prevention and Treatment, 2016, 43(7): 577-581
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2016.07.007
- 收稿日期: 2015-12-30
- 修回日期: 2016-04-18
2. 014010 包头,内蒙古科技大学包头医学院第一附属医院中心实验室;
3. 现单位:014010 包头,内蒙古包钢医院核医学科;
4. 现单位:201400 上海,上海市奉贤区奉城医院内分泌科
2. Department of Centrallab, The First Affiliated Hospital of Baotou Medical College, Inner Mongolia University of Science & Technology, Baotou 014010, China;
3. Present: Department of Nuclear Medicine, Bao Gang Hospital of Inner Mongolia, Baotou 014010, China;
4. Present: Department of Endocrinology, Shanghai Feng Xian District Feng Cheng Hospital, 201400 Shanghai, China
研究显示,基因异常表达及功能失调可导致遗传和表观遗传调控紊乱引起肿瘤的发生、发展。表观遗传学主要包括:DNA甲基化、组蛋白修饰、染色质重塑、随机染色体失活等[1-2]。细胞癌变过程中,最常见的表观遗传学改变是DNA甲基化,包括原癌基因启动子区的去甲基化和抑癌基因启动子区过度甲基化[3]。国内外关于甲状腺恶性肿瘤组织中的PTEN(phosphatase and tension homolog deleted on chromosome ten)、RASSF1A(ras association domain farmily 1A)基因启动子甲基化水平的研究已有报道,而关于结节性甲状腺疾病外周血中的检测少有报道。本研究采用甲基化特异性PCR(methylation specific PCR, MSP)和反转录—多聚酶链反应(reverse transcription polymerase chain reaction, RT-PCR)法,对结节性甲状腺疾病外周血进行研究,探讨PTEN、RASSF1A基因启动子甲基化及mRNA表达与结节性甲状腺疾病之间的关系。
1 资料与方法 1.1 研究对象收集2007—2011年间内蒙古科技大学包头医学院第一附属医院就诊的104例结节性甲状腺疾病患者的新鲜外周血。其中甲状腺腺瘤34例(腺瘤组),男16例,女18例,年龄16~69岁,中位年龄39岁;结节性甲状腺肿46例(结甲组),男18例,女28例,年龄23~71岁,中位年龄42岁;乳头状甲状腺癌(papillary thyroid carcinoma, PTC)24例(甲癌组),男13例,女11例,年龄13~68岁,中位年龄46岁;其中有颈部淋巴结转移者9例,以上病例均经病理证实。另外选取来自包头地区健康体检者30例作为对照组,男女各15例,年龄21~52岁,中位年龄40岁。
1.2 实验方法 1.2.1 外周血DNA提取受检者留取清晨空腹静脉抗凝血4 ml,其中2 ml用于抽提基因组DNA,另外2 ml用于外周血淋巴细胞分离。使用北京TIANGEN公司的血液基因组DNA提取试剂盒DP-318,提取基因DNA。
1.2.2 DNA甲基化修饰用EZ DNA Methylation-Gold Kit3甲基化试剂盒(美国ZYMO RESEARCH公司)按说明对提取的DNA进行亚硫酸氢钠处理和纯化,-20℃冰箱保存备用。
1.2.3 甲基化特异性PCR (MSP)扩增PTEN、RASSF1A甲基化引物与非甲基化引物序列参照文献[4-5],见表 1,引物由Invitrogen公司合成。PTEN、RASSF1A PCR反应体系均25μl,上下游引物均各为0.5μl,甲基化修饰后的DNA均为1μl。PTEN PCR扩增条件: 95℃预变性5 min,95℃45 s、57℃30 s、72℃30 s、33循环,72℃延伸10 min。RASSF1A PCR扩增条件:95℃预变性10 min,95℃30 s、60℃30 s、72℃30 s、35循环,72℃延伸5 min。用2%琼脂糖凝胶电泳进行检测。
TRIzol一步法提取细胞总RNA,用琼脂糖凝胶电泳检查总RNA的完整性。以提取的总RNA为模板,按照反转录试剂盒M-MLV RT提取试剂盒(美国Invitrogen公司)说明书进行cDNA合成。
1.2.5 RT-PCR法检测PTEN、RASSF1A基因引物序列参照文献[5-6],见表 1。引物由美国Invitrogen公司合成。PTEN、RASSF1A的反应体系均为25μl, 上下游引物均各为1.0μl,cDNA均为5.0μl。PTEN PCR扩增条件:94℃预变性3 min,94℃30 s、54℃30 s、72℃45 s、共33循环,72℃延伸10 min。RASSF1A PCR扩增条件:93℃预变性5 min,92℃45 s、60℃45 s、72℃45 s、共35循环,72℃延伸10 min。以β-actin作PCR体系内参照。用2%琼脂糖凝胶电泳检测。
1.3 统计学方法采用SPSS17.0统计学软件进行数据处理,采用四格表资料的卡方检验和精确检验,分析实验组与对照组间PTEN、RASSF1A基因甲基化差别及mRNA的表达情况,以P < 0.05为差异有统计学意义。
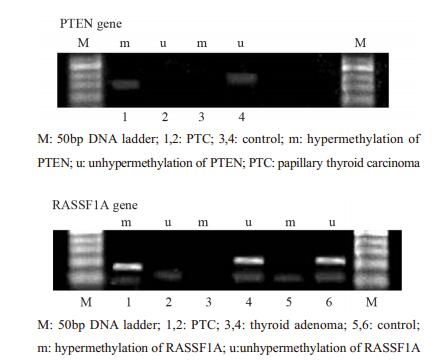
2 结果 2.1 PTEN、RASSF1A基因启动子区甲基化与结节性甲状腺疾病关系分析PTEN、RASSF1A甲基化率在甲癌组中分别为33.3%、45.8%;腺瘤组中为17.6%、20.5%;结甲组中为10.8%、13.0%。甲癌组PTEN、RASSF1A甲基化率明显高于其他两组。腺瘤组和甲癌组中PTEN、RASSF1A甲基化率分别与对照组比较, 差异均有统计学意义(均P < 0.05)。结甲组与对照组差异无统计学意义,见图 1。
|
| 图 1 结节性甲状腺疾病患者PTEN、RASSF1A基因启动子区甲基化电泳结果 Figure 1 MSP of PTEN, RASSF1A gene promoter of thyroid nodule disease |
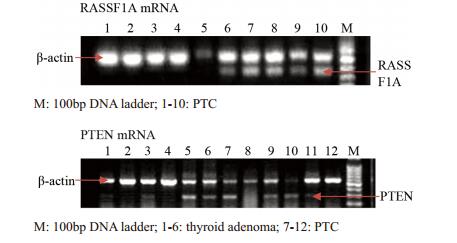
PTEN、RASSF1A基因mRNA表达阳性率在甲癌组中分别为54.2%、45.8%;腺瘤组中为73.6%、79.6%;结甲组中为89.2%、87.0%。甲癌组PTEN、RASSF1A基因mRNA表达阳性率明显低于其他两组。腺瘤组和甲癌组中PTEN、RASSF1A基因mRNA表达阳性率分别与对照组比较,差异均有统计学意义(均P < 0.05)。结甲组与对照组差异无统计学意义,见图 2。
|
| 图 2 结节性甲状腺疾病患者PTEN、RASSF1A mRNA表达结果 Figure 2 RT-PCR analysis of PTEN, RASSF1A mRNA of thyroid nodule disease |
在未检测到PTEN mRNA转录产物的样本中发现甲癌组中PTEN、RASSF1A甲基化率明显高于其他两组,腺瘤组和甲癌组分别与对照组比较,差异均有统计学意义(均P < 0.05)。结甲组与对照组差异无统计学意义,见表 2。
 |
PTEN和RASSF1A基因甲基化率与甲状腺癌患者淋巴结转移有关(均P < 0.05),与年龄、结节大小、性别无关(均P > 0.05),见表 3。
 |
PTEN和RASSF1A基因mRNA表达与甲状腺癌淋巴结转移有关(均P < 0.05),与年龄、性别、结节大小均无关(均P > 0.05),见表 4。
 |
DNA甲基化是生物体在DNA甲基转移酶(DNMTs)的作用下,以s-腺苷甲硫氨酸为甲基供体,将甲基转移到特定碱基上的过程。不同类型肿瘤中由于存在抑癌基因DNA启动子区频繁发生甲基化并导致其基因沉默的现象,而一些重要抑癌基因启动子区CpG岛高甲基化与肿瘤发生、发展的关系尤为重要[7-8]。
DNA甲基化修饰异常通常发生在肿瘤细胞上且该细胞能够被释放进入血液系统,所以血液可作为有应用前景的癌症特异性诊断工具。国内学者利用甲基化芯片检测甲状腺癌全血标本发现,血液中甲基化修饰异常的基因与甲状腺癌的发生发展有关[9]。且有报道显示不同程度的DNA甲基化水平可以鉴别甲状腺肿瘤的腺瘤和腺癌[10]。
PTEN是迄今为止发现的第一个具有双重磷酸酶活性的抑癌基因。通过调控磷酸化作用参与细胞周期的调节,在细胞的生长、增殖、黏附、迁移等方面起着重要的抗肿瘤作用。研究显示PTEN在人类多种肿瘤中发现高甲基化和基因功能失活。Alvarez-Nu?ez等[11]用MSP法在53例原发性甲状腺癌中发现52%PTEN高甲基化改变,提示PTEN启动子甲基化在甲状腺癌的发生过程中起着较大作用。殷德涛等[12]采用同样方法检测80例甲状腺乳头状癌(papillary thyroid carcinoma, PTC),25%出现甲基化,且其甲基化状态与TNM分期、病理分级及淋巴转移有关。Xing等[13]也有相同报道。
本研究结果显示甲癌组、腺瘤组分别与对照组比较差异均有统计学意义,PTEN甲基化率在甲癌组中高于腺瘤组,与Hou等[14]报道一致。结甲组PTEN甲基化率与对照组比较差异无统计学意义,提示PTEN甲基化在甲状腺癌、甲状腺腺瘤等甲状腺肿瘤中起着重要作用。另外用RT-PCR法检测发现甲癌组PTEN mRNA表达阳性率低于腺瘤组及结甲组,提示在甲状腺肿瘤的形成过程中PTEN基因高甲基化及其mRNA表达减低,且随着甲状腺肿瘤恶性程度增高,其PTEN基因甲基化逐渐增高进而抑制其mRNA转录。
在未检测到PTEN mRNA转录产物的样本中发现PTEN不同程度的甲基化改变,甲癌组、腺瘤组的甲基化率明显高于结甲组。结果表明PTEN基因启动子区CPG岛高甲基化可能抑制、下调其转录及表达,进而表达产物PTEN蛋白的减少甚至缺失,导致该基因功能失活,从而促使PTEN在甲状腺乳头状癌形成过程中抑制细胞增生、转移,促使凋亡的作用减少。国内学者认为PTEN蛋白低表达是甲状腺乳头状癌的发生、转移的重要分子机制之一,其低表达与基因启动子区过度甲基化有关[15]。PTEN基因失活原因包括PTEN基因突变、缺失及CPG岛高甲基化,有学者研究PTC的基因表达方式中发现,其可能的致癌机制包括H4/PTEN基因重排导致重组后PTEN基因失活和癌基因的激活等,而Wang等[16]研究了125例中国PTC患者, 只有9.6%的PTC患者中存在H4/PTEN基因重排。Bruni等[17]检查26例甲状腺肿瘤标本及8例细胞系,仅发现1例PTEN基因点突变。因此PTEN CPG岛高甲基化是导致其基因失活的重要原因。
RASSF1A是一种重要的肿瘤抑制基因,该基因是继p16基因以来发现的在肿瘤中甲基化程度最高、最普遍的基因之一。RASSF1A启动子区CpG岛的高甲基化而表达缺失已在广泛肿瘤谱中被发现[18]。Xing等[19]研究发现在甲状腺癌FTC、PTC中RASSF1A甲基化率均有不同程度增高,而FTC增高尤为显著,同时在甲状腺腺瘤发现增高,因此他们认为异常甲基化导致RASSF1A失活是甲状腺肿瘤发生的早期事件之一。Schagdarsurengin等[5]认为随甲状腺癌恶性程度越高RASSF1A甲基化率越高。本研究显示腺瘤组、甲状腺癌组RASSF1A甲基化率明显增高,甲状腺恶性肿瘤的甲基化程度高于甲状腺良性肿瘤,且两者之间差异有统计学意义。提示RASSF1A基因启动子区甲基化是甲状腺肿瘤中常见的分子生物学事件,腺瘤组RASSF1A基因高甲基化与对照组比较差异有统计学意义,说明在甲状腺肿瘤发生的早期即出现RASSF1A基因启动子区甲基化改变。我们用RT-PCR检测RASSF1A mRNA表达阳性率,发现甲癌组低于腺瘤组及结甲组,在甲状腺肿瘤中存在RASSF1A基因功能缺失。
通过对DNA甲基化模式的研究,人们发现肿瘤细胞中存在异常的DNA甲基化状态:基因组整体甲基化水平降低;组织特异性基因的启动子区域出现从头甲基化;癌基因多为不充分甲基化;抑癌基因过度甲基化,从而表达受抑制。本研究显示甲癌组中未检测到RASSF1A mRNA转录产物的样本中存在RASSF1A过度甲基化。抑癌基因启动子或其附近区域的DNA甲基化将直接阻碍转录因子与启动子结合,从而使基因不能转录或转录水平降低[15]。因此RASSF1A基因高甲基化改变有可能是导致其基因沉默的原因之一。很多实验已证实在人类多种恶性肿瘤中存在RASSF1A表达缺失,这与RASSF1A基因启动子CpG岛高甲基化引起RASSF1A基因转录缺失有关[20]。国外学者证实用DNA甲基化抑制剂处理基因表达缺失的细胞后,基因表达被重新激活[5]。因此RASSF1A高甲基化能致RASSF1A基因的转录失活,这种表遗传的失活是甲状腺肿瘤发生中的一个早期步骤。
本研究中PTEN、RASSF1A基因甲基化率及mRNA表达与淋巴结转移有关,差异均有统计学意义,结果显示PTEN和RASSF1A基因启动子甲基化及其表达减低甚至沉默可能会影响甲状腺癌的预后。在对甲癌组的临床指标进行分析时发现PTEN、RASSF1A基因甲基化率与年龄、性别、甲状腺结节大小没有明显相关。
近几年研究显示国内甲状腺癌发病率和病死率呈上升趋势,女性明显高于男性,乳头状甲状腺癌是美国女性发病率增长最快的恶性肿瘤[21-22]。早期发现甲状腺肿瘤分子标志物对于诊断及预后有重要影响。本研究结果显示PTEN和RASSF1A基因启动子区在甲状腺肿瘤中存在高甲基化及其mRNA存在表达减低甚至缺失,PTEN和RASSF1A基因启动子区高甲基化可能是导致其基因沉默的原因之一。另外外周血采样简便,患者易于接受,方便复查和随访,为甲状腺结节良恶性鉴别、早期分子诊断、预后监测和靶基因治疗提供客观依据,有助于加深对甲状腺肿瘤发生发展的认识,拓宽甲状腺肿瘤研究的视野。
| [1] | Stsrk LA. Epigentics online: multimedia teaching resources[J]. CBE Life Sci Educ, 2010, 9 (1) : 6–9. |
| [2] | Sharma S, Kelly TK, Jones PA. Epigenetics in cancer[J]. Carcinogenesis, 2010, 31 (1) : 27–36. |
| [3] | Song XY, Shang XL, Zhang YT. DNA Methylation in Thyroid Carcinoma[J]. Lin Chuang Er Bi Yan Hou Tou Jing Wai Ke Za Zhi, 2015, 29 (6) : 573–6. [宋现运, 尚小领, 张玉妥. DNA甲基化在甲状腺肿瘤中的研究进展[J]. 临床耳鼻咽喉头颈外科杂志,2015, 29 (6) : 573–6. ] |
| [4] | Goel A, Arnold CN, Niedzwiecki D, et al. Frequent inactivation of PTEN by promoter hypermethylation in microsatellite instability-High Sporadic Colorectal Cancers[J]. Cancer Res, 2004, 64 (9) : 3014–21. |
| [5] | Schagdarsurengin U, Gimm O, Hoang-Vu C, et al. Frequent epigenetic silencing of the CpG island promoter of RASSF1A in thyroid carcinoma[J]. Cancer Res, 2002, 62 (13) : 3698–701. |
| [6] | Tell G, Pines A, Arturi F, et al. Control of phosphatase and tensin homolog (PTEN) gene expression in normal and thyroid cells[J]. Endocrinology, 2004, 145 (10) : 4660–6. |
| [7] | Ho DH, Burggren WW. Epigenetics and transgenerational transfer: a physiological perspective[J]. J Exp Biol, 2010, 213 (1) : 3–16. |
| [8] | Aleqria-Toms JA, Baccarelli A, Bollati V. Epigenetics and lifestyle[J]. Epigenetics, 2011, 3 (3) : 267–77. |
| [9] | Liao P, Liu CZ, Luo QY, et al. Blood DNA Methylation Markers for Thyroid Cancer[J]. Huan Jing Yu Zhi Ye Yi Xue, 2012, 29 (2) : 77–82. [廖萍, 刘茶珍, 罗全勇, 等. 甲状腺癌患者血DNA甲基化分子标志物[J]. 环境与职业医学,2012, 29 (2) : 77–82. ] |
| [10] | Zeng ZP. Carry out Epigenetic research in endocrine and metabolic disease and adrenal tumors[J]. Zhonghua Nei Fen Mi Dai Xie Za Zhi, 2010, 26 (8) : 629–32. [曾正陪. 开展内分泌代谢疾病及肾上腺肿瘤的表观遗传学研究[J]. 中华内分泌代谢杂志,2010, 26 (8) : 629–32. ] |
| [11] | Alvarez-Nuñez F, Bussaglia E, Mauricio D, et al. PTEN promoter methylation in sporadic thyroid carcinomas[J]. Thyroid, 2006, 16 (1) : 17–23. |
| [12] | Yin DT, Yin FY, Zheng LY, et al. Promoter rmethylation and Protein Expression of the PTEN Gene in Papillary Thyroid Carcinoma and their correlation[J]. Zhonghua Er Bi Yan Hou Tou Jing Wai Ke Za Zhi, 2010, 45 (4) : 330–3. [殷德涛, 尹峰燕, 郑立运, 等. 甲状腺乳头状癌中PTEN基因启动子甲基化及其蛋白表达的相关性[J]. 中华耳鼻咽喉头颈外科杂志,2010, 45 (4) : 330–3. ] |
| [13] | Xing M. Gene Methylation in thyroid tumorigenesis[J]. Endocrinology, 2007, 148 (3) : 948–53. |
| [14] | Hou P, Ji M, Xing M. Association of PTEN Gene Methylation With Genetic Alterations in the Phosphatidylinositol 3-Kinase/AKT Signaling Pathway in Thyroid Tumors[J]. Cancer, 2008, 113 (9) : 2440–7. |
| [15] | Qian GY, Liang Y, Yang LJ, et al. Protein Expression and Promoter Methylation of the PTEN Gene in Papillary Thyroid Carcinoma[J]. Yi Xue Yan Jiu Za Zhi, 2011, 40 (3) : 39–43. [钱光煜, 梁勇, 杨林军, 等. PTEN异常表达及甲基化与PTC的关系[J]. 医学研究杂志,2011, 40 (3) : 39–43. ] |
| [16] | Wang YL, Wang JC, Wu Y, et al. Incidentally simultaneous occurrence of RET/ PTC, H4-PT EN and BRAF mutation in papillary thyroid carcinoma[J]. Cancer Lett, 2008, 263 (1) : 44–52. |
| [17] | Bruni P, Boccia A, Baldassarre G, et al. PTEN expressionis reduced in a subset of sporadic thyroid carcinomas:evidence that PTEN growth suppressing activity in thyroid cancer cells mediated by p27kip1[J]. Oncogene, 2000, 19 (28) : 3146–55. |
| [18] | Bi J, Gao MY, Wang YF. Promoter rmethylation of the Ras association domain family in carcinoma[J/CD]. Zhonghua Lin Chuang Yi Shi Za Zhi(Dian Zi Ban), 2012, 6(16): 4835-8. [毕婧, 高明阳, 王衍富. Ras相关区域家族基因启动子甲基化改变与肿瘤发生相关性的研究进展[J/CD].中华临床医师杂志(电子版), 2012, 6(16): 4835-8.] |
| [19] | Xing M, Cohen Y, Mambo E, et al. Early occurrence of RASSF1A hypermethylation and its mutual exclusion with BRAF mutation in thyroid tumorigenesis[J]. Cancer Res, 2004, 64 (5) : l664–8. |
| [20] | Stutterneim J, Ichou FA, den Ouden E, et al. Methylated RASSF1A is the first specific DNA marker for minimal residual disease testing in neuroblastoma[J]. Clin Cancer Res, 2012, 18 (3) : 808–14. |
| [21] | Sun JW, Xu XJ, Cai QM, et al. Epidemiological Study on Thyroid Cancer in China[J]. Zhongguo Zhong Liu, 2013, 22 (9) : 690–3. [孙嘉伟, 许晓君, 蔡秋茂, 等. 中国甲状腺癌发病趋势分析[J]. 中国肿瘤,2013, 22 (9) : 690–3. ] |
| [22] | Xing M, Haugen BR, Schlumberger M. Progress in molecular-based management of differentiated thyroid cancer[J]. Lancet, 2013, 381 (9871) : 1058–69. |
 2016, Vol. 43
2016, Vol. 43

 ,
,

