文章信息
- 不同应激原诱导肝癌SMMC-7721细胞应激反应中相关基因的筛选
- Screening of Genes Involved in Hepatoma Cells SMMC-7721 Stress Response Induced by Different Stressors
- 肿瘤防治研究, 2016, 43(6): 463-467
- Cancer Research on Prevention and Treatment, 2016, 43(6): 463-467
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2016.06.006
- 收稿日期: 2015-10-23
- 修回日期: 2015-11-30
肝癌细胞抵御应激而恶性增殖是其难治的主要机制之一。研究表明,在各种应激因子,如低氧微环境、手术刺激、化疗药物治疗等作用下,肿瘤细胞能够通过调整一系列基因的表达抵御应激并保证其继续恶性增殖。
项目组前期研究结果表明,体外细胞培养中某些试剂(G418/氯化钙)作为应激原,会诱导肝癌SMMC-7721细胞处于不同的应激状态,除细胞增殖更加活跃以外,基因芯片检测及qRT-PCR检测均发现细胞中热休克蛋白家族、金属硫蛋白家族等一些已知应激基因高表达;将含MT2A(金属硫蛋白家族中表达量最大的基因)RNAi片段的质粒转染入SMMC-7721细胞后,发现细胞的增殖得到明显抑制[1];此时的肝癌细胞周期停滞在S期[2]。由此我们推测:某些应激相关基因群的高表达,可能对肝癌细胞抵御应激而恶性增殖具有一定积极意义。然而,是不是还有一些独特的参与细胞应激的基因尚不明了,为此本研究对不同应激原作用下肝癌SMMC-7721细胞基因的表达谱进行了芯片检测及分析,并结合各个基因的国内外研究进展,寻找那些在不同应激原作用下表达趋势具有一致性且与肿瘤应激反应密切相关的基因,初步筛选可能在肝癌细胞抵御应激反应中发挥关键作用的基因群,并通过qRT-PCR检测验证基因芯片结果。
1 材料和方法 1.1 材料 1.1.1 主要实验仪器垂直式无菌无尘操作台(中国造鑫企业有限公司)、二氧化碳培养箱(美国Thermo Fisher公司)、GeneAtlas™ System(美国Affymetrix Company)、ECO实时定量PCR系统(美国Illumina公司)。
1.1.2 主要实验试剂新生小牛血清(浙江天杭生物科技有限公司)、0.25%胰酶(上海吉泰生物)、双抗(上海吉泰生物)、G418粉剂(美国Invitrogen公司)、无水氯化钙(国药集团)、TRIzol(美国Invitrogen公司)。
1.1.3 细胞株人肝癌细胞系SMMC-7721为本实验室冻存的细胞,购自中科院上海细胞所。
1.2 方法 1.2.1 常规细胞复苏及培养细胞复苏及培养参照文献[3]。
1.2.2 G418和氯化钙母液的制备RPMI 1640培养液10 ml充分混匀溶解G418粉剂96 mg或氯化钙粉剂3.552 g,分别使用一次性注射器和直径为0.20 μm的滤膜抽滤灭菌,锡箔纸包裹后于4℃冰箱保存。
1.2.3 G418、氯化钙干预后SMMC7721肝癌细胞基因芯片表达谱检测 1.2.3.1 6 孔板铺板及用药人肝癌细胞SMMC-7721在含10%胎牛血清的RPMI 1640培养液中置于37℃、5%CO2的培养箱中培养,将对数生长期的细胞制成细胞悬液,以5×105个/孔的密度,接种于6孔板,放入培养箱中培养12 h,G418组:吸弃培养液,加入RPMI 1640培养液1.6 ml及25 μlG418(终浓度为0.3 mg/ml),加液完毕,轻轻水平移动混匀,放入培养箱,培养68 h,氯化钙组:吸弃培养液,加入RPMI 1640培养液1.6 ml及50 μl氯化钙(终浓度为0.1 mol/L),设置常规培养的肝癌细胞为阴性对照,继续培养4 h。
1.2.3.2 TRIzol一步法抽提各孔总RNA吸弃各孔培养液,每孔加入1 ml TRIzol,提取各组肝癌细胞的总RNA,RNeasy Mini Kit(美国天根公司)抽提和纯化以上各组RNA,RNA Nano LabChip检测RNA质量和定量。
1.2.3.3 Affymetrix Human Gene 1.1 ST Array Strip表达谱芯片检测采用Affymetrix Human Gene 1.1ST Array Strip表达谱芯片及Ambion WT ExpressionKit(含Control RNA)、GeneChip® WT TerminalLabeling Kit、GeneAtlas™ Hybridization,Wash,and Stain Kit、GeneChip R Poly-A RNA ControlKit、GeneChip Hybridization Control Kit等试剂盒,按Affymetrix具体操作手册说明,使用GeneAtlas基因芯片系统有关设备开展探针标记、质量检测、杂交、洗涤,以及扫描等检测工作,采用iterPlier法计算基因表达读数计算值,并进行统计学处理,观察与细胞应激反应相关的基因群的差异性表达特征。
1.2.4 芯片数据处理依据检测结果和Affymetrix所建议的方法,iterPlier计算核心基因表达读数计算值(芯片读数计算值),以常规培养的正常SMMC-7721细胞组的芯片读数为基准,G418组和氯化钙组分别与之比较,ratio以≥1.1倍为上调,≤0.91倍为下调,0.91~1.1倍为无显著变化。
1.2.5 PCR引物设计根据基因芯片分析结果选取进一步研究所需的目的基因,采用Primer3(v.0.4.0)在线软件设计PCR引物,Real-time Quantitative PCR内参以GAPDH为参照(GAPDH-F:5'-GAGTCAACGGATTTGGTCGT-3';GAPDH-R:5'-GATCTCGCTCCTGGAAGATG-3')。
1.2.6 G418、氯化钙干预后肝癌SMMC-7721细胞基因qRT-PCR检测铺6孔板,方法同上。72 h后,TRIzol一步法抽提各孔细胞总RNA,按照反转录试剂盒说明,常规反转录为cDNA,进而按照“SYBR Premix Ex Taq”试剂盒说明配制PCR反应混合物,使用ECO荧光定量PCR系统进行扩增,扩增产物进行凝胶电泳,最后采用ΔΔCT法分析目的基因的相对表达量,内参基因使用GAPDH。
1.3 统计学方法采用SPSS12.0统计软件进行数据统计分析。所有计量资料均采用(x±s)表示,多组样本间比较采用单因素方差分析。P<0.05为差异有统计学意义。
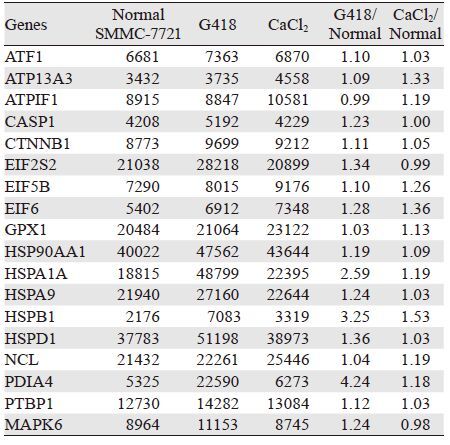
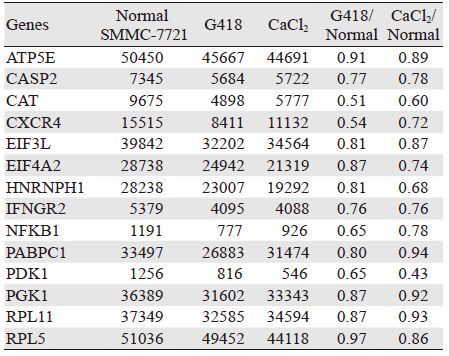
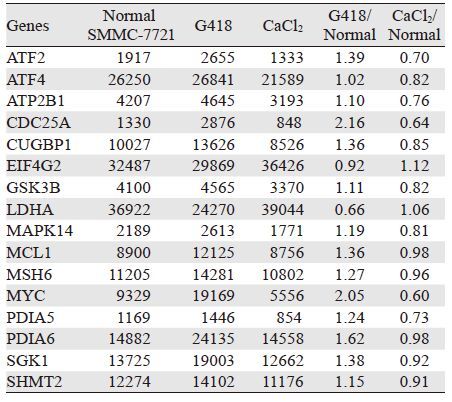
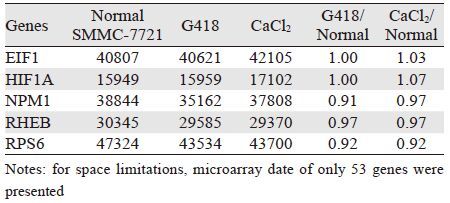
2 结果 2.1 基因芯片检测结果一共检测3张基因芯片,将均数校正至100,淘汰各组芯片读数计算值一致小于500者,共得到116个基因,结合各基因的文献研究,最终筛选出53个基因。其中,G418 0.3 mg/ml、氯化钙0.1 mol/L用药后表达一致上调者18个,见表 1;一致下调者14个,见表 2;互有上下调者16个,见表 3;无显著变化者5个,见表 4。
|
|
|
|
根据基因芯片的分析结果,通过qRT-PCR技术对筛选出的53个基因进行验证,结果显示,共有17个基因的结果与芯片结果完全吻合。其中,与正常的SMMC-7721细胞相比,5个基因在G418/CaCl2应激下,表现出显著的下调,余下的12个基因则表现出显著的上调,见表 5。
“细胞应激”是细胞对环境因素导致损伤的一种防御反应,目的是对抗伤害、修复损伤、增加对损伤的耐受性,以最终保护细胞;当难以抵御应激原,则通过诱导细胞死亡去除损伤后无法修复的细胞。研究发现,肿瘤的发生和发展与细胞应答各种应激的不同反应密切相关。譬如,长期性的病毒感染、负面精神情绪、不良生活行为等形成的慢性应激,往往促进肿瘤的发生[4-5];在实体瘤快速生长的过程中,由于肿瘤细胞增殖失控引起的大量氧气消耗及瘤内血管增长滞后,往往导致瘤内局部供氧不足,当氧浓度低于21%时,可激活各种各样的应激反应通路,诱导细胞出现自我保护、抗凋亡的表型[6]。
国内外研究陆续发现,在应激个体和对照组之间存在一些基因的差异表达[7],尤其是与细胞应激反应关系最为密切的关键基因表达都发生了显著的改变;不同的应激反应还会选择性地激发应激反应所必需的基因表达。缺氧应激常激活肿瘤细胞内HIFlα及其下游的血管内皮生成因子(VEGF)等、能量代谢因子(GIUT-1)等、细胞周期因子(cyclin-D1)等表达,促进瘤内新生血管的生成及肿瘤细胞的增殖[8];临床研究发现,患者体内高水平的HIF-lα往往预示着肿瘤侵袭性强而预后差。氧化应激常激活肿瘤细胞内谷胱甘肽(GSH)、谷胱甘肽过氧化物酶(GSH-Px)、超氧化物歧化酶(SODs)、金属硫蛋白(metallothioneins,MTs)等[9-10]。
本次基因芯片检测结果显示,在G418和氯化钙的刺激下,共有53个基因的表达量发生了显著变化;qRT-PCR验证中,共有17个基因与芯片结果完全一致。其中,除了研究较充分的与细胞应激相关的热休克家族以外,还包括与细胞生长、mRNA剪切、蛋白合成、凋亡等密切相关的基因等。
3.1 热休克蛋白家族(HSP90AA1、HSPA9、HSPA1A、HSPD1、HSPB1)HSPB1,编码热休克蛋白HSP27,研究表明,其参与了肿瘤细胞的氧化应激反应,过表达能增加肿瘤发生、转移及对化疗的抵御能力[11]。
HSP90AA1,编码热休克蛋白HSP90,在一种新型铜络合物2-24a/Cu治疗肿瘤的实验研究中发现,在2-24a/Cu能够诱导HeLa细胞发生氧化应激反应,且RNA-seq检测发现HSP90AA1的转录增强[12]。
HSPA1A和HSPA9,编码热休克蛋白HSP70,在硫链丝菌素削弱人类黑色素瘤细胞生存能力的研究中发现,硫链丝菌素用药早期能够诱导转移性黑色素瘤A375细胞出现蛋白毒性应激,并且大规模的上调包括HSPA1A在内的热休克蛋白家族成员[13]。
HSPD1,编码热休克蛋白HSP60。热休克蛋白是一种在进化上高度保守的蛋白质,广泛存在于各种生物体内,起“分子伴侣”的作用,面对各类应激原,HSPs和其他应激蛋白被大量合成以提高生物体对应激的耐受性,故又被称为应激蛋白。本次检测结果筛选到的热休克蛋白的5个编码基因中,在G418和氯化钙的作用下均出现上调,其中HSPB1上调趋势最明显,提示它们可能对肝癌细胞抵御应激反应起到一定促进作用。
3.2 促进肿瘤细胞生长、增殖、分化、侵袭的基因CTNNB1,编码β-环连蛋白,在许多肿瘤组织中都能检测到该基因的缺失或突变,CTNNB1突变导致的Wnt信号转导通路的异常激活被认为是恶性肿瘤发生的重要环节。咖啡酸苯乙酯(CAPE)通过减少氧化应激反应能够实现治疗胃癌的目的,在CAPE干预的两个胃癌细胞株23132/87中,均出现CTNNB1表达减少[14]。检测结果显示该基因表达略有上调,提示其可能对肝癌细胞抵御应激反应起到一定促进作用。
3.3 氧化应激相关基因CAT,编码过氧化氢酶,常参与肿瘤的氧化应激反应,在嗜铬细胞瘤PC12细胞中,在连翘酯苷能够保护细胞免受H2O2诱导的氧化应激,其抗氧化功能就体现在其能够提高抗氧化剂CAT的表达水平[15]。检测结果显示该基因表达一致下调,提示其抗氧化能力减弱。
3.4 蛋白质合成相关的基因RPL11,编码核糖体蛋白L11,在核糖体应激条件下,该基因上调后可通过激活P53基因、抑制myc基因的活性来抑制肿瘤细胞增殖[16]。该基因表达下调提示可能有助于肝癌细胞的增殖。
3.5 真核细胞翻译起始因子(EIF2S2、EIF5B、EIF6)真核细胞翻译起始因子是真核细胞蛋白质翻译所必需的、能够保证正确的mRNA-核糖体复合物形成的蛋白质。芯片所显示的这几个真核翻译起始因子从不同方面影响了翻译复合物的合成,是真核细胞翻译起始阶段的重要调控因子。然而,它们与肿瘤细胞应激反应之间的联系未见报道。本研究结果表明,EIF2S2、EIF5B、EIF6表达一致上调;表明应激可能会影响肝癌细胞中蛋白质的合成。
3.6 多聚腺苷酸结合蛋白(PABPC1)PABPC1,编码多聚腺苷酸结合蛋白1,它是一种能够与mRNA的Poly(A)尾结合的高度保守的蛋白质,通过这种结合方式参与mRNA的翻译并调节其稳定性。PABPC1是目前研究最为清楚的一类细胞质多聚腺苷酸结合蛋白。该基因与肿瘤的关系目前尚不清楚。PABPC1在G418作用下表达下调,提示G418可能影响了肝癌细胞mRNA的翻译。
3.7 与蛋白质的折叠相关的基因PDIA5编码蛋白质二硫键异构酶5,是一类在内质网中起作用的巯基-二硫键氧化还原酶。它通常含有CXXC(Cys-Xaa-Xaa-Cys,CXXC)活性位点,活性位点的两个半胱氨酸残基可催化底物二硫键的形成、异构及还原,主要职能是催化内质网中新生肽链的氧化折叠,另外在内质网相关的蛋白质降解途径(ERAD)、蛋白质转运、钙稳态、抗原提呈及病毒入侵等方面也起重要作用。在G418作用下,PDIA5的表达一致上调;在氯化钙应激下,PDIA5表达下调;提示G418能够有效地催化肝癌细胞内质网中新生肽链的折叠,而氯化钙的作用则可能相反。
3.8 促细胞凋亡的基因CASP1,编码半胱氨酸天冬氨酸特异性蛋白酶1,其参与的炎性反应及程序性细胞死亡能有效提高机体抵抗内源和外源各种刺激的能力,达到保护宿主的目的。然而它在肿瘤细胞应激反应中的作用,尚未见相关报道。检测结果显示在应激原作用下,CASP1表达一致上调。
3.9 干扰素γ受体(IFNGR2)IFNGR2,是Ⅱ型干扰素的受体,几乎在所有细胞中都有表达,其活化能够诱导肿瘤细胞凋亡。该基因表达一致下调,提示应激未能促进IFNGR2的活化。
3.10 与mRNA剪切相关的基因PTBP1,编码多嘧啶序列结合蛋白1,能够与mRNA前体结合从而对某些外显子选择性剪切以发挥负调控作用。在人乳腺癌MDA-MD-468细胞中,低浓度的H2O2能够选择性的下调PTBP1以调节RNA的剪切,从而诱导抗氧化剂sGC的表达[17]。检测结果显示该基因表达略上调,提示应激未对细胞内众多基因的剪切事件产生明显影响。
由此可知,在肝癌细胞SMMC-7721抵御应激而恶性增殖的过程中,有一系列基因群的表达发生了改变,揭示这些基因在肝癌细胞抵御应激反应过程中所扮演的角色,有助于加深对肝癌应激反应发生机制的认识,这对原发性肝癌的防治可能起到一定的积极作用。
| [1] | Wu ZH, Fang ZQ, Guan DY, et al. The down expression genes in rat liver cancer induced by DEN[J]. Zhong Liu Yan Jiu Yu Lin Chuang, 2006, 18 (9) : 580–4. [吴中华, 方肇勤, 管冬元, 等. 二乙基亚硝胺诱发大鼠肝癌组织下调的基因[J]. 肿瘤研究与临床,2006, 18 (9) : 580–4. ] |
| [2] | Fan M, Fang ZQ, Guan DY, et al. The expression of tumor metastasis related genes in rat's hepatocellular carcinoma and effect of several curing method[J]. Zhong Yi Yao Xue Bao, 2007, 35 (2) : 9–15. [范敏, 方肇勤, 管冬元, 等. 大鼠肝癌肿瘤转移相关基因的表达及不同中医治法作用[J]. 中医药学报,2007, 35 (2) : 9–15. ] |
| [3] | Xue SQ. Principles and techniques of cell culture in vitro[M]. Beijing: Scientific Publication, 2001 : 128 -35. [薛庆善. 体外培养的原理与技术[M]. 北京: 科学出版社, 2001 : 128 -35.] |
| [4] | Wang JY, Wang JJ, Zhang JQ. The impact of stress on the immune system and the development of tumors[J]. Lin Chuang Hui Cui, 2011, 26 (21) : 1925–8. [王继云, 王建军, 张俊权. 应激对免疫系统及对肿瘤发生发展的影响[J]. 临床荟萃,2011, 26 (21) : 1925–8. ] |
| [5] | Deng DH, Shen MH. The impact of chronic stress on the growth and metastasis of cancer[J]. Yi Xue Yan Jiu Za Zhi, 2013, 42 (4) : 305–7. [邓德厚, 沈敏鹤. 慢性应激对癌症生长及转移的影响[J]. 医学研究杂志,2013, 42 (4) : 305–7. ] |
| [6] | Crowder SW, Balikov DA, Hwang YS, et al. Cancer Stem Cells under Hypoxia as a Chemoresistance Factor in Breast and Brain[J]. Curr Pathobiol Rep, 2014, 2 (1) : 33–40. |
| [7] | Feodorova YN, Sarafian VS. Psychological stress-cellular and molecular mechanisms[J]. Folia Med (Plovdiv), 2012, 54 (3) : 5–13. |
| [8] | Kappler M, Taubert H, Schubert J, et al. The real face of HIF1α in the tumor process[J]. Cell Cycle, 2012, 11 (21) : 3932–6. |
| [9] | Li SY, Peng HJ. Changes of oxidative stress index in breast tissue[J]. Shi Yong Yi Xue Za Zhi, 2009, 25 (16) : 2626–7. [黎思毅, 彭红娟. 乳腺癌组织氧化应激反应指标的变化[J]. 实用医学杂志,2009, 25 (16) : 2626–7. ] |
| [10] | Chiaverini N, De Ley M. Protective effect of metallothionein on oxidative stress-induced DNA damage[J]. Free Radic Res, 2010, 44 (6) : 605–13. |
| [11] | Acunzo J, Katsogiannou M, Rocchi P, et al. Small heat shock proteins HSP27 (HspB1) , αB-crystallin (HspB5) and HSP22 (HspB8) as regulators of cell death[J]. Int J Biochem Cell Biol, 2012, 44 (10) : 1622–31. |
| [12] | Shen H, Zhu H, Song M, et al. A selenosemicarbazone complex with copper efficiently down-regulates the 90-kDa heat shock protein HSP90AA1 and its client proteins in cancer cells[J]. BMC Cancer, 2014, 14 : 629. |
| [13] | Qiao S, Lamore SD, Cabello CM, et al. Thiostrepton is an inducer of oxidative and proteotoxic stress that impairs viability of human melanoma cells but not primary melanocytes[J]. Biochem Pharmacol, 2012, 83 (9) : 1229–40. |
| [14] | Gencer S, Cebeci A, Irmak-Yazicioglu MB. Matrix metalloproteinase gene expressions might be oxidative stress targets in gastric cancer cell lines[J]. Chin J Cancer Res, 2013, 25 (3) : 322–33. |
| [15] | Huang C, Lin Y, Su H, et al. Forsythiaside Protects Against Hydrogen Peroxide-Induced Oxidative Stress and Apoptosis in PC12 Cell[J]. Neurochem Res, 2015, 40 (1) : 27–35. |
| [16] | Zhang GQ, Zhang ZY, Liang AH. Ribosomal protein L11 and tumor suppression[J]. Sheng Ming De Hua Xue, 2009, 29 (6) : 852–5. [张国强, 张志云, 梁爱华. 核糖体蛋白L11与肿瘤抑制[J]. 生命的化学,2009, 29 (6) : 852–5. ] |
| [17] | Cote GJ, Zhu W, Thomas A, et al. Hydrogen peroxide alters splicing of soluble guanylyl cyclase and selectively modulates expression of splicing regulators in human cancer cells[J]. PLoS One, 2012, 7 (7) : e41099. |
 2016, Vol. 43
2016, Vol. 43