文章信息
- 抑癌基因TCF21启动子甲基化在肾癌诊断及预后中的意义
- Significance of Tumor Suppressor Gene TCF21 Promoter Methylation for Diagnosis and Prognosis of Renal Cell Carcinoma
- 肿瘤防治研究, 2016, 53(5): 375-381
- Cancer Research on Prevention and Treatment, 2016, 53(5): 375-381
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2016.05.012
- 收稿日期: 2015-09-12
- 修回日期: 2016-01-04
2. 362000 泉州,福建医科大学附属泉州市第一医院泌尿外科;
3. 362000 泉州,福建医科大学附属泉州市第一医院病理科;
4. 362000 泉州,泉州市医学高等专科学校药学系;
5. 100853 北京,中国人民解放军总医院泌尿外科
2. Department of Urology, Affiliated Quanzhou First Hospital of Fujian Medical University, Quanzhou 362000, China;
3. Department of Pathology, Affiliated Quanzhou First Hospital of Fujian Medical University, Quanzhou 362000, China;
4. Department of Pharmacy, Quanzhou Medical College, Quanzhou 362000, China;
5. Department of Urology, General Hospital of PLA, Beijing 100853, China
肾癌(renal cell carcinoma,RCC)约占肾脏肿瘤的85%,居泌尿系统肿瘤的第二位,发病率及病死率约占全身恶性肿瘤的2%~3%[1]。肾癌起病隐匿,预后差,对放化疗不敏感[2, 3],30%的肾癌患者确诊时已经转移或不具备手术指征,且该类的患者2年生存率<10%[4]。目前,临床上尚缺乏一种快速、便捷、无创的早期肾癌诊断方法,且缺乏明确的特异性肿瘤标志物[5]。TCF21是编码转录因子21的基因,为肿瘤抑制基因,其在肺、肠、性腺和肾等处都有表达[6],近年来研究发现DNA甲基化异常在多种癌症包括肾癌的发生发展中起重要作用,这些因子有望成为肿瘤诊断及预后判断的分子标志物[7-10]。研究发现TCF21在肾癌中也存在甲基化水平异常[11]。TCF21甲基化及异常表达发生在许多癌症的早期,且具有特异性,因此可作为肿瘤诊断和预后判断的候选生物标志物。近年来研究发现肿瘤累及器官相关的体液(如尿液)可以作为检测异常甲基化的标本,同时尿液样本检测具有收集方便、无创性及检测精确等优点,这将给肿瘤分子检测带来极大的便利[12]。本试验应用焦磷酸测序(pyrosequencing)技术系统检测肾癌组织和尿液中TCF21甲基化水平,分析基因甲基化与肾癌发病及预后的关系,比较肾癌组织与尿液样本中TCF21甲基化检测在肾癌诊断中的敏感度和特异性,这对于深入探索肾癌早期快速、无创的基因诊断及肾癌预后监测方法的建立具有意义。
1 资料与方法 1.1 资料选择泉州市第一医院病理科2011年1月—2013年12月手术切除后经病理检查确诊的肾癌石蜡包埋标本,选择标准:(1)首次发现肾癌,并经组织病理学确诊;(2)为单一肾癌,未合并或已排除其他疾病如肾结核、肾结石、肾感染性疾病、肾良性肿瘤、肾盂肿瘤、肾间叶肿瘤、后腹腔其他肿瘤等;(3)术前均未经放疗、化疗、免疫治疗或靶向治疗等抗肿瘤治疗。入组55例肾癌患者包括男30例、女25例;年龄26~86岁,平均年龄52.85岁,以50岁为界分成两组,其中≥50岁有32人,<50岁有23人。按2009年美国癌症联合委员会(American Joint Committee on Cancer,AJCC)肾癌临床分期标准(tumor node metastasis,TNM)分为:Ⅰ期42例、Ⅱ期2例、Ⅲ期11例。按Fuhrman分级,Ⅰ+Ⅱ级共42例,Ⅲ级12例,Ⅳ级1例。肿瘤大小≥7者6例,<7者49例;吸烟者15例、不吸烟者40例;肾透明细胞癌50例、乳头状肾癌2例、多房性囊性癌1例、肾细胞癌Xp11.2易位/TFE3基因融合相关性肾癌1例、嫌色性肾细胞癌1例。在55例肾癌标本中随机选取21例进行切片获取癌旁正常组织(经资深病理科医生看片确定),同时随机留取55例肾癌患者术前尿液样本33例及正常尿液对照组15例进行焦磷酸测序。本研究经过本院伦理委员会批准,所有患者均签署知情同意书。
1.2 主要试剂及仪器石蜡切片组织基因组DNA提取试剂盒(德国QIAGEN公司);尿液基因组DNA提取试剂盒(德国QIAGEN公司);基因组DNA亚硫盐处理试剂盒(美国Zymo Research公司);PCR产物纯化试剂盒(美国Promega公司);热启动Taq核酸聚合酶(日本Takara公司);焦磷酸测序试剂(瑞典Biotage公司);PSQ96样品制备工具(PSQ96 Sample Prep Tool)、PSQ96试剂仓、PSQ96微孔板(PSQ96 Sample Prep Thermo plate Low 和 PSQ96 Plate/PSQ96 Plate Low)(德国QIAGEN公司)。链亲和素包被的磁珠(Dynabeads M-280 Streptavidin,Invitrogen)。结合缓冲液(1×Binding Buffer):10 mmol/L Tris-HCl;2 mol/L NaCl;1 mmol/L EDTA;0.1%Tween 20;去离子水溶解,用1 mol/L HCl调pH为7.6。变性缓冲液(1×Degeneration Buffer):0.2 mol/L NaOH;去离子水溶解。退火缓冲液(1×Annealing Buffer):20 mmol/L Tris-Acetat;2 mmol/L MgAc2;去离子水溶解,用4 mol/L乙酸调pH值到7.6。
1.3 实验方法基因组DNA提取:使用10 μm厚度的石蜡包埋病理切片组织6~8片,按照DNA提取试剂盒说明书提取组织中基因组DNA后使用OD-1000微量紫外分光光度计测定260 nm和280 nm处吸光度值(A),并计算DNA含量,-80℃保存备用。DNA亚硫酸盐修饰: 经OD-1000型紫外分光光度计测定DNA A260/A280比值在1.7~2.0为合格样品;取1 μg,按照 DNA Methylation-Gold Kit说明书对基因组DNA进行甲基化修饰后,-80℃保存备用。多聚酶链式反应: 采用PCR对样品中TCF21基因启动子甲基化区域进行扩增。反应体系包括亚硫酸盐处理后模板2 μl,10×PCR buffer ,0.25 u/μl Hot star Taq酶,0.5 mmol/L dNTP,上下游引物各 1 μl,总体积50 μl。以双蒸水代替模板作为空白对照。 TCF21基因甲基化测序引物序列见表 1。
焦磷酸测序检测:(1)分别取40 μl扩增产物至PSQ 96 Plate Low样品制备板A中,各加入40 μl结合缓冲液和5 μl包被有链亲和素的磁珠,将A板放入样品制备板中,振荡10 min。将结合PCR产物的磁珠转移至变性缓冲液的板B中,使双链DNA充分变性。转移结合有单链PCR产物的磁珠至100 μl退火缓冲液的板C涡旋振荡洗涤2 min。(2)测序引物杂交:将结合单链PCR产物的磁珠转入45 μl复性缓冲液中,加入5 μl测序引物,80℃杂交10 min。(3)PSQ96焦磷酸测序仪和测序反应试剂盒(Pyro Gold Reagents)检测TCF21启动子区域内甲基化位点的碱基频率。采用文献报道常用的甲基化指数公式[MI=甲基化的峰值高度/(甲基化的峰值高度+非甲基化的峰值高度)×100%]对该甲基化频率进行计算[13]。
1.4 随访方法对本研究中纳入的55例患者进行随访,采用门诊定期复诊及电话随访方式。随访时间为2011年1月—2015年8月。随访11~54月,中位生存时间27月,无失访病例,随访率100%。Kaplan-Meier法计算生存率,并绘制生存曲线,生存曲线间的比较采用Log rank检验。
1.5 统计学方法以每个标本中片段的MI均值代表其甲基化水平[14]。由于基因启动子甲基化频率变化不符合正态分布,使用SPSS19.0软件对所检测肾癌患者和癌旁正常肾组织的TCF21甲基化水平进行Mann-Whitney U非参数秩和检验,验证TCF21基因启动子甲基化水平与肾癌的相关性。甲基化水平和临床病理资料如性别、年龄、吸烟史、肿瘤分期分级和肿瘤病理类型之间的关系使用Mann-Whitney检验。相关性由Spearman Correlation评估。釆用Kaplan-Meier的方法绘制TCF21高甲基化组与TCF21低甲基化组患者的生存曲线,并通过Log rank检验,比较不同TCF21甲基化水平患者术后生存率与总生存率(首诊后)有无差异。用接收操作特征(ROC)曲线来测绘真阳性率(敏感度)和假阳性率(1-specificity),并计算曲线下的面积(AUC)。双尾P-values使用计算机辅助程序(SPSS19.0),以P≤0.05为差异具有统计学意义。
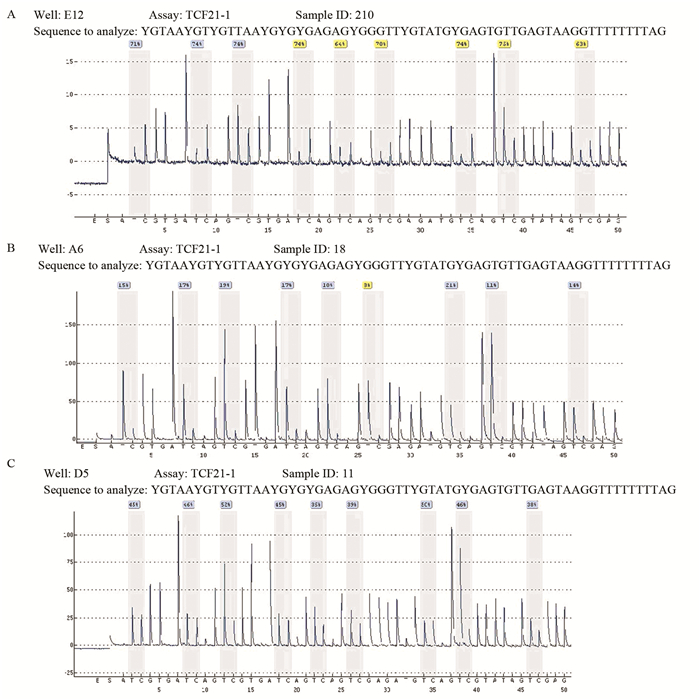
2 结果 2.1 焦磷酸测序检测肾癌组织、正常肾组织及肾癌患者尿液样本中TCF21启动子CpG位点的焦磷酸测序结果干扰背景小,测序峰清晰,与GenBank收录的序列一致,见图 1。
|
| A: renal cell carcinoma(RCC) tissues; B: normal renal tissues; C: RCC urine specimen 图 1 TCF21启动子甲基化位点焦磷酸测序检测 Figure 1 Pyrosequencing detection of TCF21 promoter methylation site |
2.2 组织中TCF21甲基化水平
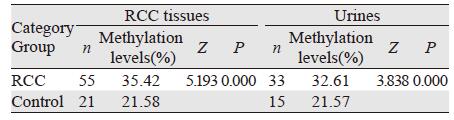
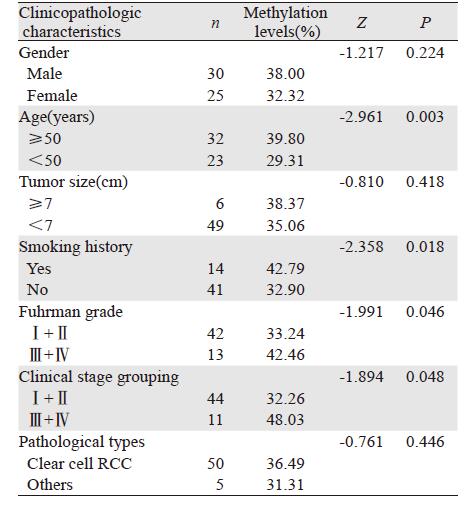
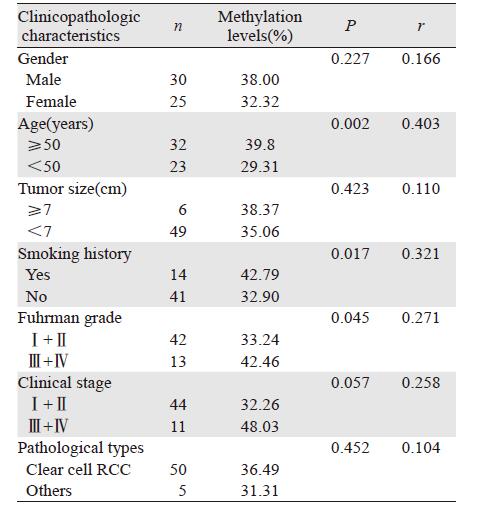
肾癌组织中TCF21基因甲基化水平明显高于癌旁正常肾组织,两者的差异有统计学意义(P=0.000),见表 2。肾癌组织中TCF21甲基化水平与不同的年龄(P=0.003)、吸烟史(P=0.018)、Fuhrman分级(P=0.046)及临床分期(P=0.048)有关,见表 3。与年龄(r=0.403,P=0.002)、吸烟史(r=0.321,P=0.017)和Fuhrman分级(r=0.271,P=0.045)呈正相关,见表 4。
 |
 |
 |
2.3 尿液中TCF21甲基化水平
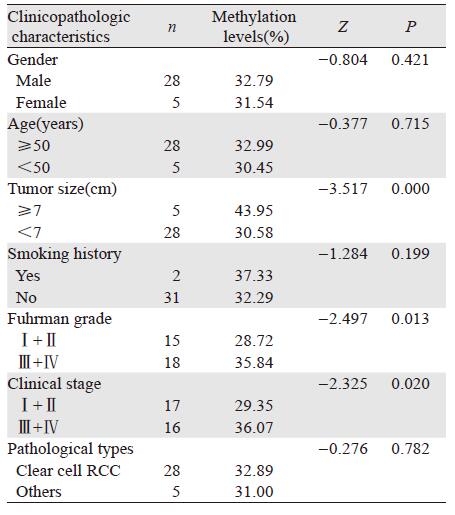
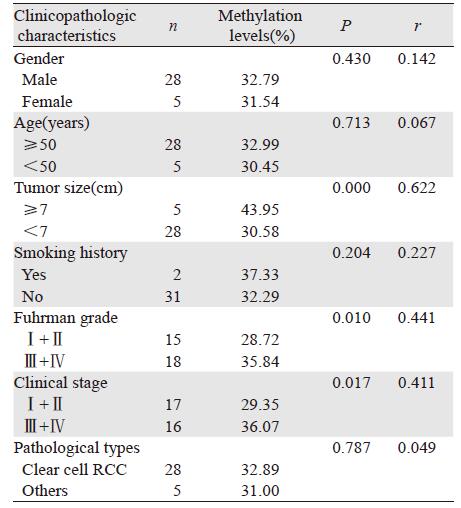
肾癌患者尿液中TCF21基因甲基化水平明显高于正常尿液样本,两者差异有统计学意义(P=0.000),见表 2;肾癌尿液样本中TCF21甲基化水平与不同的肿瘤大小(P=0.000)、Fuhrman分级(P=0.013)及临床分期(P=0.020)有关,见表 5。与肿瘤大小(r=0.662、P=0.000)、Fuhrman分级(r=0.441、P=0.010)和临床分期(r=0.411、P=0.017)呈正相关,见表 6。
 |
 |
2.4 TCF21 甲基化水平与肾癌患者预后的关系
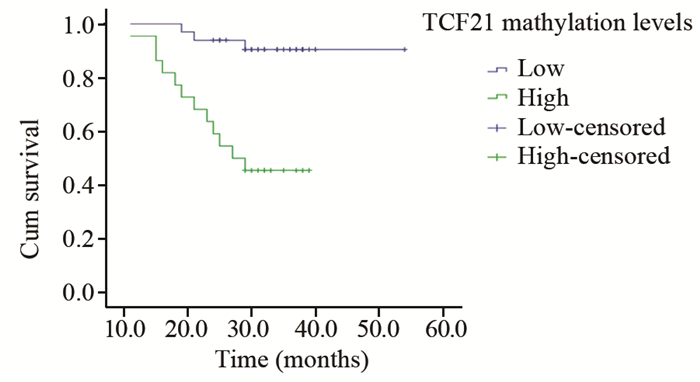
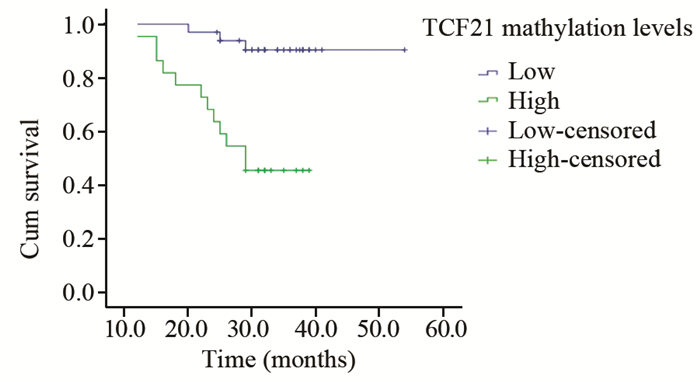
55例肾癌病例中,TCF21甲基化平均水平为35.42%。把55例病例分为两组:低甲基化组(≤ 35.42%)和高甲基化组(>35.42%),对TCF21高甲基化组与低甲基化组两组患者进行随访,随访起止时间为2011年1月—2015年8月,随访11~54月,中位生存时间27月。Kaplan-Meier绘制TCF21高甲基化组与TCF21低甲基化组术后生存曲线,见图 2,Log rank显示其生存期差异具有统计学意义(P=0.000),同时TCF21高甲基化组与低甲基化组两组患者总生存率(首诊后)也存在差异(P=0.000),见图 3。
|
| 图 2 肾癌TCF21甲基化水平相关术后生存率曲线 Figure 2 Postoperative survival rate curves of different methylation levels of TCF21 in RCC tissues |
|
| 图 3 肾癌TCF21甲基化水平相关总生存率曲线 Figure 3 Overall survival rate curves of different methylation levels of TCF21 in RCC tissues |
2.5 肾癌组织与尿液样本中TCF21甲基化水平诊断肾癌的价值
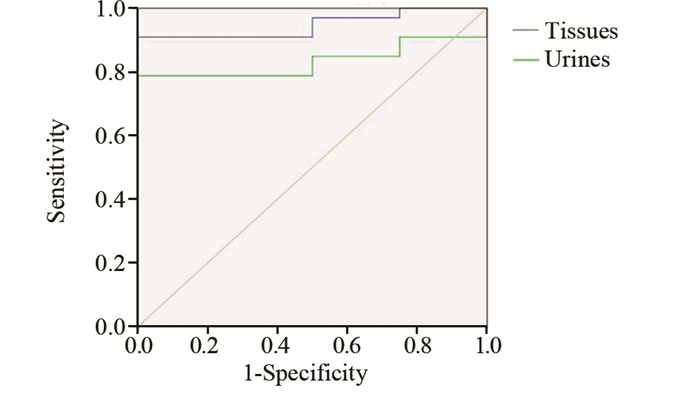
以肾癌组织与尿液样本中TCF21甲基化水平分别绘制受试者工作特征曲线(receiver operating characteristics,ROC),见图 4。以ROC曲线分析肾癌组织中TCF21甲基化水平检测诊断肾癌的效果,以TCF21甲基化水平23.61%作为cut-off值使肾癌组织中TCF21甲基化水平检测诊断肾癌的敏感度和特异性达到最高,分别为89%和61.9%。尿液样本中TCF21甲基化水平检测诊断肾癌的cut-off值是26.84%,敏感度和特异性分别为79%和100%,肾癌组织与术前尿液样本中TCF21甲基化水平检测在诊断肾癌的效价评估中,前者的敏感度及ROC曲线下面积均高于后者,两者间的差异具有统计学意义(P=0.004),肾癌组织中TCF21甲基化水平检测对肾癌的诊断效价高于尿液样本中TCF21甲基化水平检测,见表 7 。
|
| 图 4 TCF21检测肾癌组织和尿液样本的受试者工作特征曲线 Figure 4 Receiver operating characteristic (ROC) curves of TCF21 detecting RCC tissues and urine specimens |
 |
3 讨论
近年来表观遗传研究发现许多碱性螺旋-环-螺旋因子与肿瘤的发生、发展有关,肾癌组织也不例外[15]。TCF21属于碱性螺旋-环-螺旋家族,在肾和肺等组织中高度表达[16]。Robb等[17]发现肾癌组织中TCF21的表达较正常肾组织明显降低,表明TCF21与肾癌的发病有关。而DNA甲基化与细胞的生长和分化相关,与基因的表达减少密切相关,已被确认为一种重要的致癌因素[18]。本试验研究发现肾癌组织中TCF21甲基化水平明显高于正常肾组织,且差异有统计学意义,其诊断敏感度和特异性分别为89%和61.9%。而相关研究证实TCF21在肾癌组织中较正常组织表达减少与TCF21甲基化有关[19],因此TCF21有望成为肾癌诊断和疗效预测的生物标志物。
尽管肾癌起病较为隐匿,但尿脱落细胞为肾癌早期的无创性检测提供了可能[20]。研究证实用微卫星分析技术检测尿液中DNA异常可用于诊断肾癌的存在[21]。Hoque等[22]通过实时荧光定量PCR法对26例肾癌患者尿液样本中的8个基因(MGMT、CDH1、APC等)的甲基化水平进行分析,结果显示88%肾癌尿液样本中至少可检测出1个基因异常甲基化,对照组未发现明显的甲基化。本研究发现肾癌患者术前尿液样本中TCF21基因甲基化水平明显高于对照组,其诊断敏感度和特异性分别为79%和100%。研究发现大多数肾癌患者术前尿液中TCF21基因甲基化水平升高的是可以被检测到的,但是样本数较少,还有待进一步深入研究。相信随着实验技术的不断改进与完善及研究样本量的扩大,这种无创性的高通量检测技术被应用于肾癌的早期诊断与监测将成为可能。
关于肾癌的亚临床进展目前尚缺乏有效的监测手段,迫切需要寻求一种敏感、准确、方便快捷的手段对肾癌的进展、复发进行实时监测。已有相关研究证实TCF21甲基化水平与泌尿系肿瘤的分期有关,如Costa等[11]研究发现前列腺癌组织中pT3期(Pathologic T-stage,病理分期)的TCF21甲基化水平明显高于pT2期的(P=0.038)。本研究发现肾癌中肿瘤分级分期越高,TCF21甲基化水平越高,差异具有统计学意义,提示TCF21可能与肾癌的侵袭分化有关,最后我们比较了TCF21高甲基化组和TCF21低甲基化组患者术后和肾癌确诊后生存率,发现两组生存率在术后和肾癌确诊后都具有明显差异(P=0.000,P=0.000),检测TCF21甲基化水平为实时监测肾癌的进展、复发提供了可能。
综上所述,DNA甲基化在肾癌发生、发展中的机制复杂[23],如甲基化发生的相关诱因、某些特殊的CpG位点易发生甲基化的原因、肾癌甲基化谱及基因芯片的完善等,同时肾癌相关分子生物标志涉及到多种分子及信号通路参与,其机制尚有待进一步深入研究[24-26]。本试验虽然有许多不足,如未进行晚期转移性肾癌甲基化水平的分析、多基因甲基化的联合检测以及去甲基化基因治疗的研究探索等,但为国内首次使用焦磷酸测序技术对肾癌组织和尿液中TCF21甲基化进行初步探讨,为实现通过高通量检测手段联合检测组织和尿液中DNA甲基化水平,为肾癌早期诊断、早期治疗及预后监测奠定了基础。
| [1] | Junker K, Ficarra V, Kwon ED, et al. Potential role of genetic markers in the management of kidney cancer[J]. Eur Urol, 2013, 63 (2) : 333–40. |
| [2] | Karaman S, Detmar M. Mechanisms of lymphatic metastasis[J]. J Clin Invest, 2014, 124 (3) : 922–8. |
| [3] | Utsumi T, Suyama T, Imamura Y, et al. The association of CXCR3 and renal cell carcinoma metastasis[J]. J Urol, 2014, 192 (2) : 567–74. |
| [4] | Wu WF, Xin J, Wu BC, et al. Expressions and significance of Ezrin and E-cadherin in clear cell renal cell carcinoma[J]. Xian Dai Yi Yao Za Zhi, 2010, 26 (18) : 2731–3. [吴文峰, 辛军, 伍伯聪, 等. 埃兹蛋白和上皮型钙黏蛋白在肾透明细胞癌的表达及意义[J]. 现代医药杂志,2010, 26 (18) : 2731–3. ] |
| [5] | Moch H, Srigley J, Delahunt B, et al. Biomarkers inrenal cancer[J]. Virchows Arch, 2014, 464 (3) : 359–65. |
| [6] | Smith LT, Lin M, Brena RM, et al. Epigenetic regulation of the tumor suppressor gene, TCF21 on 6q23-q24 in lung and head and neck cancer[J]. Proc Natl Acad Sci U S A, 2006, 103 (4) : 982–7. |
| [7] | Pogribny IP, Rusyn I. Environmental toxicants, epigenetics, and cancer[J]. Adv Exp Med Biol, 2013, 754 : 215–32. |
| [8] | Coppedè F, Lopomo A, Spisni R, et al. Genetic and epigenetic biomarkers for diagnosis,prognosis and treatment of colorectal cancer[J]. World J Gastroenterol, 2014, 20 (4) : 943–56. |
| [9] | Khan G, Moss RA, Braiteh F, et al. Proactive strategies for regorafenib in metastatic colorectal cancer: implications for optimal patient management[J]. Cancer Manag Res, 2014, 6 : 93–103. |
| [10] | Wang W, Jia HL, Huang JM, et al. Identification of biomarkers for lymph node metastasis in early-stage cervical cancer by tissue-based proteomics[J]. Br J Cancer, 2014, 110 (7) : 1748–58. |
| [11] | Costa VL, Henrique R, Danielsen SA, et al. TCF21 and PCDH17 methylation: an innovative panel of biomarkers for a simultaneous detection of urological cancers[J]. Epigenetics, 2011, 6 (9) : 1120–30. |
| [12] | Hoque MO, Begum S, Topaloglu O, et al. Quantitation of promoter methylation of multiple genes in urine DNA and bladder cancer detection[J]. J Natl Cancer Inst, 2006, 98 (14) : 996–1004. |
| [13] | Shaw RJ, Liloglou T, Rogers SN, et al. Promoter methylation of P16, RARbeta, E-cadherin, cyclin A1 and cytoglobin in oral cancer:quantitative evaluation using pyrosequencing[J]. Br J Cancer, 2006, 94 (4) : 561–8. |
| [14] | Eckhardt F, Lewin J, Cortese R, et al. DNA methylation profiling of human chromosomes 6, 20 and 22[J]. Nat Genet, 2006, 38 (12) : 1378–85. |
| [15] | Zhou L, Chen J, Li Z, et al. Integrated profiling of microRNAs and mRNAs: microRNAs located on Xq27.3 associate with clear cell renal cell carcinoma[J]. PLoS One, 2010, 5 (12) : e15224. |
| [16] | Quaggin SE, Vanden Heuvel GB, Igarashi P. Pod-1, a mesoderm-specific basic-helix-loop-helix protein expressed in mesenchymal and glomerular epithelial cells in the developing kidney[J]. Mech Dev, 1998, 71 (1-2) : 37–48. |
| [17] | Robb L, Mifsud L, Hartley L, et al. Epicardin: A novel basic helix-loop-helix transcription factor gene expressed in epicardium, branchial arch myoblasts, and mesenchyme of developing lung, gut, kidney, and gonads[J]. Dev Dyn, 1998, 213 (1) : 105–13. |
| [18] | Gopalakrishnan S, Van Emburgh BO, Robertson KD. DNA methylation in development and human disease[J]. Mutat Res, 2008, 647 (1-2) : 30–8. |
| [19] | Ye YW, Jiang ZM, Li WH, et al. Down-regulation of TCF21 is associated with poor survival in clear cell renal cell carcinoma[J]. Neoplasma, 2012, 59 (6) : 599–605. |
| [20] | Ho CL, Tzai TS, Chen JC, et al. The molecular signature for urothelial carcinoma of the upper urinary tract[J]. J Urol, 2008, 179 (3) : 1155–9. |
| [21] | Eisenberger CF, Schoenberg M, Enger C, et al. Diagnosis of renal cancer by molecular urinalysis[J]. J Natl Cancer Inst, 1999, 91 (23) : 2028–32. |
| [22] | Hoque MO, Begum S, Topaloglu O, et al. Quantitative detection of promoter hypermethylation of multiple genes in the tumor, urine, and serum DNA of patients with renal cancer[J]. Cancer Res, 2004, 64 (15) : 5511–7. |
| [23] | CancerGenome Atlas Research Network. Comprehensive molecular characterization of clear cell renal cell carcinoma[J]. Nature, 2013, 499 (7456) : 43–9. |
| [24] | Ngo TC, Wood CG, Karam JA. Biomarkers of renal cell carcinoma[J]. Urol Oncol, 2014, 32 (3) : 243–51. |
| [25] | Maroto P, Rini B. Molecular biomarkers in advanced renal cell carcinoma[J]. Clin Cancer Res, 2014, 20 (8) : 2060–71. |
| [26] | Tan PH, Cheng L, Rioux-Leclercq N, et al. Renal tumors: diagnostic and prognostic biomarkers[J]. Am J Surg Pathol, 2013, 37 (10) : 1518–31. |
 2016, Vol. 53
2016, Vol. 53



