文章信息
- 长链非编码RNA LOC100294362对乳腺癌细胞增殖和侵袭的影响
- Effect of Long Non-coding RNA LOC100294362 on Proliferation and Invasion of Breast Cancer Cells
- 肿瘤防治研究, 2016, 43(5): 366-370
- Cancer Research on Prevention and Treatment, 2016, 43(5): 366-370
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2016.05.010
- 收稿日期: 2015-11-17
- 修回日期: 2016-01-18
2. 421001 衡阳,南华大学生理学教研室
2. Department of Physiology, University of South China, Hengyang 421001, China
乳腺癌是女性最常见的恶性肿瘤之一,但其发病机制仍未完全阐明,因此进一步深入研究乳腺癌的发病机制及寻找其生物诊断标志物,将为乳腺癌的防治提供新的方法。
近年研究表明,长链非编码RNA(long non-coding RNA,lncRNA)具有多种生物学功能,并在染色质的转录、剪接、翻译、表观遗传学调控等多种生物学进程中发挥重要的调控作用[1, 2]。研究显示:lncRNA的表达异常可导致包括肿瘤在内的多种疾病的产生[3, 4]。在乳腺癌的研究中,一些lncRNAs(如HOTAIR、H19、SRA等)被证明是致癌的,而一些lncRNAs(如GAS5、XIST等)被证明是抑癌的,他们参与细胞生长、凋亡、迁移和浸润[5]。LOC100294362是我们实验室筛选的一种乳腺癌相关的lncRNAs分子,其生物学特性尚未见相关文献报道。因此,本研究通过检测乳腺癌组织及细胞中LOC100294362的表达情况,应用Real-time PCR、MTT、Transwell小室和Western blot等方法检测过表达或沉默LOC100294362对MCF-7细胞增殖和侵袭能力的影响,并探讨其作用机制,为临床诊断、预后提供可能的标志物,为乳腺癌的干预治疗提供可能的潜在的治疗靶点。
1 材料与方法 1.1 主要试剂及材料人乳腺癌MCF-7、MX-1、MDA-MB-231、SK-BR3和MCF10A细胞购于美国ATCC公司,L-DMEM培养液(货号:12200036)、胰蛋白酶(货号:25200-056)和胎牛血清(货号:16000044)均购于美国Gibco公司,MTT(货号:M-2128)染料均购于Sigma公司,Transwell 小室(货号:3421)购自加拿大Costar公司;Matrigel基质胶(货号:356234)购自加拿大BD Biosciences公司。转染试剂脂质体2000(货号:11668019)、TRIzol和Real-time PCR试剂盒购自美国Invitrogen公司;引物由上海生物工程有限公司合成;p53抗体(货号:AP062)购于美国细胞信号公司;其他试剂均为国产分析纯试剂。
1.2 组织标本收集30例样本来自南华大学第一附属医院2000—2010年被诊断为乳腺癌并接受手术的患者,均经病理严格鉴定(分期Ⅱ~Ⅳ;美国癌症联合会癌症分期指南第7版)。在获得患者同意并签署知情同意书,手术切除乳腺癌组织后,立即置于液氮中冻存,用于提取RNA。
细胞培养将上述所有细胞接种于6 cm碟中,加入含10%胎牛血清的L-DMEM培养液,在37℃、5%CO2培养箱中培养,待细胞生长至80%时,0.25%胰酶消化传代。
1.4 总RNA提取和定量反转录PCR(qRT-PCR)用TRIzol试剂提取组织或细胞中的总RNA,紫外分光光度计测定其纯度及浓度,随后将RNA反转录为cDNA,使用SYBR Green进行qRT-PCR实验分析LOC100294362和GAPDH的表达,GAPDH作为内参。引物序列如下:LOC100294362上游: 5'-TATGCGATGAGGGTCTCAATGC-3',下游:5'-AGGATCGACACCTGTTGGTG GA-3'和GAPDH上游:5'-AGGTCGGAGTCAACGGATTTG-3',下游:5'- GTGATGGCATGGACTGTGGT-3'。Real-time PCR反应体系为20 μl,反应条件94℃预变性2 min,94℃变性30 s,58℃退火30 s,72℃延伸30 s,共30个循环。LOC100294362的相对表达量用2-ΔΔCt计算。
1.5 LOC100294362过表达质粒的构建及转染LOC100294362序列被合成和亚克隆至PCDH载体上,应用脂质体2000介导的方法将LOC100294362质粒及空载体(PCDH)转染至6孔平板上培养的MCF-7细胞中,48 h后收集细胞,qRT-PCR检测其过表达情况和转染效率,Western blot分析p53蛋白表达。
1.6 siRNA干扰实验按脂质体2000的说明书操作,将脂质体2000与LOC100294362的siRNA(si-LOC100294362)、对照siRNA(siCon)混匀,室温放置20 min后,将其滴入培养有MCF7细胞的培养皿中,混匀培养。48 h后收集细胞进行qRT-PCR和Western blot分析。
1.7 细胞增殖试验采用MTT法,将MCF-7细胞按每孔5×103个细胞接种于96孔板中,每孔体积100 μl,待细胞长到50%~60%融合时更换无血清的DMEM培养24 h,沉默或过表达LOC100294362,分别于转染后4 h、1 d、2 d、3 d、5 d、7 d后进行检测。弃去培养液,每孔分别加入新鲜培养液180 μl,置细胞培养箱中平衡30 min后,每孔加入0.5%的MTT溶液20 μl,继续培养4 h后终止培养。然后将培养液倒尽吸干,每孔加入150 μl DMSO,37℃振荡15 min,在酶标仪上选择570 nm波长,测定各孔的光密度值。每个处理组设6个复孔,实验重复3次。
1.8 细胞体外侵袭实验小室接种细胞前一晚,用预冷的无血清培养液以1:4的体积比稀释Matrigel,以50 μl每孔包被Transwell小室。MCF-7细胞转染48 h后,调整密度至2.0×105个每毫升,将200 μl各组细胞悬液移入小室内,小室植入24孔板内,在小室下层加入500 μl含10%FBS的完全培养液,培养箱孵育24 h后,取出Transwell小室,用无菌棉签擦去上室面细胞及Matrigel,甲醛固定,结晶紫染色,在显微镜下计数5个高倍镜视野穿膜的细胞,求出每个视野平均穿膜细胞数,作为评价其侵袭能力的指标。实验重复3次。
1.9 Western blot法分析提取各组细胞蛋白质并测定蛋白质浓度,取蛋白样品30 μg进行SDS-PAGE电泳,转膜、封闭、加入抗p53抗体(1:1000)4℃摇床过夜,洗涤后加入辣根过氧化酶标记的二抗,室温2~4 h,充分洗涤后与ECL化学发光试剂反应,曝光后扫描。
1.10 统计学方法采用SPSS18.0软件进行统计分析,所有数据以(x ±s)表示,组间比较采用配对t检验,P < 0.05为差异有统计学意义。
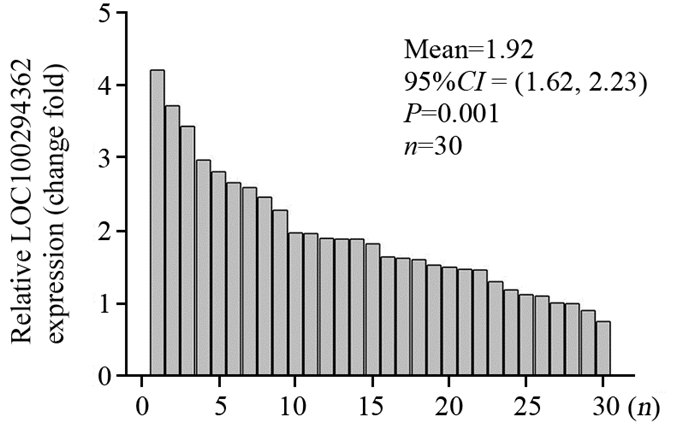
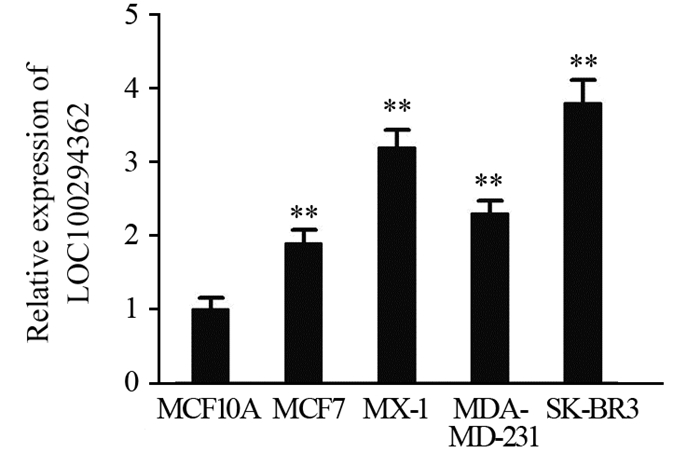
2 结果 2.1 LOC100294362在乳腺癌组织和细胞中的表达将30例乳腺癌患者癌组织与癌旁正常组织进行配对,使用qRT-PCR分别检测LOC100294362的水平,结果用GAPDH标准化。结果显示乳腺癌组织中,LOC100294362的表达水平较正常组织的平均表达水平高,见图 1。检测4种乳腺癌细胞系(MCF-7、MX-1、MDA-MB-231和SK-BR3) 和MCF10A(对照组)中LOC100294362的表达水平,结果显示,LOC100294362在乳腺癌细胞中也高表达,见图 2。提示LOC100294362可能与乳腺癌发生发展有关。
|
| The relative LOC100294362 expression levels of 30 pairs of breast cancer tissues and normal adjacent tissues were detected by quantitative PCR (multiple relation), which were arranged from high to low 图 1 长链非编码RNA LOC100294362在乳腺癌组织和癌旁组织中的表达 Figure 1 Expression of long non - coding RNA LOC100294362 in normal and breast cancer tissues |
|
图 2
长链非编码RNA LOC100294362在乳腺癌细胞中的相对表达 (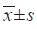 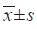 |
2.2 过表达LOC100294362对MCF-7细胞增殖和浸润的影响
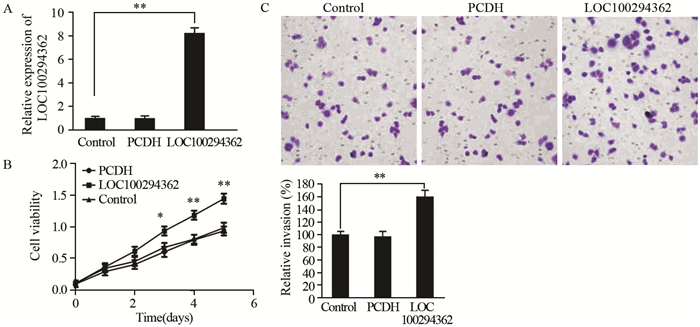
本研究将空白对照质粒PCDH和过表达LOC100294362的质粒转染入MCF-7细胞中,转染48 h后进行qRT-PCR分析LOC100294362的表达。实验结果显示,转染LOC100294362的MCF-7细胞LOC100294362的表达显著上调,说明转染成功,见图 3A。MTT实验显示,转染了LOC100294362的MCF-7细胞数量在3、5、7天后显著高于对照组(PCDH组),提示LOC100294362具有原癌活性,能够促进癌症细胞增殖,见图 3B。鉴于LOC100294362对肿瘤恶性生物学行为的影响,进一步验证LOC100294362对肿瘤侵袭活性的影响。在转染LOC100294362后,将细胞接种于Transwell小室里,培养48 h,然后染色,计数,统计穿过Matrigel胶的细胞数。实验发现过表达LOC100294362后,细胞的侵袭活性明显增加,见图 3C。
|
A: the LOC100294362 expression in MCF-7 cells transfected with PCDH and LOC100294362; B: the effect of over-expressed LOC100294362 on MCF-7 cells growth; C: the effect of over-expressed LOC100294362 on MCF-7 cells invasion(×200); *: P < 0.05,**: P < 0.01, compared with control group
图 3
过表达LOC100294362对MCF-7细胞增殖和浸润的影响 (  |
2.3 沉默LOC100294362对MCF-7细胞增殖和浸润的影响
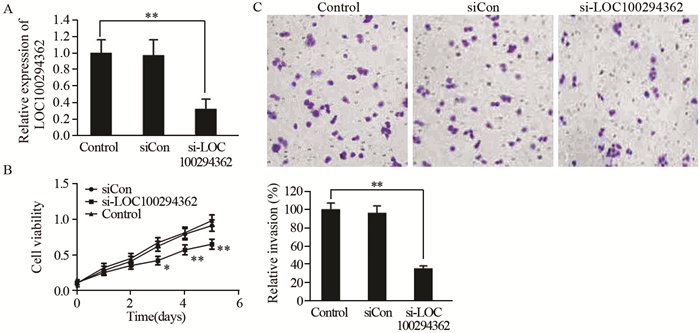
为了验证设计的siRNA对LOC100294362的干扰效率,MCF-7细胞转染了阴性对照siRNA(siCon),该干扰片段与人的基因没有任何同源性,并转染了特异性敲除LOC100294362的siRNA片段(si-LOC100294362),48 h后收集细胞,qRT-PCR分析LOC100294362的表达,结果发现:与MCF-7细胞相比,转染siCon的MCF-7细胞组LOC100294362的表达无显著性差异,而转染si-LOC100294362的细胞组LOC100294362表达显著降低,提示该特异性作用于LOC100294362的siRNA能够有效地干扰其靶基因的表达,见图 4A。MTT实验显示,MCF-7细胞沉默LOC100294362后,随着时间的延长,MCF-7细胞增殖能力逐渐减弱,提示LOC100294362可抑制MCF-7细胞的增殖,见图 4B。此外,细胞浸润实验显示:沉默MCF7细胞LOC100294362后,细胞的侵袭活性明显下降,见图 4C。
|
A: the LOC100294362 expression in MCF-7 cells transfected with siCon and si-LOC100294362; B: the effect of silencing LOC100294362 on MCF-7 cells growth; C: the effect of silencing LOC100294362 on MCF-7 cells invasion (×200); *: P < 0.05, **: P < 0.01, compared with control group
图 4
沉默LOC100294362对MCF-7细胞增殖和浸润的影响 (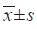 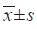 |
2.4 过表达或沉默LOC100294362对MCF-7细胞p53蛋白表达的影响
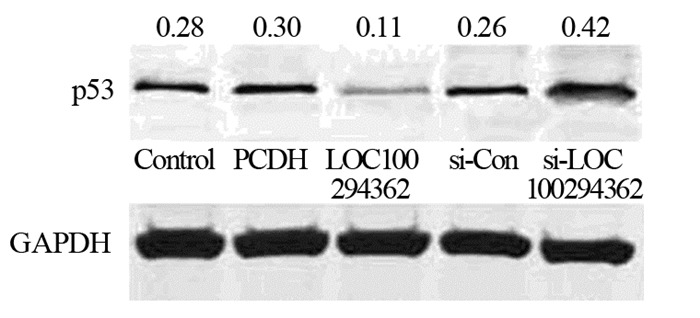
与PCDH组相比,过表达LOC100294362可降低MCF-7细胞p53蛋白表达;然而,沉默MCF-7细胞LOC100294362后,与siCon相比,si-LOC100294362组MCF-7细胞p53蛋白表达显著升高,见图 5。提示,LOC100294362在乳腺癌中可能通过抑制p53的表达而发挥促进肿瘤生长的作用。
|
| The value of control was set as 1, and the relative amounts of the other bands were marked on the p53 strip in the digital form after comparing with control group 图 5 LOC100294362对MCF7细胞p53蛋白表达的影响 Figure 5 Effects of LOC100294362 on protein level of p53 in MCF7 cells |
3 讨论
乳腺癌是世界范围内威胁女性健康最常见的恶性肿瘤之一,在我国也呈逐年上升趋势,其易侵袭转移的特性是导致乳腺癌患者最终死亡的重要原因,同时也是患者手术及化疗后乳腺癌复发的主要原因[6],因此,探索乳腺癌发生发展的分子机制对于改善乳腺癌患者的生存具有重要意义。
非编码RNA是指各种不翻译成蛋白质的RNA分子,其中长链非编码RNA(lncRNA)是一组内源性、长度>200个核苷酸、缺少特异完整的开放阅读框和无蛋白编码功能的RNA,多数由RNA聚合酶Ⅱ转录生成[1]。由于非编码RNA不直接参与编码蛋白质,因此最初人们认为这些RNA是没有意义的,但是通过对机体各种生理和病理过程的观察,逐渐发现lncRNA可以通过基因标记、染色质重塑、细胞周期调控、剪接调控、mRNA降解和翻译调控等多种方式发挥其生物学功能,可在表观遗传水平、转录水平和转录后水平调控基因的表达,广泛参与机体的生理和病理过程。
大量研究证实,lncRNA的变异和调节异常可导致包括肿瘤在内的多种疾病的发生[3, 4]。因此确定癌症相关的lncRNA并研究其分子和生物学功能对理解肿瘤分子生物学及其进展具有重要的意义。已有文献报道lncRNA在乳腺癌中的作用及其机制[7-9, 10]。Huang等[7]报道长链非编码RNA UCA1通过抑制p27(Kip1)促进乳腺癌细胞生长;Shi等[8]证明过表达LOC554202促进乳腺癌细胞增殖和迁移,反之,沉默LOC554202抑制乳腺癌细胞增殖和迁移;Silva等[9]研究表明LSINCT5在乳腺癌和卵巢癌中过表达并促进细胞的增殖;Gupta等[10]则发现HOTAIR通过重塑染色质促进乳腺癌的转移;同时许多研究发现HOTAIR与多种肿瘤(乳腺癌、肝癌、结直肠癌、胰腺癌、鼻咽癌等)的发生发展密切相关[11],这为临床早期诊断和预后判断提供了一类新的标志物,也为肿瘤复发转移治疗提供了潜在靶点和新的治疗思路。
本实验通过对临床乳腺癌患者样本和4种乳腺癌细胞中LOC100294362表达的定量检测,发现LOC100294362在乳腺癌组织和细胞中的表达均高于正常乳腺组织和细胞,提示其表达上调可能与乳腺癌有关,但其在乳腺癌发病过程中的具体作用及对乳腺癌细胞生物学行为的影响,目前尚不清楚。为此,本研究将合成的LOC100294362序列亚克隆至PCDH载体上,应用脂质体2000介导的方法将其转染入乳腺癌MCF-7细胞,上调其在MCF-7细胞中的表达,发现过表达LOC100294362可促进MCF-7细胞增殖和浸润。反之,通过基因沉默的方法干扰该长链非编码RNA,发现沉默LOC100294362后,MCF-7的增殖能力明显降低,侵袭能力明显减弱。提示,LOC100294362在乳腺癌的增殖和浸润中发挥重要作用。
研究表明,乳腺癌的增殖、浸润和转移是个多步骤的复杂过程,与抑癌基因、致癌基因、细胞外基质等多种因素密切相关[12]。本实验结果表明,提高MCF-7细胞中LOC100294362的表达可抑制p53蛋白的表达;反之,沉默LOC100294362可提高p53蛋白的表达,提示lncRNA LOC100294362在乳腺癌发生发展中可能通过抑制p53的激活而发挥促癌作用。但是,LOC100294362对MCF-7细胞增殖的影响应不仅限于p53这一条通路,可能还通过其他通路调控MCF-7细胞生长。此外,LOC100294362通过何种机制下调p53蛋白表达,p53蛋白下降后又通过何种途径影响MCF-7细胞增殖和浸润,本研究并未深入,需要进一步探究。
综上所述,LOC100294362对乳腺癌MCF-7细胞的生物学行为有促进作用,提示LOC100294362可能参与乳腺癌的发生发展。抑制其表达,可以有效抑制乳腺癌的发展。因此,LOC100294362有可能成为乳腺癌分子诊断的标志物和治疗的新靶点。
| [1] | Guttman M, Amit I, Garber M, et al. Chromatin signature reveals over a thousand highly conserved large non-coding RNAs in mammals[J]. Nature, 2009, 458 (7235) : 223–7. |
| [2] | Wang KC, Chang HY. Molecular mechanisms of long noncoding RNAs[J]. Mol Cell, 2011, 43 (6) : 904–14. |
| [3] | Gibb EA, Brown CJ, Lam WL. The functional role of long non-coding RNA in human carcinomas[J]. Mol Cancer, 2011, 10 : 38. |
| [4] | Zhang BB, Yin Y, Huang ZH. New Research of Long Noncoding RNA in Tumor[J]. Zhong Liu Fang Zhi Yan Jiu, 2014, 41 (6) : 669–73. [张彬彬, 殷媛, 黄朝晖. 长链非编码RNA在肿瘤中的研究进展[J]. 肿瘤防治研究,2014, 41 (6) : 669–73. ] |
| [5] | Liu Y, Sharma S, Watabe K. Roles of lncRNA in breast cancer[J]. Front Biosci (Schol Ed), 2015, 7 : 94–108. |
| [6] | Fiorio Pla A, Gkika D. Emerging role of TRP channels in cell migration: from tumor vascularization to metastasis[J]. Front Physiol, 2013, 4 : 311. |
| [7] | Huang J, Zhou N, Watabe K, et al. Long non-coding RNA UCA1 promotes breast tumor growth by suppression of p27 (Kip1)[J]. Cell Death Dis, 2014, 5 : e1008. |
| [8] | Shi Y, Lu J, Zhou J, et al. Long non-coding RNA Loc554202 regulates proliferation and migration in breast cancer cells[J]. Biochem Biophys Res Commun, 2014, 446 (2) : 448–53. |
| [9] | Silva JM, Boczek NJ, Berres MW, et al. LSINCT5 is over expressed in breast and ovarian cancer and affects cellular proliferation[J]. RNA Biol, 2011, 8 (3) : 496–505. |
| [10] | Gupta RA, Shah N, Wang KC, et al. Long non-coding RNA HOTAIR reprograms chromatin state to promote cancer metastasis[J]. Nature, 2010, 464 (7291) : 1071–6. |
| [11] | Cao LP, Wu J, Zheng SS. Research progress of long non-coding RNA HOTAIR in the human cancers[J]. Zhongguo Yi Xue Ke Xue Za Zhi, 2013, 3 (13) : 28–31. [曹林平, 吴健, 郑树森. 长链非编码RNA HOTAIR在肿瘤中的研究进展[J]. 中国医学科学杂志,2013, 3 (13) : 28–31. ] |
| [12] | Deng XL, Zhang WH. Research advances of MMPs and invasion and metastasis of breast cancer[J]. Zhonghua Zhong Liu Fang Zhi Za Zhi, 2011, 18 (23) : 1893–5. [邓晓莉, 张文海. MMPs与乳腺癌侵袭转移研究的现状[J]. 中华肿瘤防治杂志,2011, 18 (23) : 1893–5. ] |
 2016, Vol. 43
2016, Vol. 43


