文章信息
- CD44和CD24标记的宫颈癌细胞亚群特性
- Characteristics of CD44 and CD24-marked Cervical Cancer Cells Subgroups
- 肿瘤防治研究, 2016, 43(5): 345-349
- Cancer Research on Prevention and Treatment, 2016, 43(5): 345-349
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2016.05.006
- 收稿日期: 2015-04-22
- 修回日期: 2015-09-10
2. 050011 石家庄,河北医科大学第四医院妇产科
2. Department of Obstetrics and Gynecology, The Fourth Hospital of Hebei Medical University, Shijiazhuang 050011, China
宫颈癌是危害女性健康的最常见恶性肿瘤之一。目前临床治疗主要通过手术、放疗和化疗等手段。早期宫颈癌预后良好,但中晚期宫颈癌治疗效果差,其主要原因是病灶的转移和复发[1],肿瘤干细胞(cancer stem cell,CSC)的研究结果可以合理的解释上述现象。肿瘤干细胞理论认为,少量CSC无限增殖可以导致肿瘤,与non-CSC相比,CSC具有自我更新、多向分化和体内外形成肿瘤的能力[2-3]。López等[4]研究证实宫颈癌组织及宫颈癌细胞系中存在具有CSC特性的细胞;Qing等[5]发现射线反复多次照射肿瘤细胞可以导致放疗抵抗;谢玲玲等[6]研究则表明长期多次分割剂量β射线照射HeLa细胞可富集宫颈癌干细胞。尽管在肿瘤干细胞方面已经获得了一些有价值的研究成果,然而仍有许多问题尚需进一步阐明,例如:何为宫颈癌肿瘤干细胞(cervical cancer stem cells,CCSC)的特异表面标志物,如何分离纯化出CCSC并研究其抵抗放化疗、导致肿瘤转移及复发机制等。本研究通过流式细胞仪分选获得CD44+/CD24+Siha细胞,并探讨其是否具备干细胞特性。
1 材料与方法 1.1 主要材料人宫颈鳞癌Siha细胞株(鳞癌)由河北医科大学第四医院科研中心细胞库馈赠。NOD/SCID小鼠购自北京华阜康生物科技股份有限公司。RPMI1640培养液购自美国Gibco公司,胎牛血清购自杭州四季青公司,Transwell小室购自美国BD公司,Anti-Human/Mouse CD44 PE、Rat IgG2b K control PE、Anti-Human CD24 FITC、FITC Mouse IgG1K Isotype Control购自美国eBioscience公司,DMEM/F12基础培养液购自美国Hyclone公司,EGF、bFGF购自美国BD公司,B27购自美国Invitrogen公司,流式分选仪(FACS Aria TM购自美国Becton Dickinson and Company公司),医用电子直线加速器为美国瓦里安公司。
1.2 方法 1.2.1 细胞培养置于饱和湿度5%CO2、37℃条件下培养,采用含10%灭活胎牛血清的RPMI1640完全培养液,每2~3天换液1次,待细胞与细胞融合度达到85%左右时传代。
1.2.2 流式细胞仪检测及分选细胞收集对数生长期的Siha细胞,离心,避光条件下以PBS重悬细胞调至浓度为1×106个每毫升。加入CD44-anti-PE(0.625 μl每管)和CD24-anti-FITC(0.25 μl每管)抗体,同时每种抗体设同型对照,4℃避光孵育30 min。离心后PBS重悬细胞调至细胞浓度约为1×108个每毫升。在1 h内上机检测,利用FACS检测并分选得到的CD44+/CD24+ Siha细胞亚群。
1.2.3 悬浮培养细胞将分选获得的CD44+/CD24+Siha细胞、亲代Siha细胞以1 000个每毫升的密度接种在新鲜配制无血清培养液,置于低黏附力培养瓶中常规培养,每天观察细胞的生长状态,计算成球率(成球率=成球数/接种细胞数×100%)。
1.2.4 小鼠体内致瘤实验实验分组:16只裸鼠随机分为2组,收集CD44+/CD24+Siha细胞、亲代Siha细胞制备单细胞悬液,离心后用含有基质胶的RPMI 1640培养液重悬细胞,计数并调整浓度为1×106个每毫升,无菌注射器抽取1 ml细胞悬液皮下注射于NOD/SCID小鼠的右前肢背侧,观察动物一般情况、瘤体生长情况及计算瘤体的体积[游标卡尺测瘤体的长和宽,体积=(长×宽2)/2]。绘制生长曲线。40天后断颈法处死小鼠,解剖取出瘤体测量、拍照并送至病理科检测。
1.2.5 细胞照射及透射电子显微镜检测细胞的超微结构形态采用瓦里安电子直线加速器6 MVX线为放射源,源皮距100 cm照射,剂量率300 cGy/min,机架旋转180°,培养瓶底部放置1 cm有机玻璃垫。4 Gy辐射前后的CD44+/CD24+Siha细胞亚群、亲代Siha细胞,消化、离心收集细胞,调整浓度至1×105/ml,固定、 脱水、包埋、烘烤、切片、双染色,最后透射电子显微镜观察并摄相保存。
1.2.6 Transwell小室侵袭实验检测两组细胞侵袭能力的差异。取稀释后的Matrigel胶均匀铺于Transwell小室8 μm微孔聚碳酸酯膜上,将小室放入24孔板中,置入37℃、5%CO2细胞培养箱中30 min使胶固化。两组细胞制成单细胞悬液,离心后无血清培养液调整细胞密度为1×105个每毫升。吸取两组细胞悬液200 μl,均匀滴加在Transwell上室内,在24孔板中(下室)加入含有20%胎牛血清的培养液100 μl,并缓慢将Transwell小室放入24孔板中。每组设4个复孔,37℃、5%CO2恒温培养箱中培养24 h。PBS洗2遍,用棉签拭去上室上层未迁移的细胞,PBS洗1次,95%乙醇中固定30 min,晾干,0.1%结晶紫染色20 min,PBS洗3次,小室底面朝上放置于载玻片上。高倍显微镜下计数穿膜细胞。
1.3 统计学方法应用SPSS21.0统计软件进行数据处理,采用均数±标准差(x± s)或中位数±四分位数间距(M±QR)描述其分布,用t检验、单因素方差分析或秩和检验比较各组差异,P<0.05为差异有统计学意义。
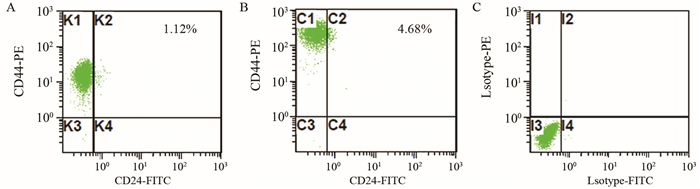
2 结果 2.1 FCM检测不同组细胞中CD44+/CD24+的比例Siha细胞中CD44+/CD24+Siha比例为1.12%,经2 Gy反复辐射25次的Siha细胞被称为耐放疗细胞,耐放疗细胞中CD44+/CD24+Siha比例为4.68%,见图 1。
|
| 图 1 流式细胞仪检测细胞中CD44+/CD24+Siha比例 Figure 1 Proportion of CD44+/CD24+ cells in Siha cells detected by flow cytometry |
2.2 悬浮培养法检测两组细胞成球能力情况
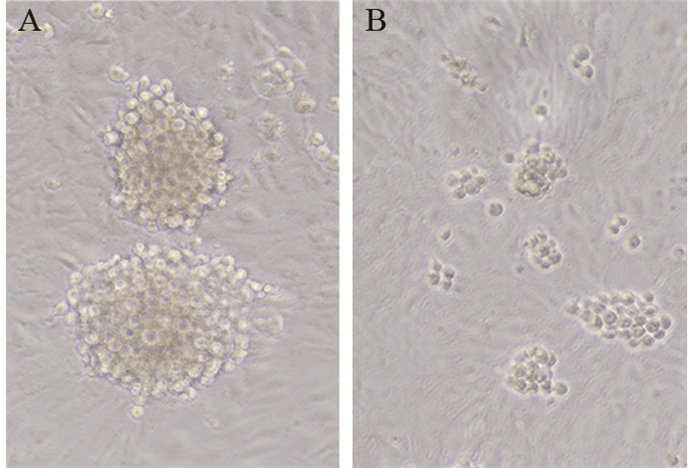
CD44+/CD24+Siha细胞成球时间早并且可以形成致密、体积较大的细胞球。CD44+/CD24+Siha细胞组成球率为(36.0±4.52)%,而亲代Siha细胞组成球率为(6.1±2.85)%,两组之间比较,差异有统计学意义(P=0.00125),见图 2。
|
| A: CD44+/CD24+Siha cells group; B: parent Siha cells group 图 2 两组细胞第10天球囊体积情况 (×200) Figure 2 Mammosphere forming capability of two groups at 10th day (×200) |
2.3 裸鼠移植瘤的生长情况及移植瘤随时间体积的变化情况
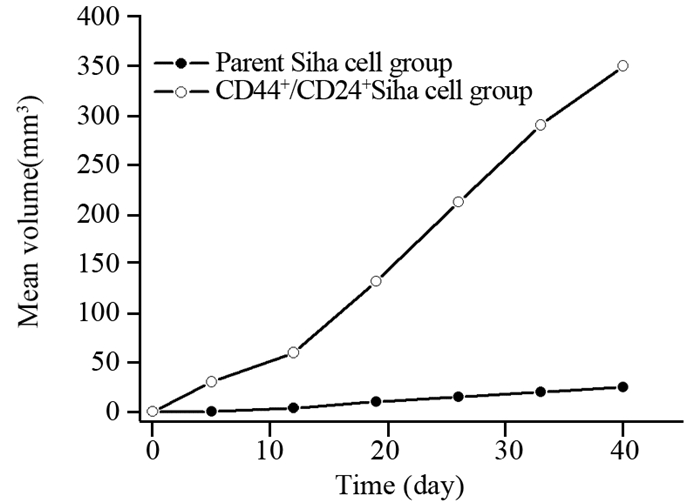
CD44+/CD24+Siha细胞组接种(4.5±3.25)天NOD/SCID小鼠可触及米粒样结节形成,最终成瘤率为100%;亲代Siha细胞组接种(13.0±6.0)天NOD/SCID小鼠可触及米粒样结节形成,最终成瘤率为87.5%。CD44+/CD24+Siha细胞组致瘤时间早,成瘤率高,与亲代Siha细胞组成瘤时间比较,差异有统计学意义(P=0.0135)。两组裸鼠移植瘤体积在不同时间的比较,CD44+/CD24+Siha细胞组和亲代Siha细胞组在第5、12、19、26、33和40天移植瘤体积比较差异均有统计学意义(P=0.0052)。按瘤体体积绘制生长曲线,可以看出CD44+/CD24+Siha细胞组移植瘤生长速度较快,实验后期亲代Siha细胞组移植瘤生长速度有加快的趋势,但生长速度远落后于CD44+/CD24+Siha细胞组,见表 1、图 3~4。
|
| 图 3 两组移植瘤生长曲线 Figure 3 Growth curves of transplantation tumor in two groups |

|
| A: CD44+/CD24+Siha cells; B: parent Siha cells 图 4 两组裸鼠移植瘤比较 Figure 4 Comparison of transplantation tumors between two groups of nude mice |
 |
2.4 透射电子显微镜观察辐射前后两组细胞内部结构变化
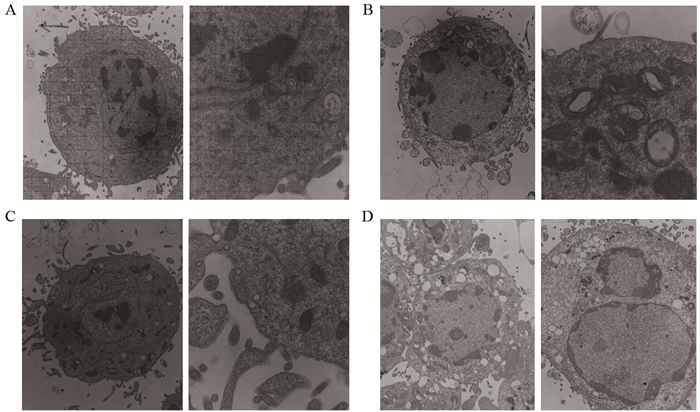
经4 Gy辐射后CD44+/CD24+Siha细胞组其细胞膜完整,核膜及核质较完整,细胞质内容物未见明显变化。而亲代Siha细胞组其细胞可见细胞膜不光滑,细胞质内容物较少,出现较多囊泡,核质聚集固缩,染色质边集,可见凋亡小体出现,见图 5。
|
| A: CD44+/CD24+Siha cells group before 4Gy radiation; B: CD44+/CD24+Siha cells group after 4Gy radiation(×15 000; ×20 000); C: parent Siha cells group before 4Gy radiation; D: parent Siha cells group after 4Gy radiation (×15 000; × 20 000) 图 5 透射电子显微镜观察辐射前后CD44+/CD24+Siha细胞、亲代Siha细胞内部结构 Figure 5 Intracellular ultrastructure of CD44+/CD24+ Siha cells and parent Siha cells observed by transmission electron microscopy |
2.5 Transwell法检测两组细胞体外侵袭能力的影响
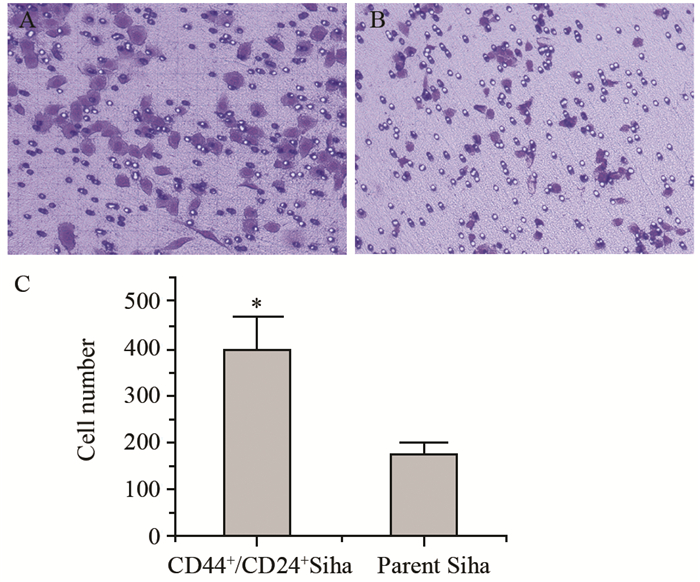
CD44+/CD24+Siha细胞平均迁移细胞数为(400.11±67.31),亲代Siha细胞平均迁移细胞数为(173.89±23.18)。CD44+/CD24+Siha细胞组平均迁移细胞数明显高于亲代Siha细胞组,差异具有统计学意义(P=0.0145),见图 6。
|
| *: P<0.05, compared with parent Siha cells; A: CD44+/CD24+Siha cells; B: parent Siha cells 图 6 两组细胞经4 Gy辐射后的迁移细胞数 (×400) Figure 6 Effects of 4Gy radiation on invasion capabilities of two groups detected by Transwell assay (×400) |
3 讨论
CD44是一种糖蛋白,属于未分类的黏附分子,作为受体识别透明质酸(HA)和胶原蛋白Ⅰ、Ⅳ等,参与周围细胞、细胞间质之间的特异性粘连过程,参与细胞的迁移、增殖。而CD24分布于细胞膜,是糖基化的黏附分子,它与肿瘤细胞的增殖、侵袭和转移有关[7-8]。本课题组预实验发现经过2 Gy反复辐射Siha细胞25次,CD44+/CD24+Siha细胞亚群比例较辐射前明显升高,已有研究表明CD44和CD24在胰腺癌、脑胶质瘤及乳腺癌细胞中被认为是肿瘤干细胞的标志物[9-10]。基于此,我们推测CD44+/CD24+可能是宫颈癌干细胞的表面标志物。本实验利用流式细胞技术成功分选出CD44+/CD24+Siha细胞,其比例稳定在1.5%左右,符合CSC低比例特性。进一步实验结果表明,随体外培养代数的增加,CD44+/CD24+Siha细胞亚群能够再次分化成non-CD44+/CD24+Siha细胞亚群,预示着CD44+/CD24+ Siha细胞亚群具有多向分化潜能的干细胞特性。无血清悬浮培养法被认为是富集、鉴定CSC的有效方法,成球生长是CSC的特性,无血清悬浮培养时分化细胞由于不能适应无血清条件逐渐凋亡,而未分化细胞通过不对称性分裂形成由同一克隆起源的干细胞构成细胞集落。悬浮培养CD44+/CD24+Siha细胞时,形成的悬浮细胞球囊体积大且致密,出现时间早,其成球能力更强,而亲代Siha细胞形成球囊体积小,但也能够成球,证实亲代Siha细胞中存在少量的CSCs,在无血清培养液条件下少量CSC细胞进行细胞分裂形成细胞球。目前NOD/SCID小鼠体内致瘤实验已经成为鉴定CSC的金标准。不仅能够证明CSC高致瘤特性,还能反映肿瘤具有自我更新、无限增殖能力。本实验采用等量的CD44+/CD24+Siha细胞、亲代Siha细胞接种于NOD/SCID小鼠皮下,裸鼠的成瘤速度、各时间点两组瘤体体积均出现明显统计学差异。CD44+/CD24+Siha细胞组成瘤时间早、成瘤体积大,表明CD44+/CD24+Siha细胞具有高致瘤性。使用4 Gy作为照射剂量,既可以使细胞免于致死性照射而导致残存细胞明显减少,又能验证不同细胞组放疗抗性的差异。透射电子显微镜观察4 Gy照射后各细胞组的形态特征,发现CD44+/CD24+Siha细胞组其细胞膜完整,核膜及核质完整,细胞质内容物未见明显变化。而亲代Siha细胞组可见细胞膜不光滑,细胞质内容物少,出现较多囊泡,核质聚集固缩,染色质边集,从细胞内部形态学变化可见CD44+/CD24+Siha细胞组表现出较强的抗辐射性。我们认为CD44+/CD24+Siha细胞组辐射前后形态特征差异与细胞的放射抵抗性有关,但细胞形态结构区别与其放射抵抗内在关系尚不明确,有待从细胞形态结构学方面深入探讨其分子生物学机制。Transwell侵袭实验是利用聚碳酸酯膜模拟肿瘤细胞在趋化因子的作用下穿透细胞外基质的过程,研究肿瘤细胞的侵袭能力。结果表明,CD44+/CD24+Siha细胞组较亲代Siha细胞组的侵袭和转移能力强。
以上结果表明,宫颈癌细胞系Siha中CD44+/CD24+细胞亚群特性与干细胞特性具有较高的一致性,可能为宫颈癌干细胞的特异性表面标志物,通过流式分选的CD44+/CD24+细胞极有可能达到富集宫颈癌干细胞的目的。
| [1] | Thun MJ, DeLancey JO, Center MM, et al. The global burden of cancer: priorities for prevention[J]. Carcinogenesis, 2010, 31 (1) : 100–10. |
| [2] | Kim RK, Kim MJ, Yoon CH, et al. A new 2-pyrone derivative, 5-bromo-3-(3-hydroxyprop-1-ynyl)-2H-pyran-2-one, suppresses stemness in glioma stem-like cells[J]. Mol Pharmacol, 2012, 82 (3) : 400–7. |
| [3] | Fong MY, Kakar SS. The role of stem cells and the side population in epithelial ovarian cancer[J]. Histol Histopathol, 2010, 125 (1) : 113–20. |
| [4] | López J, Poitevin A, Mendoza-Martínez V, et al. Cancer-initiating cells derived from established cervical cell lines exhibit stem-cell markers and increased radioresistance[J]. BMC Cancer, 2012, 12 : 48–61. |
| [5] | Qing Y, Yang XQ, Zhong ZY, et al. Microarray analysis of DNA damage repair gene expression profiles in cervical cancer cells radioresistant to 252Cf neutron and X-ray[J]. BMC Cancer, 2010, 10 : 71. |
| [6] | Xie LL, Lu HW, Zhong YY, et al. Fractionated-dose irradiation enriching cervical cancer stem cells in vitro[J]. Zhongshan Da Xue Xue Bao, 2012, 33 (3) : 330–5. [谢玲玲, 卢淮武, 钟沅月, 等. 分割剂量射线照射富集宫颈癌肿瘤干细胞的研究[J]. 中山大学学报,2012, 33 (3) : 330–5. ] |
| [7] | Mccleary-Wheeler AL, McWilliams R, Fernandez-Zapico ME. Aberrant signaling pathways in pancreatic cancer: a two compartment view[J]. Mol Carcinog, 2012, 51 (1) : 25–39. |
| [8] | Al-Hajj M, Wicha MS, Benito-Hernandez A, et al. Prospective identification of tumorigenic breast cancer cells[J]. Proc Natl Acad Sci U S A, 2003, 100 (7) : 3983–8. |
| [9] | Li C, Heidt DG, Dalerba P, et al. Identification of pancreatic cancer stem cells[J]. Cancer Res, 2007, 67 (3) : 1030–7. |
| [10] | Dalerba P, Cho RW, Clarke MF. Cancer stem cells: models and concepts[J]. Annu Rev Med, 2007, 58 : 267–84. |
 2016, Vol. 43
2016, Vol. 43


