文章信息
- 宁忠华,裴红蕾,徐国平,韩阳,奚丹,黄瑾. 2014.
- NING Zhonghua, PEI Honglei, XU Guoping, HAN Yang, XI Dan, HUANG Jin. 2014.
- 增殖细胞核抗原、p53和Nm23的表达以及辅助放疗对进展期胸段食管鳞癌患者术后的预后影响
- Impact of PCNA, p53 and Nm23 Expression and Adjuvant Radiotherapy on Prognosis of Advanced Thoracic Esophageal Squamous Cell Carcinoma Patients After Operation
- 肿瘤防治研究, 2014, 41(11): 1209-1214
- Cancer Research on Prevention and Treatment, 2014, 41 (11): 1209-1214
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2014.11.051
-
文章历史
- 收稿日期:2013-09-04
- 修回日期:2014-01-15
食管癌是我国高发恶性肿瘤,手术和放疗是 食管癌的主要治疗方法;对于进展期食管癌,单 独手术和单独放疗的效果仍然欠佳,综合治疗是 进展期食管癌的最佳选择[1]。目前对于术后辅助放 疗的生存获益仍有不同观点。Xiao等[2, 3]报道淋巴 结转移数是胸段食管鳞癌患者的重要预后因素, 对于有淋巴结转移或者Ⅲ期的食管鳞癌,术后辅 助放疗能明显改善生存;但最近也有研究认为食 管癌根治术后辅助放疗并没有显示出明显的生存 获益[4]。荟萃分析结果显示对于胸段食管癌术后 辅助治疗没有生存获益[5]。对于所有胸段食管癌 根治术后患者不加选择的应用辅助放疗可能是不 恰当的,笔者回顾了苏州大学附属第三医院放射 肿瘤科222例进展期胸段食管鳞癌术后患者的临 床病理资料,分析PCNA(proliferating cell nuclear antigen)、p53和Nm23蛋白的表达以及术后放疗对 于进展期胸段食管鳞癌的预后意义,探讨影响进 展期胸段食管癌术后放疗疗效的生物学因素。
1 资料与方法 1.1 临床资料收集2005年3月—2009年12月我院222例进展 期胸段食管鳞癌术后病例,其中男177例,女45 例,年龄38~79岁(中位年龄60岁),术后病理均 为鳞状细胞癌。术后病理标本由2名经验丰富的病 理科医师阅片。分期采用AJCC第7版分期标准[6]。 术前未行放化疗。术后接受辅助放疗患者有121 名,未放疗患者有101名。术后放疗患者均在术后 4~6周内开始行三维适形放疗。术后放疗后未行辅 助化疗。放疗前卡氏评分≥70,肝肾功能及血常 规在正常范围,CT或PET/CT检查无脏器转移。
1.2 术后病理肿瘤部位有胸上段25例、胸中段145例、胸下 段43例和多中心9例。TNM分期为Ⅱ期123例、Ⅲ 期99例。病理分级为高分化105例、中分化102例 和低分化15例。脉管癌栓13例,切缘阳性11例。
1.3 放疗方法患者靶区勾画:术后若有残留病灶或残留 转移淋巴结则勾画为GTV,CTV勾画为瘤床、 吻合口和纵隔淋巴引流区。GTV、CTV外放0.5 cm为PGTV和PTV。处方剂量:PGTV照射量为 (60~66)Gy/(30~33)fx,中位照射剂量64 Gy。 PTV照射量为(50~60)Gy/(25~30)fx,中位照 射剂量54 Gy。正常组织限量:脊髓max<45 Gy; 两肺V20<28%、V30<20%,两肺平均剂量<13 Gy;心脏V40<50%;胸腔胃V40<50%。
1.4 免疫组织化学检测p53、PCNA、Nm23单克隆抗体和SP试剂盒均 为福州迈新生物技术公司产品。常规福尔马林固 定标本,石蜡包埋并切片,免疫组织化学用SP法,用 已知阳性的乳腺癌标本作阳性对照,磷酸缓冲液 (PBS)代替一抗作阴性对照。免疫组织化学结 果评价标准:随机选择5个视野,总共计数500个 细胞,无细胞着色为0分,≥1%~20%细胞着色计1 分,≥20%~50%细胞着色计2分,≥50%以上细胞 着色计3分。阳性染色强度按以下标准区分:无棕 黄色计0分,微弱棕黄色计1分,中等强度棕黄色 计2分,深棕色计3分。将上述两种评分之积作为 评判标准,分数为0~1者视为阴性表达,≥2分者 作为阳性表达。
1.5 统计学方法数据分析采用SPSS 17.0软件。以Chi-Square 和Fisher-exact检验有关因素和复发转移的相关 性,并将P<0.2的因素纳入Binary logistic回归模型 Forward法进行多因素分析复发或转移的影响因 素。以Kaplan-Meier法估计生存率,Log rank 法 检验生存差异和单因素生存分析。Cox回归模型 Forward法进行多因素生存分析。P<0.05为差异有 统计学意义。
2 结果 2.1 患者随访结果截至2012年12月31日,随访3~93月(中位随 访时间31月),失访6例,随访率 97.3%。至随访 截止日58.6%(130/222)患者死亡,其中死于复 发或转移124例、其他非肿瘤性疾病4例、第二原 发癌2例。总计发生食管癌复发或转移138例(其 中区域淋巴结转移53例、肝转移12例、肺转移13 例、胸膜转移5例、脑转移4例、骨转移3例、吻合 口复发3例、其他4例、多发性转移41例)。
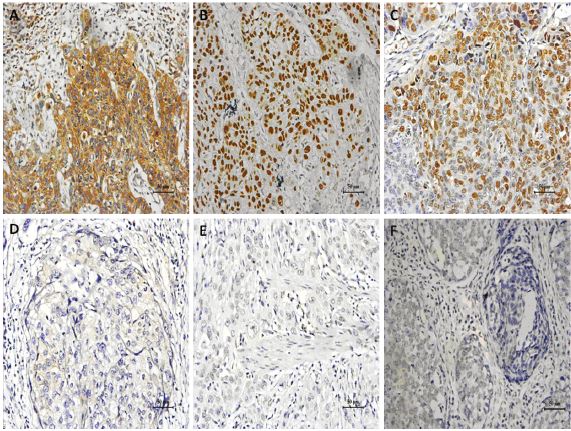
2.2 免疫组织化学检测结果PCNA和p53表达在肿瘤细胞核内,呈棕黄色 颗粒。而Nm23表达在胞质,呈黄色颗粒,见图 1。 PCNA阳性表达率为35.6%(79/222),p53阳性 表达率为55.4%(123/222),Nm23阳性表达率为 70.7%(157/222)。
|
| A-C: positive expression,D-F: negative expression; A,D:expression of Nm23; B,E: expression of p53; C,F:expression of PCNA 图 1 Nm23、p53和PCNA在进展期胸段食 管鳞癌患者中的表达(×200) Figure 1 Positive expression and negative expression of Nm23,p53 and PCNA(×200) |
PCNA与p53的表达水平均与肿瘤细胞病理分级密切相关;分化程度越差,PCNA和p53阳性表 达率越高。Nm23的表达与临床病理因素无明显相 关性,见表 1。
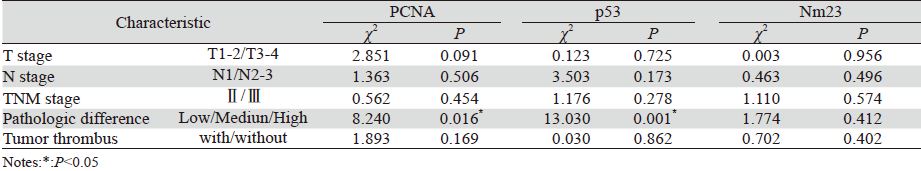 |
Chi-square检验显示PCNA阳性、p53阳性、 肿瘤分化差、分期晚以及未辅助放疗的进展期胸 段食管鳞癌患者术后的复发或远处转移率明显提 高。Binary多因素分析显示PCNA、p53表达、肿瘤 分期和辅助放疗是影响进展期胸段食管鳞癌患者 术后局部复发或远处转移的独立因素,病理分级 和脉管癌栓间未达统计学意义,见表 2。
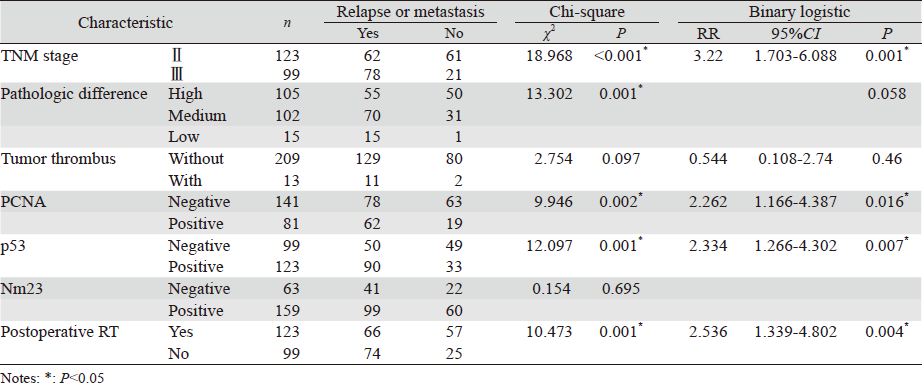 |
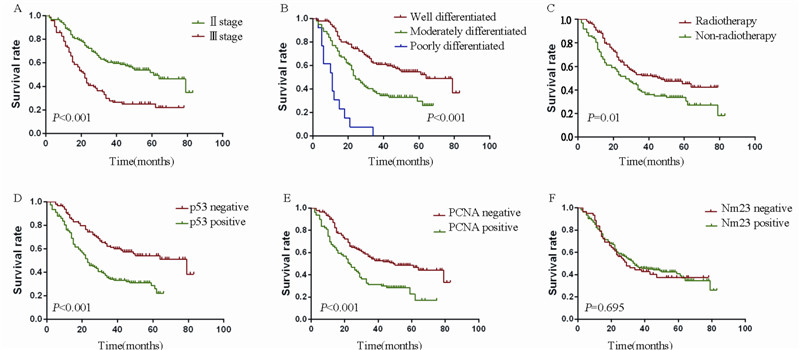
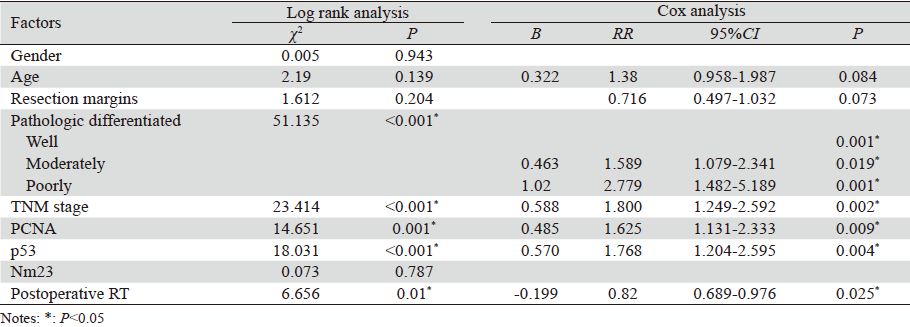
全组3、5年生存率分别为45.8%、40%。中 位生存期为33月。Ⅱ、Ⅲ期患者5年生存率分别 为51.8%和25.1%(Ρ<0.001)。术后放疗组和单 独手术组患者5年生存率分别为45.3%和33.6% (Ρ=0.01)。高、中、低分化组患者5年生存率 分别为54.9%、29.8%和0%(Ρ<0.001)。p53阴 性和p53阳性患者5年生存率分别为54.3%和28.9% (Ρ<0.001)。PCNA低表达和PCNA高表达组患 者5年生存率分别为48.7%和22.8%(Ρ=0.001)。 Log rank单因素分析显示PCNA表达、p53表达、术 后放疗、肿瘤病理分级和TNM分期是影响进展期 胸段食管鳞癌术后患者总生存率的预后因素,而 性别、年龄、发生部位和Nm23表达不影响预后。 Cox多因素分析显示PCNA表达(Ρ=0.009)、p53 表达(Ρ=0.004)、术后放疗(Ρ=0.025)、病理分 级(Ρ=0.001)和TNM分期(Ρ=0.002)是影响进展 期胸段食管鳞癌患者术后总生存率的独立预后因 素,见图 2、表 3。
|
| A:TNM stage; B:differentiation; C:radiotherapy; D:p53 expression; E:PCNA expression; F: Nm23 expression 图 2 TNM分期、术后放疗和病理分级以及PCNA、p53和Nm23表达对进展期期胸段食管鳞癌术后的生存影响 Figure 2 The impact of TMN stage,adjuvant radiotherapy,pathological grading,PCNA,p53 and Nm23 expression on the prognosis of advanced thoracic esophageal squamous cell carcinoma patients after operation |
 |
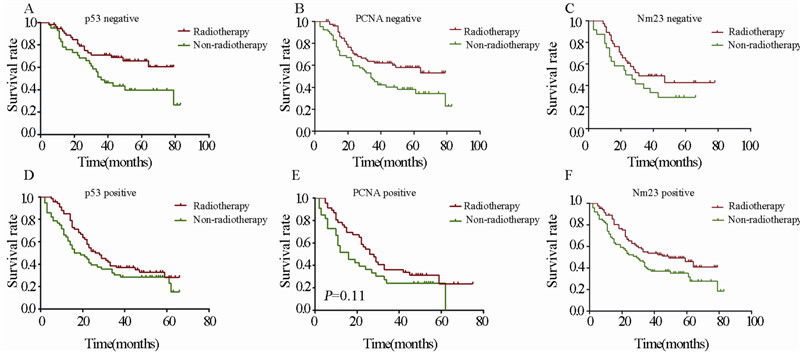
p53阴性组患者术后放疗较未放疗明显提高了 5年生存率(65.9% vs. 39.7%,Ρ=0.02)。p53阳性 组患者术后放疗与未放疗的5年生存率比较差异无 统计学意义(28.1% vs. 28.6%,Ρ=0.13)。PCNA阴 性组患者术后放疗较未放疗明显提高了5年生存率 (58.1% vs. 38.3%,Ρ=0.01)。PCNA阳性组患者 术后放疗与未放疗的5年生存率比较差异无统计学 (23.5% vs. 24.2%,Ρ=0.11)。Nm23阴性组患者术 后放疗与未放疗的5年生存率比较差异无统计学明 显(44% vs. 35.1%,Ρ=0.089)。Nm23阳性组患者术后放疗与未放疗的5年生存率比较差异无统计学 意义(42.9% vs. 33.3%,Ρ=0.187),见图 3。
|
| A-C:negetive expression of p53,PCNA and Nm23; D-E:positive expression of p53,PCNA and Nm23 图 3 术后辅助放疗对PCNA、p53和Nm23阴性和阳性表达患者的生存影响 Figure 3 The impact of adjuvant radiotherapy on the prognosis of patients with negative and positive expression of PCNA, p53 and Nm23 |
放疗不良反应在可接受范围内,总计出现3级 急性放射性肺炎1例、吻合口漏1例、吻合口狭窄 需要进行扩张者6例,未出现胸腔胃溃疡大出血。
3 讨论食管癌术后放疗可以杀灭手术后残留的临 床病灶和淋巴引流区的微转移灶,降低局部复发 率,但是食管癌根治术后辅助放疗对提高生存期 的作用目前还有争议。Xiao等[2]报道对于可切除 的进展期胸段食管鳞癌,术后辅助放疗能明显改 善Ⅲ期患者长期生存,术后放疗后的5年生存率为 35.1%明显优于单独手术组的13.1%;本研究中术 后放疗组患者5年生存率45.3%明显优于单独手术 组的33.6%,与上述研究相仿。也有研究[4]认为对 于食管癌根治术后有淋巴结转移的患者辅助放疗 并没有显示出明显的生存获益,但是这项研究没 有对不同分期患者进行分层分析。Malthaner等[5]荟 萃分析结果显示胸段食管癌术后辅助治疗没有生 存获益,因为该项研究所纳入的临床研究病例数 较少,而且放疗多采用二维放疗技术,所以其结 果值得商榷。对于胸段食管鳞癌术后是否需要辅 助放疗,尤其是进展期胸段食管鳞癌患者,需要分 析生物学指标以区分能从辅助放疗中获益的患者。 本研究结果提示PCNA和p53表达是预测本组食管 鳞癌患者术后放疗后预后的重要生物学因素。
PCNA是细胞周期标志蛋白,参与DNA复制、 修复,调控细胞周期,促进细胞增殖[7]。PCNA可 以在多种恶性肿瘤中高表达,有研究表明PCNA 参与食管癌的发生和进展[8]。Kii等[9]报道Ⅱ~Ⅲ期 食管鳞癌的PCNA阳性表达率为37%,但未提及 PCNA表达与临床病理因素的相关性。本组患者 PCNA阳性率与之相仿,PCNA表达与食管癌细胞 分化程度和复发转移相关,PCNA阳性患者分化程 度较阴性患者差,并且复发转移风险也明显高于 阴性患者。有报道表明PCNA表达与不能手术切除 的食管癌根治性放疗后的预后相关,PCNA低表达 者根治性放疗后的预后较好[9, 10],目前以往还没有 PCNA表达与可切除的胸段食管鳞癌术后放疗预后 的相关报道。本研究结果表明PCNA阴性的胸段食 管鳞癌术后放疗后的预后更好,其术后放疗后的5 年生存率为58.1%,相反阳性患者仅为23.5%。而 且PCNA阳性组患者术后放疗与未放疗的5年生存 率比较无明显差异。本研究结果表明PCNA阴性 的食管鳞癌患者术后可以给予辅助放疗,而对于 PCNA阳性的患者,术后放疗后的预后仍较差,需 要寻求更好的治疗方法。
抑癌基因p53主要参与DNA修复、调控细胞周 期和诱导细胞凋亡,维持基因组稳定和抑制肿瘤 生长。抑癌基因p53的突变导致原有野生型p53功 能丧失,并促进肿瘤细胞增殖、侵袭和转移,与 多种肿瘤的发生和进展有关[11]。以往研究报道在食管癌中p53的阳性率在30%~49.8%[12, 13, 14, 15],本组患 者p53表达率高达55.4%,考虑是p53阳性评价标准 差异所致。Lam等[12]研究表明在食管鳞癌中p53表 达与肿瘤分化程度密切相关。我们的结果也显示 p53的表达与临床病理因素有密切相关性。一项小 样本研究报道p53表达是胸段食管癌术后放化疗的 预后因素,p53阴性患者的预后优于p53阳性患者[13]。 但有研究表明p53表达与局部晚期食管鳞癌放化疗 后的预后无关[14],另一项研究也表明p53表达与食 管癌术后生存无关[15]。上述研究结果不一致考虑 与研究对象选择差异有关。而本研究结果提示p53 表达是影响进展期胸段食管癌患者术后复发或转 移的独立预后因素,p53表达阴性患者的预后明显 较p53阳性患者要好,而且p53表达能够预测进展 期胸段食管鳞癌术后放疗的疗效,p53表达阴性患 者术后放疗明显比p53表达阳性患者获益更大(5 年生存率65.9% vs. 28.1%)。反之,p53阳性患者 术后放疗与未放疗的5年生存率比较无明显差异, 对于p53阳性患者需要联合化疗或靶向治疗以提高 疗效。
Nm23编码产物为核苷二磷酸激酶,与肿瘤转 移、血管生成、细胞凋亡和DNA突变等密切相关[16]。 刘静等[17]报道Nm23低表达与食管鳞癌术后预后不 良有关,但其他研究[18, 19]报道Nm23表达与食管癌 临床病理特征无明显相关性,也与食管癌术后生 存无关。本研究同样提示Nm23表达不影响胸段食 管鳞癌患者术后放疗后的复发或转移,与进展期 胸段食管鳞癌患者术后的病理特征和预后也无明 显相关性。
总之,PCNA和p53表达状态以及术后放疗是 影响进展期胸段食管鳞癌术后的关键预后因素, 但是Nm23表达状态不影响进展期胸段食管鳞癌术 后的预后。术后放疗能明显改善进展期胸段食管鳞 癌术后患者的预后,PCNA和p53表达阴性的进展期 胸段食管鳞癌患者术后辅助放疗的临床获益更大。
| [1] | Almhanna K, Strosberg JR. Multimodality approach for locally advanced esophageal cancer[J]. World J Gastroenterol, 2012, 18 (40): 5679-87. |
| [2] | Xiao ZF, Yang ZY, Liang J, et al. Value of radiotherapy after radical surgery for esophageal carcinoma: a report of 495 patients[J]. Ann Thorac Surg, 2003, 75 (2): 331-6. |
| [3] | Xiao ZF, Yang ZY, Miao YJ, et al. Influence of number of metastatic lymph nodes on survival of curative resected thoracic esophageal cancer patients and value of radiotherapy: report of 549 cases[J]. Int J Radiat Oncol Biol Phys, 2005, 62 (1): 82-90. |
| [4] | Li Q, Wu SG, Gao JM, et al. Impact of esophageal cancer staging on overall survival and disease-free survival based on the 2010 AJCC classification by lymph nodes[J]. J Radiat Res, 2013, 54 (2): 307-14. |
| [5] | Malthaner RA, Wong RK, Rumble RB, et al. Neoadjuvant or adjuvant therapy for resectable esophageal cancer: a systematic review and meta-analysis[J]. BMC Med, 2004, 2: 35. |
| [6] | Rice TW, Blackstone EH, Rusch VW. 7th edition of the AJCC Cancer Staging Manual: esophagus and esophagogastric junction[J]. Ann Surg Oncol, 2010, 17 (7): 1721-4. |
| [7] | Strzalka W, Ziemienowicz A. Proliferating cell nuclear antigen (PCNA): a key factor in DNA replication and cell cycle regulation[J]. Ann Bot, 2011, 107 (7): 1127-40. |
| [8] | Kimos MC, Wang S, Borkowski A, et al. Esophagin and proliferating cell nuclear antigen (PCNA) are biomarkers of human esophageal neoplastic progression[J]. Int J Cancer, 2004, 111 (3): 415-7. |
| [9] | Kii T, Takiuchi H, Kawabe S, et al. Evaluation of prognostic factors of esophageal squamous cell carcinoma (stage II-III) after concurrent chemoradiotherapy using biopsy specimens[J]. Jpn J Clin Oncol, 2007, 37 (8): 583-9. |
| [10] | Sugahara S, Ohara K, Takahashi A, et al. Prognostic significance of the PC10 index for patients with stage II and III oesophageal cancer treated with radiotherapy[J]. Acta Oncol, 1999, 38 (8): 1057-62. |
| [11] | Muller PA, Vousden KH. p53 mutations in cancer[J]. Nat Cell Biol, 2013, 15 (1): 2-8. |
| [12] | Lam KY, Loke SL, Chen WZ, et al. Expression of p53 in oesophageal squamous cell carcinoma in Hong Kong Chinese[J]. Eur J Surg Oncol, 1995, 21(3): 242-7. |
| [13] | Tachibana M, Yoshimura H, Kinugasa S, et al. Postoperative chemotherapy vs. chemoradiotherapy for thoracic esophageal cancer: a prospective randomized clinical trial[J]. Eur J Surg Oncol, 2003, 29 (7): 580-7. |
| [14] | Shimoji H, Miyazato H, Nakachi A, et al. Expression of p53, bcl-2, and bax as predictors of response to radiotherapy in esophageal cancer[J]. Dis Esophagus, 2000, 13 (3): 185-90. |
| [15] | Yamamoto Y, Yamai H, Seike J, et al. Prognosis of esophageal squamous cell carcinoma in patients positive for human epidermal growth factor receptor family can be improved by initial chemotherapy with docetaxel, fluorouracil, and cisplatin[J]. Ann Surg Oncol, 2012, 19 (3): 757-65. |
| [16] | Boissan M, Dabernat S, Peuchant E, et al. The mammalian Nm23/ NDPK family: from metastasis control to cilia movement[J]. Mol Cell Biochem, 2009, 329 (1-2): 51-62. |
| [17] | Liu J, Wang YK, Liu Y, et al. The effect of postoperative chemotherapy after esophagectomy on the survival rate to patients with original squamous cell carcinoma of esophagus[J]. Zhonghua Liu Xing Bing Xue Za Zhi, 2004, 25 (4): 346-50. [刘静, 王永康, 刘莹, 等.术后辅助化疗对食管鳞状细胞癌患者生存率的影响[J]. 中华流行病学杂志, 2004, 25 (4): 346-50.] |
| [18] | Szumilo J, Skomra D, Chibowski D, et al. Immunoexpression of nm23 in advanced esophageal squamous cell carcinoma[J]. Folia Histochem Cytobiol, 2002, 40 (4): 377-80. |
| [19] | Sarris M, Konopka M, Lee CS. Differential expression of the nm23 protein in the progression of oesophageal adenocarcinoma[J]. Pathology, 2003, 35 (1): 37-41. |
 2014, Vol. 41
2014, Vol. 41


