文章信息
- 细胞周期蛋白G2在人甲状腺乳头状癌K1细胞中的表达及其对K1细胞增殖凋亡的影响
- CCNG2 Expression and Its Effect on Proliferation and Apoptosis of Thyroid Papillary Cancer K1 Cells
- 肿瘤防治研究, 2017, 44(7): 460-464
- Cancer Research on Prevention and Treatment, 2017, 44(7): 460-464
- http://www.zlfzyj.com/CN/10.3971/j.issn.1000-8578.2017.16.1088
- 收稿日期: 2016-09-05
- 修回日期: 2017-03-08
甲状腺癌是内分泌系统及头颈部肿瘤中最常见的恶性肿瘤。每年新发恶性肿瘤病例中甲状腺癌病例占1%~5%。据流行病学研究显示近30年来,甲状腺癌发病率在全球范围内呈持续快速增长趋势[1]。目前甲状腺癌的治疗以手术为主,但术后患者常常面临喉返神经损伤、甲状旁腺功能低下及终身服用促甲状腺激素(TSH)抑制剂带来的多种并发症风险,同时甲状腺癌易复发,20%的甲状腺癌患者会面临二次手术或多次手术的风险[2]。基于目前甲状腺癌的发病现状及治疗的局限性,提示要取得甲状腺癌治疗的新进展就要在分子水平方面对甲状腺癌发病机制做深入研究。CCNG2是细胞周期蛋白家族的一员,由Horne等[3]于1997年首先报道了关于CCNG2克隆的研究。与其他细胞周期蛋白不同的是CCNG2负向调控细胞周期、抑制肿瘤细胞增殖[4-5]。由于其特殊的对抗肿瘤的作用及发现较晚成为近来科学家研究的新热点。本研究探讨了CCNG2对甲状腺乳头状癌K1细胞增殖、凋亡的影响,并进一步研究CCNG2与癌症发生相关信号通路的关系,期望部分阐明其负性调控细胞周期的机制,为以CCNG2为靶点的甲状腺癌治疗提供实验依据。
1 材料与方法 1.1 细胞株及试剂甲状腺乳头状癌细胞(K1)购自欧洲细胞培养中心。基因合成pEGFP-N1-CCNG2(上海吉玛制药有限公司),质粒提取试剂盒和Lipofectamine2000脂质体转染试剂盒(美国Invitrogen公司),Opti-MEMI减血清培养液(美国Gibco公司),四甲基偶氮唑蓝(MTT)(美国Sigma公司),Annexin V FITC PI(美国BD公司),兔抗人CCNG2抗体(英国EterLife公司),兔抗人P53抗体和兔抗人MDM2抗体(美国Affinity公司)。
1.2 建立CCNG2基因过表达的K1细胞株根据GenBank数据库人CCNG2基因序列(NM_004345.2)由上海吉玛公司设计并合成载入了CCNG2基因的质粒pEGFP-N1-CCNG2。取对数生长期K1细胞100 μl接种于96孔板,用含10%胎牛血清的RPMI1640培养液,置于37℃、5%CO2饱和湿度培养箱中培养,待细胞生长融合度达80%~90%时准备接受转染,根据Lipofectamine2000说明书推荐设置不同比例的质粒与转染试剂转染K1细胞,转染24 h后在倒置荧光显微镜下观察荧光,筛选最佳质粒与转染试剂Lipofectamine2000转染比例为0.2 μg DNA:1 μl Lipofectamine2000=1:5;以最佳比例转染不同融合度细胞,转染24 h后在倒置荧光显微镜下观察荧光,筛选出最佳转染细胞融合度为50%~60%。以上筛选结果作为后续实验转染条件。
1.3 MTT比色法检测细胞增殖取对数生长期的K1细胞,以每孔100 μl约1×105个细胞的密度接种于96孔板。实验分组:实验组(转染CCNG2基因质粒组)、阴性对照组(转染空载质粒)、空白对照组(未转染组)。分别于转染24、48、72、96 h时取出相应的96孔板,加入MTT溶液(5 mg/ml)10 μl,37℃反应4 h。吸弃各孔中培养液,每孔加入DMSO 100 μl,充分振荡溶解结晶。酶标仪检测吸光度值(A值),检测波长为490 nm,调零孔设定为加DMSO不加细胞的孔。测得各组3个A值取均数表示细胞的增殖情况,并绘制生长曲线,计算生长抑制率。生长抑制率(%)=(A值空白对照组-A值实验组)/A值空白对照组×100%。上述实验至少重复三次。
1.4 流式细胞术检测细胞凋亡常规细胞传代于25 cm2细胞培养瓶中,细胞生长融合度达50%~60%时进行转染。实验分组同1.3。转染48 h后消化、收集、洗涤细胞。1×Binding Buffer重悬细胞,使细胞浓度为每毫升1×106个。取100 μl细胞悬液,约1×105个细胞于5 ml离心管中,分别加入5 μl Annexin V FITC和5 μl PI。轻柔混合细胞与染料,避光、常温(25℃)孵育15 min。各组加入400 μl 1×Binding Buffer于1 h内上流式细胞仪检测细胞凋亡情况。实验重复三次。
1.5 Western blot检测CCNG2、MDM2、P53蛋白表达情况实验分组同1.3。分组提取细胞总蛋白,收集、洗涤细胞,RIPA裂解细胞,4℃、14 000 r/min离心15 min,取上清液,-80℃保存备用。Bradford蛋白定量试剂盒测定蛋白浓度。按每孔蛋白上样量50 μg进行SDS-PAGE电泳,稳压冰浴电转至硝酸纤维素膜。5%脱脂奶粉室温封闭1 h,一抗孵育4℃过夜(CCNG2 1:200,P53 1:500,MDM2 1:500,GAPDH 1:1000),漂洗,二抗(1:5 000)37℃孵育2 h。BioRad凝胶成像系统成像,图像分析软件测定条带灰度值(OD值),目的蛋白与GAPDH的OD值的比值代表蛋白质的相对表达量。
1.6 免疫组织化学染色法检测CCNG2、MDM2、P53蛋白表达情况制备爬片置于6孔板,取对数生长期的细胞种板。转染48 h后染色。按照免疫组织化学试剂盒说明书操作。4%多聚甲醛中浸泡1 h固定爬片,PBS洗涤爬片。梯度酒精脱水。3%H2O2、室温孵育10 min,消除内源性过氧化酶的活性,PBS洗涤。柠檬酸高压修复抗原,PBS洗涤。滴加山羊血清室温封闭20 min,PBS洗涤。CCNG2、MDM2、P53抗体(稀释比例1:200),湿盒内4℃过夜。次日取出湿盒,PBS洗涤。生物素化二抗,37℃恒温箱孵育30 min,PBS洗涤。滴加辣根过氧化物酶标记的链霉卵白素,37℃恒温箱孵育30 min,PBS洗涤。DAB显色,梯度酒精脱水,二甲苯透明,中性树胶封片,图像采集。
1.7 统计学方法以上实验均重复3次或以上,结果以均数±标准差(x±s)表示。计量资料行正态性检验及方差齐性检验后采用方差分析,多组数据两两比较采用LSD-t检验,所有实验数据均用SPSS17.0统计学软件进行统计学处理,P < 0.05为差异有统计学意义。
2 结果 2.1 转染效率的优化pEGFP-N1-CCNG2转染K1细胞24 h后在倒置荧光显微镜下观察,可见细胞呈绿色荧光,表明已成功转入pEGFP-N1-CCNG2质粒。不同比例DNA与转染试剂Lipofectamine2000混合转染细胞,转染效率有差异,其中DNA(μg):Lipofectamine2000(μl)为1:5时转染效率最高,达(77.33±3.79)%(P=0.000);以DNA(μg):Lipofectamine2000(μl)为1:5的不同细胞融合度接受转染时,转染效率有差异,以细胞融合度达50%~60%时转染效率最佳,为(90.33±1.53)%(P=0.000)。
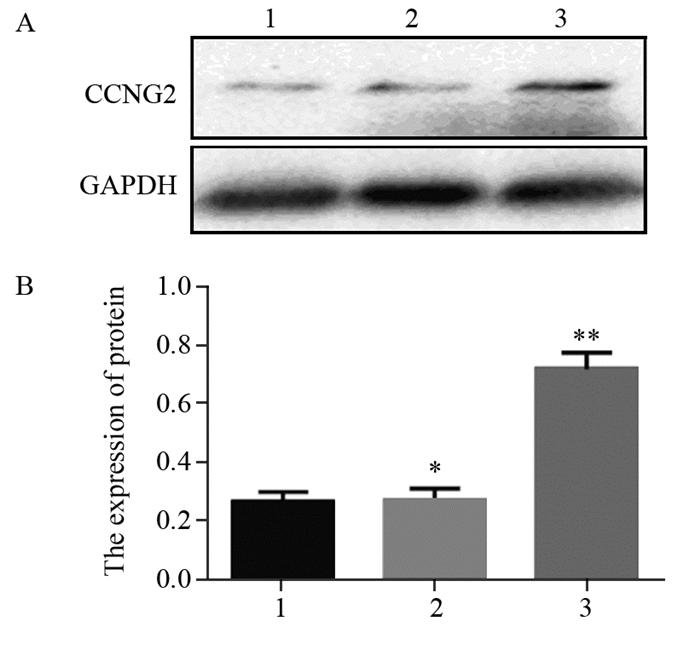
2.2 CCNG2基因过表达检测结果转染48 h后,实验组CCNG2蛋白相对表达量较空白对照组、阴性对照组显著升高(0.72±0.053)vs.(0.36±0.032)、(0.37±0.040)(P=0.000, P=0.000),空白对照组、阴性对照组之间比较差异无统计学意义(P=0.376)。说明成功地将CCNG2基因转染K1细胞并建立CCNG2过表达的甲状腺乳头状癌K1细胞系,见图 1。
|
| 1: blank control group; 2: negative control group; 3: cells transfected with CCNG2; **: P < 0.05, compared with blank control and negative control group; *: P > 0.05, compared with blank control group 图 1 Western blot检测各组PTC K1细胞CCNG2蛋白表达情况 Figure 1 Expression of CCNG2 protein in each group of PTC K1 cells detected by Western blot |
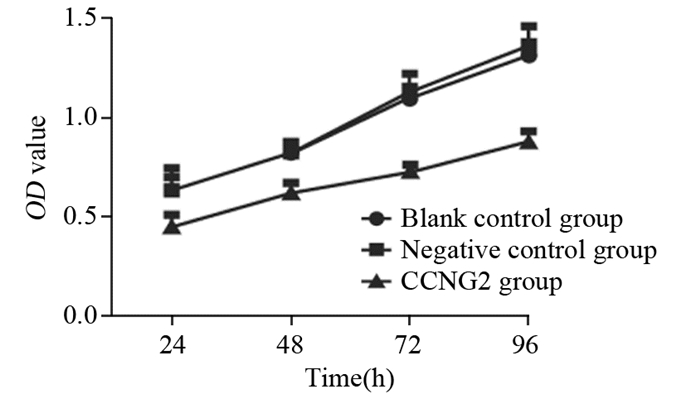
分别于转染24、48、72、96 h时MTT检测细胞增殖情况,计算生长抑制率,实验组各时间点抑制率分别为29.69%、25.30%、35.40%、32.51%,于转染72 h生长抑制最明显。实验组与对照组相比抑制作用明显,差异有统计学意义(P=0.000),空白对照组与阴性对照组比较各点A值差异均无统计学意义(P=0.167),见图 2。
|
| 图 2 不同时间各组PTC K1细胞增殖抑制率曲线 Figure 2 Proliferation inhibition rate curves of PTC K1 cells at different time points in each group |
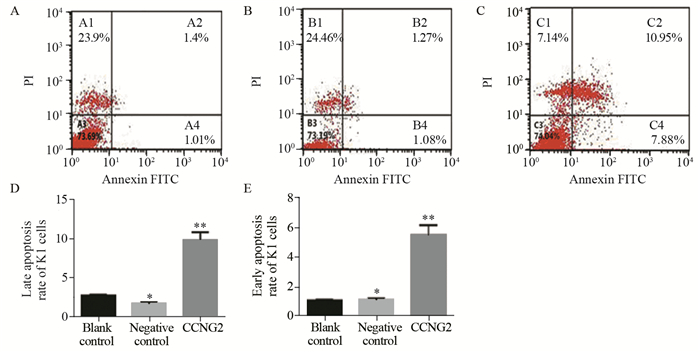
转染48 h后,实验组较空白对照组、阴性对照组早期凋亡率明显升高((5.48±0.35)% vs.(1.06±0.05)%、(1.12±0.09)%)(P=0.000, P=0.000),空白对照组与阴性对照组比较差异无统计学意义(P=0.185);实验组较空白对照组、阴性对照组晚期凋亡率明显升高((9.90±0.94)% vs.(1.98±0.34)%、(1.58±0.28)%)(P=0.000, P=0.000),空白对照组与阴性对照组间比较差异无统计学意义(P=0.095),见图 3。
|
| A: blank control; B: negative control; C: cells transfected with CCNG2; D: the late apoptosis of K1 cells; E: the early apoptosis rate of K1 cells; **: P < 0.05, compared with blank control and negative control group; *: P > 0.05, compared with blank control group 图 3 FCM检测48 h后各组PTC K1细胞早期凋亡与晚期凋亡情况 Figure 3 Late and early apoptosis rates of PTC K1 cells in each group after 48 h detected by FCM |
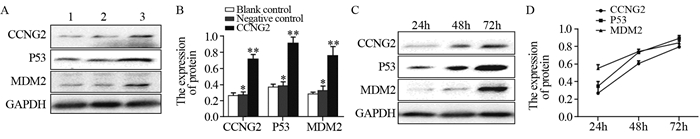
转染48 h后检测CCNG2、P53、MDM2蛋白表达情况,实验组CCNG2蛋白相对表达量较空白对照组、阴性对照组有显著升高(0.72±0.053)vs.(0.36±0.032)、(0.37±0.040)(P=0.000, P=0.000),而两对照组间差异无统计学意义(P=0.376)。P53蛋白相对表达量实验组较空白对照组、阴性对照组明显升高(0.91±0.080)vs.(0.37±0.036)、(0.39±0.047)(P=0.000, P=0.000),两对照组间差异无统计学意义(P=0.295)。MDM2蛋白相对表达量实验组较空白对照组、阴性对照组升高(0.76±0.111)vs.(0.29±0.021)、(0.33±0.058)(P=0.001, P=0.002),两对照组间差异无统计学意义(P=0.162),见图 4A、B。
|
| A: the bands of Western blot in 48 h; C: the bands of Western blot; B, D: the staticstic figure; 1: blank control group; 2: negative control; 3: cells transfected with pEGFP-N1-CCNG2; **: P < 0.05, compared with blank control and negative control group; *: P > 0.05, compared with blank control; the expression of CCNG2, P53 and MDM2 protein were all up-regulated and consistent with CCNG2 protein 图 4 Western blot检测各组PTC K1细胞CCNG2、MDM2和P53蛋白表达情况 Figure 4 Expression of CCNG2, MDM2 and P53 protein in each group of PTC K1 cells detected by Western blot |
分别于转染CCNG2 24、48、72 h后检测CCNG2、P53、MDM2蛋白表达情况,随时间增加CCNG2蛋白相对表达量增加(0.27±0.08)、(0.61±0.03)、(0.80±0.07),各时间点蛋白相对表达量差异有统计学意义(P=0.000),P53及MDM2蛋白相对表达量分别随时间增加而升高,与CCNG2蛋白表达升高具有一致性,见图 4C、D。
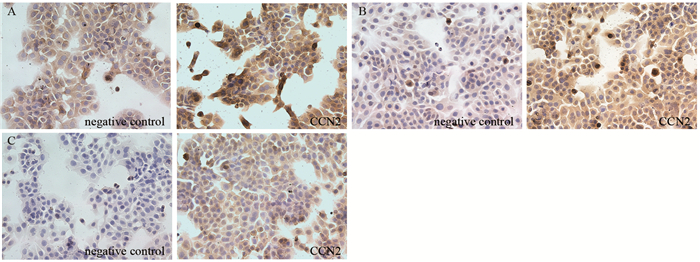
2.6 免疫组织化学染色法结果转染pEGFP-N1-CCNG2 48 h后实验组CCNG2、P53、MDM2蛋白表达阳性水平明显高于对照组,见图 5。
|
| A: the expression of CCNG2 protein; B: the expression of P53 protein; C: the expression of MDM2 protein 图 5 免疫细胞化学染色法检测各组PTC K1细胞CCNG2、MDM2和P53蛋白表达(×400) Figure 5 Expression of CCNG2, MDM2 and P53 protein in each group of PTC K1 cells detected by immunohistochemistry (×400) |
甲状腺癌分子发病机制研究中发现PI3K-AKT、MDM2-P53、RASSF1-MST1-FOXO3、NF-κB、WNT-β-catenin、HIF-1α及甲状腺刺激激素受体信号通路等多条信号通路在甲状腺癌的发病中发挥重要作用[6]。本研究中的关键因子CCNG2就与上述多种信号通路存在密切关系[7-9],结合CCNG2本身所具有的肿瘤负性调控作用,提示其可能成为新的甲状腺癌治疗靶点。本研究利用瞬时转染技术,构建人CCNG2基因过表达的甲状腺乳头状癌K1细胞系,通过对CCNG2转染组与未转染、阴性转染组细胞增殖、凋亡、蛋白表达等的检测探讨CCNG2对甲状腺癌发生、发展的影响。
本研究结果表明,在与对照组(未转染、阴性转染组)的比较中实验组(CCNG2转染组)表现出明显的细胞增殖抑制效应(P < 0.05)。与Sun等在结直肠癌、食管癌、前列腺癌、神经胶质细胞瘤等实验中的研究结果一致[10-14]。流式细胞术检测细胞凋亡实验中,CCNG2过表达的K1细胞在早期及晚期均表现出一定的促凋亡作用(P < 0.05),且以晚期促凋亡作用更明显。
实验转染48 h后检测发现实验组CCNG2、P53蛋白表达水平均明显上调(P < 0.05),相同条件下行免疫组织化学实验可见实验组染色阳性明显,与Western blot实验结果一致。进一步实验中分别用Western blot法检测转染pEGFP-N1-CCNG2质粒24、48、72 h后,发现CCNG2蛋白表达量持续增加,同时检测到P53蛋白的一致性增加,与已有报道对CCNG2基因具有肿瘤负性调控作用的研究结果一致[10, 13],结合本实验结果推测这种负性肿瘤调控作用很可能是通过上调抑癌基因P53的表达实现的。我们同时检测到在CCNG2过表达的K1细胞中MDM2表达上调,且随着CCNG2表达增加,MDM2表达出现一致性增加。这一结果看似与MDM2-P53信号途径作用结果矛盾,考虑由于MDM2与P53的相互作用在一个平衡的体系中,表达情况取决二者相对表达水平,过量的P53积累可激活MDM2转录、表达。二者的相互作用可能还受到其他多种因素直接或间接影响,这将是进一步研究CCNG2在肿瘤细胞增殖、凋亡中的作用的新方向。
综上所述,本研究发现CCNG2基因能够抑制甲状腺乳头状癌K1细胞增殖、促进K1细胞的凋亡。同时CCNG2能够上调抑癌基因P53蛋白的表达水平,因此推测CCNG2负性调控肿瘤细胞的作用部分原因为上调P53蛋白的表达。作为近来研究的热点,细胞周期家族新成员CCNG2的作用及对细胞周期的调控机制还有诸多有待研究的问题,随着研究的不断深入,CCNG2将有望成为未来对抗肿瘤的新“武器”。
| [1] | Fortuny JV, Guigard S, Karenovics W, et al. Surgery of the thyroid: recent developments and perspective[J]. Swiss Med Wkly, 2015, 145: w14144. |
| [2] | Edafe O, Wadsley J, Harrison BJ, et al. Treatment related morbidity in differentiated thyroid cancer-a survey of clinicians[J]. Thyroid Res, 2014, 7(1): 3. DOI:10.1186/1756-6614-7-3 |
| [3] | Horne MC, Donaldson KL, Goolsby GL, et al. Cyclin G2 is up-regulated during growth inhibition and B cell antigen receptor-mediated cell cycle arrest[J]. J Biol Chem, 1997, 272(19): 12650–61. DOI:10.1074/jbc.272.19.12650 |
| [4] | Zimmermann M, Arachchige-Don AS, Donaldson MS, et al. Elevated cyclin G2 expression intersects with DNA damage checkpoint signaling and is required for a potent G2/M checkpoint arrest response to doxorubicin[J]. J Biolog Chem, 2012, 287(27): 22838–53. DOI:10.1074/jbc.M112.376855 |
| [5] | Faradji F, Bloyer S, Dardalhon-Cuménal D, et al. Drosophila melanogaster Cyclin G coordinates cell growth and cell proliferation[J]. Cell Cycle, 2011, 10(5): 805–18. DOI:10.4161/cc.10.5.14959 |
| [6] | Xing M. Molecular pathogenesis and mechanisms of thyroid cancer[J]. Nat Rev Cancer, 2013, 13(3): 184–99. DOI:10.1038/nrc3431 |
| [7] | Bernaudo S, Salem M, Qi X, et al. Cyclin G2 inhibits epithelial-to-mesenchymal transition by disrupting Wnt/β-catenin signaling[J]. Oncogene, 2016, 35(36): 4816–27. DOI:10.1038/onc.2016.15 |
| [8] | Fujimura A, Michiue H, Cheng Y, et al. Cyclin G2 Promotes Hypoxia-Driven Local Invasion of Glioblastoma by Orchestrating Cytoskeletal Dynamics[J]. Neoplasia, 2013, 15(11): 1272–81. DOI:10.1593/neo.131440 |
| [9] | Ramachandiran S, Adon A, Guo X, et al. Chromosome instability in diffuse large B cell lymphomas is suppressed by activation of the noncanonical NF-κB pathway[J]. Int J Cancer, 2015, 136(10): 2341–51. DOI:10.1002/ijc.v136.10 |
| [10] | Sun GG, Zhang J, Hu WN. CCNG2 expression is downregulated in colorectal carcinoma and its clinical significance[J]. Tumor Biol, 2014, 35(4): 3339–46. DOI:10.1007/s13277-013-1440-5 |
| [11] | Chen JQ, Liu CJ, Wen HX, et al. Changes in the expression of cyclin G2 in esophageal cancer cell and its significance[J]. Tumor Biol, 2014, 35(4): 3355–62. DOI:10.1007/s13277-013-1442-3 |
| [12] | Cui DW, Cheng YJ, Jing SW, et al. Effect of cyclin G2 on proliferative ability of prostate cancer PC-3 cell[J]. Tumor Biol, 2014, 35(4): 3017–24. DOI:10.1007/s13277-013-1389-4 |
| [13] | Li WJ, Liu GL, Yu F, et al. CCNG2 Suppressor Biological Effects on Thyroid Cancer Cell through Promotion of CDK2Degradation[J]. Asian Pac J Cancer Prev, 2013, 14(10): 6165–71. DOI:10.7314/APJCP.2013.14.10.6165 |
| [14] | 陈祥龙, 何克菲, 陈筱婷. CCNG2在神经胶质瘤组织中的表达及其临床意义[J]. 中国肿瘤临床, 2014, 14(4): 237–41. [ Chen XL, He KF, Chen XT. Expression and clinical significance of CCNG2 in glioblastoma patients[J]. Zhongguo Zhong Liu Lin Chuang, 2014, 14(4): 237–41. ] |
 2017, Vol. 44
2017, Vol. 44


