慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD)主要累及患者的肺部、心脏等, 为临床上较为常见的疾病。临床研究证实, COPD患者常常伴随肺动脉高压以及肺动脉平滑肌细胞增殖等, 而平滑肌细胞的增殖将导致肺动脉管腔变窄, 气道进一步阻塞, 引起右心室心肌功能受损[1]。有研究表明, 80%左右COPD伴肺动脉高压患者易出现右心衰竭和死亡[2]。抑制平滑肌细胞增殖、抗炎是目前治疗COPD的基本治疗原则和方法。姜黄素具有改善COPD内皮功能的作用[3]。但目前有关姜黄素对肺动脉平滑肌细胞的作用及机制研究报道较少。本研究旨在探讨姜黄素对COPD大鼠平滑肌细胞的作用及其机制, 以期为临床进一步研究该药以及治疗方法提供理论基础。
1 材料与方法 1.1 实验仪器与试剂垂直电泳槽、转移电泳槽购自美国Bio-Rad有限公司, ABI2720实时定量PCR仪和Hema9600基因扩增仪购自美国ABI公司, 酶标仪购自美国Thermo公司, 低温离心机购自美国Thermo Stratos公司, 光学显微镜购自日本Olympus公司。
JAK2、磷酸化(p-) JAK2、SCOS-3单克隆抗体、增殖细胞核抗原(PCNA)、Bax、Bcl-2兔抗鼠抗体购自美国Cell Signaling Technology公司, STAT (STAT1、STAT3、STAT5)以及磷酸化STAT (p-STAT1、p-STAT3、p-STAT5)单克隆抗体购自美国Santa Cruz公司, Trizol试剂盒购自美国Invitrogen公司, RNA酶抑制剂购自北京Promega公司。姜黄素购自美国Sigma-Aldrich公司。
1.2 实验动物及分组清洁级雄性Wistar大鼠75只购自安徽医科大学实验动物中心, 平均体质量为(230±20) g, 分笼饲养, 每笼5只, 相对湿度50%左右, 室温25 ℃左右, 光照时间12 h, 每隔1 d更换一次垫料, 保持笼内干燥。所有大鼠随机分为正常对照组, 模型对照组, 姜黄素小剂量组、中剂量组以及大剂量组, 每组15只。本研究获得安徽医科大学伦理委员会批准。
1.3 动物模型的建立参照李泽庚等[4-5]建立的COPD大鼠模型, 每天将大鼠置于恒温[(43±1)℃]水槽中强制性游泳30 min, 而后放到熏烟箱中采用香烟熏1 h, 最后将大鼠放到低氧常温常压装置内7 h, 采用自动化测氧仪监控装置内氧气浓度在(10.0±0.5)%, 造模每周进行6 d。于第7天暂停, 连续造模6周。
姜黄素粉末溶于DMSO中, 配成50 mmol/L的原液并置于-20 ℃冰箱中保存备用。采用DMEM培养基稀释部分原液, 配成实验所需浓度, DMSO的终浓度小于0.1%。大鼠每天造模结束后, 给予口服灌胃处理, 其中正常对照组和模型对照组每天均给予0.9%氯化钠溶液10 mL/kg; 其它组给予不同浓度姜黄素, 即姜黄素小剂量组给予1.0 mol/L姜黄素, 姜黄素中剂量组给予1.5 mmol/L姜黄素, 姜黄素大剂量组给予3 mmol/L姜黄素, 按照10 mL/kg剂量每只大鼠每天灌胃1次, 直到造模结束。所有大鼠均于造模结束次日检测各项指标。
1.4 各组大鼠右心室相关指数的测定 1.4.1 右心室收缩压(right ventricle systolic pressur, RVSP)的测定根据相关参考文献[6], 采用戊巴比妥钠(40 mg/kg)腹腔注射的方式将大鼠麻醉后, 在大鼠右侧颈外静脉插入聚乙烯导管直到肺动脉干, 稳定10 min后, 采用YP101型压力转换传感器以及YSD-4G型生理记录仪检测大鼠平均肺动脉压力, 以mmHg表示(1 mmHg=0.133 kPa)。
1.4.2 右心室肥大指数(right ventricular mass index, RVMI)的测定测定RVSP值后, 将大鼠放血处死, 迅速开胸取出心脏及肺组织。沿房室交界处除去左右心房以及周围大血管, 留取右心室(RV)以及左心室和室间隔(LV+S), 采用滤纸吸干组织中多余的水分并经电子天平分别称取质量, 计算RV质量与(LV+S)质量的比值, 即为RVMI值。
1.5 HE染色法检测肺动脉组织学形态将处死的大鼠左肺组织采用大头针固定在泡沫板上, 并用手术刀在距离肺的尖部0.5 cm处切取肺组织, 并将组织固定在中性甲醛中24 h, 取出后, 经乙醇脱水、石蜡包埋、切片后, 再进行HE染色, 光学显微镜下观察各组肺血管形态。另取直径为100 μm左右的肺动脉, 采用ICM-102细胞图像分析软件对其形态进行定量统计, 以血管壁横断面积占血管横断面积的比值(WA, %)作为衡量低氧肺血管重构的指标。
1.6 免疫组织化学法检测PCNA、凋亡相关蛋白Bcl-2、Bax将处死的大鼠左肺组织采用大头针固定在泡沫板上, 并用手术刀在距离肺的尖部0.5 cm处切取肺组织, 分离剥取直径为100 μm左右的肺动脉, 采用4%的多聚甲醛固定, 石蜡包埋, 制成厚度为5 μm的切片, 免疫组织化学染色; 切片脱蜡, 加入一抗后4 ℃过夜, 再加入二抗, 脱水封片。在显微镜下采用光学显微镜下观察5个不同视野中PCNA、Bcl-2及Bax的阳性细胞数, 然后进行统计分析。
1.7 TUNEL细胞凋亡试剂盒检测平滑肌细胞的凋亡按照TUNEL试剂盒(罗氏公司提供)说明书操作, 将大鼠左侧肺组织进行石蜡包埋、切片后加入20 μg/mL蛋白酶K、0.3%双氧水以及0.1%TritonX-100, 而后加入TUNEL反应液(50 μL TdT+450 μL dUTP)、加入标记荧光素抗体的HRP封闭以及DAB显色试剂盒进行显色, 在光学显微镜下进行镜检。在显微镜下, 随机选取直径在100 μm左右的肺动脉, 统计500个肺动脉平滑肌细胞中凋亡细胞数, 得出凋亡指数(AI), AI (%)=凋亡细胞数/总细胞数×100%。
1.8 蛋白质印迹法检测SOCS-3/JAK2/STAT通路相关蛋白的表达取实验各组左侧肺组织100 mg, 加入200 μL细胞裂解液以及蛋白酶抑制剂后充分匀浆, 将液体吸出置于冰上裂解45 min, 低温离心机以16 069×g, 离心30 min, 取上清液, 采用考马斯亮蓝染色法进行总蛋白质定量。蛋白质样品与5×SDS上样缓冲液混合均匀(体积比为4:1), 100 ℃煮沸7~8 min, 采用10% SDS-PAGE制胶, 在120 V电压, 恒定电流200 mA下进行电泳2 h, 湿转至硝酸纤维膜上, 以5%的脱脂奶粉TBST缓冲液4 ℃封闭过夜, 加入一抗, 即兔抗鼠单克隆抗体SOCS-3、JAK2、p-JAK2、STAT (STAT1、STAT3、STAT5)以及磷酸化STAT (p-STAT1、p-STAT3、p-STAT5)。TBST洗膜三次后, 与结合有辣根过氧化物酶标记的二抗(山羊抗小鼠IgG)室温孵育1 h; 然后再次TBST洗膜三次后, 采用化学发光试剂盒进行显色, X胶片进行曝光显影, 依据胶片扫描所得灰度值进行比较。
1.9 统计学方法采用SPSS 19.0统计软件包对所得数据进行分析以及ImageJ 4.2对图片进行扫描处理。正态分布的计量资料采用均数士标准差(x±s)表示, 组内两两比较用Bonferroni检验, 组间比较采用单因素方差分析, 以P<0.05为差异有统计学意义。
2 结果 2.1 各组大鼠RVSP值、RVMI值比较研究结果显示, 模型对照组RVSP值、RVMI值均高于正常对照组(均P < 0.05);姜黄素大剂量组和中剂量组RVSP、RVMI均低于模型对照组(均P < 0.05), 见表 1。该结果提示, 姜黄素能够降低COPD模型组的RVSP值和RVMI值, 改善肺动脉和血管重塑的病理生理变化。
| (x±s) | |||
| 组别 | n | RVSP (mmHg) | RVMI (%) |
| 正常对照组 | 15 | 15.23±2.35 | 20.19±2.97 |
| 模型对照组 | 15 | 33.67±3.91* | 28.58±3.04** |
| 姜黄素小剂量组 | 15 | 30.98±4.01 | 28.08±3.11 |
| 中剂量组 | 15 | 24.27±3.17# | 23.03±2.47# |
| 大剂量组 | 15 | 24.19±3.08# | 22.77±2.51# |
| RVSP:右心室收缩压; RVMI:右心室肥大指数.与正常对照组比较, *P < 0.05, **P < 0.01;与模型对照组比较, #P < 0.05. | |||
HE染色结果显示, 与正常对照组比较, 模型对照组血管壁增厚、平滑肌细胞数量增多, 核细胞染色加深; 而姜黄素中剂量组和大剂量组细胞壁变薄、平滑肌细胞数量相对较少, 染色较浅, 见图 1。正常对照组, 模型对照组, 姜黄素小剂量组、中剂量组和大剂量组WA分别为(31.5±4.8)%、(63.2±5.5)%、(54.5±4.6)%、(41.8±4.1)%、(40.2±5.0)%, 模型对照组WA高于正常对照组(P < 0.05), 姜黄素中剂量组和大剂量组WA均低于模型对照组(均P < 0.05)。该结果提示姜黄素能够改善COPD模型血管重塑, 减少平滑肌细胞数量。
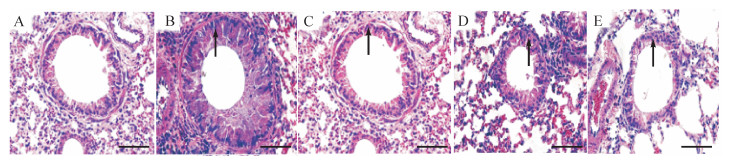
|
| A:正常对照组血管壁及管腔正常; B:模型对照组血管壁明显增厚, 管腔变窄; C:姜黄素小剂量组血管壁变薄; D:姜黄素中剂量组血管壁变薄; E:姜黄素大剂量组血管壁变薄, 管腔增宽.箭头表示血管壁, 标尺=100 μm. 图 1 各组大鼠肺动脉组织形态学改变(HE染色) Fig. 1 Histomorphology changes in pulmonary artery tissues in each group (HE staining) |
模型对照组PCNA、Bcl-2相对表达量高于正常对照组(均P < 0.05), 而Bax相对表达量低于正常对照组(P < 0.05)。姜黄素中剂量组和大剂量组PCNA相对表达量低于模型对照组(均P < 0.05), 而Bax相对表达量高于模型对照组(P < 0.05)。各姜黄素给药组Bcl-2相对表达量与模型对照组差异无统计学意义(P < 0.05), 见表 2、图 2。该结果提示姜黄素能促进Bax表达, 抑制PCNA的表达。
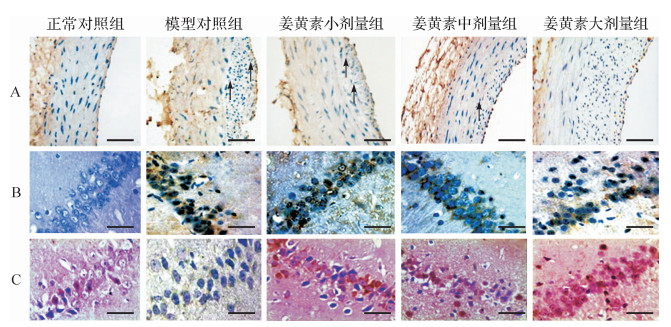
|
| A:免疫组织化学检测PCNA的表达情况.正常对照组呈正常血管组织学形态; 模型对照组可见多数细胞染成棕黄色; 姜黄素小剂量组可见棕黄色细胞数量相对减少; 姜黄素中剂量组可见棕黄色细胞数量明显减少; 姜黄素大剂量组可见棕黄色细胞数量也明显减少.B:免疫组织化学检测Bcl-2的表达情况.模型对照组可见多数细胞染成黄色; 姜黄素小剂量组可见多数细胞质染成黄色; 姜黄素中剂量组可见较多数细胞质染成黄色; 姜黄素大剂量组可见较多数细胞质染成黄色.C:免疫组织化学检测Bax的表达情况.模型对照组可见细胞质褐色颗粒表达显著减少; 姜黄素小剂量组可见细胞质褐色颗粒表达显著增多; 姜黄素中剂量组可见多数细胞质染成褐色; 姜黄素大剂量组几乎全部细胞质染成褐色.黑色箭头指示阳性细胞, 标尺=50 μm.PCNA:增殖细胞核抗原. 图 2 各组免疫组织化学检测PCNA、Bcl-2及Bax的表达情况 Fig. 2 The expressions of PCNA, Bcl-2 and Bax detected by immunohistochemistry in each group |
| (x±s) | ||||
| 组别 | n | PCNA | Bcl-2 | Bax |
| 正常对照组 | 15 | 10.23±1.98 | 9.66±1.26 | 21.36±3.64 |
| 模型对照组 | 15 | 45.69±6.67 | 69.26±9.21 | 6.79±1.23 |
| 姜黄素小剂量组 | 15 | 40.21±5.21 | 64.21±7.36 | 35.77±4.98 |
| 中剂量组 | 15 | 30.17±4.14 | 56.11±5.09 | 38.63±5.24 |
| 大剂量组 | 15 | 15.66±1.94 | 53.28±3.65 | 52.81±6.13 |
| PCNA:增殖细胞核抗原. | ||||
模型对照组平滑肌细胞形态完整、基本无固缩; 姜黄素中剂量组和大剂量组平滑肌细胞出现固缩、细胞内出现空泡, 姜黄素小剂量组基本无变化, 见图 3。定量分析结果显示, 正常对照组, 模型对照组, 姜黄素小剂量组、中剂量组和大剂量组AI分别为(12.70±0.57)%、(1.23±0.22)%、(5.10±0.67)%、(32.40±0.76)%、(33.50±0.49)%, 模型对照组AI低于正常对照组(P < 0.05), 姜黄素中剂量组和大剂量组均高于模型对照组(均P < 0.01)。该结果提示, 姜黄素能够促进肺动脉血管平滑肌细胞凋亡。
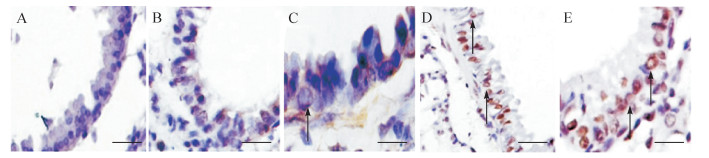
|
| A:正常对照组; B:模型对照组可见细胞形态完整; C:姜黄素小剂量组出现部分平滑肌细胞固缩; D:姜黄素中剂量组可见较多平滑肌细胞固缩、出现空泡; E:姜黄素大剂量组几乎全部平滑肌细胞固缩、出现空泡.箭头指示平滑肌细胞出现固缩、空泡, 标尺=50 μm. 图 3 各组TUNEL检测肺动脉血管平滑肌细胞凋亡情况 Fig. 3 Apoptosis of pulmonary vascular smooth muscle cells in each group |
模型对照组p-JAK2、p-STAT1、p-STAT3蛋白均高于正常对照组(均P < 0.05), SOCS-3蛋白低于正常对照组(P < 0.01), 而p-STAT5与正常对照组差异无统计学意义(P>0.05);各姜黄素给药组p-JAK2蛋白的表达均低于模型对照组(均P < 0.01), SOCS-3蛋白的表达均高于模型对照组(均P < 0.01), 姜黄素大剂量组和中剂量组p-STAT3、p-STAT5蛋白的表达均低于模型对照组(均P < 0.05), 此外, 姜黄素大剂量组p-STAT1低于模型对照组(P < 0.05), 见图 4。该结果提示, 姜黄素可激活SOCS-3/JAK/STAT通路, 促进SOCS-3表达, 而抑制p-JAK2、p-STAT3及p-STAT5蛋白的表达。
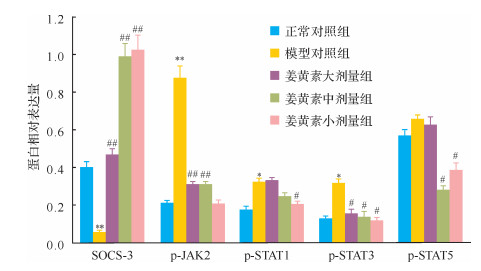
|
| 与正常对照组比较, *P < 0.05, **P < 0.01;与模型对照组比较, #P < 0.05, ##P < 0.01. 图 4 姜黄素对SOCS-3/JAK/STAT蛋白表达的影响 Fig. 4 Effect of curcumin on SOCS-3/JAK/STAT pathway |
COPD主要是由长期气道阻塞导致患者肺泡缺氧以及二氧化碳潴留, 引起肺血管收缩、肺血管重构等临床症状, 严重时可导致肺动脉高血压症、右心衰竭症甚至是死亡[7]。肺血管重塑是导致COPD进一步恶化的关键原因。导致肺血管重塑的原因有慢性炎症、低氧或者缺氧等。低氧导致肺内高血压, 从而促进肺动脉纤维母细胞和内皮细胞的促有丝分裂因子、生长因子的释放, 而这些因子的释放进一步促进平滑肌细胞、成纤维细胞的增殖并进一步刺激细胞外基质的产生, 导致肺动脉血管壁增厚, 加重气道阻塞[8]。肺动脉高压是以肺动脉压力以及肺部血管阻力升高为特点的病理生理综合征, 其主要病理机制为血管收缩、血管重塑, 导致右心室负荷增加, 右心衰竭。RVSP、RVMI是反映肺动脉及血管重塑的指标。本研究结果显示, 模型对照组大鼠RVMI、RVSP明显高于正常对照组, 这也印证了以往的研究结论[9]。COPD患者肺动脉管增厚明显, 管腔明显变窄, 出现WA明显增大, 本研究结果也证实了这一病理变化。
肺动脉平滑肌细胞在胚胎血管发育期为合成表型, 处于增殖状态; 而出生后该细胞由合成表型转为收缩型, 处于静止状态, 主要维持肺部血管的张力和正常血管构型。当机体出现低氧等刺激时, 该细胞则又转化为合成表型, 从而进入增殖状态[10]。研究表明, COPD患者平滑肌细胞增加数量高于非COPD患者[11], 本研究结果也证实, COPD大鼠血管壁增厚、TUNEL染色阳性细胞数少于正常对照组, COPD大鼠AI低于正常对照组, 这些结果均证实COPD大鼠存在明显的血管壁增厚、平滑肌细胞增殖现象。
姜黄素是从传统中药姜黄中提取的主要有效成分, 近年来研究证实其具有抗炎、抗氧化、降血脂的作用[12]; 同时姜黄素具有促进COPD患者内皮祖细胞一氧化氮合酶、一氧化氮释放的作用, 从而改善血管内皮功能[13]。本研究结果证实, 姜黄素中、大剂量组具有抑制COPD大鼠平滑肌细胞增殖、降低细胞中PCNA表达, 改善肺血管重塑, 从而降低RVSP、RVMI的作用; 姜黄素中、大剂量组能够促进促凋亡蛋白Bax表达, 促进肺动脉血管平滑肌细胞凋亡。笔者推测, 姜黄素改善COPD大鼠肺动脉高压的作用可能与其促进平滑肌细胞凋亡的作用有关。
JAK/STAT信号通路是多种细胞因子信号转导的重要途径, 其参与细胞的分化、增殖以及凋亡等环节[14]。JAK为蛋白酪氨酸激酶, 其下游的信号为转录激活子STAT家族, 激活的JAK能够使酪氨酸受体各位点出现磷酸化, 从而与STAT结合, 导致STAT磷酸化。细胞因子信号转达抑制因子(SOCS)家族为JAK/STAT信号通路转导的负向调节蛋白。目前JAK/STAT通路中参与细胞因子与信号转导关系最为密切的是JAK2、STAT1、STAT3、STAT5。有研究证实, JAK2、STAT3参与平滑肌细胞的增殖[15], 也有研究说明JAK2、STAT1以及STAT3均参与炎症反应[16], 而炎症反应是导致平滑肌细胞增殖的一个重要原因。本研究结果显示, 姜黄素中剂量组和大剂量组具有降低JAK2、p-STAT3、p-STAT5蛋白表达, 提高SOCS蛋白表达的作用。氧化低密度脂蛋白、活性氧等因子能够激活JAK/STAT途径而达到基因调控的目的, 其调控的基因有凋亡相关基因(如Fas、Bcl-2、Bax)和炎性相关基因(如COX-2、IL-6等[17]。PCNA为细胞内与DNA合成相关的因子, 能够反映细胞进入增殖周期的情况, 是反映细胞增殖潜能的指标。有研究表明, JAK2/STAT途径能够刺激颗粒细胞, 进而影响PCNA的表达[18]。本研究结果显示, 模型对照组PCNA表达量高于正常对照组, 说明COPD患者肺动脉平滑肌细胞增殖是导致肺动脉高压的一个原因, 而姜黄素能够显著抑制PCNA的表达, 其作用机制可能与JAK2/STAT途径被抑制有关。有研究表明, JAK2特异性抑制剂AG490能够抑制平滑肌细胞凋亡, 促进抗凋亡蛋白Bcl-2的表达[19]。本研究结果提示, 姜黄素中剂量组和大剂量组能够促进Bax的表达, 而对Bcl-2表达影响较小, 从而Bcl-2/Bax比值降低。提示姜黄素促进平滑肌细胞凋亡的作用机制可能通过刺激SOCS/JAK/STAT信号途径, 进而激活下游Bax蛋白的表达、促进平滑肌细胞的凋亡, 最终改善COPD模型大鼠的平均动脉压和RVMI。
本研究结果提示, 姜黄素可以促进COPD模型大鼠平滑肌细胞凋亡, 这一作用机制可能与刺激SOCS/JAK/STAT信号途径, 进而激活下游Bax表达有关, 这为临床COPD研究提供了一定的实验基础, 也为COPD治疗方案调整提供了思路。
| [1] | LIN H H, MURRAY M, COHEN T, et al. Effects of smoking and solid-fuel use on COPD, lung cancer, and tuberculosis in China:a time-based, multiple risk factor, modelling study[J]. Lancet, 2008, 372 (9648) :1473–1483. doi:10.1016/S0140-6736(08)61345-8 |
| [2] | BUSTACCHINI S, CHIATTI C, FURNERI G, et al. The economic burden of chronic obstructive pulmonary disease in the elderly:results from a systematic review of the literature[J]. Curr Opin Pulm Med, 2011, 17 (Suppl 1) :S35–S41. |
| [3] | 黄美健, 朱成圣, 姚航平, 等. 姜黄素对慢性阻塞性肺疾病患者外周血内皮祖细胞数量及功能的影响[J]. 中国临床药学杂志, 2015, 24 (3) : 147–152. HUANG Meijian, ZHU Chengsheng, YAO Hangping, et al. Effects of curcumin on number and function of endothelial progenitor cells derived from peripheral blood of chronic obstructive pulmonary disease patients[J]. Chinese Journal of Clinical Pharmacy, 2015, 24 (3) :147–152. (in Chinese) |
| [4] | 肖诗亮, 高思海, 杨辰垣. 常压缺氧性大鼠肺动脉高压模型的改进[J]. 临床心血管杂志, 2001, 17 (4) : 190. XIAO Shiliang, GAO Sihai, YANG Chenyuan. Improved pressure hypoxic pulmonary hypertension in rats model[J]. Journal of Clinical Cardiology, 2001, 17 (4) :190. (in Chinese) |
| [5] | 李泽庚, 王传博, 彭波, 等. 慢性阻塞性肺疾病痰瘀阻肺证大鼠模型的建立[J]. 天津中医药, 2010, 27 (1) : 43–45. LI Zegeng, WANG Chuanbo, PENG Bo, et al. Establishment of rat model of chronic obstructive pulmonary disease with stagnated phlegm obstructing lung[J]. Tianjin Journal of Traditional Chinese Medcine, 2010, 27 (1) :43–45. (in Chinese) |
| [6] | 丁亚光, 齐建光, 杜军保, 等. 通过微量渗透泵应用肾上腺髓质素对大鼠低氧肺动脉高压的调节作用[J]. 实用儿科临床杂志, 2005, 20 (7) : 628. DING Yaguang, QI Jianguang, DU Junbao, et al. Effect of adrenomedullin subcutaneously administered by mini-osmotic pump on hypoxic pulmonary hypertension in rats[J]. Journal of Applied Clinical Pediatric, 2005, 20 (7) :628. (in Chinese) |
| [7] | NAJJAR I, FAGARD R. STAT1 and pathogens, not a friendly relationship[J]. Biochimie, 2010, 92 (5) :425–444. doi:10.1016/j.biochi.2010.02.009 |
| [8] | MORENO P R, PURUSHOTHAMAN K R, FUSTER V, et al. Intimomedial interface damage and adventitial inflammation is increased beneath disrupted atherosclerosis in the aorta:implications for plaque vulnerability[J]. Circulation, 2002, 105 (21) :2504–2511. doi:10.1161/01.CIR.0000017265.52501.37 |
| [9] | REVERMANN M, NEOFITIDOU S, KIRSCHNING T, et al. Inhalation of the BK (Ca)-opener NS1619 attenuates right ventricular pressure and improves oxygenation in the rat monocrotaline model of pulmonary hypertension[J]. PLoS One, 2014, 9 (1) :e86636. doi:10.1371/journal.pone.0086636 |
| [10] | 张晓丹, 王力维, 王淑静, 等. 葛根素通过调控活性氧对缺氧诱导的PASMCs增殖的影响[J]. 中国中药杂志, 2015, 40 (15) : 3027–3033. ZHANG Xiaodan, WANG Liwei, WANG Shujing, et al. Effect of puerarin on hypoxia induced proliferation of PASMCs by regulating reactive oxygen[J]. China Journal of Chinese Materia Medica, 2015, 40 (15) :3027–3033. (in Chinese) |
| [11] | PARADA A, KLAASSEN J, LISBOA C, et al. Reduction of physical activity in patients with chronic obstructive pulmonary disease[J]. Rev Med Chil, 2011, 139 (12) :1562–1572. doi:10.4067/S0034-98872011001200005 |
| [12] | MOERMANS C, HEINEN V, NGUYEN M, et al. Local and systemic cellular inflammation and cytokine release in chronic obstructive pulmonary disease[J]. Cytokine, 2011, 56 (2) :298–304. doi:10.1016/j.cyto.2011.07.010 |
| [13] | 朱成圣, 黄美健, 梁斌, 等. 姜黄素对COPD患者内皮祖细胞一氧化氮分泌及内皮型一氧化氮合酶表达的影响[J]. 中药药理与临床, 2014, 30 (2) : 168–171. ZHU Chengsheng, HUANG Meijian, LIANG Bin, et al. Effects of curcumin on nitric oxide secretion and endothelial nitric oxide synthase expression in endothelial progenitor cells of COPD patients[J]. Pharmacology and Clinics of Chinese Materia Medica, 2014, 30 (2) :168–171. (in Chinese) |
| [14] | 王霄, 杨易, 刘洁, 等. JAK2-STAT3信号通路在白介素-1β经动脉外膜给药致平滑肌细胞增殖迁移中的作用[J]. 第三军医大学学报, 2012, 34 (6) : 512–517. WANG Xiao, YANG Yi, LIU Jie, et al. Role of JAK2-STAT3 signaling pathway in smooth muscle cell proliferation and migration induced by medication of IL-1β through arterial adventitia in mice[J]. Journal of Third Military Medical University, 2012, 34 (6) :512–517. (in Chinese) |
| [15] | SHIBATA R, KAI H, SEKI Y, et al. Inhibition of STAT3 prevents neointima formation by inhibiting proliferation and promoting apoptosis of neointimal smooth muscle cells[J]. Hum Gene Ther, 2003, 14 (7) :601–610. doi:10.1089/104303403321618128 |
| [16] | HIWATASHI K, TAMIYA T, HASEGAWA E, et al. Suppression of SOCS3 in macrophages prevents cancer metastasis by modifying macrophage phase and MCP2/CCL8 induction[J]. Cancer Lett, 2011, 308 (2) :172–180. doi:10.1016/j.canlet.2011.04.024 |
| [17] | WANG X, SHAW S, AMIRI F, et al. Inhibition of the Jak/STAT signaling pathway prevents the high glucose-induced increase in tgf-beta and fibronectin synthesis in mesangial cells[J]. Diabetes, 2002, 51 (21) :3505–3509. |
| [18] | 王超君, 李冬华, 邢燕, 等. JAK2/STAT通路参与过氧化氢抑制小鼠原代颗粒细胞增殖的研究[J]. 生殖医学, 2015, 24 (4) : 316–321. WANG Chaojun, LI Donghua, XIN Yan, et al. Inhibitory effect of hydrogen peroxide on proliferation of mouse granulosa cells is associated with JAK2/STAT3 pathway[J]. Journal of Reproductive Medicine, 2015, 24 (4) :316–321. (in Chinese) |
| [19] | GROTE K, LUCHTEFELD M, SCHIEFFER B. JANUS under stress-role of JAK/STAT signaling pathway in vascular diseases[J]. Vascul Pharmacol, 2005, 43 (5) :357–363. doi:10.1016/j.vph.2005.08.021 |



