急性颅脑损伤的发病率居高不下,欧洲的发病率为235人/10万[1],北美更是高达790人/10万[2],而我国颅脑创伤的发病率也在200~300人/10万[3],已成为当今社会造成人群致死致残以及情感认知障碍的主要原因[4]。部分患者病情会进一步恶化,呈进展性颅脑损伤,使患者的危险性增加5倍,导致较高的致残率及致死率[5, 6]。研究表明,脑挫裂伤是进展性颅脑损伤的高危因素之一[5, 7, 8]。因此,及早判断进展性颅脑损伤并提前干预,已成为治疗的关键。本研究旨在通过回顾性分析脑挫裂伤患者的临床资料,探讨脑挫裂伤患者发生进展性脑挫裂伤的高危因素及与预后的相关性,从而为临床诊治提供参考依据。
1 对象与方法 1.1 脑挫裂伤纳入标准和剔除标准纳入标准:①有明确的颅脑外伤史;②伤后8 h内行首次颅脑CT检查,24 h 内颅脑CT复查;③首次颅脑CT检查即表现有点片状高密度出血灶,符合脑挫裂伤诊断标准[9]。
剔除标准:①开放性颅脑损伤;②入院后需急诊开颅手术;③合并有胸腹部损伤、四肢及骨盆骨折等多发伤;④休克;⑤年龄18周岁以下或孕妇;⑥入院前已有慢性阻塞性肺疾病、冠状动脉粥样硬化性心脏病、2型糖尿病、血友病、肝病、恶性肿瘤等可能影响凝血功能的慢性疾病;⑦近3个月内有过抗凝治疗。
1.2 进展性脑挫裂伤定义颅脑CT复查显示有脑挫裂伤体积扩大、其他部位新出现脑挫裂伤及新发颅内血肿,且增加的体积为首次颅脑CT检查显示脑挫裂伤体积的30%以上定义为进展性脑挫裂伤[5],见图 1。脑挫裂伤体积及血肿量按公式A×B×C/2(cm3)计算[10],A与B分别代表挫裂伤体积及血肿最大层面的长轴与短轴,C代表病灶厚度;如超过一处病灶,则计算每一处体积的总和。
|
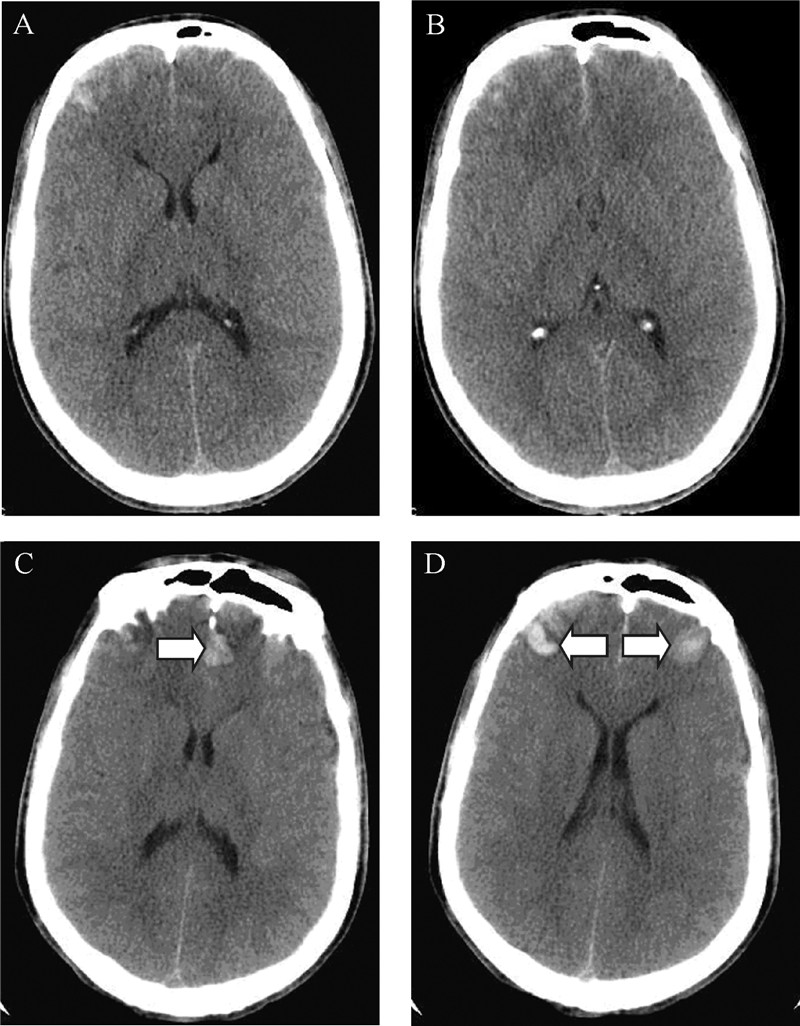
| 图 1 进展性脑挫裂伤CT表现 Fig.1 Computed tomography scans of progressive brain contusion A、B图为患者外伤后50 min行首次颅脑CT检查显示双侧额叶脑挫裂伤;C、D图为距首次颅脑CT检查间隔3 h后复查CT显示双侧额叶脑挫裂伤范围扩大(箭头所示). |
收集2012年1月至2013年10月于浙江萧山医院急诊入院并且行首次颅脑CT检查即发现有脑挫裂伤的颅脑损伤患者共132例,其中男性94例,女性38例,年龄18~83岁。进展组70例,其中男性48例,女性22例,年龄18~77岁;非进展组62例,其中男性46例,女性16例,年龄18~83岁。所有病例至少由两名神经外科主治医师及以上职称医生评估后决定患者的分组。
1.4 观察指标收集两组患者入院时的性别、年龄、受伤原因、格拉斯哥昏迷评分(Glasgow Coma Score,GCS)、受伤至首次颅脑CT检查时间、两次CT检查间隔时间、首次CT检查显示脑挫裂伤及血肿体积、中线移位、是否并有其他类型颅脑损伤(颅骨骨折、创伤性蛛网膜下腔出血、硬膜外血肿、硬膜下血肿)、脑挫裂伤部位、是否合并有高血压病及2型糖尿病、血清低密度脂蛋白胆固醇(LDL-C)水平及凝血功能相关指标如凝血酶原时间(PT)、活化部分凝血活酶时间(APTT)、血浆纤维蛋白原(FDP)、D-二聚体和血小板计数。
1.5 随访及预后判断随访至患者外伤后6个月。根据改良Rankin量表(mRS)评分判断预后,mRS≥4分为预后不良,mRS<4分为预后良好[11]。
1.6 统计学方法采用SPSS 20.0统计软件进行统计学处理,计量资料以均数±标准差(±s)表示,组间比较行独立样本t检验;计数资料行χ2检验;对可能的危险因素进一步行多因素Logistic回归分析;P<0.05表示差异有统计学意义。
2 结 果 2.1 影响进展性脑挫裂伤发生单因素分析对是否进展性脑挫裂伤两组相关因素进行单因素分析,结果患者入院时GCS、首次颅脑CT检查显示脑挫裂伤体积、中线移位、合并有颅骨骨折、蛛网膜下腔出血、硬膜外血肿、硬膜下血肿、脑挫裂伤部位、D-二聚体、合并有2型糖尿病这些因素差异有统计学意义(均P<0.05)。而患者的年龄、性别、病因、受伤至首次CT检查时间间隔、两次CT检查间隔时间、PT、APTT、FDP、血小板计数、LDL-C、是否合并高血压病等因素差异则无统计学意义(均P>0.05)。见表 1。
| [(±s)或n(%)] | ||||
| 因 素 | 非进展组(n=62) | 进展组(n=70) | 检验值 | P值 |
| 年龄(岁) | 46.77±17.71 | 51.43±18.55 | -1.039 | 0.303 |
| 性别构成 男性 | 46(74.2) | 48(68.6) | 0.507 | 0.476 |
女性 | 16(25.8) | 22(31.4) | ||
| 受伤原因 车祸伤 | 35(56.5) | 46(65.7) | 1.190 | 0.552 |
坠落伤 | 18(29.0) | 16(22.9) | ||
打击伤 | 9(14.5) | 8(11.4) | ||
| 入院时GCS 13~15 | 38(61.3) | 21(30.0) | 14.050 | 0.001 |
9~12 | 13(21.0) | 20(28.6) | ||
3~8 | 11(17.7) | 29(41.4) | ||
| 受伤至首次CT检查间隔时间(h) | 1.52±1.21 | 1.47±0.87 | 0.016 | 0.987 |
| 两次CT检查间隔时间(h) | 7.17±6.23 | 5.14±4.53 | 1.885 | 0.064 |
| 脑挫裂伤体积(cm3) | 6.52±5.52 | 14.38±13.39 | -3.035 | 0.003 |
| 中线移位距离(mm) | 0.25±1.40 | 2.65±1.63 | -2.644 | 0.010 |
| 合并颅骨骨折例数 | 26(41.9) | 50(71.4) | 11.709 | 0.001 |
| 合并蛛网膜下腔出血例数 | 30(48.4) | 58(82.9) | 17.580 | 0.000 |
| 合并硬膜外血肿例数 | 10(16.1) | 24(34.3) | 5.668 | 0.017 |
| 合并硬膜下血肿例数 | 4(6.5) | 23(32.9) | 15.241 | 0.000 |
| 损伤部位 额部 | 16(25.8) | 19(27.1) | 14.591 | 0.006 |
颞部 | 25(40.3) | 20(28.6) | ||
顶部 | 11(17.7) | 4(5.7) | ||
枕部 | 4(6.5) | 3(4.3) | ||
多部位 | 6(9.7) | 24(34.3) | ||
| PT(s) | 12.25±2.01 | 12.22±1.45 | 0.074 | 0.942 |
| APTT(s) | 25.27±3.87 | 24.96±3.45 | 0.342 | 0.734 |
| FDP(g/L) | 2.29±0.80 | 2.21±0.72 | 0.450 | 0.654 |
| D-二聚体(mg/L) | 4.72±3.79 | 8.13±5.33 | -2.487 | 0.015 |
| 血小板计数(109/L) | 203.39±53.27 | 203.31±56.66 | 0.005 | 0.996 |
| LDL-C(mmol/L) | 2.15±0.61 | 2.48±0.93 | -1.664 | 0.101 |
| 合并高血压病例数 | 22(35.5) | 24(34.3) | 0.021 | 0.885 |
| 合并2型糖尿病例数 | 2(3.2) | 16(22.9) | 10.759 | 0.001 |
对单因素分析结果有统计学意义的相关因素进行多因素Logistic回归分析,发现入院时GCS、首次颅脑CT检查显示脑挫裂伤体积、合并蛛网膜下腔出血、合并2型糖尿病是影响进展性脑挫裂伤发生的独立危险因素(均P<0.05)。见表 2。
| 因 素 | 回归系数 | OR值 | 95% CI | P值 |
| 入院时GCS | -2.345 | 0.096 | 0.014~0.650 | 0.016 |
| 脑挫裂伤体积 | 0.627 | 1.873 | 1.136~3.087 | 0.014 |
| 脑挫裂伤部位 | -1.795 | 0.166 | 0.007~4.233 | 0.277 |
| 中线移位 | -0.186 | 0.830 | 0.442~1.561 | 0.564 |
| 合并蛛网膜下腔出血 | 3.880 | 48.431 | 1.742~1 346.499 | 0.022 |
| 合并颅骨骨折 | 2.565 | 12.991 | 0.676~249.797 | 0.089 |
| 合并硬膜外血肿 | 0.164 | 1.178 | 0.134~10.346 | 0.882 |
| 合并硬膜下血肿 | 1.137 | 4.076 | 1.306~13.550 | 0.997 |
| D-二聚体 | -0.129 | 0.879 | 0.695~1.112 | 0.283 |
| 合并2型糖尿病 | 5.569 | 262.099 | 3.714~18 497.504 | 0.010 |
非进展组和进展组患者伤后6个月mRS评分良好分别为58例(93.5%)和51例(72.9%),两组预后差异有统计学意义(χ2=9.783,P<0.05)。
3 讨 论进展性脑挫裂伤与诸多因素相关,阐明这些高危因素,从而提前干预,对于提高抢救成功率,改善预后有重要的意义。
目前,对于“进展性脑挫裂伤”的定义尚未完全统一。最早由Dought[12]在1938年提出“延迟性颅内血肿”的概念。后来,Gudeman等[13]提出了“迟发性创伤性颅内血肿”的概念,但众多学者把创伤性颅内动脉瘤破裂引起的迟发性出血纳入这一研究范围[14, 15, 16]。而Oertal等[17]提出“进展性 出血性损伤”更多的指硬膜外血肿、硬膜下血肿、创伤性蛛网膜下腔出血及脑实质内挫伤形成的血肿。颅脑CT检查可以发现,脑挫裂伤与单纯的颅内血肿不同,表现为挫裂伤脑组织与颅内血肿相混合。Kurland等[18]在最近研究中把脑挫裂伤范围的扩大、新出现的脑挫裂伤及颅内出血纳入了进展性脑挫裂伤的研究范畴。因此,在本研究中,我们把CT复查发现有脑挫裂伤范围扩大以及新发挫裂伤和颅内出血规定为进展性脑挫裂伤。而不同的学者在研究中对于增加的体积规定相对比较接近,Oertel等[17]规定为增加25%,Alahmadi等[5]则定为30%,White等[19] 在研究中设为33%,本文资料将新增加体积定为30%,与当前的研究方法一致。
老年人合并高血压病、2型糖尿病及高脂血症概率相对较高,患者血管弹性减退、脆性增加,更易出现颅内迟发性出血[8]。Yuan等[20]对468例患者资料研究显示,年龄大于57岁是患者发生进展性出血的高危因素,而性别差异则无统计学意义。但Roof等[21] 则认为女性的孕激素和雌激素对阻止进展性出血有一定作用。本研究单因素分析结果显示,两组患者年龄、性别、LDL-C水平、是否合并高血压病差异无统计学意义,两组患者是否合并2型糖尿病差异有统计学意义。这可能与本研究病例相对偏少,平均年龄相对偏小有关。Alahmadi等[5]对98例患者的研究结果亦显示年龄、性别比较差异无统计学意义。Iaccarino等[22]在新近研究中则认为,70岁以上患者需结合有无高血压病、2型糖尿病、心脏病进行多因素分析更具有临床意义。本文资料多因素回归分析显示2型糖尿病是进展性脑挫裂伤的高危因素。Amanda等[23]认为高血糖引起红细胞变形能力降低,血黏度升高,加剧脑组织微循环障碍,造成大量乳酸与酮体堆积,导致脑组织缺血、缺氧、水肿、坏死,促进了迟发性颅内损伤的进展。
目前,国内对颅脑外伤的数据统计显示,车祸伤仍是首要的致伤因子[3]。本研究也发现,因车祸所致进展性和非进展脑挫裂伤组均占一半以上(65.7%和56.5%),因此,降低交通事故发生率对于控制颅脑损伤的发生率可能有一定的作用,但尚无明确的依据预判车祸对脑挫裂伤的病情是否有影响。伤后GCS是评估颅脑损伤患者意识状态、伤情严重程度及预后的重要指标之一,能够快速、客观地判断患者的伤情[24]。本文资料表明,进展性脑挫裂伤组GCS为3~8分的占41.4%,13~15分的占30%,非进展性脑挫裂伤组则分别为17.7%和61.3%,入院时两组GCS差异有统计学意义,提示伤后GCS低、意识障碍程度深、伤情严重者更容易发生进展性脑挫裂伤。Iaccarino等[22]在研究中发现,86例入院GCS为3~8分的患者中,有32例(37.2%)颅脑CT复查发现病情进展而行手术治疗;而在GCS大于8分的251例中,只有14例(5.6%)进行了手术治疗。Alahmadi等[5]对97例进展性脑挫裂伤患者研究发现,GCS大于13分的患者中无因进展性脑挫裂伤行手术治疗。本文资料多因素回归分析亦显示GCS是进展性脑挫裂伤的高危因素。
本研究结果显示进展性脑挫裂伤患者和非进展性脑挫裂伤患者受伤至首次颅脑CT检查平均时间比较接近(分别为1.52 h与1.47 h),两次CT检查间隔时间相对有差距(分别为7.17 h与5.14 h),差异无统计学意义。随着院前急救体系的完善,颅脑外伤后患者都可以及时到达医院进行急救,因此首次颅脑CT检查能在第一时间完成,但进行CT复查的时间仍有争议。目前有研究表明,合并有脑挫裂伤的中、重型颅脑损伤患者,即使没有神经系统症状、体征的加重,也需要进行计划性颅脑CT复查以提前发现进展性脑挫裂伤在影像学的表现[25]。Joseph研究团队[26]则认为神经系统症状、体征的变化才是决定CT复查时间的主要依据。研究发现进展性脑挫裂伤大多发生在伤后12 h内,但也可发生在受伤后3~4天[4]。因此CT复查时机仍应结合神经系统症状、体征的变化。Juratli等[11]研究发现,脑挫裂伤最大层面直径大于3 cm者占进展性脑挫裂伤患者70.4%,而在非进展性脑挫裂伤患者中只占11.4%,脑挫裂伤体积与病情进展相关。本文资料亦显示,首次颅脑CT检查脑挫裂伤的体积是进展性损伤的危险因素。李雪元等[8]研究也表明了首次颅脑CT检查颅内出血量大于10 cm3,其发生进展性出血的相对风险为6.12倍。Yuan等[20]则发现中线移位5 mm以上,更易出现进展性出血性损伤。其原因可能为较大范围脑挫裂伤后损伤较多微血管,内皮细胞损伤肿胀,血管痉挛闭塞,血小板及白细胞聚集黏附,血细胞外溢,释放神经毒性物质,从而引起继发性脑损伤[4, 27]。同时,本文资料显示进展性脑挫裂伤患者中多部位损伤比例(34.3%)明显高于非进展性脑挫裂伤患者(9.7%),可能多部位损伤造成的挫裂伤体积相对较大有关,这与Iaccarino等[22]研究结论基本一致。我们的结果通过单因素比较分析,脑挫裂伤合并有骨折、蛛网膜下腔出血、硬膜外/下血肿是进展性损伤的危险因素。这与骨折后持续板障出血、损伤脑膜动脉出血引起硬膜外血肿有关,沈合春等[28]研究显示,颅骨骨折合并硬膜外血肿发生进展性损伤的相对风险为2.22倍。国外研究发现,脑挫裂伤合并蛛网膜下腔出血及硬膜下血肿是进展性脑挫裂伤的危险因素[4, 7, 29]。Tong等[30]研究发现,进展性脑挫裂伤患者与非进展性脑挫裂伤患者蛛网膜下腔出血比例分别为67.72%与47.39%,硬膜下血肿比例分别为20.63%与4.99%,差异均有统计学意义。本文资料多因素分析结果显示,蛛网膜下腔出血是高危因素。其原因可能为在血管外红细胞刺激下,脑血管痉挛致血管壁缺血、坏死,继而引发出血[4, 31]。
由于研究方式差异,颅脑损伤后凝血功能异常发生率达10.0%~97.5%,平均为32.7%[32]。Juratli等[11]认为创伤介导的凝血功能障碍已成为进展性脑挫裂伤的危险因素。引起凝血功能障碍的机制尚不明确,可能与挫裂伤脑组织释放组织因子激活内源性及外源性凝血途径有关[4, 33]。Cohen等[34]研究则表明,脑组织损伤引起灌注不足,其可能通过C蛋白途径导致严重的凝血功能障碍。本研究结果显示,两组间D-二聚体差异有统计学意义,单因素分析结果D-二聚体是进展性脑挫裂伤的危险因素。Yuan 等[21]研究发现,进展性脑挫裂伤患者PT>14 s、APTT>40 s、FDP<2 g/L、D-二聚体≥5 mg/L、血小板计数<100×109/L的比例明显高于非进展性脑挫裂伤患者。结合本研究结果,进展组与非进展组D-二聚体平均值为8.13 mg/L与4.72 mg/L,与Yuan等研究结论基本一致,两组间PT、APTT、FDP、血小板计数差异无统计学意义,可能与病例数偏少有关。Chhabra等[35]对208例单纯颅脑损伤患者研究也发现,入院时D-二聚体升高是创伤性颅脑损伤后凝血功能异常进展的独立危险因素。
本研究结果显示,非进展性脑挫裂伤患者预后优于进展性脑挫裂伤患者,两组伤后6个月mRS≥4分比例分别为6.5%和27.1%,进展性脑挫裂伤患者有更高的致死致残率。Juratli 等[11]研究进展性脑挫裂伤发生率为43.5%,伤后1年评估预后,mRS≥4分的患者比例较非进展性脑挫裂伤组高4倍。经多因素回归分析,入院时GCS、脑挫裂伤体积、合并有蛛网膜下腔出血和2型糖尿病是进展性脑挫裂伤的独立危险因素。因此,对于意识障碍严重、脑挫裂伤范围大、合并有蛛网膜下腔出血及2型糖尿病的患者更应高度重视,密切注意神经系统症状和体征变化,加强监护,对进展性脑挫裂伤早期作出诊断,及时处理,减少继发性脑损伤,从而提高抢救成功率及患者生存质量。
本研究提示的进展性脑挫裂伤独立危险因素对临床医师判断脑挫裂伤的预后具有重要的价值。但研究本身有不足之处,如病例数量相对不足,有待于积累资料作进一步深入分析,并开展相关的前瞻性研究。
| [1] | TAGLIAFERRI F, COMPAGNONE C, KORSICM M, et al. A systematic review of brain injury epidemiology in Europe[J]. Acta Neurochir(wien), 2006,148(3):255-268. |
| [2] | FEIGIN V L, THEADOM A, BARKER-COLLO S, et al. Incidence of traumatic brain injury in New Zealand: a population-based study[J]. Lancet Neurol, 2013,12(1):53-64. |
| [3] | 马定军,刘佰运,郝淑煜,等. 颅脑创伤数据库平台的建立与初步应用[J].中华神经外科杂志,2014,30(2):159-161. MA Ding-jun, LIU Bai-yun, HAO Shu-yu, et al. Establishment of database platform in traumatic brain injury field and its preliminary application[J]. Chinese Journal of Neurosurgery, 2014,30(2):159-161. (in Chinese) |
| [4] | KURLAND D, HONG C, AARABI B, et al. Hemorrhagic progression of a contusion after traumatic brain injury: a review[J]. J Neurosurg, 2012,29(1):19-31. |
| [5] | ALAHMADI H, VACHHRAJANI S, CUSIMANO M D. The natural history of brain contusion: an analysis of radiological and clinical progression[J]. J Neurosurg, 2010,112(5):1139-1145. |
| [6] | ALLARD C B, SCARPELINI S, RHIND S G, et al. Abnormal coagulation tests are associated with progression of traumatic intracranial hemorrhage[J]. J Trauma, 2009,67(5):959-967. |
| [7] | SON S, YOO C J, LEE S G, et al. Natural course of initially non-operated cases of acute subdural hematoma: the risk factors of hematoma progression[J]. J Korean Neurosurg, 2013,54(3):211-219. |
| [8] | 李雪元,马 林,王新军,等. 急性颅脑损伤后进展性出血性损伤高危因素分析[J].重庆医学,2014,43(8):915-917. LI Xue-yuan, MA Lin, WANG Xin-jun, et al. Evaluation on the related high-risk factors of progressive hemorrhagic injury after acute traumatic brain injury[J]. Chongqing Medicine, 2014,43(8):915-917.(in Chinese) |
| [9] | 王忠诚, 张玉琪. 王忠诚神经外科学[M]. 第2版,武汉:湖北科学技术出版社,2015:397-399. WANG Zhong-cheng, ZHANG Yu-qi. WANGZHONGCHENG Neurosurgery[M]. 2nd Ed. Wuhan: Hubei Science and Technology Press, 2015:397-399. (in Chinese) |
| [10] | KOTHARI R U, BROTT T, BRODERICK J P, et al. The ABCs of measuring intracerebral hemorrhage volumes[J]. Stroke, 1996, 27(8):1304-1305. |
| [11] | JURATLI T A, ZANG B, LITZ R J, et al. Early hemorrhagic progression of traumatic brain contusions: frequency, correlation with coagulation disorders, and patient outcome: a prospective study[J]. J Neurotrauma, 2014,31(17):1521-1527. |
| [12] | DOUGHT R G. Posttraumatic delayed intracerebral hemorrhage[J]. South Med J, 1938,31(3):254-256. |
| [13] | GUDEMAN S K, KISHORE P R, MILLER J D, et al. The genesis and significance of delayed traumatic intracerebral hematoma[J]. Neurosurgery, 1979,5(3):309-313. |
| [14] | KAPLAN M, OZVEREN M F, TOPSAKAL C, et al. Asymptomatic interval in delayed traumatic intracerebral hemorrhage: report of two cases[J]. Clin Neurol Neurosurg, 2003,105(3):153-155. |
| [15] | HORIUCHI T, NAKAGAWA F, MIYATAKE M, et al. Traumatic middle cerebral artery aneurysm: case report and review of the literature[J]. Neurosurg Rev, 2007,30(3):263-267. |
| [16] | YANG T C, LO Y L, HUANG Y C, et al. Traumatic anterior cerebral artery aneurysm following blunt craniofacial trauma[J]. Eur Neurol, 2007,58(4):239-245. |
| [17] | OERTEL M, KELLY D F, MCARTHUR D, et al. Progressive hemorrhage after head trauma: predictors and consequences of the evolving injury[J]. J Neurosurg, 2002,96(1):109-116. |
| [18] | KURLAND D, HONG C, AAREBI B, et al. Hemorrhagic progression of a contusion after traumatic brain injury: a review[J]. J Neurotrauma, 2012,29(1):19-31. |
| [19] | WHITE C L, GRIFFITH S, CARON J L. Early progression of traumatic cerebral contusion: characterization and risk factors[J]. J Trauma, 2009,67(3):508-515. |
| [20] | YUAN F, DING J, CHEN H, et al. Predicting progressive hemorrhage injury after traumatic brain injury: derivation and validation of a risk score based on admission characteristics[J]. J Neurotrauma,2012,29(12):2137-2142. |
| [21] | ROOF R L, HALL E D. Gender differences in acute CNS trauma and stroke: neuroprotective effects of estrogen and progesterone[J]. J Neurotrauma,2000,17(5):367-388. |
| [22] | IACCARINO C, SCHIAVI P, PICETTI E, et al. Patients with brain contusion: predictors of outcome and relationship between radiological and clinical evolution[J]. J Neurosurg, 2014,120(4):908-918. |
| [23] | AMANDA M, LAIRD M D, PRESTON R, et al. Relationship of early hyperglycemia to mortality in trauma patients[J]. J Trauma, 2004,56(5):1058-1062. |
| [24] | MARMAROU A, LU J, BUTCHER I, et al. Prognostic value of the Glasgow Coma Scale and pupil reactivity in traumatic brain injury assessed pre-hospital and on enrollment: an IMPACT analysis[J]. J Neurotrauma, 2007,24(2):270-280. |
| [25] | WURMB T E,SCHLERETH S,KREDEL M,et al. Routine follow-up cranial computed tomography for deeply sedated, intubated, and ventilated multiple trauma patients with suspected severe head injury[J]. Biomed Res Int, 2014,2014:361949. |
| [26] | JOSEPH B, AZIZ H, PANDIT V, et al. A three-year prospective study of repeat head computed tomography in patients with traumatic brain injury[J]. J Am Coll Surg, 2014,219(1):45-51. |
| [27] | DE REUCK J. Risk factors for late-onset seizure related to cerebral contusions in adults with a moderate traumatic brain injury[J]. Clin Neurol Neruosurg, 2011,113(6):469-471. |
| [28] | 沈合春,钱志远,郑达理,等. 急性颅脑损伤后进展性出血性损伤极高危因素分析及定时复查CT时间探讨[J].中华神经医学杂志, 2011,10(7):735-740. SHEN He-chun, QIAN Zhi-yuan, ZHENG Da-li, et al. High-risk factors of progressive hemorrhagic injury after acute traumatic brain injury and its time for first scheduled brain CT[J]. Chinese Journal of Neuromedicine, 2011,10(7):735-740. (in Chinese) |
| [29] | LEUNG G K, NG G K, HO W, et al. Impact of a multidisciplinary trauma team on the outcome of acute subdural haematoma[J]. Injury, 2012,43(9):1419-1422. |
| [30] | TONG W S, ZHENG P, XU J F, et al. Early CT signs of progressive hemorrhagic injury following acute traumatic brain injury[J]. Neuroradiology, 2011,53(5):305-309. |
| [31] | LEUNG G K, NG G K, HO W, et al. Impact of a multidisciplinary trauma team on the outcome of acute subdural haematoma[J]. Injury, 2012,43(9):1419-1422. |
| [32] | HARHANGI B S, KOMPANJE E J, LEEBEEK F W, et al. Coagulation disorders after traumatic brain injury[J]. Acta Neurochir(Wien), 2008,150(2):165-175. |
| [33] | HALPERN C H, REILLY P M, TURTZ A R, et al. Traumatic coagulopathy: the effect of brain injury[J]. J Neurotrauma, 2008,25(8):997-1001. |
| [34] | COHEN M J, BROHI K, GANTER M T, et al. Early coagulopathy after traumatic brain injury: the role of hypoperfusion and the protein C pathway[J]. J Trauma, 2007,63(6):1254-1261. |
| [35] | CHHABRA G, SHARMA S, SUBRAMANIAN A, et al. Coagulopathy as prognostic marker in acute traumatic brain injury[J]. J Emerg Trauma Shock, 2013,6(3):180-185. |



