| 基于超声衰减参数评估超声联合临床参数模型对肝脏脂肪含量的预测价值 |
肝脏脂肪异常沉积超过肝脏总重量的5%为肝脂肪变性,患病率约29.2%,且呈逐年上升趋势,可引起肝脏代谢功能障碍,增加代谢相关脂肪性肝病、肝硬化、肝细胞癌患病风险[1]。早期精准诊断和定量分析肝脏脂肪含量有助于疾病诊断、肝移植评估、减少并发症及肝脏相关死亡率[2]。肝活检、肝脏MRI质子密度脂肪分数(proton density fat fraction,PDFF)可精准评估肝脏脂肪含量,然而因活检为侵入性、MRI-PDFF检查费用高且禁忌证多等原因,导致两者临床利用率低。近年来,超声衰减参数(ultrasound-guided attenuation parameter,UGAP)已用于肝脏脂肪定量分析中,虽便捷、准确性高,但由于设备要求较高无法普及[3]。因此,寻找一种高效评估肝脏脂肪含量的方法是临床亟待解决的问题。本研究构建超声脂肪肝程度、内脏脂肪、皮下脂肪、甘油三酯等多参数联合的预测模型,并以UGAP测量结果衰减系数(attenuation coefficient,AC)为诊断标准,评估该模型对肝脏脂肪含量的预测价值,旨在为临床提供一种简便、高效量化肝脏脂肪、评估脂肪肝的方法。
1 资料与方法 1.1 一般资料选取2023年8月至2024年6月在我院体检者。纳入标准:①年龄≥18岁;②临床资料完整,超声检查48 h内行血脂及肝功能等检查。排除标准:①超声图像显示不清;②近期使用可能干扰肝脏脂肪浸润的药物;③患有严重精神类疾病或意识障碍无法配合者。
共纳入615例,其中68例行MRI-PDFF检查;余547例行预测模型的构建与验证,按7∶3比例随机分为训练集(380例)和验证集(167例)。本研究已通过医院伦理委员会审核(批号:2024HL-379)。
收集训练集和验证集受试者的临床资料,包括年龄、性别、BMI、空腹血糖、总胆固醇、甘油三酯、丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天冬氨酸氨基转移酶(aspartate transaminase,AST)等。
1.2 仪器与方法615例均行超声检查,采用GE20彩色多普勒超声诊断仪。受试者取仰卧位,伸展右上肢至头部,充分扩展肋间隙。选用凸阵探头(频率2~5 MHz),垂直放置探头,通过肋间隙对肝Ⅴ段行常规超声检查,并根据肝脏回声强度、肝肾回声对比、肝内血管和膈肌的清晰度,判断脂肪肝程度(无、轻度、中度和重度)[4];测量内脏脂肪厚度(visceral fat thickness,VFT),将探头置于脐上1 cm,测量双侧腹直肌间腹白线至腹主动脉前壁的距离[5](图 1),结果取双侧平均值。使用线阵探头(频率2~9 MHz)测量皮下脂肪厚度(subcutaneous fat thickness,SFT):将探头置于脐上1 cm,左右移动探头测量腹部两侧皮肤至腹直肌外缘距离(图 2),最终结果取双侧平均值[5]。激活UGAP模式,嘱患者屏住呼吸3~5 s,记录不同帧上连续回波UGAP-AC平均值,注意避开胆管、血管等伪影(图 3)。
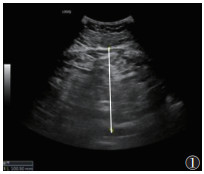 |
| 图 1 常规超声测量腹部内脏脂肪厚度(VFT)示意图 |
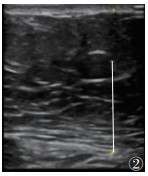 |
| 图 2 常规超声测量皮下脂肪厚度(SFT)示意图 |
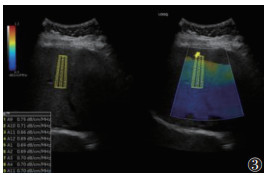 |
| 注:蓝色代表该区域图像质量良好,测量时取样框尽量位于该区域内;红色代表该区域图像质量欠佳,测量时应避开 图 3 肝脏超声衰减参数(UGAP)声像图 |
68例采用Philips Prodiva 1.5 T MRI扫描仪,行mDixon-Quant序列扫描。受试者取仰卧位,线圈中心与剑突下缘平齐,呼吸门控软管置于腹前壁正中,呼气末屏气扫描获取图像。扫描参数:Scan mode 3D,TR 6.5 ms,TE 1.15 ms,视野375 mm×297 mm×201 mm,体素3.00 mm×3.02 mm×6.00 mm。后经自动重建、靶区勾画等步骤计算各肝段PDFF值,选取肝Ⅴ段PDFF值作为最终观察指标(图 4)。操作时注意避开大血管、胆管、病变、伪影等的干扰。
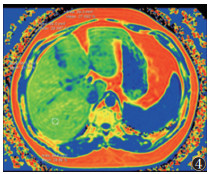 |
| 注:测量肝Ⅴ段PDFF值 图 4 肝脏MRI质子密度脂肪分数(PDFF)图 |
1.3 统计学方法
采用SPSS 25.0软件行统计学分析。采用Kolmogorov-Smirnov检验观察变量是否符合正态分布,服从正态分布时以x±s表示,不服从正态分布以M(P25,P75)表示;分类变量以例(%)表示。计量资料的组间比较(如训练集与验证集)行独立样本t检验;分类变量与等级变量的比较行χ2检验。相关性分析:双变量满足正态分布者行Pearson相关分析;不满足正态分布者行Spearman相关分析,分析UGAP-AC值与MRI-PDFF值相关性、肝脏脂肪含量与各参数之间相关性,以及UGAP-AC值与模型预测值之间的相关性。相关强度判定标准:
68例行MRI-PDFF检查的受试者中,男39例,女29例;年龄18~56岁,平均(47.23±15.42)岁。MRI-PDFF值为1.98~34.55,平均18.09;UGAP-AC值为0.35~0.98 dB/cm·MHz,平均0.73 dB/cm·MHz;Spearman相关检验表明,两者呈高度相关(r=0.931)。
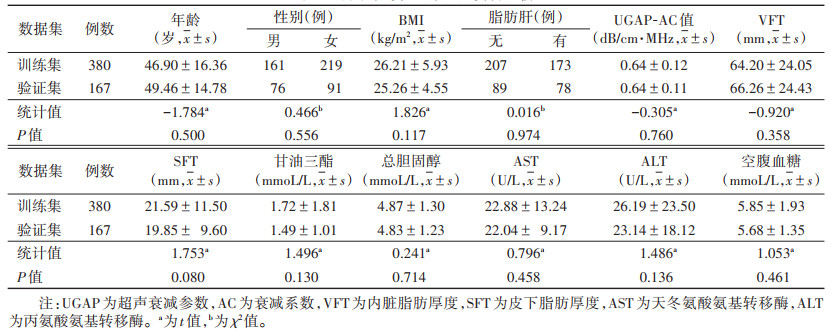
2.2 训练集与验证集一般资料比较训练集与验证集年龄、性别、BMI、脂肪肝、UGAP-AC值、VFT、SFT、甘油三酯、总胆固醇、AST、ALT、空腹血糖差异均无统计学意义(均P>0.05)(表 1)。
| 表 1 训练集与验证集一般资料比较 |
 |
2.3 肝脏脂肪含量与脂肪厚度及临床指标之间的相关性
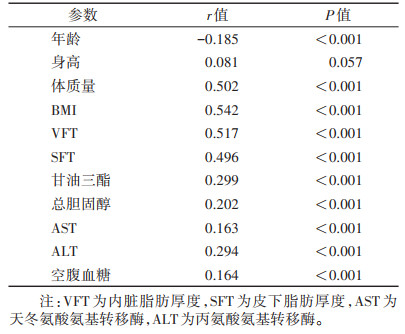
Pearson相关性分析表明,UGAP-AC值与体质量、BMI、VFT、SFT呈中度相关,与年龄、甘油三酯、总胆固醇、AST、ALT、空腹血糖呈弱相关(均P<0.001);与身高无明显相关性(P>0.05)(表 2)。
| 表 2 肝脏脂肪含量与相关参数的相关性 |
 |
2.4 回归模型的构建及验证
在训练集中对11个变量采用逐步法多重线性回归分析确定与UGAP-AC值显著相关的因素。最终将超声诊断脂肪肝程度、VFT、SFT和甘油三酯纳入预测模型,构建方程如下:Logit(AC预测值)=0.427+0.082×脂肪肝程度+0.001×SFT+0.000 388×VFT+0.003×甘油三酯。其中脂肪肝程度赋值标准:无=1,轻度=2,中度=3,重度=4。该预测模型R2为0.834,调整混杂因素后R2为0.832,标准误为0.048,D-W值为1.983,模型拟合效果良好。
Pearson相关分析发现,模型预测值与UGAP-AC值高度相关(r=0.906)。绘制ROC曲线对模型效能进行评估,AUC为0.985(图 5),当模型预测值的截断值为0.57时,其对脂肪肝的预测效能最佳,敏感度1.00,特异度0.91。
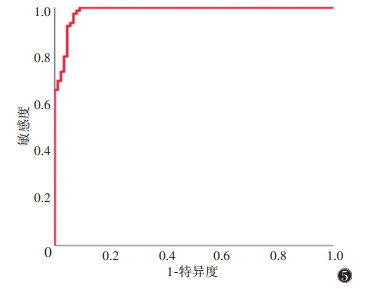 |
| 图 5 预测模型预测脂肪肝的ROC曲线 |
3 讨论
脂肪肝即肝细胞内出现异常脂肪堆积是代谢相关脂肪性肝病、酒精性脂肪肝及各类肝毒性疾病的标志,若不及时发现易进展为肝纤维化、肝硬化、肝癌。早期、高效识别普通人群脂肪肝可减少并发症及肝相关死亡率[6-7]。其中肝活检、MRI-PDFF诊断准确性高,但因医疗条件、患者接受度等限制过多,导致临床利用率较低;超声检查方便快捷,为临床评估脂肪肝最常用的检查方法。UGAP可通过对固定基波射频信号(4.0 MHz)的回收及后处理得到AC值,从而实现脂肪肝超声诊断由半定量至定量的转变,其扫描方式简单、可重复性强、准确性高,避免了不必要的活检,是实现肝脏脂肪量化的技术之一。本研究表明,UGAP-AC值与MRI-PDFF值呈高度相关(r=0.931),与既往研究[8]一致。Ogino等[8]将患者肝脏Ⅴ段UGAP与肝活检结果对比,两者呈显著正相关(r=0.81,P<0.01)。Kang等[9]研究发现,UGAP区分脂肪肝的诊断效能佳,AUC为0.821,与MRI-PDFF值(0.829)相当,与MRI-PDFF呈强正相关(相关系数0.704),且B型超声(0.766)及CAP(0.788)。但UGAP为超声新技术,目前临床普及率较低,因此本研究以UGAP-AC为诊断标准构建回归模型,实现肝脏脂肪的定量预测,在无法行UGAP检查时,可用此模型间接估算肝脏脂肪含量。
临床指标纳入方面,现有的肝脏脂肪预测模型多由简单参数(BMI、臀围、腰围、腰高比等)与血生化指标共同构建[10-13]。但BMI、腹围等指标与肝脏脂肪关系易受脂肪分布差异等多因素影响,与肝脏脂肪含量相关性显著低于皮下脂肪、内脏脂肪等影像学指标[14],建立的模型可靠性欠佳、准确性有限。因此,为提高预测模型准确性,本研究将常规超声检查结果纳入预测模型。常规超声可定量测量皮下脂肪、内脏脂肪面积,且可通过肝实质回声或血管及横膈膜的模糊程度半定量评估脂肪肝类别[15],所构建的预测模型可在实现定量评估肝脏脂肪的同时提高预测准确性。
本研究显示,除常规超声评估的脂肪肝程度指标外,甘油三酯也是影响预测结果的重要指征。正常情况下,肝脏可将总胆固醇、甘油三酯转化为脂蛋白发挥作用,但肝脏脂肪过度沉积导致总胆固醇、甘油三酯无法被机体正常吸收利用,随着其不断分泌与合成,最终在体内蓄积。VFT与SFT亦与预测结果密切相关,进一步分析发现内脏脂肪与肝脏脂肪的相关性大于皮下脂肪。Nauli等[16]指出,与皮下脂肪不同,内脏脂肪过度代谢产生的游离脂肪酸更易通过门静脉循环分流至肝脏合成脂肪并沉积,导致脂肪肝的形成。Elguezabal等[14]发现,肝脏脂肪与VFT的相关系数为0.645,优于本研究(0.517),考虑代谢表型、遗传易感性因素、饮食习惯、运动习惯等差异影响研究结果,须进一步研究证实。
本研究中模型的预测值与UGAP-AC值高度相关(r=0.906),且绘制ROC曲线后发现,当模型预测值的截断值为0.57时,对脂肪肝的预测效能最佳,AUC为0.985,敏感度1.00,特异度0.91。结果表明,通过对VFT、SFT测量及脂肪肝严重程度评估,可避免脂肪沉积个体差异对预测模型的影响,帮助超声医师在评估脂肪肝程度时,将定性指标转化为定量指标,提高脂肪肝诊断的准确性。
本研究存在的不足:主要分析肝脏脂肪含量,未按照是否存在脂肪肝进行分组观察,导致ALT、AST、空腹血糖等与肝脏脂肪含量呈弱相关性;验证集样本量较小;纳入受试者的脂肪肝比例不平衡。后续将扩大样本量、细化研究指标进一步分析。
综上所述,超声UGAP可无创定量评估肝脏脂肪含量,与MRI-PDFF值呈强相关性。二维超声诊断的脂肪肝程度、VFT、SFT,结合甘油三酯建立的预测模型结果与UGAP-AC值高度相关,在无法行UGAP检查时,可用此模型间接估算肝脏脂肪含量。
| [1] |
POUWELS S, SAKRAN N, GRAHAM Y, et al. Non-alcoholic fatty liver disease (NAFLD): a review of pathophysiology, clinical management and effects of weight loss[J]. BMC Endocr Disord, 2022, 22(1): 63. DOI:10.1186/s12902-022-00980-1 |
| [2] |
WANG M, TANG S, LI G, et al. Comparative study of ultrasound attenuation analysis and controlled attenuation parameter in the diagnosis and grading of liver steatosis in non-alcoholic fatty liver disease patients[J]. BMC Gastroenterol, 2024, 24(1): 81. DOI:10.1186/s12876-024-03160-8 |
| [3] |
KURODA H, ABE T, FUJIWARA Y, et al. Diagnostic accuracy of ultrasound-guided attenuation parameter as a noninvasive test for steatosis in non-alcoholic fatty liver disease[J]. J Med Ultrason (2001), 2021, 48(4): 471-480. DOI:10.1007/s10396-021-01123-0 |
| [4] |
赵斌, 钟池, 王振华. 胰岛素抵抗的脑梗死患者内脏脂肪堆积及其相关因素[J/CD]. 中华脑血管病杂志(电子版), 2011, 5(2): 108-115.
|
| [5] |
黄影蓓. 非肥胖型PCOS不孕患者超声检测肥胖指标的临床价值[J]. 中国计划生育学杂志, 2017, 25(8): 543-545. |
| [6] |
GUO X, WANG F, TEODORO G, et al. Liver steatosis segmentation with deep learning methods[J]. Proc IEEE Int Symp Biomed Imaging, 2019, 2019: 24-27. |
| [7] |
王盛甲, 朱高旺, 陈鑫, 等. 代谢相关脂肪性肝病全肝脂肪测定: LAVA-Flex和IDEAL-IQ技术测定全肝脂肪分数与PDFF一致性研究[J]. 中国中西医结合影像学杂志, 2025, 23(3): 273-278. |
| [8] |
OGINO Y, WAKUI N, NAGAI H, et al. The ultrasound-guided attenuation parameter is useful in quantification of hepatic steatosis in non-alcoholic fatty liver disease[J]. JGH Open, 2021, 5(8): 947-952. DOI:10.1002/jgh3.12615 |
| [9] |
KANG K A, LEE S R, JUN D W, et al. Diagnostic performance of a novel ultrasound-based quantitative method to assess liver steatosis in histologically identified nonalcoholic fatty liver disease[J]. Med Ultrason, 2023, 25(1): 7-13. DOI:10.11152/mu-3815 |
| [10] |
BEDOGNI G, BELLENTANI S, MIGLIOLI L, et al. The fatty liver index: a simple and accurate predictor of hepatic steatosis in the general population[J]. BMC Gastroenterol, 2006, 6: 33. DOI:10.1186/1471-230X-6-33 |
| [11] |
QIN Z W, REN Q N, ZHANG H X, et al. Development and validation of a novel non-invasive test for diagnosing nonalcoholic fatty liver disease in Chinese children[J]. World J Pediatr, 2024, 20(4): 413-421. DOI:10.1007/s12519-023-00704-y |
| [12] |
ZHOU X, LIN X, CHEN J, et al. Clinical spectrum transition and prediction model of nonalcoholic fatty liver disease in children with obesity[J]. Front Endocrinol (Lausanne), 2022, 13: 986841. DOI:10.3389/fendo.2022.986841 |
| [13] |
龙炽慧, 刘坚, 汪鹏, 等. 定量CT对无酗酒者肝脏脂肪含量的测量及对肝脏脂肪含量影响因素的研究[J]. 中国中西医结合影像学杂志, 2023, 21(4): 440-443. |
| [14] |
ELGUEZABAL RODELO R G, PORCHIA L M, TORRES-RASGADO E, et al. Visceral and subcutaneous abdominal fat is associated with non-alcoholic fatty liver disease while augmenting metabolic syndrome's effect on non-alcoholic fatty liver disease: a cross-sectional study of NHANES 2017-2018[J]. PLoS One, 2024, 19(2): e0298662. DOI:10.1371/journal.pone.0298662 |
| [15] |
赵一冰, 周丹, 贾鹏, 等. 超声诊断非酒精性脂肪肝与CT定量测量腹部脂肪分布的相关性[J]. 中国医学影像技术, 2020, 36(12): 1843-1847. |
| [16] |
NAULI A M, MATIN S. Why do men accumulate abdominal visceral fat?[J]. Front Physio, 2019, 10: 1486. |
 2025, Vol. 23
2025, Vol. 23


