| 瘤周水肿DTI参数对高级别胶质瘤IDH突变状态的诊断价值 |
2. 四川大学华西公共卫生学院/四川大学华西第四医院放射科, 四川 成都 610041
2. West China School of Public Health of Sichuan University, Radiology Department of West China Fourth Hospital of Sichuan University, Chengdu 610041, China
高级别胶质瘤(high-grade glioma,HGG)是颅内最常见、最具侵袭性的恶性肿瘤,占成人中枢神经系统肿瘤的50%~60%,预后较差,中位生存期为12~15个月,5年生存率<7%[1-3]。HGG(WHO Ⅳ级胶质瘤),主要包括星形细胞瘤[异柠檬酸脱氢酶(isocitrate dehydrogenase,IDH)突变型]和胶质母细胞瘤(IDH野生型),IDH突变型胶质瘤预后相对较好[4-5],因此,治疗前确定IDH状态十分重要。T2 FLAIR错配征目前被广泛应用于低级别胶质瘤(low-grade glioma,LGG)IDH突变状态的评估,特异度极高(接近100%),但敏感度较低,其在HGG中的应用较少[6-7],诊断效能尚不清楚。此外,多种影像学征象被用于鉴别IDH突变型和IDH野生型HGG,IDH突变型肿瘤多表现为边缘清楚、信号均匀、强化不明显等;而IDH野生型肿瘤血流量更大、血管通透性更高[8-9]。与LGG相比,HGG常伴不同程度的瘤周肿瘤细胞浸润,常规MRI图像上不可见[10],手术难以根除。IDH状态与胶质瘤的瘤周水肿范围相关[10],有学者将瘤体周围不同距离瘤周水肿(水肿近侧-远侧)的影像学参数特点差异用于指导个性化治疗[11]。近年来,DWI、DTI、扩散峰度成像(diffusion kurtosis imaging,DKI)被用来诊断HGG,各向异性分数(fraction anisotropy,FA)、ADC值则是用来评估IDH状态的潜在影像学参数[12]。本研究通过测量HGG瘤体与瘤周水肿的DTI参数,评估各参数预测IDH突变的诊断效能。
1 资料与方法 1.1 一般资料从公开数据库癌症图像档案(The Cancer Imaging Archive,TCIA)数据库下载UCSF-PDGM胶质瘤数据集(https://www.cancerimagingarchive.net/collection/ucsf-pdgm/)[13-14]。该数据集包含501例胶质瘤患者术前头颅MRI图像数据及病理诊断结果,图像采集时间为2015—2021年。
纳入标准:①Ⅳ级脑胶质瘤(WHO 2021版中枢神经系统肿瘤分类);②年龄18~65岁;③可获得1p/19q、IDH突变和O6-甲基鸟嘌呤-DNA甲基转移酶(MGMT)状态;④完整的T1WI、T2WI、T2 FLAIR、T1WI增强扫描、DTI序列资料;⑤图像质量良好。排除标准:①肿瘤位于脑室内或完全位于中线结构上;②双侧肿瘤或多发水肿灶;③肿瘤完全坏死;④肿瘤或水肿范围太小(参照分割图像无法放置ROI);⑤仅行活检。最终共纳入177例,男107例,女70例;年龄19~65岁,平均(52.2±10.8)岁;IDH突变型(Ⅳ级星形细胞瘤)22例(突变组),IDH野生型(胶质母细胞瘤)155例(野生组);MGMT阳性134例,阴性43例;全切120例,次全切57例。本研究经成都西区医院伦理委员会批准(批号:XQYY-EC-20240901)。
1.2 参数测量图像均行脱敏处理并转化为NIFTI格式,同时行涡流校正、运动校正和基于深度学习的颅骨剥离,图像分割与标注由算法自动完成,并经人工校正。
DTI参数测量使用DSI studio(版本2024.1.9,https://dsi-studio.labsolver.org/)软件,参数包括FA值、平均扩散率(mean diffusivity,MD)、轴向扩散率(axial diffusivity,AD)和径向扩散率(radial diffusivity,RD)。由2位分别具有5、6年工作经验的医师在不知道病理结果的情况下独立勾画圆形ROI,直径5 mm(图 1a),并在瘤体强化区域、瘤周水肿近侧、瘤周水肿远侧分别测量2次DTI参数取平均值并记录;在瘤体侧ROI对称的脑实质区域手动勾画ROI,将肿瘤侧DTI参数除以对侧DTI参数得到FA、MD、AD和RD相对值(rFA、rMD、rAD、rRD)[12]。脑肿瘤存在占位效应、无法直接进行镜像操作或对称位置为脑室或脑沟时,可在邻近位置或层面勾画ROI。
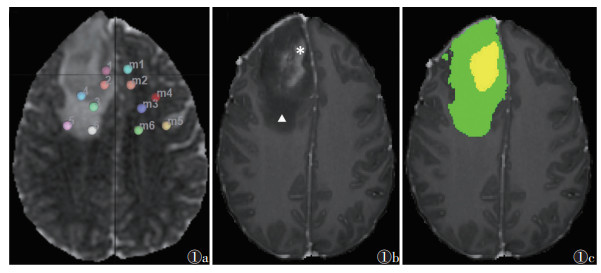 |
| 注:图1a为测量DTI参数时的ROI放置,ROI 1~2、3~4、5~6分别放置在肿瘤强化区域、不强化/瘤周水肿的近侧及远侧区域,ROI m1~m6分别表示镜像对侧大脑半球区域的ROI放置;图1b为T1WI增强扫描图像,可见肿瘤强化区域呈高信号(*),瘤周水肿不强化呈低信号(▲);图1c显示数据集自带的分割图像上分别对应黄色区域和绿色区域,可使ROI准确放置 图 1 ROI勾画示意图 |
肿瘤体积采用ITK-SNAP(版本3.8,http://www.itksnap.org/)软件。通过软件自带肿瘤分割数据(图 1b,1c),直接获取强化体积、坏死体积、水肿体积,并计算肿瘤体积(肿瘤体积=强化体积+坏死体积)、体积比(强化/瘤体、水肿/瘤体、坏死/瘤体及强化/水肿)。
1.3 统计学方法使用R4.2.1软件进行统计分析。采用ICC评估2位医师测量DTI各参数的一致性,ICC为0.2~0.4表示一致性一般,0.4~0.6表示一致性中等,0.6~0.8表示一致性较强,>0.8表示一致性很强[15]。连续变量行Kolmogorov-Smirnov检验,符合正态分布以x ± s表示,组间比较行独立样本t检验;不符合正态分布以M(P25,P75)表示,组间比较行Wilcoxon秩和检验。比较2组各参数,差异有统计学意义的参数采用ROC曲线评估其诊断效能,AUC>0.7为诊断效能较好。诊断效能较好的指标进一步行联合诊断试验,包括联合诊断预测因子及系列试验(串联及并联试验),AUC及约登指数均较高的参数行logistic回归分析,计算联合诊断预测因子,评估其诊断效能。通过串联及并联试验计算诊断效能最佳的参数组合,评估其净敏感度、净特异度及约登指数。以P < 0.05为差异有统计学意义。
2 结果 2.1 一致性分析2位医师测量的FA瘤体、MD瘤体、AD瘤体、RD瘤体、FA水肿近侧、MD水肿近侧、AD水肿近侧、RD水肿近侧、FA水肿远侧、MD水肿远侧、AD水肿远侧、RD水肿远侧一致性为中等至很强(ICC为0.541~0.890,均P < 0.05),各相对值一致性为一般至中等(ICC为0.260~0.527,均P < 0.05)。
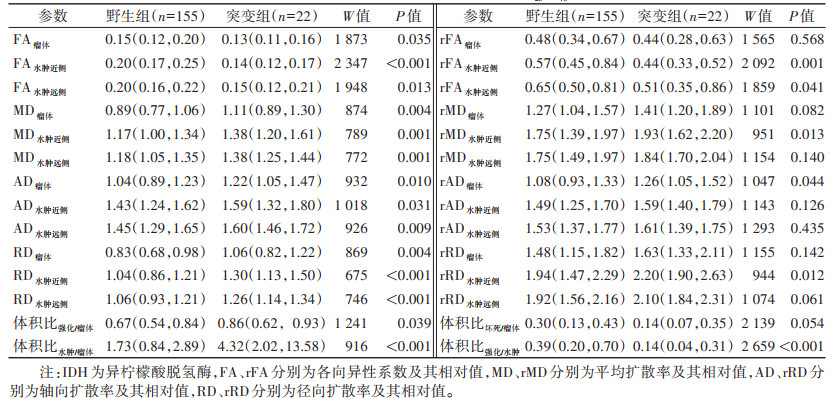
2.2 2组各参数比较除体积比坏死/瘤体、rFA瘤体、rMD瘤体、rMD水肿远侧、rAD水肿近侧、rAD水肿远侧、rRD瘤体、rRD水肿远侧,2组其余各DTI参数及其相对值差异均有统计学意义(均P < 0.05)(表 1)。其中,野生组的体积比强化/水肿高于突变组,野生组体积比水肿/瘤体、体积比强化/瘤体低于突变组(均P < 0.05)。野生组FA瘤体、FA水肿近侧、FA水肿远侧、rFA水肿近侧、rFA水肿远侧均高于突变组,MD瘤体、MD水肿近侧、MD水肿远侧、AD瘤体、AD水肿近侧、AD水肿远侧、RD瘤体、RD水肿近侧、RD水肿远侧及rMD水肿近侧、rAD瘤体、rRD水肿近侧、rRD水肿远侧均低于突变组(均P < 0.05)。
| 表 1 IDH野生组与突变组各参数比较[M(P25,P75)] |
 |
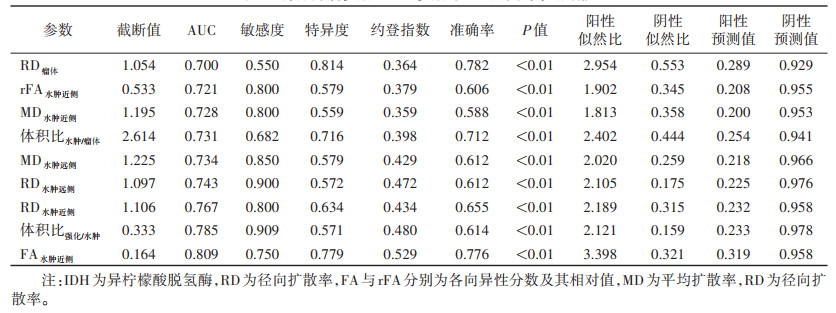
ROC曲线显示,AUC及约登指数最高的参数分别为FA水肿近侧、体积比强化/水肿、RD水肿近侧、RD水肿远侧、MD水肿远侧,其敏感度分别为0.750、0.909、0.800、0.900、0.850,特异度分别为0.779、0.571、0.634、0.572、0.579(表 2)。对上述参数进行联合诊断,联合诊断预测因子=exp(-2.398×体积比强化/水肿-14.017×FA水肿近侧-4.648×MD水肿远侧+1.890×RD水肿近侧+7.482×RD水肿远侧-3.770),当截断值为0.162时,敏感度为0.800,特异度为0.826,约登指数为0.626,AUC为0.866,诊断效能优于各参数单独诊断(图 2)。对上述参数进行串联及并联试验,结果表明,各参数串联试验诊断效能均有提升,RD水肿远侧与体积比强化/水肿这一组合的约登指数最高,其次分别是MD水肿远侧与体积比强化/水肿、FA水肿近侧与体积比强化/水肿、MD水肿远侧与RD水肿远侧、RD水肿远侧与FA水肿近侧(表 3)。体积比强化/水肿小而RD水肿远侧高为IDH突变的可能更高(图 3,4)。
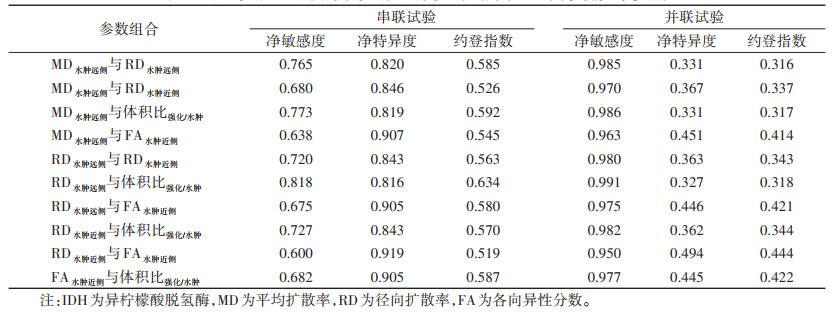
| 表 2 部分肿瘤参数及DTI参数对IDH突变的诊断效能 |
 |
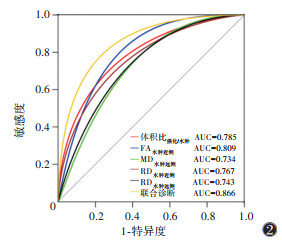 |
| 图 2 各参数单独及联合诊断的ROC曲线 |
| 表 3 用于诊断IDH突变的串联试验及并联试验结果(AUC最高的前5个参数) |
 |
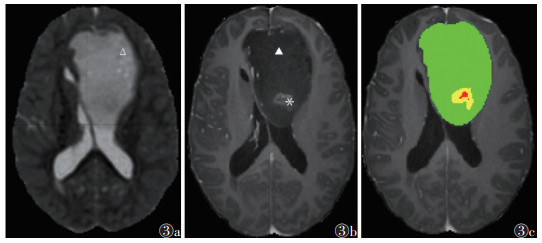 |
| 注:患者,男,43岁;图3a为RD图,可见瘤周水肿远侧区域呈高信号(Δ);图3b,3c分别为T1WI增强扫描图像、分割图像,可见肿瘤强化范围较小(图3b*,图3c黄色区域),瘤周水肿范围大(图3b▲,图3c绿色区域),即体积比强化/水肿小 图 3 Ⅳ级星形细胞瘤异柠檬酸脱氢酶(IDH)突变型的体积比强化/水肿及径向扩散率(RD)图 |
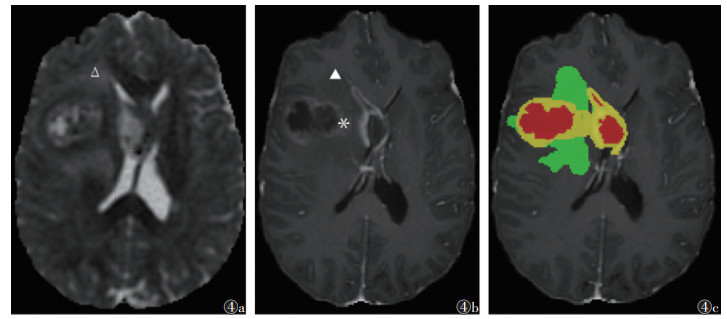 |
| 注:患者,女,58岁,IDH野生型胶质母细胞瘤;图4a为RD图,可见瘤周水肿远侧区域呈稍高信号(Δ);图4b,4c分别为T1WI增强扫描图像、分割图像,可见肿瘤强化范围较大(图4b*,图4c黄色区域),瘤周水肿范围较小(图4b▲,图4c绿色区域),即体积比强化/水肿大 图 4 胶质母细胞瘤异柠檬酸脱氢酶(IDH)野生型的体积比强化/水肿及径向扩散率(RD)图 |
3 讨论
IDH突变与否对HGG治疗方法的选择有重要影响。HGG行全切除术时需切除肿瘤周围部分不强化/水肿区域,对IDH突变Ⅳ级星形细胞瘤患者的预后有所改善,但对胶质母细胞瘤患者的预后改善有限[16-17]。约90%的IDH突变型HGG患者会发生MGMT启动子甲基化,可提高替莫唑胺化疗反应,因此MGMT启动子甲基化和IDH突变被认为是HGG良好预后的预测因子[18]。既往研究认为不明显强化的胶质瘤,以及位于额叶的HGG更易发生IDH突变,但常规MRI征象对鉴别IDH突变存在争议[19-20],故引入多模态扫描方法。
DWI、DTI及DKI等扩散序列均在IDH突变胶质瘤的鉴别中具有重要作用。Zhao等[21]发现DKI与DTI均能鉴别胶质瘤的IDH突变情况,其中轴向峰度值诊断效能最高,但AUC仅为0.72。Zhu等[22]采用DKI鉴别LGG的IDH突变情况,各参数的AUC为0.707~0.778,提示单独应用某一种扩散指标并不能很好地区分IDH突变肿瘤。本研究采用多个DTI参数联合诊断HGG的IDH突变情况,其中FA值主要反映水分子各向异性扩散程度,MD、AD、RD反映水分子总扩散、轴位及垂直方向的水分子扩散活动。取得了较好的诊断效能,AUC为0.866。Halefoglu等[23]研究证实,ADC均值能较好地区分IDH突变的HGG(AUC=0.866),且相对ADC值(rADC)诊断效能更高(AUC=0.939),说明ADC对分子表型判断具有巨大潜能,与本研究结果相似。
此外,动态磁敏感对比增强灌注加权成像(dynamic susceptibility contrast-perfusion weighted imaging,DSC-PWI)也被用于鉴别HGG的IDH突变状态,其关键指标为相对脑血容量(relative cerebral blood volume,rCBV)。Pons-Escoda等[24]发现,rCBV对HGG的IDH突变状态的诊断效能较高(AUC=0.811)。Xing等[25]利用rADC与rCBV联合预测HGG的IDH突变情况,进一步提高了诊断效能(AUC=0.895)。本研究联合诊断包含了5个参数,临床应用存在一定不便。本研究通过串联试验(降低了净敏感度,但提升了净特异度)确定了兼具敏感度和特异度的诊断性指标组合,RD水肿远侧与体积比强化/水肿联合约登指数最高,表明水肿远侧区域垂直方向的水分子扩散活动越强,强化区域相对水肿区域比例越小,则越倾向于诊断为IDH突变的HGG。这符合Ⅳ级的星形细胞瘤较胶质母细胞瘤更不易侵袭性生长的特点,肿瘤细胞沿神经纤维的浸润性生长,使水分子的径向扩散受到影响。既往研究报道,HGG瘤周水肿体积相对较小常与IDH突变相关,由于IDH野生型HGG的凝血途径激活和血管内血栓形成导致肿瘤过度缺氧,表现为较多坏死成分和非强化区域[26]。推测上述参数联合可反映胶质瘤细胞沿神经纤维浸润情况,以及通过反映细胞代谢状态来推断分子表型。
本研究存在的局限性:①仅选择了常规DTI的扩散相关参数,未考虑ADC值、rADC值等,这可能对联合诊断的诊断效能存在影响。②数据来源于单一数据集,未来可能需多中心前瞻性的数据进一步验证本研究结果。③对水肿范围较大的肿瘤,仅将其划分为水肿区域近远侧并勾画ROI,可能无法反映整个水肿区域的扩散指标,需进一步讨论。
综上所述,DTI参数能鉴别HGG的IDH是否存在突变,联合诊断时诊断效能进一步提升。RD水肿远侧与体积比强化/水肿的串联诊断具有最高的诊断效能。
| [1] |
RODRIGUEZ B, RIVERA D, ZHANG J Y, et al. Magnetic hyperthermia therapy for high-grade glioma: a state-of-the-art review[J]. Pharmaceuticals (Basel), 2024, 17(3): 300. |
| [2] |
WELLER M, WEN P Y, CHANG S M, et al. Glioma[J]. Nat Rev Dis Primers, 2024, 10(1): 33. |
| [3] |
WHITE J, WHITE M P J, WICKREMESEKERA A, et al. The tumour microenvironment, treatment resistance and recurrence in glioblastoma[J]. J Transl Med, 2024, 22(1): 540. |
| [4] |
尹文娅. MRI影像组学预测高级别胶质瘤术腔周围水肿带复发的研究[D]. 成都: 成都医学院, 2023.
|
| [5] |
冀晓莉. 高级别胶质瘤治疗后生存评估[D]. 石家庄: 河北医科大学, 2020.
|
| [6] |
LASOCKI A, BUCKLAND M E, DRUMMOND K J, et al. Conventional MRI features can predict the molecular subtype of adult grade 2-3 intracranial diffuse gliomas[J]. Neuroradiology, 2022, 64(12): 2295-2305. |
| [7] |
KAPSALAKI E Z, BROTIS A G, TSIKRIKA A, et al. The role of the t2-flair mismatch sign as an imaging marker of idh status in a mixed population of low- and high-grade gliomas[J]. Brain Sci, 2020, 10(11): 874. |
| [8] |
冀晓莉, 全冠民, 张可心, 等. IDH突变与高级别胶质瘤治疗后MRI表现及预后的关系[J]. 放射学实践, 2021, 36(2): 169-175. |
| [9] |
张劲松, 邓佳敏, 尚磊, 等. 幕上IDH突变型与野生型胶质细胞瘤MRI强化特征分析[J]. 中华神经外科疾病研究杂志, 2018, 17(6): 492-495. |
| [10] |
DASGUPTA A, GERAGHTY B, MARALANI P J, et al. Quantitative mapping of individual voxels in the peritumoral region of IDH-wildtype glioblastoma to distinguish between tumor infiltration and edema[J]. J Neurooncol, 2021, 153(2): 251-261. |
| [11] |
RATHORE S, AKBARI H, DOSHI J, et al. Radiomic signature of infiltration in peritumoral edema predicts subsequent recurrence in glioblastoma: implications for personalized radiotherapy planning[J]. J Med Imaging (Bellingham), 2018, 5(2): 021219. |
| [12] |
符媚媚. 基于DKI和DTI预测高级别胶质瘤MGMT启动子甲基化状态及其与Ki-67表达程度的相关性研究[D]. 海口: 海南医学院, 2021.
|
| [13] |
CALABRESE E, VILLANUEVA-MEYER J E, RUDIE J D, et al. The university of california san francisco preoperative diffuse glioma MRI dataset[J]. Radiol Artif Intell, 2022, 4(6): e220058. |
| [14] |
CALABRESE E, RUDIE J D, RAUSCHECKER A M, et al. Feasibility of simulated postcontrast MRI of glioblastomas and lower-grade gliomas by using three-dimensional fully convolutional neural networks[J]. Radiol Artif Intell, 2021, 3(5): e200276. |
| [15] |
WANG L, SHEN J, DAS S, et al. Diffusion tensor imaging of the C1-C3 dorsal root ganglia and greater occipital nerve for cervicogenic headache[J]. Korean J Pain, 2020, 33(3): 275-283. |
| [16] |
冯哲斌, 孔东生, 冯世宇, 等. 异柠檬酸脱氢酶基因状态对弥漫性胶质瘤手术策略的影响研究进展[J]. 解放军医学院学报, 2023, 44(8): 928-932. |
| [17] |
田传帅, 朱正阳, 周佳南, 等. 多b值三指数模型对成人弥漫性胶质瘤异柠檬酸脱氢酶基因突变状态的评估价值[J]. 中国中西医结合影像学杂志, 2025, 23(1): 102-107. |
| [18] |
谢致岩. 扩散加权成像预测脑胶质瘤IDH突变与MGMT启动子甲基化共现的研究[D]. 青岛: 青岛大学, 2023.
|
| [19] |
席华泽, 周俊林. 分形维数对高级别胶质瘤异柠檬酸脱氢酶-1基因突变状态和Ki-67指数的评估价值[J]. 中国中西医结合影像学杂志, 2024, 22(2): 127-132. |
| [20] |
LASOCKI A, TSUI A, GAILLARD F, et al. Reliability of noncontrast-enhancing tumor as a biomarker of IDH1 mutation status in glioblastoma[J]. J Clin Neurosci, 2017, 39: 170-175. |
| [21] |
ZHAO J, WANG Y L, LI X B, et al. Comparative analysis of the diffusion kurtosis imaging and diffusion tensor imaging in grading gliomas, predicting tumour cell proliferation and IDH-1 gene mutation status[J]. J Neurooncol, 2019, 141(1): 195-203. |
| [22] |
ZHU H, XIE Y, LI L, et al. Diffusion along the perivascular space as a potential biomarker for glioma grading and isocitrate dehydrogenase 1 mutation status prediction[J]. Quant Imaging Med Surg, 2023, 13(12): 8259-8273. |
| [23] |
HALEFOGLU A M, CAMURCUOGLU E, TANIK C, et al. Predictive role of magnetic resonance imaging in the distinction of isocitrate dehydrogenase (IDH) mutant grade 4 astrocytomas versus glioblastomas[J]. Acta Radiol, 2023, 64(6): 2074-2086. |
| [24] |
PONS-ESCODA A, NAVAL-BAUDIN P, VIVEROS M, et al. DSC-PWI presurgical differentiation of grade 4 astrocytoma and glioblastoma in young adults: rCBV percentile analysis across enhancing and non-enhancing regions[J]. Neuroradiology, 2024, 66(8): 1267-1277. |
| [25] |
XING Z, ZHANG H, SHE D, et al. IDH genotypes differentiation in glioblastomas using DWI and DSC-PWI in the enhancing and peri-enhancing region[J]. Acta Radiol, 2019, 60(12): 1663-1672. |
| [26] |
SAHU A, PATNAM N G, GODA J S, et al. Multiparametric magnetic resonance imaging correlates of isocitrate dehydrogenase mutation in who high-grade astrocytomas[J]. J Pers Med, 2022, 13(1): 72. |
 2025, Vol. 23
2025, Vol. 23


