| 高分辨力MRI脂肪抑制T2WI联合DWI对肛瘘检测效果的评价 |
2. 江苏大学附属医院影像科,江苏 镇江 212001
肛瘘是一个线性肉芽组织感染的通道,连接于肛周或直肠至肛门周围的皮肤,其壁由炎性肉芽组织和纤维组织构成[1],好发于青壮年男性。肛瘘不仅可引起局部疼痛和刺激感,还可成为全身感染源,最常见的症状为流脓(约65%的病例)[2]。肛瘘有时可致急性脓肿,需立即手术,大多数简单的瘘管可通过瘘管切开解除。肛瘘治疗的目的是消除原发口、相关通道和继发口而不致肛门失禁[3]。成功的手术依赖于术前准确评价原发性瘘管的走行及继发性瘘管延伸[4]。术前MRI检查目的在于明确瘘管的内口及走行,并为手术方案的选择提供参考依据。因此,本研究试图通过评价高分辨力MRI脂肪抑制T2WI联合DWI在检测肛瘘中的作用,并与术后结果进行对比,以探讨肛瘘术前MRI检查的重要性。
1 资料与方法 1.1 一般资料对丹阳市中医院2016年1月至2017年11月63例已行高分辨力MRI扫描且经手术证实的59例肛瘘患者的临床和影像学资料进行分析,其中男52例,女7例;年龄22~70岁,平均(41.87±9.74)岁。主要表现为肛区疼痛、不适,肛周皮肤红肿、出现硬结、瘘口及分泌物。伴发克隆恩病7例,溃疡型结肠炎4例,2型糖尿病3例及直肠癌术后2例。排除标准:已行手术、妊娠、幽闭恐惧症、安装心脏起搏器及图像不符合诊断要求患者。
1.2 仪器与方法采用Siemens 1.5 T 16通道超导型MRI成像仪,盆腔相控阵线圈。患者取仰卧位。扫描序列包括SE和FSE:T1WI TR/TE 420 ms/18 ms,层厚3 mm,层距0.3 mm,矩阵240×256,轴位、冠状位及矢状位T2WI TR/TE 3 100 ms/125 ms,层厚3 mm,层距0.3 mm,矩阵240×256;脂肪抑制轴位T2WI TR/TE 4 250 ms/102 ms,层厚3 mm,层距0.3 mm,矩阵240×256;轴位DWI TR/TE 6 500 ms/105 ms,层厚4 mm,层距0.4 mm,FOV 300 mm×300 mm,b值为0、500和1 000 s/mm2。
1.3 图像分析MRI图像由2名MRI诊断医师(具有5年以上MRI工作经验)独立进行盲法分析,包括原发性及继发性瘘管的数量、走行、内口位置及是否伴脓肿。瘘管定义为条状或椭圆形长T1、长T2信号影;原发性瘘管是指连接于肛周或直肠至肛门周围皮肤的异常通道;继发性瘘管是指与原发性瘘管相连、直径小于原发性瘘管、可有独立内口的细小分支。肛周脓肿定义为盆底或括约肌间脂肪间隙内在DWI上呈圆形或类圆形异常聚集的高信号、ADC呈低信号;瘘管内口按肛管时钟表方向进行定位。瘘管的分级采用St. James大学医院分级系统[5]:Ⅰ级,单纯括约肌间线性瘘管;Ⅱ级,括约肌间复杂瘘管;Ⅲ级,单纯经括约肌瘘管;Ⅳ级,经括约肌的复杂瘘管;Ⅴ级,肛提肌上和经肛提肌瘘管及括约肌外瘘管。
1.4 统计学分析采用SPSS 18.0软件,计量资料以x±s表示,计数资料以率(%)表示。以P<0.05差异为有统计学意义。
2 结果本组63例中,59例经手术证实为肛瘘,共71条瘘管及62个内口。Ⅰ级20例(图 1),Ⅱ级12例(9例伴脓肿)(图 2),Ⅲ级11例(图 3),Ⅳ级13例(其中3例伴坐骨直肠间隙脓肿、5例伴坐骨肛管间隙脓肿和2例伴肛周皮下脂肪间隙脓肿)(图 4),Ⅴ级2例(其中1例伴脓肿)及括约肌外瘘管1例伴脓肿形成。49例为单一瘘管,2条瘘管8例,3条瘘管2例;56例为单一内口,3例有2个内口。高分辨力MRI脂肪抑制T2WI联合DWI诊断结果与手术结果的关系见表 1。高分辨力MRI脂肪抑制T2WI联合DWI对原发性瘘管检测的敏感度、特异度、阳性预测值和阴性预测值分别为98.31%(58/59)、75.00%(3/4)、98.31%(58/59)、75.00%(3/4),继发性瘘管分别为83.33%(10/12)、98.04%(50/51)、90.91%(10/11)、96.15%(50/52),对脓肿的诊断敏感度和特异度分别为100.00%(21/21)和97.62%(41/42),对内口的诊断敏感度及阳性预测值分别为96.77%(60/62)及98.36%(60/61),瘘管分级的诊断准确率为98.31%(58/59)。
 |
| 图 1 男,25岁,单纯括约肌间线性瘘管(Ⅰ级) 图 1a,1b 轴位及冠状位脂肪抑制T2WI显示瘘管位于内外括约肌间(箭头) 图 1c 轴位脂肪抑制T2WI显示乙状结肠壁增厚(箭头),提示炎性肠病 |
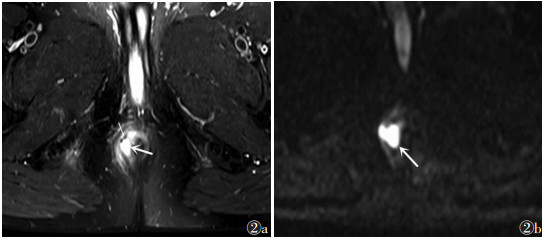 |
| 图 2 男,31岁,括约肌间复杂瘘管(Ⅱ级) 图 2a 轴位脂肪抑制T2WI显示内外括约肌间脓肿(粗箭)、内见点状气体信号影(细箭) 图 2b b值=1 000 s/mm2的DWI显示脓肿呈高信号 |
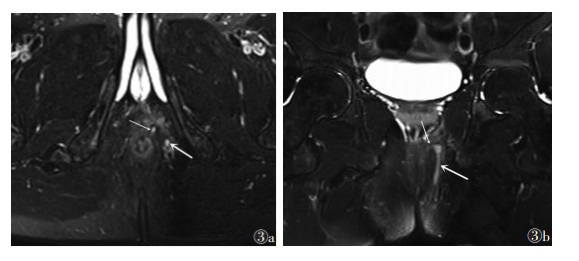 |
| 图 3 男,43岁,单纯经括约肌瘘管(Ⅲ级) 图 3a 轴位脂肪抑制T2WI显示瘘管内口(细箭)、瘘管位于外括约肌的外侧(粗箭) 图 3b 冠状位脂肪抑制T2WI显示瘘管经内外括约肌(细箭)走行于外括约肌的外侧(粗箭) |
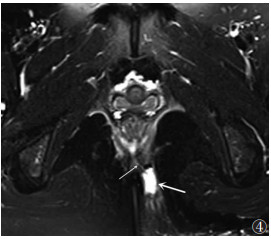 |
| 图 4 男,37岁,经括约肌的复杂瘘管(Ⅳ级),轴位脂肪抑制序列T2WI显示坐骨直肠脂肪间隙脓肿(粗箭)及经内外括约肌的瘘管(细箭) |
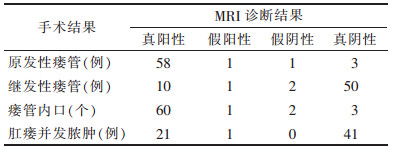
| 表 1 高分辨力MRI脂肪抑制T2WI联合DWI与手术结果的对比 |
 |
3 讨论
传统的瘘管造影、超声和CT因对肛瘘的诊断价值有限,应用已越来越少。MRI软组织分辨力高、可任意平面成像且脂肪抑制序列对液体敏感,不仅可清晰显示瘘管走行及其伴发疾病,还可显示与盆底结构间的关系,同时还可对盆腔其他病变进行评价(如炎性肠病),因此在肛瘘中的应用越来越广泛。MRI冠状位可清晰显示肛提肌和耻骨直肠肌,轴位可清晰显示括约肌间隙,因而冠状位和轴位图像在肛瘘的评价中具有重要意义。
本组63例中,经肛肠手术证实原发性瘘管59例,高分辨力MRI脂肪抑制T2WI联合DWI对原发瘘管的诊断敏感度为98.31%,稍高于陈均等[6]报道的95.3%,可能与本组采用高分辨力MRI扫描可更加清晰显示瘘管结构及脂肪抑制序列对液体更加敏感有关。韦小梅等[7]采用高分辨力MRI增强扫描对主瘘管的诊断敏感度为98.99%,与本组结果一致。已有学者[8]提议采用脂肪抑制T2WI替代增强扫描,本研究支持这一观点。本组1例假阳性患者,手术证实为特殊性窦道感染所致,微生物学检查提示克雷伯杆菌感染,回顾性分析术前影像,病灶主要表现为局灶性,未发现与肛周皮肤相通的瘘管;1例假阴性患者,手术及病理证实为肉芽肿性炎症,回顾术前影像发现脂肪抑制T2WI及DWI呈不连续的线状稍高信号影。
21例脓肿均可通过高分辨力MRI脂肪抑制T2WI联合DWI进行正确诊断,并可明确脓肿和肛提肌及耻骨直肠肌间关系。1例假阳性患者,MRI提示脓肿,但手术证实为炎性积液,据Dohan等[9]报道区分肛瘘并发炎性积液和脓肿的最佳ADC阈值为1.186×10-3 mm2/s,而本例假阳性患者ADC值为1.627×10-3 mm2/s,大于该阈值,支持炎性积液的诊断。本组MRI对脓肿诊断的敏感度为100.00%,与韦小梅等[7]报道一致,其采用增强扫描,与本组扫描时间差别不大,但增强扫描增加检查费用,且对比剂本身亦可引起不良反应,如肾源性系统性纤维化等。
肛肠手术可探查继发性瘘管12条,而采用高分力MRI脂肪抑制T2WI联合DWI可正确诊断10例。2例MRI开始时未发现,但术后回顾性分析时可正确识别。MRI对继发性瘘管诊断的敏感度为83.33%,与韦小梅等[7]等报道一致,但高于张得旺等[10]报道的76.5%。本组继发瘘管较高的敏感性可能与采用的薄层扫描方式及脂肪抑制序列可更好显示瘘管有关。Singh等[8]同时采用MRI评价马蹄形瘘管(继发性瘘道伴不在中线两侧的水平方向延伸),并报道MRI对马蹄形瘘管诊断的敏感度和特异度分别为87.50%和95.24%,而本组未对马蹄形瘘管单独进行分析。
MRI不能清晰区分内括约肌和肛门黏膜,因此有时内口位置是根据瘘道所在括约肌间的位置大致进行推测。Halligan等[11]认为括约肌间脓液最大区域可能是内口所在位置。本组经手术证实共62个内口,MRI正确诊断60例,其对内口的诊断敏感度及阳性预测值分别为96.77%及98.36%,与Singh等[8]报道的95.83%和97.87%相近。1例假阳性患者,手术证实为窦道口;2例内口呈假阴性,可能与内口较小、处于闭合状态、瘘管为非活动性及缺乏液体对比有关。
大多数原发性瘘管的走行与肛周腺体位置相关,因此,瘘管的分级主要根据瘘管的走行。目前,主要有2种分级系统:Parks分级系统[12]和St. James大学医院分级系统。本组59例采用St. James大学医院分级系统,58例可正确分级,准确率达98.31%。
本研究的局限性:①样本数量有限,还需大样本数据进一步证实;②MRI检查费用较高,限制了在基层医院的开展,高分辨力MRI扫描时间较常规MRI扫描时间更长;③仅限于原发性病变,不包括复发或已手术的病例。
总之,高分辨力MRI脂肪抑制T2WI联合DWI对肛瘘患者原发瘘管、继发瘘管、内口及其伴发的脓肿具有较高的诊断敏感性和特异性,可作为肛瘘术前的常规检查方法。
| [1] |
唐晓雯, 王中秋. MRI技术在复杂型肛瘘诊断中的应用进展[J]. 放射学实践, 2016, 31(11): 1105-1109. |
| [2] |
Vanbeckevoort D, Bielen D, Vanslembrouck R, et al. Magnetic resonance imaging of perianal fistulas[J]. Magn Reson Imaging Clin N Am, 2014, 22: 113-123. DOI:10.1016/j.mric.2013.07.008 |
| [3] |
Kumar N, Agarwal Y, Chawla AS, et al. MRI of perianal fisstulae: a pictorial kaleidoscope[J]. Clin Radiol, 2015, 70: 1451-1461. DOI:10.1016/j.crad.2015.09.001 |
| [4] |
Waniczek D, Adamczyk T, Arendt J, et al. Usefulness assessment of preoperative MRI fistulography in patients with perianal fistulas[J]. Pol J Radiol, 2011, 76: 40-44. |
| [5] |
Morris J, Spencer JA, Ambrose NS. MR imaging classification of perianal fistulas and its implications for patient management[J]. Radiographics, 2000, 20: 623-635. DOI:10.1148/radiographics.20.3.g00mc15623 |
| [6] |
陈均, 陆锦贵, 吴青山, 等. 扩散加权成像结合常规序列在复杂性肛瘘中的应用价值[J]. 中国CT和MRI杂志, 2015, 13(12): 95-101. DOI:10.3969/j.issn.1672-5131.2015.12.031 |
| [7] |
韦小梅, 邓德茂, 梁玲艳, 等. 3.0 T高分辨率MRI在肛瘘分型与内口定位中的应用价值[J]. 磁共振成像, 2017, 8(5): 354-358. |
| [8] |
Singh K, Singh N, Thukral CL, et al. Magnetic resonance imaging (MRI) evaluation of perianal fistulae with surgical correlation[J]. J Clin Diagn Res, 2014, 8: 1-4. DOI:10.1111/crj.2014.8.issue-1 |
| [9] |
Dohan A, Eveno C, Oprea R, et al. Diffusion-weighted MR imaging for the diagnosis of abscess complicating fistula-in-ano:preliminary experience[J]. Eur Radiol, 2014, 24: 2906-2915. DOI:10.1007/s00330-014-3302-y |
| [10] |
张得旺, 李欣, 唐光健, 等. 肛瘘术前MRI征象与手术病理结果对照研究[J]. 中国医学影像学杂志, 2014, 22(6): 441-445. |
| [11] |
Halligan S, Stoker J. Imaging of fistula in ano[J]. Radiology, 2006, 239: 18-33. DOI:10.1148/radiol.2391041043 |
| [12] |
Parks AG, Gordon PH, Hardcastle JD. A classification of fistula-in-ano[J]. Br J Surg, 1976, 63: 1-12. DOI:10.1002/(ISSN)1365-2168 |
 2018, Vol. 16
2018, Vol. 16


